富生酮氨基酸饮食改善高脂诱导小鼠非酒精性脂肪肝*
徐玲,马红艳,肖斌,高陈林
(1.泸州医学院附属医院 内分泌代谢科,四川 泸州 646000;2.四川医科大学基础医学院 生物化学教研室,四川 泸州 646000)
论著
富生酮氨基酸饮食改善高脂诱导小鼠非酒精性脂肪肝*
徐玲1,马红艳1,肖斌2,高陈林1
(1.泸州医学院附属医院 内分泌代谢科,四川 泸州 646000;2.四川医科大学基础医学院 生物化学教研室,四川 泸州 646000)
摘要:目的探讨富生酮氨基酸(KAA)饮食对高脂诱导小鼠非酒精性脂肪肝的影响及机制。方法C57BL雄性小鼠随机分4组,给予常规饮食(NC)、高脂饮食(HFD)、富生酮氨基酸高脂饮食(HFDKAAR)以及高脂喂养8周后改为富生酮氨基酸高脂饮食(HFD→HFDKAAR)喂养。每周测进食量、体重,16周后行腹腔内注射葡萄糖耐量实验后处死小鼠,测肝重量、内脏脂肪重量、肝脂质沉积、Kupffer细胞聚集及肿瘤坏死因子-α(TNF-α)和白介素-1β(IL-1β)mR NA表达。结果各组小鼠摄入热卡比较差异无统计学意义。与NC组比较,HFD组小鼠体重和内脏脂肪重量增加,伴随胰岛素抵抗,肝脂质沉积和Kupffer细胞数量显著增加,TNF-α和IL-1β mR NA表达增加(P<0.05)。与HFD组比较,HFDKAAR及HFD→HFDKAAR组小鼠体重、内脏脂肪下降,胰岛素抵抗均减轻(P<0.05),肝脏Kupffer细胞的数量及脂质沉积减少,TNF-α和IL-1β mR NA的高表达均被逆转(P<0.05)。结论高脂膳食能诱导出非酒精性脂肪肝小鼠模型,富生酮氨基酸饮食可抑制高脂诱导的肝脏Kupffer细胞的表达,显著改善高脂饮食诱导的肥胖、胰岛素抵抗、肝脂质沉积,减轻肝脏的炎症损伤。
关键词:氨基酸;非酒精性脂肪肝病;代谢综合征
生酮氨基酸(ketogenic amino acid,KAA)是指分解代谢过程中能转变成酮体的的氨基酸,不能在体内合成,属于必须氨基酸。一些临床和动物实验显示氨基酸参与的代谢异常与多种疾病的发生发展有关。目前有学者报道生酮氨基酸能减轻脂肪肝及改善胰岛素抵抗,也有与之相反的报道,因此从非酒精性脂肪肝(non-alcoholic fatty liver disease,NAFLD)的病因学和治疗学的角度看氨基酸代谢,其作用还存在争议。本实验用高脂饮食诱导小鼠NAFLD,用富生酮氨基酸饮食作为干预因素,观察小鼠的血糖、胰岛素抵抗指数、肝脏脂质沉积和肝脏巨噬细胞、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白介素-1β(Interleukin-1β,IL-1β)mRNA的表达,旨在进一步探讨富生酮氨基酸饮食对NAFLD的作用及可能机制,为防治非酒精性脂肪肝提供新的依据。
1 材料与方法
1.1一般材料
1.1.1实验动物清洁级8周龄体重为20~23 g 的C57BL雄性小鼠(四川医科大学动物实验室提供),动物饲料(日本Ajinomoto公司)。
1.1.2主要实验材料实时荧光定量聚合酶链反应(real-time quantitative polymerase chain reaction,Real-time qPCR)试剂盒(日本TaKaRa公司),大鼠抗小鼠单克隆F4/80抗体(英国AbD Serotec公司),罗丹明标记荧光二抗(美国Jackson Immuno Research公司),胰岛素酶联免疫吸附法(enzyme-linked immunosorbent assay,ELISA)试剂盒(日本MIoBS公司),微量血糖仪(上海罗氏诊断)。
1.2实验方法
1.2.1动物分组将32只小鼠随机分组,分别给予普通饮食(normal control,NC)(n=8)、高脂饮食[52%脂肪(high fat diet,HFD)](n=16)、富含生酮氨基酸的高脂饮食(8%生酮氨基酸+52%脂肪HFDKAAR)(n= 8)喂养;喂养8周后再将高脂饮食组小鼠随机分为两组,一组继续原高脂饮食喂养(n=8),另一组改为富生酮氨基酸高脂饮食喂养(HFD→HFDKAAR)(n= 8)。具体饮食配方参照文献[1],每周测进食量和体重 [第8、12周时因腹腔注射葡萄糖耐量试验(intraperitoneal glucose tolerance test,IPGTT)故停测进食量],共喂养16周。
1.2.2血糖、胰岛素水平的检测各组小鼠喂养16周后,禁食6h,测体重后腹腔内注射葡萄糖(1g/kg),分别在注射葡萄糖前、注射葡萄糖后15、30、60、90和120min测血糖,绘制曲线并依据公式计算曲线下面积(area under curve,AUC)[mmol/(L·h)]=(0 min血糖值+30min血糖值)×0.5/2+(30min血糖值+60min血糖值)×0.5/2+(60min血糖值+120min血糖值)× 1/2;同时收集注射葡萄糖前、注射葡萄糖后15、30和60 min尾静脉血,用ELISA方法测各时间点小鼠血浆中胰岛素浓度,根据血糖和胰岛素浓度计算胰岛素抵抗指数(insulin resistance index,IRI),公式为:IRI=葡萄糖(mmol/L)×胰岛素(mIU/L)/22.5。
1.2.3油红O染色测肝细胞脂质沉积处死小鼠取肝组织,优化的切片温度(opti-mum cutting temperature,OCT)包埋冷冻切片(8μm),10%甲醛固定,60%异丙醇处理后行油红O染色20 min,70%甘油封片,显微镜下观察肝细胞中脂质沉积。
1.2.4R eal-time qPCR检测肝细胞中炎症因子TNF-α和IL-1β mR NA表达处死小鼠,Trizol提肝脏总RNA,按试剂盒逆转录成互补脱氧核糖核酸(complementary DNA,cDNA)。引物、染料由日本TaKaRa公司合成。将cDNA按Real-time qPCR体系(20μl)反应,18 S作为管家基因。TNF-α:正向引物5'-GTTCTATGGCCCAGACCCTCAC-3',反向引物5'-GGCACCACTAGTTGGTTGTCTTTG-3';IL-1β:正向引物5'-TCCAGGATGAGGACATGAGCAC-3',反向引物5'-GAACGTCACACACCAGCAGGTTA-3';18S:正向引物5'-TTCTGGCCAACGGTCTAGACAAC -3',反向引物5'-CCAGTCGTCTTGGTGTGCTGA-3'。反应条件:95℃预变性30 s,95℃变性5 s,60℃退火30 s,扩增40个循环后收集数据绘制动力学曲线读取Ct值,扩增重复3次。将各组目的基因Ct值与管家基因Ct值相减得△Ct,再将各组的△Ct与正常对照组的△Ct相减得△△Ct,最后根据2-△△Ct值进行统计分析。
1.2.5免疫荧光染色检测肝脏 F4/80巨嗜细胞(kuffer cells,KCs)表达处死小鼠取肝组织,OCT包埋冷冻切片(5μm),每组随机选4张切片,丙酮处理,2%牛血清白蛋白封闭后加大鼠抗小鼠F4/80单克隆抗体(1∶100),室温孵育,再经TRITC荧光标记的二抗室温反应(1∶200),4',6-二脒基-2-苯基吲哚封片,免疫荧光显微镜观察肝脏F4/80阳性KCs数量,每组随机选10个视野行F4/80阳性细胞计数进行统计分析。
1.3统计学方法
采用SPSS 13.0统计软件进行数据分析,计量数据以均数±标准差(±s)表示,各组均数的比较用方差分析,两两比较用方差分析的SNK-q检验,P< 0.05为差异有统计学意义。
2 结果
2.1各组小鼠的进食量比较
与NC组比较,HFD、HFDKAAR及HFD→HFDKAAR组小鼠每周进食量稍减少;而HFD、HFDKAAR及HFD →HFDKAAR3组间小鼠每周进食量基本一致。经不同饮食提供的热量矫正后,各组小鼠每天进食热量差异无统计学意义(F=1.703,P=0.212)。见图1。
2.2各组小鼠体重、肝脏重量、内脏脂肪重量、内脏脂肪/体重百分比比较
HFD组小鼠与对照组比较体重增加,HFDKAAR组及HFD→HFDKAAR组小鼠体重较HFD组减轻,经SNK-q检验方差分析后,差异有统计学意义(P=0.000、0.032和P=0.000)。HFD组小鼠内脏脂肪(肠系膜和附睾脂肪组织)重量及内脏脂肪/体重百分比高于NC组(P=0.001和0.002)。富生酮氨基酸饮食喂养16周后,不管是HFDKAAR组还是HFD→HFDKAAR组小鼠肝脏重量、内脏脂肪重量及内脏脂肪/体重百分比与HFD组比较均下降,差异有统计学意义。见表1。
2.3各组小鼠糖耐量及胰岛素抵抗的比较
IPGTT结果显示,与NC组比较,HFD组小鼠各时间点血糖、胰岛素浓度、IRI上升,表现出糖耐量异常和胰岛素抵抗。与HFD组比较,HFDKAAR及HFD→HFDKAAR组小鼠各时间点血糖、胰岛素浓度、IRI均降低,特别是HFDKAAR组注射葡萄糖30min后胰岛素浓度[(0.78±0.46)ng/ml]较HFD组[(1.24± 0.38)ng/ml]下降,注射葡萄糖60 min后HFDKAAR组血糖 [(13.96±3.08)mmol/L]较HFD组 [(21.35± 4.36)mmol/L]下降,经SNK-q检验方差分析后,差异有统计学意义(P=0.035和0.034)。HFD组小鼠AUC[(37.93±2.17)]较NC组[(24.73±1.42)]增加41.25% (P=0.000);与HFD组小鼠比较,HFDKAAR组小鼠AUC[(28.22±1.38)]下降23.73%(P=0.000),HFD→HFDKAAR组小鼠AUC[(31.49±1.17)]下降13.91%(P= 0.002)。见图2。
2.4各组小鼠肝脏TNF-α和IL-1β mRNA表达比较
Real-time qPCR结果显示,与NC组比较,HFD组小鼠肝脏组织中炎症因子TNF-α和IL-1β mRNA的表达分别增加2.56和3.29倍;与HFD组比较,HFDKAAR组和HFD→HFDKAAR组小鼠肝脏组织中TNF-α和IL-1β mRNA的高表达都被抑制。见表2和图3。
2.5各组小鼠肝脏F4/80 KCs表达的比较
免疫荧光染色显示F4/80在肝成熟KCs表面表达。NC组小鼠肝脏F4/80阳性细胞数为(2.33± 0.75)/视野,HFD组小鼠肝脏F4/80阳性细胞数为(9.70±1.96)/视野,HFD组小鼠肝脏KCs表达较NC组增加(P=0.000);与HFD组比较,不管是HFDKAAR组[F4/80阳性细胞数为(3.40±0.84)/视野]还是HFD→HFDKAAR组[F4/80阳性细胞数为(4.00±0.82)/视野],小鼠肝脏KCs表达均下降,差异有统计学意义(P=0.000)。见图4。
2.6各组小鼠肝细胞脂质沉积的比较
NC组小鼠肝细胞脂质沉积较少,HFD组小鼠肝细胞脂质沉积较NC组增加,脂滴增大;与HFD组比较,不管是HFDKAAR组还是HFD→HFDKAAR组,小鼠肝细胞脂质沉积均减少,脂滴缩小。见图5。
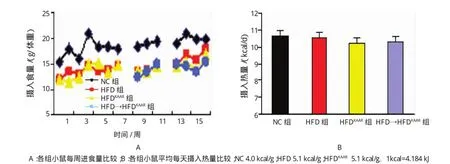
图1 各组小鼠的进食量比较

图2 各组小鼠血糖、胰岛素浓度、IRI及AUC比较
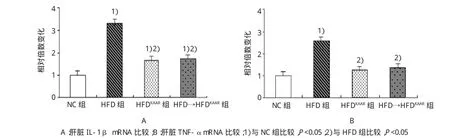
图3 各组小鼠肝脏IL-1β和TNF-α mRNA表达比较
表1 各组小鼠体重、肝脏重量、内脏脂肪重量及内脏脂肪/体重百分比的比较(n=8±s)
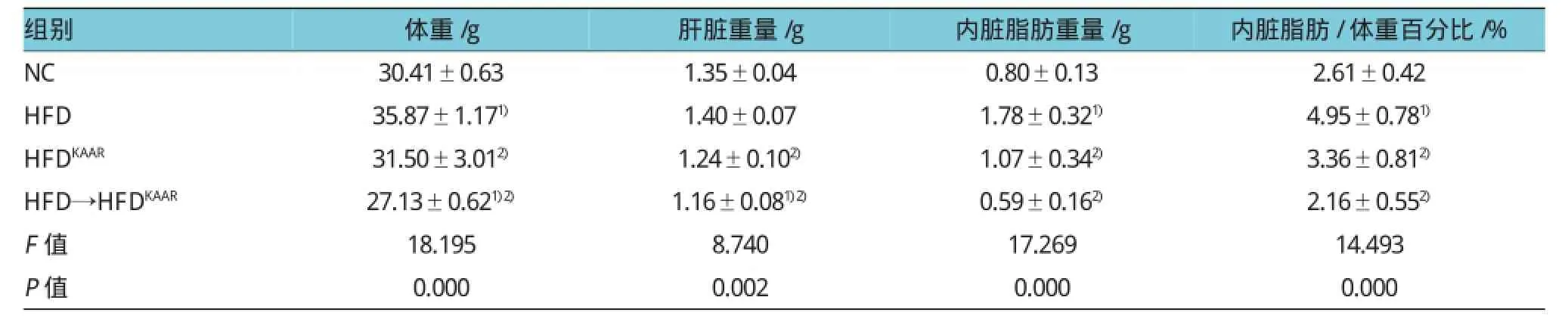
表1 各组小鼠体重、肝脏重量、内脏脂肪重量及内脏脂肪/体重百分比的比较(n=8±s)
注:1)与NC组比较,P<0.05;2)与HFD组比较,P<0.05
组别内脏脂肪/体重百分比/% NC 30.41±0.63 1.35±0.04 0.80±0.13 2.61±0.42 HFD 35.87±1.171) 1.40±0.07 1.78±0.321) 4.95±0.781)体重/g 肝脏重量/g 内脏脂肪重量/g HFDKAARHFD→HFDKAAR31.50±3.012)27.13±0.621)2)1.24±0.102)1.16±0.081)2)1.07±0.342)0.59±0.162)3.36±0.812)2.16±0.552)F值 18.195 8.740 17.269 14.493 P值 0.000 0.002 0.000 0.000
表2 各组小鼠肝脏TNF-α和IL-1β mRNA表达比较 (n=6±s)

表2 各组小鼠肝脏TNF-α和IL-1β mRNA表达比较 (n=6±s)
注:1)与NC组比较,P<0.05;2)与HFD组比较,P<0.05
组别IL-1β mRNA 2-△△CtNC 32.29±0.32 1.00±0.45 1.00±0.38 TNF-αmRNA Ct值IL-1β mRNA Ct值18S mRNA Ct值25.53±0.22 18.76±0.18 TNF-αmRNA 2-△△CtHFD HFDKAAR31.25±0.34 31.87±0.41 24.25±0.23 18.38±0.42 24.78±0.32 18.47±0.30 2.56±0.871)1.24±0.392)3.29±1.371)1.67±0.401)2)HFD→HFDKAAR 31.94±0.241.34±0.262) 1.73±0.331)2)24.72±0.24 18.66±0.24 F值13.032 7.627 P值 0.000 0.002
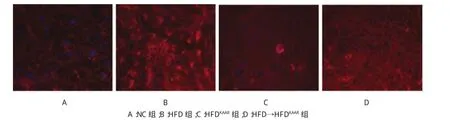
图4 各组小鼠肝脏F4/80 KCs表达比较 (免疫荧光染色×400)

图5 各组小鼠肝细胞脂质沉积比较 (油红O染色×400)
3 讨论
随着人们生活方式的改变,NAFLD已成为西方发达国家最为普遍的慢性肝病,近年来我国的发病率也大幅攀升。NAFLD不仅可进展为肝硬化、肝癌,还与机体胰岛素抵抗、2型糖尿病等代谢性疾病密切相关[2]。公认的NAFLD病理生理改变核心是肝脏胰岛素抵抗,故NAFLD被看作是代谢综合征在肝脏的表现[3],其发生、发展的机制未完全明确。如何有效防治NAFLD等代谢性疾病一直是研究的热点。
KAA是指分解代谢过程中能转变成酮体的氨基酸,有异亮氨酸、亮氨酸、赖氨酸、色氨酸、苯丙氨酸、苏氨酸和酪氨酸。这些氨基酸不能在体内合成,属于必须氨基酸。近年氨基酸代谢异常与NAFLD等代谢性疾病发生发展的关系越来越受到重视。有报道补充支链氨基酸可降低小鼠心脏和骨骼肌的氧化应激,延长小鼠寿命[4-5]。新近报道长期生酮饮食可以转变机体氨基酸代谢水平,改善肥胖及脂肪性肝炎[6]。SOLERTE等[7]发现口服异亮氨酸等生酮氨基酸混合制剂能改善老年2型糖尿病胰岛素抵抗。YASUSHI等[1]发现生酮氨基酸饮食能显著抑制小鼠肝脏脂质合成并预防脂肪肝和胰岛素抵抗的发生。国内宋文琪等[8]报道,单纯性肥胖患儿的血清氨基酸水平严重失衡,且普遍存在胰岛素抵抗。金玲凤等[9]发现高脂饮食诱导的SD大鼠NAFLD肝内蛋白质组学随着肝内脂肪的聚集而改变。叶春等[10]发现运动使NAFLD大鼠血清中支链氨基酸上升,芳香族氨基酸明显下降,肝功能明显好转。但与之相反,NEWGARD等[11]报道持续氨基酸灌注会通过活化mTOR通路而导致胰岛素抵抗,氨基酸代谢如何参与NAFLD等代谢性疾病的发生、发展未完全明确,有必要进一步研究。
KCs是定居于肝血窦的单核巨噬细胞,是体内最大的巨噬细胞群。巨噬细胞作为炎症因子的经典来源,激活的KCs产生多种细胞因子如TNF-α、白介素-6等。KCs在NAFLD等代谢性疾病发生机制中的作用已越来越受到关注[12-14]。F4/80是KCs的特异性表达表面抗原,本研究利用F4/80抗体对肝组织行免疫荧光染色检测肝KCs的数量及募集情况。
前期预实验中发现,小鼠高脂喂养8周开始出现糖耐量异常和肝脂质沉积,所以本研究干预组有HFD组和HFD→HFDKAAR组,旨在观察富KAA饮食能否改善高脂饮食诱导的小鼠脂肪肝,同时也观察已经出现脂肪肝的小鼠,再用富KAA饮食能否改善或逆转脂肪肝。研究发现,高脂饮食能诱导肝脂肪变性,KCs增多聚集,炎症因子表达显著增加,与黄海琇等[15]报道NAFLD早期阶段,KCs已经呈现出经典激活巨噬细胞M1型,TNF-α等炎症因子明显增加一致。本研究中笔者发现,饮食中增加生酮氨基酸含量没有影响小鼠食欲。在摄入相同卡路里、相同脂肪情况下,不管是HFDKAAR组还是HFD→HFDKAAR组小鼠肝脂肪变性、胰岛素抵抗、肥胖等均明显改善或被逆转;肝脏炎症因子TNF-α和IL-1β mRNA的高表达均明显被抑制,可能与减少高脂饮食所诱导的小鼠肝脏KCs的聚集密切相关。
综上所述,高脂膳食能构建出NAFLD小鼠模型,中长期的富生酮氨基酸饮食可抑制肝脏KCs的激活,显著改善或逆转高脂饮食诱导的肥胖、胰岛素抵抗、肝脏脂质沉积,减轻肝脏的炎症损伤。
参考文献:
[1]YASUSHI N,NATSUMI N,NAHOKO S,et al.Ketogenic essential amino acids modulate lipid synthetic pathways and prevent hepatic steatosis in mice[J].PLoS One,2010,5(8):e12057.DOI: 10.1371/journal.pone.0012057.
[2]PARASH O,HAMID S.Are we ready for a new epidemic of under recognized liver disease in South Asia especially in Pasistin?Non alcoholic fatty liver disease[J].JPak Med Assoc, 2013,63(3):95-99.
[3]HE B,LIU L,YU C,et al.Roux-en-Y gastric bypass reduces lipid overaccumulation in liver by upregulating hepatic autophagy in obese diabetic rats[J].Obes Surg,2015,25(1):109-118.
[4]ALESSANDRAV,GIUSEPPEDA,ENZO N.Branched-chain amino acids,mitochondrial biogenesis,and healthspan:an evolutionary perspective[J].Aging,2011,3(5):464-478.
[5]GIUSEPPE D A,MAURIZIO R,ANNALISA C,et al.Branchedchain amino acid supplementation promotes survival and supports cardiac and skeletal muscle mitochondrial biogenesis in middle-aged mice[J].Cell Metab,2010,12(10):362-372.
[6]DOURIS N,MELMAN T,PECHERERJM,et al.Adaptive changes in amino acid metabolism permit normal longevity in mice consuming a low-carbohydrate ketogenic diet[J].Biochim Biophys Acta,2015,1852(10):2056-2065.
[7]SOLERTE S B,GAZZARUSO C,SCHIFINO N,et al.Metabolic effects of orally administered amino acid mixture in elderly subjects with poorly controlled type 2 diabetes mellitus[J].Am J Cardiol,2004,93(8):23-29.
[8]宋文琪,李时莲,张美和,等.单纯性肥胖儿童血清氨基酸水平分析[J].中国儿童保健杂志,2011,19(4):580-583.
[9]金玲凤,刘小伟,卢放根,等.大鼠非酒精性脂肪肝形成过程中肝脏蛋白质组动态变化的研究[J].中国现代医学杂志,2014,24(21): 26-32.
[10]叶春,何执静.长期游泳运动对非酒精性脂肪肝大鼠血清氨基酸谱的影响及分析[J].南京师大学报(自然科学版),2015,38(2):122-127.
[11]NEWGARD C B,AN J,BAIN J R,et al.A branched-chain amino acid-related metabolic signature that differentiates obese and lean humans and contributes to insulin resistance[J].Cell Metab,2009,9(4):311-326.
[12]ZENG T S,LIU F M,ZHOU J,et al.Depletion of kupffer cells attenuates systemic insulin resistance,inflammation and improves liver autophagy in high-fat diet fed mice[J].Endocr J,2015,62(7): 615-626.
[13]王军英,王红梅.非酒精性脂肪肝患者血清TNF-α、IL-6水平及意义[J].中国现代医学杂志,2013,23(33):42-46.
[14]BISWAS SK,CHITTEZHATH M,SHALOVA I N,et al.Macrophage polarization and plasticity in health and disease[J].Immunol Res,2012,53(1/2/3):11-24.
[15]黄海琇.非酒精性脂肪性肝病中Kupffer细胞激活方式的研究[D].杭州:浙江大学,2013.
(申海菊编辑)
中图分类号:R 589.2
文献标识码:A
DOI:10.3969/j.issn.1005-8982.2016.13.005
文章编号:1005-8982(2016)13-0022-06
收稿日期:2015-12-11
*基金项目:四川省卫生厅科研基金(No:120330)
Ketogenic essential amino acid replacement diet ameliorates nonalcoholic fatty liver disease in high-fat diet mice*
Ling Xu1,Hong-yan Ma1,Bin Xiao2,Chen-lin Gao1
(1.Department of Endocrinology,the Affiliated Hospital of Luzhou Medical College,Luzhou,Sichuan 646000,China;2.Department of Biochemistry,College of Basic Medical Sciences,Sichuan Medical University,Luzhou,Sichuan 646000,China)
Abstract:Objective To reveal the effects of ketogenic amino acid(KAA)replacement diet in the high-fat diet-induced nonalcoholic fatty liver disease in mice.Methods C57BL male mice were randomly fed with a conventional diet(NC group),high-fat diet(HFD group)or KAA-fortified HFD(HFDKAAR group);and 8 weeks after HFD initiation,the HFD-fed mice were randomly divided into two groups:one group of mice was fed the same HFD,the other group was fed HFDKAAR(HFD→HFDKAAR).The metabolic status and biochemical evaluations were performed 16 weeks after the initiation of experimental food.Blood glucose was measured by intraperitoneal glucose tolerance test.Insulin levels in plasma were measured using ELISA,the insulin resistance index(IRI)and area under curve(AUC)were calculated.The mesenteric and epididymal fat tissues and liver were weighed.Frozen liver sections were used for evaluation of hepatic steatosis and accumulation of Kupffer cells labeled by f4/80 via Oil Red O staining and immunofluorescence method respectively.The expressions ofTNF-α andIL-1βmRNA were measured by real-time qPCR.Results All the mice ate almost similar calories.Compared to the NC group,the HFD-fed mice displayed significantly heavier body weight and intra-abdominal fat weight,severer hepatic steatosis,deterioration of glucose tolerance,and significantly-enhanced macrophage accumulation in liver;interestingly,these changes were reversed after rich-KAA diet administration.Furthermore,real-time qPCR showed hepaticTNF-α andIL-1β mRNA expressions were up-regulated in the HFD fed mice(P<0.05),these changes were dramatically ameliorated by taking rich-KAA diet(P<0.05).Conclusions Our data demonstrate that rich-KAA diet could significantly ameliorate HFD-induced hepatic steatosis,obesity and glucose intolerance via normalizing the macrophage accumulation.KAA replacement diet could be a potential nutritional intervention for treatment in patients with metabolic defects.
Keywords:amino acid;non-alcoholic fatty liver disease;metabolic syndrome

