纳米多孔Co-Ni-B/Cu-BTC复合材料的制备及其催化水解氨硼烷的研究*
程 军,邹勇进,向翠丽,郑良军,孙立贤,徐 芬,刘淑生
(桂林电子科技大学 广西信息材料重点实验室,材料科学与工程学院,广西 桂林 541004)
纳米多孔Co-Ni-B/Cu-BTC复合材料的制备及其催化水解氨硼烷的研究*
程军,邹勇进,向翠丽,郑良军,孙立贤,徐芬,刘淑生
(桂林电子科技大学 广西信息材料重点实验室,材料科学与工程学院,广西 桂林 541004)
摘要:首次通过化学还原法制备了纳米多孔Co-Ni-B/Cu-BTC复合材料,在Co-Ni-B合金中掺入金属框架化合物Cu-BTC后有效地提高了复合材料的比表面积,其形貌由团聚的纳米粒子变成纳米多孔结构,复合材料的催化性能也得到显著的提高,用于催化氨硼烷的水解,表现出良好的催化活性。在30 ℃时,催化水解氨硼烷制氢的反应速率到达2 670mL/(min·g),其水解反应的活化能为22.4kJ/mol,与文献相比,表现出较大的优势。所制备的复合材料还具有良好的化学稳定性,表现出重要的应用前景。
关键词:Co-Ni-B/Cu-BTC;催化水解;复合材料;氨硼烷
0引言
氢能作为洁净的二次能源,近年来受到广泛的关注。然而,氢的储存与制备技术仍然是制约氢能商业化应用的关键技术。相比于高压气瓶储氢和低温液化储氢,固态材料储氢在操作安全性、能源效率及储氢容量方面均具有显著优势,被认为是最具发展前景的储氢方式。固态储氢材料历经数10年发展,已形成金属氢化物、配位金属氢化物、氨基化合物、物理吸附剂等多个可逆储氢材料分支。但研究表明,已知可逆储氢材料在温和操作温度(<85 ℃)下的储氢容量仅为1%~3%(质量分数),远低于车载氢源的应用需求(≥6.5%(质量分数))。近年来,高容量化学氢化物日渐成为新兴的研究热点,在其带动下,储氢材料领域呈现出可逆/非可逆储氢材料并行发展的研究格局。不同于可逆储氢材料,化学氢化物在完成放氢后,需通过集中式化工过程完成氢化物再生,其分离处理放氢/吸氢环节的技术特点和优异的近室温可控放氢性能为研发实用型移动氢源系统提供了新的广阔研究空间。在众多的化学氢化物储氢材料中,氨硼烷(NH3BH3,AB)水解制氢近年来受到广泛关注,其理论储氢密度可以达到19.6%(质量分数),而且可以在室温条件下实现氢气的可控释放,不会对环境造成污染[1-3]。在一般条件下,氨硼烷易溶于水,纯的氨硼烷在水中也很稳定,实现燃料液于室温条件下的安全贮存,而加入催化剂则可显著加速水解反应。因此,可以通过控制催化剂与氨硼烷燃料液的接触与分离实现即时按需制氢。围绕氨硼烷催化水解可控制氢技术,各国的科研工作者开展了大量研究[4-6]。
但氨硼烷的水解反应受到催化剂的制约,研究表明,Pt、Ru、Rh、Ir、Pd等贵金属及其合金能够有效地催化氨硼烷水解放氢[7]。但贵金属价格昂贵,在地壳中稀少的储量极大限制了其规模化应用。 因此,发展新型非贵金属基催化剂是成为储氢材料研究的重要目标之一。目前,氨硼烷水解的非贵金属催化剂研究主要集中在Co基催化剂上[8]。但所制备的Co基纳米催化剂很容易团聚,降低了催化剂和反应液的接触面积,严重影响了催化剂的活性。氨硼烷水解催化反应为异相催化反应,因此,催化剂的表面积和其催化活性密切相关。为了提高Co基合金的催化活性,文献中报道了多种方法来提高其表面积,过渡金属元素合金化法、模板法、载体法等。但采用金属有机框架化合物来提高Co基合金的催化活性的研究尚未见报道。Cu-BTC因其具有高的比表面积和良好的催化活性而受到广泛关注[9-11],本文首次通过化学还原法在Co基合金中引入金属有机框架化合物Cu-BTC,发现在合金中掺入Cu-BTC后有效地提高了合金的比表面积,其形貌也有团聚的纳米粒子变成多孔的复合材料,有效地提高了复合材料的比表面积,并考察了复合材料对氨硼烷水解的催化特性。
1实验
1.1Co-Ni-B/Cu-BTC复合材料的制备
实验中所用的试剂NaBH4、CoSO4·7H2O、NiSO4·7H2O、CuSO4·5H2O均为分析纯,去离子水配制。Cu-BTC的合成参照文献[12]的方法。取4gCoSO4·7H2O、1gNiSO4·7H2O溶于100mL去离子水中,称取0.1gCu-BTC颗粒加入到上述溶液中,超声分散30min。取2gNaBH4溶于20mL去离子水中,在搅拌的条件下,逐滴滴加到上述溶液中。溶液迅速变黑,并伴有大量的气泡放出。滴加完毕后,让溶液在搅拌的条件下,继续反应1h。 然后,过滤,洗涤,在60 ℃真空干燥。为了便于对比,采用同样方法制备了Co-B、Ni-B、Co-Ni-B、Co-Ni-Cu-B合金,其中在制备Co-Ni-Cu-B合金的过程中CuSO4·5H2O的浓度为 1g/L。
1.2复合材料的性能及表征
样品的表面形貌在日本JEOL6360LV型扫描电镜上观察。粉末样品粘在样品支架上面的导电胶上,样品测试前经镀金处理。样品的表面元素分布及含量由其附带的OxfordX射线能谱仪(EDX)HitachiS4800测定完成。XRD在Philips1820X射线衍射仪上完成,使用铜靶Kα光源(λ=1.5418nm),Ni滤波石墨单色器,管电压为40kV,管电流为40mA。XPS在SCIENTAESCA250型X射线光电子能谱仪上完成。材料的比表面积和孔分布采用氮气物理吸附法进行测定,实验在美国康塔仪器公司生产的Autosorb1型物理吸附仪上进行。测试前将样品在110 ℃抽真空处理3h以上,然后在低于焙烧温度50 ℃的条件下继续抽真空4h以上,使真空度达到1.33×10-3Pa左右。最后在液氮温度(-196 ℃)下进行测试,根据静态法测量吸附-脱附等温线(BET)。
1.3复合材料的表征
采用排水法收集水解产生的气体,实验装置图如图1所示,称取0.05gCo-Ni-B/Cu-BTC的催化剂,将其置于广口瓶中,然后将瓶子用橡皮塞密封,称取0.15gNH3BH3溶于10mL的水溶液中,用注射器吸取溶液,注入广口瓶中,此时通过记录单位时间内排出的水的量测定水解的速度。在测试催化剂的稳定性时,待NH3BH3水解完全后,将催化剂过滤,洗涤并重复使用,测试NH3BH3的水解反应速率。
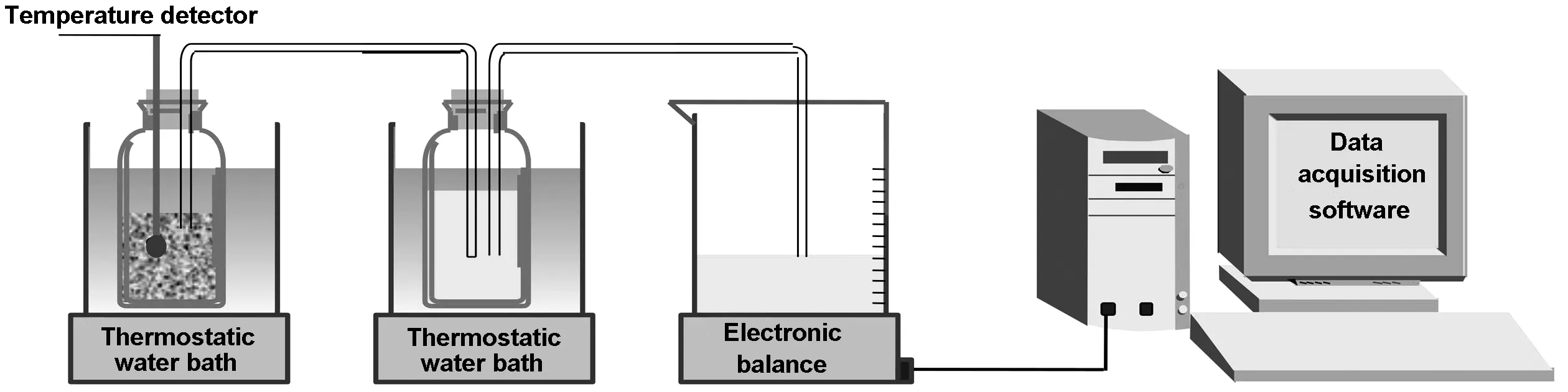
图1 Co-Ni-B/Cu-BTC催化水解NH3BH3的装置示意图
Fig1SchematicdiagramofthehydrogengenerationsystembyhydrolysisofNH3BH3withCo-Ni-B/Cu-BTCpowdercatalysts
2结果与讨论
2.1催化剂表征
2.1.1扫描电镜及能谱分析
图2分别为Co-Ni-B、Co-Ni-Cu-B、Co-Ni-B/Cu-BTC的电镜照片和EDX图谱。从图2可以看出,在超声化学还原的条件下Co-Ni-B和Co-Ni-Cu-B合金均为团聚的纳米颗粒,而在溶液中分散Cu-BTC纳米粒子后,得到了多孔的蜂窝状结构的复合材料,孔径的大小均匀,这有可能是由于Cu-BTC的掺入,改变了Co-Ni-B合金的成核的过程,从而形成了大量的蜂窝状结构的复合材料。大多数过渡金属盐可以在还原剂的作用下,形成具有催化作用非晶合金结构,通常用作催化剂的金属主要以Co、Ni为主。但传统方法所制备的Co基纳米催化剂很容易团聚,降低催化剂和反应液的接触面积,严重影响了催化剂的活性[8]。本文通过纳米Cu-BTC粒子的诱导,在水溶液中合成纳米多孔Co-Ni-B/Cu-BTC复合材料。EDX分析显示,多孔材料主要由Co、Ni、Cu、C、O几种元素组成,这4种元素的含量分别为53.49%,14.84%,1.27%,19.45%和10.95%。其中样品中氧的存在可能是由于在样品处理的过程中发生了部分氧化造成的[13]。
2.1.2物理吸附及XRD分析
为了考察复合材料的比表面积和孔径分布性质,测试了复合材料的氮气物理吸附实验,如图3所示。实验结果表明,Cu-BTC的比表面为1 247m2/g,这和文献报道的结果接近[12]。Co-Ni-B/Cu-BTC的BET表面积和孔容分别为339m2/g和0.185cm3/g,而未经掺杂的Co-Ni-B的BET表面积和孔容分别为335m2/g和0.005cm3/g,这表明掺杂了Cu-BTC后,复合材料的比表面积有所提高,而且掺杂后孔容显著增大,提高了37倍。同时复合材料孔径分布从20nm增大到25nm。为了提高非晶Co基合金的比表面积,文献通常采用的方法是在合金中引入过渡金属元素或掺与其它纳米载体材料[14],本文首次采用纳米Cu-BTC颗粒的诱导下制得了多孔Co-Ni-B/Cu-BTC复合材料,这些多孔结构有效的提高了材料的比表面积,增大了催化剂和溶液的接触面积,可能会有效地提高催化剂的催化活性。

图2 复合材料的扫描电镜照片
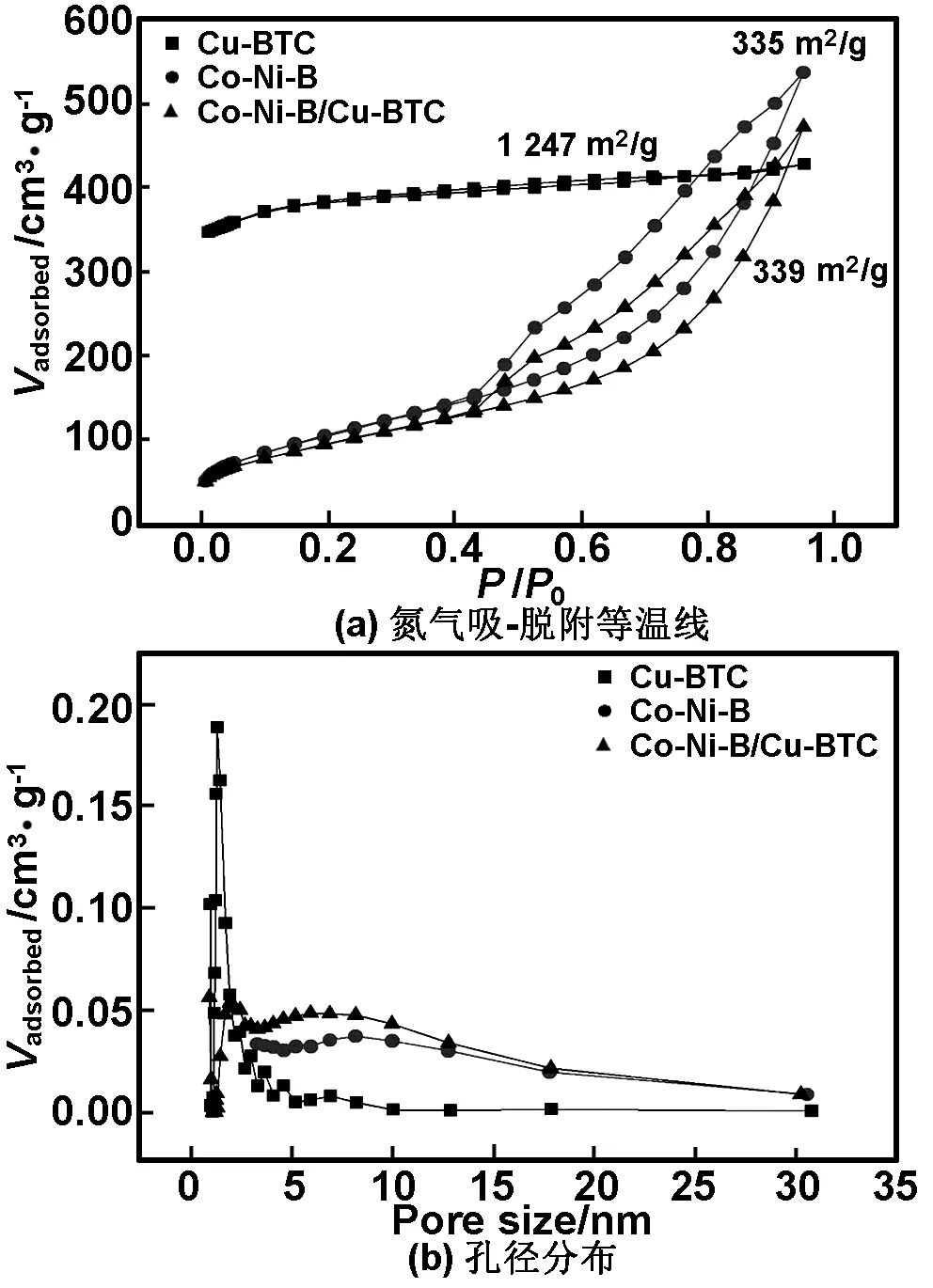
图3复合材料在77K时的氮气吸脱附等温线及孔径分布
Fig3N2adsorptionanddesorptionisothermat77Kofthecompositematerialsandporedistribution
图4为Cu-BTC、Co-Ni-B、Co-Ni-B/Cu-BTC的XRD图谱。从图4看出,Cu-BTC纳米颗粒在XRD图谱上表现出特有的特征峰[12]。Co-B基合金通常表现出非晶的性质,而本文制备的Co-Ni-B和Co-Ni-B/Cu-BTC合金在40°左右出现一个较强的宽化峰,这有可能是Co-Ni-B和Co-Ni-B/Cu-BTC发生部分晶化造成的。而在Co-Ni-B/Cu-BTC的XRD图谱中,没有发现Cu-BTC的特征峰,这是由于Cu-BTC在被Co-Ni-B包覆的过程中,发生了水解,从而使其在复合材料中的含量减少,Co-Ni-B较强的非晶衍射峰掩盖Cu-BTC的特征吸收峰。
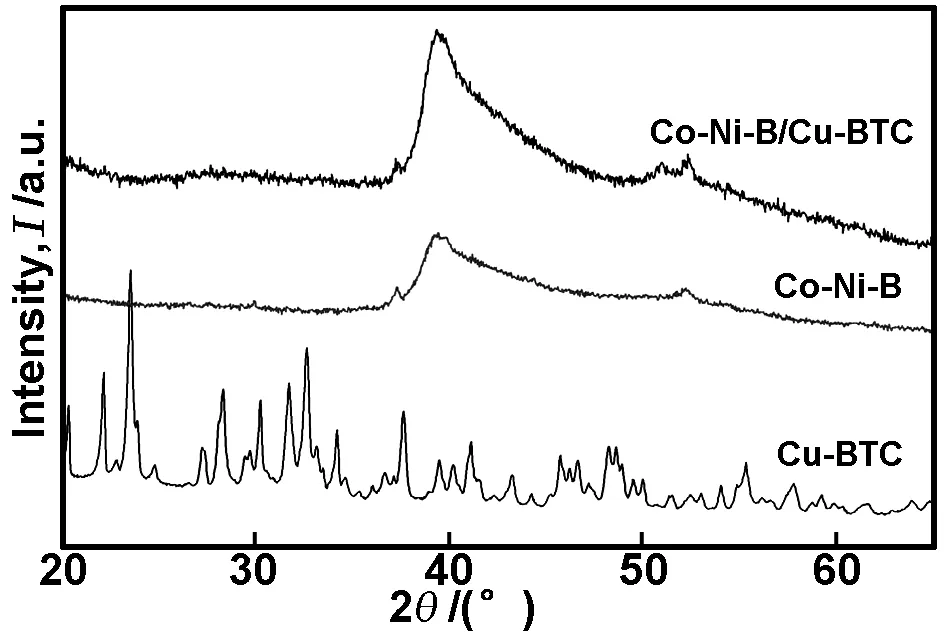
图4 Co-Ni-B/Cu-BTC复合材料的XRD图谱
Fig4XRDpatternsofCo-Ni-B/Cu-BTCcompositematerial
2.1.3XPS分析
为了进一步分析复合材料中Cu的电子状态,对Co-Ni-B/Cu-BTC和Co-Ni-Cu-B进行了XPS分析。如图5(a)所示, 在Co-Ni-B/Cu-BTC复合材料中,对Cu2p3/2去卷积后发现,在934.2eV的峰为Cu0的特征峰,表明Cu-BTC在溶液中发生水解并被还原,同时在937.1,942.5,946.1eV为Cu2+的特征峰, 其中在937.1eV特征峰可归因于Cu-BTC中的Cu—O的键合[10],这表明复合材料中还有部分Cu-BTC未发生分解,而在Co-Ni-Cu-B合金中只检测到Cu0的特征峰(图5(b))。
2.2催化剂性能测试
图6(a)为在30 ℃,0.05g的不同催化剂催化水解0.75%的NH3BH3水溶液的放氢曲线。
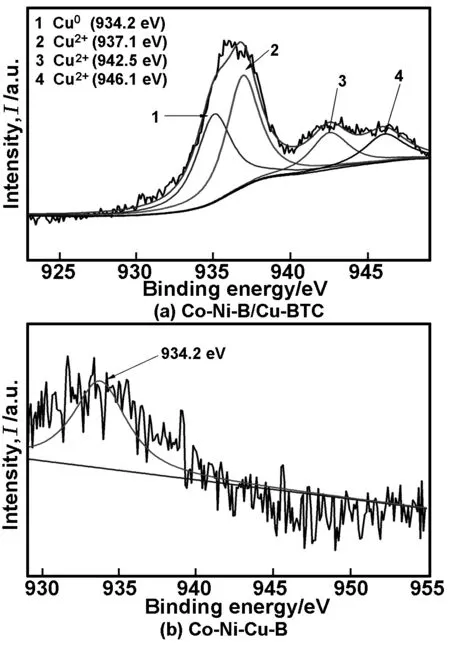
图5Co-Ni-B/Cu-BTC和Co-Ni-Cu-B的Cu2p3/2XPS图谱
Fig5Cu2p3/2XPSspectraofCo-Ni-B/Cu-BTCandCo-Ni-Cu-B
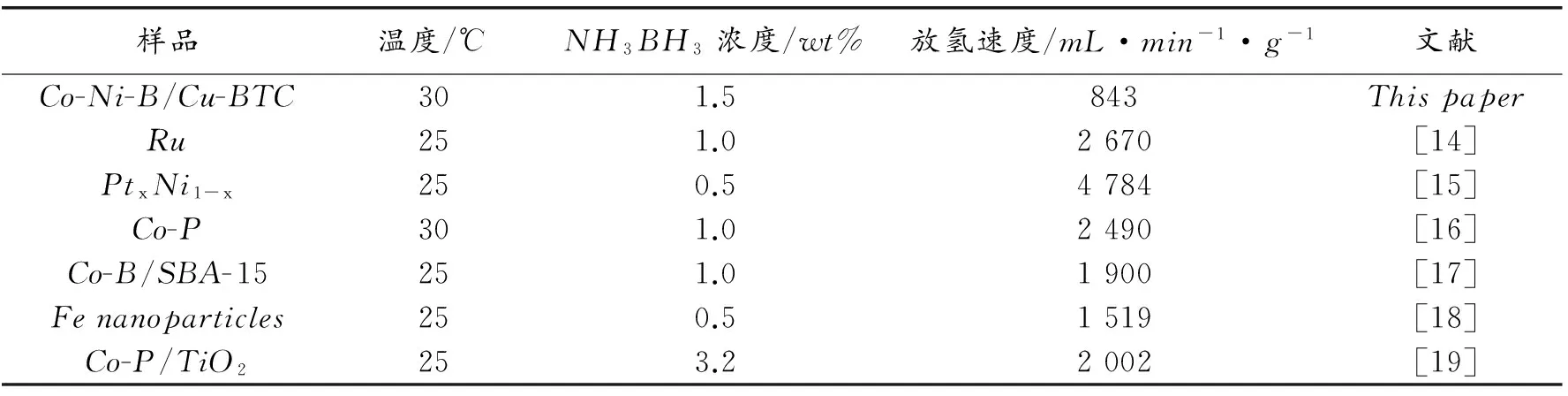
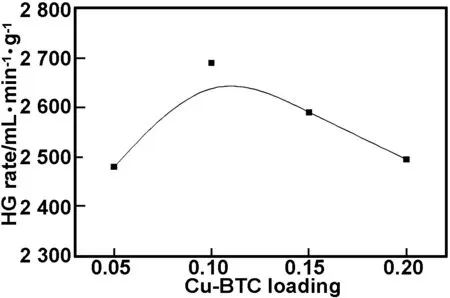
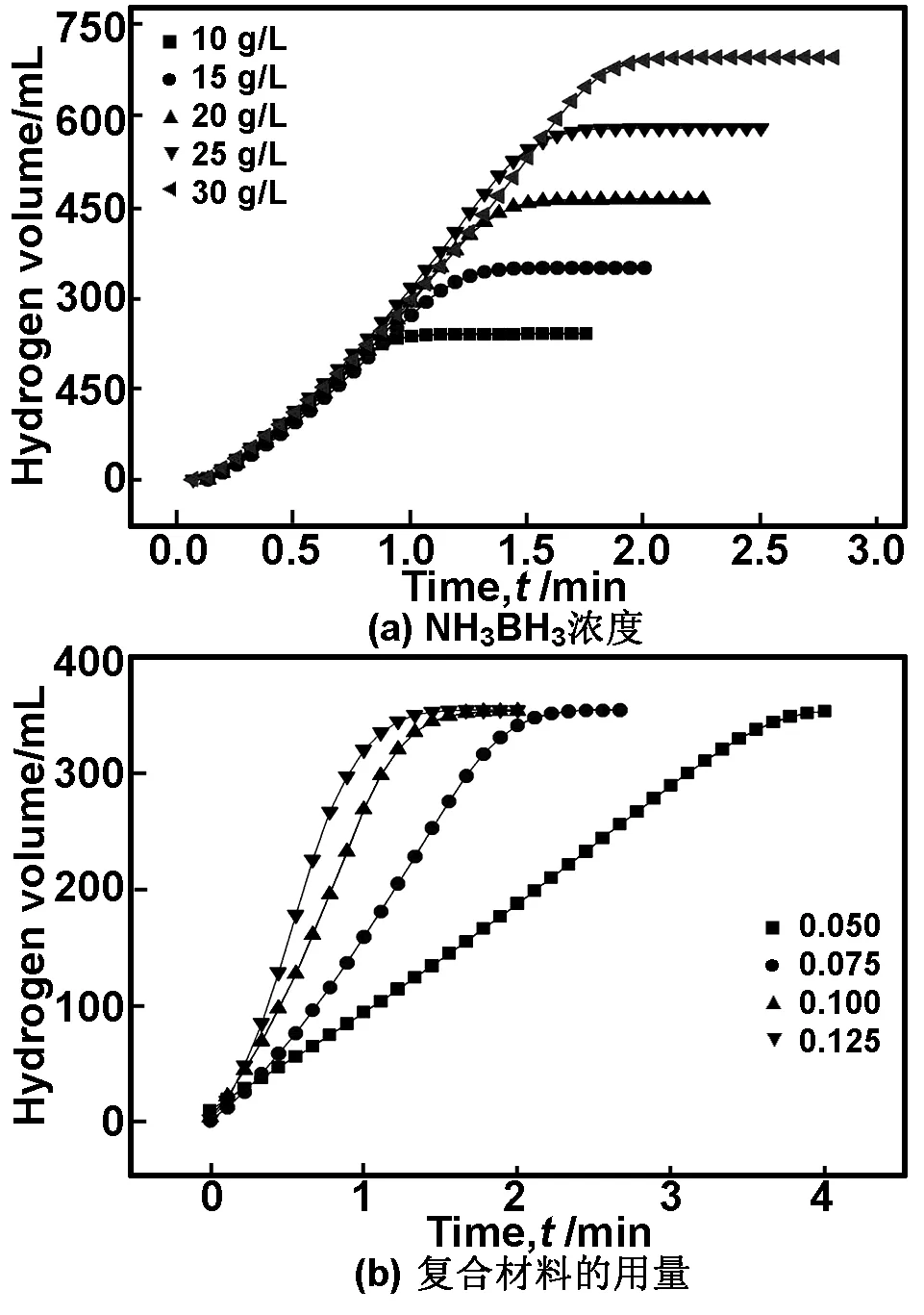
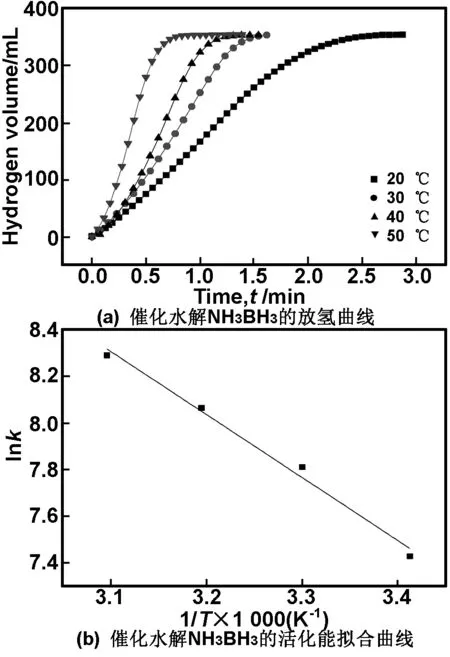
从图6(a)可以看出,水解放氢量随着水解时间增加而成线性的增加,几乎不需要诱导时间。根据放氢曲线的斜率可以计算出催化剂催化NH3BH3水解速度的平均速率。其催化水解反应速率按照Ni-B 图6Co-Ni-B/Cu-BTC复合材料的水解NH3BH3放氢曲线和Co-Ni-B/Cu-BTC和Ni-Co-Cu-B合金的催化水解NH3BH3的放氢性能比较 Fig6HydrogengenerationyieldasafunctionofreactiontimeobtainedbyhydrolysisofNH3BH3withCo-Ni-B/Cu-BTCcatalystsandcomparisonofcatalyticactivityforCo-Ni-B/Cu-BTCandNi-Co-Cu-BbyhydrolysisofNH3BH3 表1列举了文献所报道的催化剂的水解NH3BH3放氢速度与本文的比较。从表1可以看出,所制备的纳米多孔Co-Ni-B/Cu-BTC复合材料的催化水解NH3BH3放氢速度低于PtxNi1-x合金,远高于采用非贵金属催化剂以及贵金属Ru。这可能是由于Co-Ni-B和Cu-BTC的协同催化作用以及其独特的多孔结构的原因,从而使催化反应活性显著增加。 表1 制备的催化剂的水解NH3BH3最大放氢速度与文献比较 由上可知,Cu-BTC颗粒直接影响了Co-Ni-B的表面形貌,并提高了Co-Ni-B的催化活性。为此研究了Cu-BTC掺杂量对其催化水解NH3BH3放氢速率的影响。从图7可以看出,随着Cu-BTC掺杂量的增加,水解反应活性逐渐增加,当掺杂量达到0.1g时,反应速度达到最大。而且随着复合物材料中Cu-BTC含量增大后,对材料的形貌、结构(XRD)进一步分析发现,其形貌和结构没有发现明显的变化。当掺杂量进一步增大时,水解反应速度降低。这可能是由于适量的Cu-BTC添加可以提高其催化活性,当用量过大,催化活性反而下降。因此,本文在制备Co-Ni-B/Cu-BTC复合材料时,Cu-BTC的用量选为0.1g。 图7Cu-BTC的掺入量对水解NH3BH3放氢速率的影响 Fig7TheeffectofCu-BTCamountonthehydrogengenerationratebyhydrolysisofNH3BH3 图8(a)为不同NH3BH3浓度下,复合材料催化剂催化NH3BH3水解的放氢曲线,从图8(a)可以看出,随着NH3BH3浓度的增加,其产氢速率几乎没有变化,只是其产氢量成倍的增加,进一步的说明了NH3BH3的水解反应相对于催化剂来讲为零级反应。图8(b)为复合材料Co-Ni-B/Cu-BTC的用量对其催化NH3BH3水解的放氢速率的影响曲线,从图8(b)可以看出,随着复合材料用量的不断增加,其产氢速率也随之加快,相对于催化剂,表现出一级反应的特征,这和文献[13]的报道也是一致的。 图8NH3BH3浓度对复合材料的催化水解NH3BH3放氢速率以及复合材料的用量对水解NH3BH3放氢速率的影响 Fig8TheeffectofNH3BH3concentrationandtheamountofcatalystonthehydrogengenerationratebyhydrolysisofNH3BH3 2.3水解反应活化能 图9(a)为Co-Ni-B/Cu-BTC催化剂在不同温度下催化水解NH3BH3的放氢曲线。从图9(a)可以看出,随着温度的升高,放氢速度明显加快。由上可知,NH3BH3的水解反应为零级反应[13],根据一级反应速率方程 可以拟合计算得到催化水解反应的活化能为22.4kJ/mol(图9(b))。本文所计算的活化能与文献报道的NH3BH3水解用催化剂Co-W-B/Nifoam(29kJ/mol)[20],nanoporousnickelspheres((27±1)kJ/mol)[21]所得到的活化能都要低。比文献报道的Co-B/SBA-15 ((43±2)kJ/mol)[17],Ru@SiO2(38.2kJ/mol)[22]和Ni0.99Pt0.01(49.27kJ/mol)[23]要低得多。这进一步说明所制备的多孔Co-Ni-B/Cu-BTC纳米复合材料具有优良的催化性能。 图9多孔Co-Ni-B/Cu-BTC复合材料在不同温度下催化水解NH3BH3的放氢曲线及活化能拟合曲线 Fig9HydrogengenerationyieldasafunctionoftimeobtainedbyhydrolysisofNH3BH3withcompositeCo-Ni-B/Cu-BTCcatalystsatdifferenttemperaturesandcalibrationcurveofactivationenergy 2.4催化剂稳定性 为了进一步考察了催化剂水解反应的稳定性,考查了催化剂在循环使用后的水解反应速度。在催化剂循环使用了10次后,其水解反应速度由2 670mL/min·g降低至1 820mL/min·g,水解反应速度降低了约31.8%左右。而文献报道的合金催化剂Co-W-B-P/Ni在循环了10次后,催化活性降低了32%[12],这与文献报道的结果相当,表明所制备的催化剂具有良好的稳定性。 3结论 在采用化学还原方法制备了Co-Ni-B/Cu-BTC纳米合金材料,在纳米Cu-BTC颗粒的诱导下,Co-Ni-B/Cu-BTC形成纳米多孔结构,用于NH3BH3水解的催化剂,表现出良好的催化活性和稳定性,其水解反应速率较Co-Ni-B有显著提高,达到2 670mL/min·g,其水解反应的活化能为22.4kJ/mol。由于催化剂的制备简单且原料来源广泛,因此具有良好的应用前景。 参考文献: [1]BasuS,BrockmanA,GagareP,etal.ChemicalkineticsofRu-catalyzedammoniaboranehydrolysis[J].JPowerSources,2009, 188:238-243. [2]TetsuoU,YanJ,ZhangX,etal.HollowNi-SiO2nanosphere-catalyzedhydrolyticdehydrogenationofammoniaboraneforchemicalhydrogenstorage[J].JPowerSources,2009, 191: 209-216. [3]PatelN,FernandesR,GuellaG,etal.Amorphouscobalt-boron/nickelfoamasaneffectivecatalystforhydrogengenerationfromalkalinesodiumborohydridesolution[J].ApplCatalB:Environ,2010, 95:137-143. [4]DemirciUB,BernardS,ChiriacR,etal.HydrogenreleasebythermolysisofammoniaboraneNH3BH3andthenhydrolysisofitsby-product[BNHx][J].JPowerSources, 2011, 193: 279-286. [5]OzgurO,ErkI,NahitA,etal.HydrogenproductionfromammoniaboraneviahydrogeltemplatesynthesizedCu,Ni,Cocomposites[J].ScienceDirect, 2011, 36:8209-8216. [6]PatelN,FernandesR,EdlaR,etal.SuperiorhydrogenproductionratebycatalytichydrolysisofammoniaboraneusingCo-Bnanoparticlessupportedovermesoporoussilicaparticles[J].CatalCommun, 2012, 23:39-42. [7]SinghSK,IizukaY,XuQ.Nickel-palladiumnanoparticlecatalyzedhydrogengenerationfromhydroushydrazineforchemicalhydrogenstorage[J].IntJHydrogenEnergy,2011, 36:11794-11801. [8]ChoKW,KwonHS.EffectsofelectrodepositedCoandCo-Pcatalystsonthehydrogengenerationpropertiesfromhydrolysisofalkalinesodiumborohydridesolution[J].CatalToday, 2007, 120:298-304. [9]WangCY,GongQ,ZhaoY,etal.Stabilityandhydrogenadsorptionofmetal-organicframeworkspreparedviadifferentcatalystdopingmethods[J].JCatal, 2014, 318:128-142. [10]ZukalaB,OpanasenkoM,RubesM,etal.Adsorptionofpentaneisomersonmetal-organicframeworksCu-BTCandFe-BTC[J].CatalToday, 2015, 243:69-75. [11]SunZ,LiG,ZhangY,etal.Ag-Cu-BTCpreparedbypostsyntheticexchangeaseffectivecatalystforselectiveoxidationoftoluenetobenzaldehyde[J].CatalCommun, 2015, 59:92-96. [12]ChowdhuryP,BikkinaC,MeisterD,etal.ComparisonofadsorptionisothermsonCu-BTCmetalorganicframeworkssynthesizedfromdifferentroutes[J].MicroporousMesoporousMater, 2009, 117:406-413. [13]XiangC,ChengJ,SheZ,etal.FabricationandcharacterizationofanovelnanoporousCo-Ni-W-Bcatalystforrapidhydrogengeneration[J].RSCAdv, 2015, 5:163-166. [14]PatelN,MiotelloA.ProgressinCo-Brelatedcatalystforhydrogenproductionbyhydrolysisofboron-hydrides:areviewandtheperspectivestosubstitutenoblemetals[J].IntJHydrogenEnergy, 2015, 40:1429-1464. [15]YangX,ChengF,LiangJ,etal.PtxNi1-xnanoparticlesascatalystsforhydrogengenerationfromhydrolysisofammoniaborane[J].IntJHydrogenEnergy, 2009, 34:8785-8791. [16]EomK,ChoK,KwonH.HydrogengenerationfromhydrolysisofNH3BH3byanelectroplatedCo-Pcatalyst[J].IntJHydrogenEnergy, 2010,35:181-186. [17]PatelN,FernandesR,GuptaS,etal.Co-Bcatalystsupportedovermesoporoussilicaforhydrogenproductionbycatalytichydrolysisofammoniaborane:astudyoninfluenceofporestructure[J].ApplCatalB:Environ, 2013, 140:125-132. [18]YanJ,ZhangX,HanS,etal.Iron-nanoparticle-catalyzedhydrolyticdehydrogenationofammoniaboraneforchemicalhydrogenstorage[J].AngewChemIntEd,2008, 47: 2287-2289. [19]RakapM.Hydrogengenerationfromthehydrolyticdehydrogenationofammoniaboraneusingelectrolesslydepositedcobalt-phosphorusasreusableandcost-effectivecatalyst[J].JPowerSources,2014, 265:50-56. [20]YangJ,ChengF,LiangJ,etal.Hydrogengenerationbyhydrolysisofammoniaboranewithananoporouscobalt-tungsten-boron-phosphoruscatalystsupportedonNifoam[J].IntJHydrogenEnergy, 2011, 36:1411-1417. [21]CaoCY,ChenCQ,LiW,etal.Nanoporousnickelspheresashighlyactivecatalystforhydrogengenerationfromammoniaborane[J].ChemSusChem,2010, 3:1241-1244. [22]YaoQ,ShiW,FengG,etal.UltrafineRunanoparticlesembeddedinSiO2nanospheres:highlyefficientcatalystsforhydrolyticdehydrogenationofammoniaborane[J].JPowerSources, 2014, 53:257- 263. [23]DuJ,ChengF,SiM,etal.NanoporousNi-basedcatalystsforhydrogengenerationfromhydrolysisofammoniaborane[J].IntJHydrogenEnergy, 2013, 38:5768-5774. PreparationofnanoporousCo-Ni-B/Cu-BTCcompositeanditsapplicationforcatalyzingthehydrolysisofNH3BH3 CHENGJun,ZOUYongjin,XIANGCuili,ZHENGLiangjun,SUNLixian,XUFen,LIUShusheng (GuangxiKeyLaboratoryofInformationMaterials,GuilinUniversityofElectronicTechnology,Guilin541004,China) Abstract:Inthispaper,nanoporousCo-Ni-B/Cu-BTCcatalysthasbeenfirstlypreparedbyin-situchemicalreductionundersonication.AftertheintroductionofCu-BTCparticlesinCo-Ni-Balloy,thespecificsurfaceareaofthecompositewassubstantiallyimproved.Themorphologywasalsochangedfromaggregatednanoparticlestonanoporousstructure.Furthermore,thecatalyticactivityofcompositewasenhancedgreatlyforthehydrolysisofNH3BH3.Ahighrateofhydrogengenerationhasbeenmonitoredat2 670mL/(min·g)at30 ℃inNH3BH3solution.Theactivationenergyofthehydrolysis22.4kJ/molisobtained.Thepreparationofcompositehasgoodchemicalstabilityandhasalsobeenexplored. Keywords:Co-Ni-B/Cu-BTC;catalytichydrolysis;compositecatalyst;NH3BH3 文章编号:1001-9731(2016)06-06152-06 * 基金项目:国家自然科学基金资助项目(51461011, 51201041, 51201042, 51361005, 51371060);广西自然科学基金资助项目(2013GXNSFCA019006, 2013GXNSFBA019243, 2014GXNSFAA118318, 2012GXNSFGA060002);广西研究生教育创新计划资助项目(YCSZ2015153) 作者简介:程军(1988-),男,河南信阳人,硕士,师承邹勇进教授,从事纳米金属功能材料研究。 中图分类号:TQ423 文献标识码:A DOI:10.3969/j.issn.1001-9731.2016.06.027 收到初稿日期:2015-07-13 收到修改稿日期:2015-09-21 通讯作者:邹勇进,E-mail:zouy@guet.edu.cn