借鉴经典改进实验,重构观念突出方法
摘要:在教学设计及实施中,依托化学史,根据逐步递进的演示实验链提出假设及问题链,激发学生思考、交流讨论,帮助学生在现代科技前沿与经典实验赏析、课堂实验探究的反思对比、分析归纳过程中完成守恒观的构建,形成科学研究方法的初步认识。
关键词:经典;实验;观念;方法;化学反应;质量关系
文章编号:1008-0546(2016)08-0076-03 中图分类号:G633.8 文献标识码:B
doi:10.3969/j.issn.1008-0546.2016.08.025
“质量守恒定律”[1]是初中化学教学中的一个非常重要的定律,蕴含着丰富的化学发展史及科学方法的教育价值。宋心琦教授认为,中学化学教学能够使学生终身受益的,不是具体的化学专业知识,而是影响他们世界观、人生观和价值观的化学思想观念,不是诸如分类、实验、计算等特殊的方法和技能,而是影响他们思维方式和问题解决能力的具有化学特点的认识论和方法论。学生能否牢固地、准确地、哪怕只是定性地建立起基本的化学观念应当是中学化学教学的第一目标[2]。为此,笔者去年11月在苏州市初中课改展示活动上开设了有关“质量守恒定律”的研讨课,并于今年2月在江苏省教学新时空“名师讲堂”进行展播。以下是笔者对这节课的回顾与思考。
一、教学目标设计
1. 素材地位
“化学反应中的质量关系”的核心内容是质量守恒定律,它是分析物质在化学反应中的质量关系的理论依据,它的应用贯穿于整个中学化学。从质量及其变化角度对物质进行研究,不但是化学研究的重要方法,也是化学学习的重要方法。
纵观化学史,质量守恒定律是18世纪科学发展史上最辉煌的成就之一,它的发现经历了百年风霜,浸透了数位科学家前赴后继的努力,不仅是科学家们智慧的结晶,也体现了科学家们的坚持不懈的科学精神,它的发现史就是一场革命史。化学史的内容在很大程度上反映了科学家的探究活动与方法,可以作为学生理解科学探究、掌握科学方法的范例。
2. 目标定位
(1)知识与技能
①认识质量守恒定律;
②从微观角度理解质量守恒定律的内涵,能运用质量守恒定律解释常见化学反应的质量关系。
(2)过程与方法
①实验探究化学反应前后的质量关系,尝试应用定量方法来研究问题和分析问题的实验方法,感受设计科学实验的一般步骤和方法;
②通过运用比较、分析、归纳、概括等方法来感受由感性到理性、由个别到一般的研究问题的科学归纳方法。
(3)情感态度与价值观
①通过对比太空轨道舱与地球实验室称量物质质量方法的差异,并借助课堂演示实验,认识科学结论要靠大量的实验加以验证的科学思维品质;
②通过质量守恒定律的发现史认识定量研究对于化学科学发展的重要作用。
3. 教学重点
质量守恒定律概念的建立,质量守恒定律的理解及科学思想方法的构建。
4. 教学方法
笔者在课堂科学探究教学中设计实施了递进式“演示实验链”,并由此创设了对应的“问题链”,激发学生的思维冲突和开展热烈讨论;让学生在欣赏当今太空失重实验与近代经典化学实验的对比、分析过程中,构建物质守恒观和了解科学归纳法。
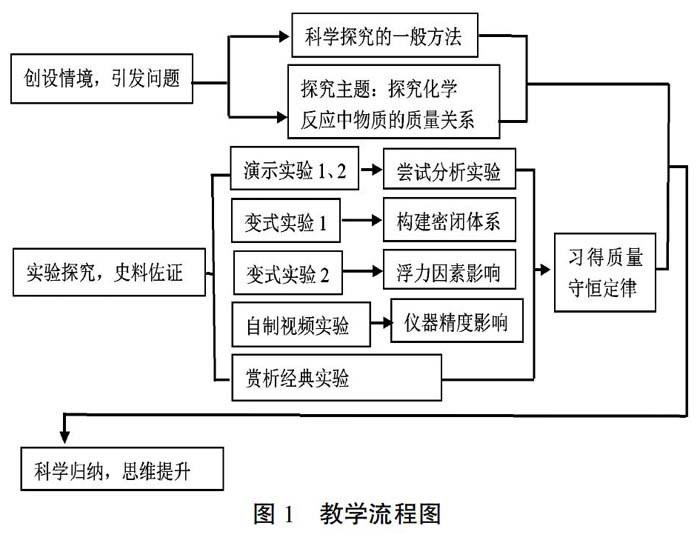
二、教学流程
这节课主要有“创设情境,引发问题”“实验探究,史料佐证”“科学归纳,思维提升”三大教学环节。
三、教学过程回放
1. 创设情境,引发问题
【视频引入】2013年著名宇航员王亚萍的“太空课堂”节选:太空称重。
【视频引入意图】 表面上看这是一个简单的称重实验,但其中蕴含着丰富的科学道理,当环境由地球实验室扩展到太空中“天宫一号”时,科学实验的原理就由地球重力环境下的托盘天平的杠杆原理变化为“牛顿第二定律”,实验步骤及选用的仪器也随之改变:太空“质量测量仪”通过弹簧产生力并测出力的加速度,再算出质量。以此启发学生得出进行任何一项科学实验的一般方法:明确研究的目标及对象;考虑科学实验的环境因素;确定与探究思路相关的原理及步骤;选取适当的仪器设备。
2. 实验探究,史料佐证
这节课最重要的环节是通过5个演示实验、视频实验、经典实验赏析形成的实验链及相关问题链组成的。
(1)敞口容器实验
【演示实验1】[3]硫酸铜溶液和氢氧化钠溶液反应前后质量的测定
实验仪器:锥形瓶(盛放氢氧化钠溶液)、(盛放硫酸铜溶液)、电子天平(精度0.1g)。
实验步骤:
①用精度为0.1g的电子天平称量敞口盛放氢氧化钠溶液的锥形瓶和盛放硫酸铜溶液的试剂瓶,天平示数为m1(即为反应前物质总质量)。
②将硫酸铜溶液滴入装有氢氧化钠溶液的锥形瓶中,天平示数仍为m1(即为反应后物质总质量)。
实验现象:锥形瓶中有蓝色絮状沉淀产生,天平示数不变。
结论:该实验中m(总物质)反应前 = m(总物质)反应后
【演示实验2】[3]石灰石与稀盐酸反应前后质量的测定
实验仪器:锥形瓶(装少量石灰石)、试剂瓶(稀盐酸)、电子天平(精度0.1g)。
实验步骤:
①用精度为0.1g的电子天平称量敞口盛放少量石灰石的锥形瓶和盛放稀盐酸的试剂瓶,天平示数为m2(即为反应前物质总质量)。
②将稀盐酸滴入装有少量石灰石的锥形瓶中,待不再产生气体时称量整套装置,天平示数为m3(即为反应后物质总质量)。
实验现象:锥形瓶中有大量气泡冒出,m2 > m3。
【设问1】 m(总物质)反应前 与m(总物质)反应后不等吗?
注:托盘天平的使用在小学六年级科学课上及初二物理课上都学习过,不作为本节课的教学内容,为了提高课堂效率,我采用了学生日常熟悉的电子天平,特别标注天平的精度为0.1g。
【设问2】根据这两个实验得出相反的结论。你对化学反应前后质量关系有什么猜想?以上两个实验能否证明我们的想法?
【讨论】根据“演示实验1”得出反应前物质的总质量等于反应后物质的总质量,分析“演示实验2”中反应后质量减小的原因,并提出要在密闭装置中进行实验探究的改进方法。
【设问3】“演示实验2”中反应前后质量不等的原因是什么?你能否对实验装置进行改进而达到预期实验目标?
学生讨论后,提出改进方案,教师选取其中方案,让学生上台演示如下实验。
(2)“刚性”密闭容器实验
【变式实验1】变敞开反应容器为密闭刚性容器实验。
实验仪器:带盖塑料瓶(装少量石灰石)、小试管(内装稀盐酸)、棉线、电子天平(精度0.1g)。
实验步骤:
①将内装少量稀盐酸的小试管放入塑料瓶中,试管口用棉线悬于塑料瓶外。
②用精度为0.1g的电子天平称量整套装置的质量,天平示数为m4。
③将棉线放入塑料瓶中,旋紧瓶盖,倾斜塑料瓶,稀盐酸流入瓶中,待不再冒出气泡后再次称量整套装置的质量。天平示数仍为m4,即为反应后物质总质量。
④打开瓶盖再次称量整套装置的质量,天平示数为m5。
实验现象:盐酸流入塑料瓶中,有气泡冒出,由于瓶盖的作用,未有气体散逸至空气中。前两次称量读数相等。打开瓶盖,听到“呲”的一声,气体扩散,天平示数m4>m5。
结论:①该实验中m(总物质)反应前 = m(总物质)反应后;
②“演示实验2”中反应后质量减轻的原因是气体生成物散逸到空气中。
(3)“弹性”密闭容器实验
【变式实验2】变“刚性”密闭容器为“弹性”密闭容器实验。
实验仪器:锥形瓶(装少量石灰石)、小试管(内装稀盐酸)、小气球、电子天平(精度0.1g)。
实验步骤:
①将内装少量稀盐酸的小试管放入锥形瓶中,用小气球套住锥形瓶口,形成密闭容器。
②用精度为0.1g的电子天平称量整套装置的质量,天平示数为m6。
③倾斜锥形瓶,稀盐酸流入瓶中。
④将装置放在电子天平上不断读数。
实验现象:锥形瓶内有气泡冒出,小气球不断胀大,天平示数不断减小。
【设问4】 改进方案的变式实验也是密闭装置,天平示数为何随着气球的胀大而减小呢?(引出气体浮力因素影响质量测量问题。)
(4)自制“视频”实验
【视频播放】“白磷燃烧”前后质量变化的实验(课前本人在实验室做的实验录像)。
[视频片段1]在盛有少量细沙的锥形瓶里加入一小块白磷,在酒精灯上加热玻璃棒,用玻璃棒引燃白磷,用精度为0.1g的电子天平称量白磷在敞口的锥形瓶中燃烧前后整个装置的质量。发现:白磷燃烧前后天平示数相等。
【设问5】敞口装置,有大量白烟冲出,天平称量后仍然相等,为什么?
[视频片段2]在盛有少量细沙的锥形瓶里加入一小块白磷,在酒精灯上加热玻璃棒,用玻璃棒引燃白磷,用精度为0.01g的电子天平称量白磷在敞口的锥形瓶中燃烧前后整个装置的质量。发现:白磷燃烧后天平示数先减小,冷却后,天平示数增加。
【设问6】换用精度0.01g的电子天平,天平示数先减小,待锥形瓶冷却后,示数又增大为什么?
【PPT图片定格】两次实验用的电子天平的精度画面。
【讨论】天平精度对称量实验的影响。
【过渡】 历史上化学家们是怎样研究这个问题的呢?
(5)教材经典实验
【赏析经典】教师带领学生对教材中有关“拉瓦锡测定空气组成实验”进行阅读赏析:这个实验可谓是一箭三雕。第一,验证了空气是混合物;第二,提出了氧化学说;第三,定量证明了质量守恒定律。这个实验值得品味的地方很多,我们着重来看两个方面。一个是化学体系的选择、二是实验装置的设计。
科学家的严谨使他们眼睛里容不得半点瑕疵,而拉瓦锡时代的工具和技术(小于0.2%的质量变化就觉察不出来)不能满足严格的要求。直到20世纪初,德国、英国化学家分别进行了精密度极高的实验(0.0001g),可检测到质量变化的万分之一克,这个差别在实验误差范围之内。至此,科学家一致承认了这一定律。
【诵读经典】 这是在学生经历了若干个课堂实验及化学史学习后的诵读,学生的体会一定是丰满的,思维也一定是多角度的,既是学生思维整理阶段也可以从中得以提升。
3. 科学归纳,思维提升
【学生活动】阅读书本、观察图片,寻找质量守恒定律的微观解释。
[结束语]原子、分子从假说到理论的发展过程,都是在科学实验事实的“逼迫”下,不断修正的历史的过程。科学需要大胆甚至疯狂的猜想,不过再疯狂的科学猜想最终都须通过科学实证的检验。猜想与实证是科学进步的一对翅膀……
【视频播放】《与霍金一起了解宇宙》的片头。
四、教后总结
通过这节课,笔者将化学实验与化学史中经典实验案例结合,试图使学生理解质量守恒定律的内涵,感受设计科学实验的一般步骤和方法,认识定量研究对于化学科学发展的重要作用,从而达到构建元素观、守恒观和学习、了解科学归纳法的目的。
质量守恒定律是在大量科学实验的基础上抽象和概括出的所有化学反应遵循的规律,课堂教学中突出实验教学是重中之重。笔者灵活运用教材中的演示实验,改进实验的呈现方式,增设了创新实验。不同条件下的化学变化称量实例多次营造了认知冲突,不断激发学生浓厚的学习兴趣和探究的动力。如:同样在敞口锥形瓶中完成的两个演示实验,称量结果“不变”与“变轻”首次引发学生对如何定量研究化学变化进行思考;由刚性与弹性密闭容器对比形成质量的差异,让学生认知浮力因素带来的微妙刺激;“白磷燃烧”的视频实验再次形成悬念,使学生首次体会到称量仪器的精度对定量化学实验的影响和意义。以上三组课堂实验都以反常的现象和结果使课堂高潮迭起,达到“激疑”“激趣”“激情”[3]进而“诱思”的教学效果。
在教学策略的设计上,以突出学科观念和科学方法的构建为主线,大胆打破课堂时间和空间的局限,让学生充分感受化学学科的魅力。笔者先由太空称重与地面称重的对比,将学生的兴趣迅即调动起来,自然地引入本节课的课题。再创设多种不同情境下的化学变化称量实例,让学生初步体验科学探究的过程。接着引导学生对拉瓦锡经典实验的赏析→化学史的引入→方法归纳,最终以霍金探索宇宙奥秘的短片结束,巧妙地呼应了课的开场。质量守恒定律的概念及应用在教学中固然重要,但是其中隐藏的学科思想方法更加重要,也是往往被一般的课堂教学所忽略的。
参考文献
[1] 王祖浩主编.义务教育教科书:化学(九年级 上册)第2版[M].上海:上海教育出版社,2013:101-103
[2] 宋心琦,胡美玲.对中学化学的主要任务专论和教材改革的看法[J].化学教育,2001,22(9):9-13
[3] 王祖浩主编.义务教育教科书化学(九年级 上册)第2版[M].上海:上海教育出版社,2013:102
[4] 杨砚宁,毛明. 巧设情境激活课堂——“揭秘浓硫酸”课堂教学案例剖析[J].化学教育,2012,33(12):14-16

