前列腺假增生性癌的临床病理特征分析
丁丰平,章力
(新昌县人民医院,浙江 新昌 312500)
前列腺假增生性癌的临床病理特征分析
丁丰平,章力
(新昌县人民医院,浙江 新昌 312500)
目的 观察前列腺假增生性癌的临床病理学特征并探讨其鉴别诊断要点。 方法 回顾性分析6例经病理确诊的前列腺假增生性癌的临床特点、组织形态学特征、免疫组化表达以及随访信息。 结果 组织学上3例表现为结节状推挤性生长,2例表现为复杂的分支状生长,1例表现为腺病样结构。肿瘤腺体中等偏大,6例内均局灶可见不同程度的腺体囊性扩张伴乳头状内摺,但缺乏明确的纤维血管轴心。6例肿瘤细胞均呈低柱状排列,4例胞浆浅染,1例呈黄瘤样泡沫状改变。4例瘤细胞核局灶可见明显增大的核仁,2例核仁不明显。4例肿瘤腺腔内可见无定形粉染层状物聚集,3例腺腔内可见多边形结晶体形成,1例局灶可见腺腔内粘液分泌。4例可见过渡为典型的腺泡型腺癌。免疫组化染色6例均弥漫表达PSA和雄激素受体,4例弥漫或局灶表达p504s,6例均基底细胞标志物表达缺失。 结论 前列腺假增生性癌罕见,组织形态多变,仔细的形态学分析并结合免疫组化染色有助于鉴别。
前列腺;假增生性癌;临床病理;诊断;鉴别诊断
腺泡性腺癌是前列腺癌最常见的组织学类型。组织学诊断前列腺腺癌主要取决于以下特点∶(1)明显增大的核仁;(2)神经侵犯、纤维粘液样结节、肾小球样结构以;(3)基底细胞丢失。2016年世界卫生组织(WHO)泌尿男生殖器官肿瘤分类[1]将前列腺腺泡性腺癌分为几个特殊的组织学亚型,其中包括萎缩性癌、泡沫细胞样癌、微囊性癌、假增生性癌等。前列腺假增生性癌罕见,顾名思义其组织学上类似于前列腺增生,很容易误诊。目前国内文献对其病理学特点的研究尚不多见,因此,本文回顾性分析6例前列腺假增生性癌的临床病理特征,着重讨论其诊断和鉴别诊断要点。
1 资料与方法
1.1 一般资料 选择新昌县人民医院2003年1月~2013年1月收治的前列腺假增生性癌6例,所有病例均重新回顾HE和免疫组化染色切片,依据2016年WHO泌尿男生殖器官肿瘤病理学分类诊断标准明确诊断[1]。6例发病年龄69~81岁,平均74.1岁。3例表现为排尿不畅,2例表现为尿频,1例为查体偶然发现。术前血清PSA水平53.8~97.6ng/mL,平均66.9ng/mL。直肠指诊3例表现为不规则结节状肿大。4例为本院根治切除标本,在外院行穿刺活检均诊断为前列腺腺癌;2例为本院穿刺活检所见。
1.2 方法 标本经4%甲醛固定,常规脱水、石蜡包埋、4μm切片、HE染色。镜下观察肿瘤的生长方式、腺体大小、腺腔内分泌物,有无伴随的普通型腺泡性腺癌或其他类型的癌,瘤细胞胞浆和细胞核的特点,有无神经侵犯、脉管侵犯、前列腺外扩散等。免疫组化染色采用EnVision两步法,PSA、p504s、p63、雄激素受体、ck34be12等一抗以及二抗、DAB显色剂为北京中杉金桥公司产品。在免疫组化过程中均进行阳性和阴性对照。免疫组化染色依据是否存在染色信号而判断为阴性或阳性。随访采用电话询问,随访时间从初次手术确诊至2016年1月。
2 结果
2.1 镜下表现 低倍镜下,3例表现为结节状推挤性生长(图1),2例表现为复杂的分支状生长,1例表现为腺病样结构;6例肿瘤均局灶可见肿瘤于良性腺体之间浸润性生长。肿瘤腺体中等偏大,6例均局灶可见不同程度的腺体囊性扩张伴乳头状内摺(图2),但缺乏明确的纤维血管轴心。6例肿瘤细胞均呈低柱状排列,核位于基底部,无假复层排列(图3)。1例为典型的双嗜性胞浆,4例胞浆浅染,1例呈黄瘤样泡沫状改变。高倍镜下,4例瘤细胞核局灶可见明显增大的核仁(图4),2例核仁不明显。4例肿瘤腺腔内可见无定形粉染层状物聚集,3例腺腔内可见多边形结晶体形成 (图5),1例局灶可见腺腔内粘液分泌。4例根治切除标本,均可见假增生性癌过渡为典型的小腺泡型腺癌,占据肿瘤体积20%~50%;假增生性癌Gleason评分均为3+3=6,腺泡性腺癌3例为Gleason3+3=6,1例为Gleason 3+4=7。另2例穿刺活检标本仅为假增生性癌,Gleason评分均为3+3=6。6例肿瘤中,2例可见周围神经累犯,1例可见局灶的前列腺外扩散。6例均未见脉管内侵犯。背景前列腺组织表现为增生性或萎缩性改变,偶尔可见少量慢性炎细胞浸润。
2.2 免疫组化 6例肿瘤均弥漫表达PSA和AR,4例肿瘤弥漫或表达p504s,2例p504s阴性。基底细胞标志物ck34be12(图6)与p63等均为阴性,背景中良性前列腺腺体的基底细胞表达可作为阳性对照。
2.3 随访 3例获得随访资料,其中2例为前列腺另治切除,1例穿刺活检在外院行前列腺根治切除术,术后均未接受进一步治疗,随访时间12~59个月,平均31.4个月,后均未见PSA复发或转移。
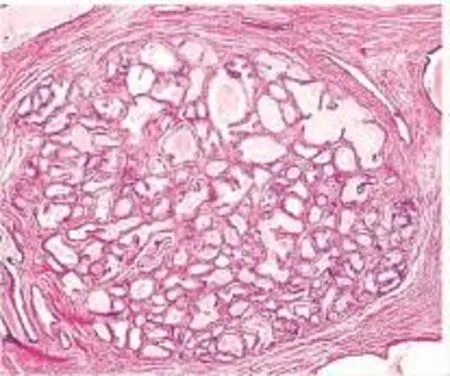
图1 低倍镜下肿瘤细胞呈结节状生长(HE×40)
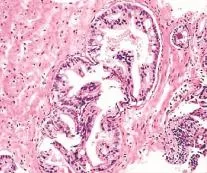
图2 腺体囊性扩张伴有乳头状内摺(HE×100)
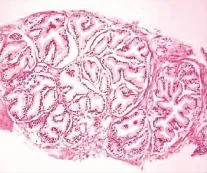
图3 肿瘤腺体胞浆浅染,单层排列,核位于基底部(HE×100)

图4 瘤细胞局灶可见明显增大的核仁(HE×400)

图5 腺腔内多边形结晶体形成(HE×400)
3 讨论

图6 免疫组化染色ck34be12示基底细胞完全丢失,右边良性腺体做为内对照。(EnVison×200)
前列腺假增生性癌是一种罕见类型的腺泡性腺癌亚型,在穿刺活检标本中发生率约2%,在根治切除标本中的发生率约11%[2]。大多数假增生性癌与普通型前列腺腺泡性腺癌并存,仅少数为纯的泡沫样癌;或表现为逐渐过渡,或表现为远离普通前列腺腺癌的单独癌灶。本文4例根治切除标本均可见过渡为典型的腺泡性腺癌,2例为纯的假增生性癌。2例纯的假增生性癌均为穿刺活检所见,因此,推测也有可能普通的腺泡性腺癌在穿刺活检中并未被取样到。据文献报道,假增生性癌占据肿瘤的比例2%~80%,平均22%[3],本文假增生性癌占据的比例为20%~50%,与文献报道符合。临床上,前列腺假增生性癌的发病年龄和术前血清PSA水平与普通型腺癌并无明显区别。相比较而言,半数左右的假增生性癌起源于前列腺移行区,而移行区正是前列腺增生好发的部位,因此,在术前PSA升高不明显的情况下,假增生性癌在临床上可能被误认为是普通型增生,此时穿刺活检显得十分必要。
组织学上,前列腺假增生性癌酷似良性前列腺增生。2016年WHO分类界定假增生性癌的低倍镜生长方式包括较大的腺体伴有乳头状内褶,腔面弯曲伴分支状小管;总体上病变以结节状生长方式为主,但至少局灶区可见良性腺体之间的穿插性生长[1]。病变可位于移行区或外周区。瘤细胞柱状单层排列,伴有丰富的浅染胞浆。本文1例肿瘤表现为黄瘤样泡沫状胞浆,在中文文献中尚属首次报道。Humphrey等[4]报道将近20%的假增生性癌腺腔内可见良性前列腺增生的无定形粉染层状物聚集,本文4例肿瘤内可见这一特点。大多数假增生性癌至少局灶可见明显的核仁,但这一特点相比于普通的前列腺癌并不明显,有时候需要高倍镜下仔细观察。与普通的前列腺癌相比,假增生性癌同样可见腺腔内多边形结晶和粘液分泌,这些都是诊断恶性的辅助形态学表现。按照2014年国际泌尿病理协会的诊断标准[5],大多数假增生性癌的Gleason评分为3+3=6分,偶尔病变结节清楚时可为Gleason3+2或2+3=5分。文献报道5%到9%的病例可见神经侵犯[3-4]。免疫表型上,仅77%的假增生性癌表达p504s,有时可仅为局灶表达,本文2/3弥漫或局灶表达p504s,基底细胞标志物染色显示肿瘤腺体周围基底细胞完全丢失。最近的研究表明,与HOXB13G84E基因突变相关的家族性前列腺癌常见表现为假增生性癌的特点[1]。
假增生性癌由于其复杂多变的组织学构型,相对温和的细胞学特征以及较少表达p504s,因而很容易误诊为良性前列腺增生或其它恶性前列腺肿瘤。(1)以大腺体结构为主的良性前列腺增生∶病变常见于前列腺移行区,背景中前列腺间质也可见增生;增生的导管或腺泡常见上皮不规则簇状突起,与假增生性癌非常相似,在穿刺活检中容易混淆。假增生性癌区别良性前列腺增生的要点包括∶至少局灶的核仁增大;常见与普通的腺泡性腺癌并存;腺腔内多边形结晶;神经侵犯(如果有);免疫组化基底细胞完全消失。(2)高级别前列腺上皮内瘤变 (HGPIN),微乳头型或簇状型HGPIN∶两者均具有至少局灶的恶性上皮特点,但免疫表型前者常见完整的基底细胞围绕而后者却完全消失。(3)非典型腺瘤样增生(AAH),又称为“前列腺腺病”∶组织学上表现为小而密集的腺体与大而扩张的腺体的混合性增生,大腺体常见腔面弯曲和乳头状内褶,然而与假增生性癌不同,免疫组化染色AAH腺体周围常见碎片状的基底细胞围绕,p504s一般为阴性。(4)前列腺导管腺癌∶常见腔面上皮呈乳头状增生,但与假增生性癌不同,导管腺癌的乳头常见真正的纤维血管轴心,被覆上皮假复层且深染,异型性明显。
预后上,前列腺假增生性癌由于其Gleason评分较低,大多数预后较好。总体预后主要取决于肿瘤的分期以及伴随的普通型腺癌的Gleason分级。本文6例肿瘤中1例伴有Gleason3+4=7分的普通型腺泡性腺癌的肿瘤出现包膜外扩散。3例获得随访,随访12~59个月,后均未见PSA复发或转移。
前列腺假增生性癌罕见,形态学上具有明显的异质性,容易与其它具有相似外观的良恶性前列腺病变相混淆,仔细的形态学分析并辅以免疫组化染色可帮助其诊断和鉴别诊断。
[1] Moch H,Humphrey PA,Ulbright TM,et al.WHO classification of tumours of the urinary system and male genital organs. Lyon∶IARC Press,2016∶138
[2] Shah RB,Zhou M.Prostate Biopsy Interpretation∶An Illustrated Guide.Berlin∶Springer,2012∶79
[3] Levi AW,Humphrey PA.Pseudohyperplastic prostatic adenocarcinoma on needle biopsy and simple prostatectomy.Am J Surg Pathol,2000,24(10)∶1039
[4] Humphrey PA.Pseudohyperplastic prostatic adenocarcinoma. Am J Surg Pathol,1998,22(12)∶1239
[5] Epstein J I,Egevad L,Amin MB,et al.The 2014 International Society of Urological Pathology (ISUP)Consensus Conference on Gleason Grading of Prostatic Carcinoma∶Definition of Grading Patterns and Proposal for a New Grading System. Am J Surg Pathol,2016,40(2)∶244

