在线二维反相色谱法快速测定维生素AD制剂中维生素A、D的含量
张艳海,张大伟,曹 莹,金 燕*
(1.赛默飞世尔科技(中国)有限公司,上海 201206;2.黑龙江农垦总医院,黑龙江 哈尔滨 150088;
3.上海市兽药饲料检测所,上海 201103)
在线二维反相色谱法快速测定维生素AD制剂中维生素A、D的含量
张艳海1,张大伟2,曹莹3,金燕1*
(1.赛默飞世尔科技(中国)有限公司,上海201206;2.黑龙江农垦总医院,黑龙江哈尔滨150088;
3.上海市兽药饲料检测所,上海201103)
摘要:建立了在线二维液相色谱法快速同时测定维生素AD制剂中维生素A和D的含量。依据药典对系统适应性的要求,选择一种极性嵌合的C18柱(Accucore polar premium)作为二维色谱柱,再依据疏水减法模型原理和待测样品的脂溶性特点,选择C8柱作为一维色谱柱,一维和二维分离均采用甲醇、乙腈和水作为流动相。样品经乙醇提取后直接进样分析,采用双梯度液相色谱右泵作为一维分析泵,完成含量较高的维生素A定量及维生素D的净化;采用左泵作为二维分析泵,维生素D及前维生素D在二维色谱柱上实现分离和定量。根据维生素D在一维色谱上的出峰起止时间,确定切割时间窗口,以500 μL定量环收集含有目标物的馏分,检测波长分别为264 nm和325 nm。采用外标法完成对维生素D和前维生素D的定量。整个过程在密闭系统中自动化完成。维生素A在0.1~250 mg/L,维生素D在0.02~50.0 mg/L范围内线性关系较好,相关系数(r)大于0.999;维生素D的回收率为89.9%~98.9%,连续进样的精密度和重现性的RSD分别为0.48%和1.2%,表明方法的精密度和重现性较好。
关键词:二维液相色谱;在线分离;维生素D;维生素A;前维生素D;维生素AD滴剂
维生素A(Vitamin A)是指具有与全反式视黄醇(All-trans retinol)同样生物活性的一类相关化合物,包括视黄醛、视黄酯(维生素A醋酸酯或棕榈酸酯)[1],具有促进机体生长、维持表皮完整等功能,是人体必需的营养素之一,其前体主要是存在于多种植物中的胡萝卜素[2]。在结构上,维生素A类化合物由β-紫罗兰酮环连接4个带有共轭双键的异戊二烯单位构成(见图1),因此存在多种顺反异构体,其中天然形式为全反式维生素A,其次为13-顺式维生素A。维生素D(Vitamin D)属于甾醇类化合物,除了B环开环和A环3位羟基外,其主体骨架结构与类固醇相似。维生素D主要包括维生素D2(麦角钙化醇,Ergocalciferol)和维生素D3(胆钙化醇,Cholecalciferol)两种同效的维生素,前者较后者在侧链上多了1个双键和1个甲基(图1)。人体在280~320 nm的紫外线照射下,皮肤中的7-脱氢胆固醇可转化成前维生素D,再转化成维生素D3。维生素D2通常是由植物或酵母菌中的麦角固醇在紫外线所介导的光异构化作用下产生[3]。维生素D的基本作用是促进钙和磷的吸收,缺乏维生素D,会影响钙的吸收和骨代谢[4],最终引起佝偻病、软骨症或骨质疏松症等。
作为药品的维生素AD制剂在2010版中国药典和美国药典35版(USP35)均有收载,其中维生素D受到光热影响,易产生前维生素D(Pre-vitamin D3)、反式维生素D3(Transvitamin D3)、速甾醇(Tachysterol)和光甾醇(Lumisterol)等,其转化途径见图2。因各异构体结构相近,需要结合正相和反相色谱才能实现各异构体分离[5]。中国药典附录维生素D测定法[6]第二法和USP35 <581>[7]维生素D测定法,需要同时对前维生素D和维生素D进行定量,由于前维生素D含量较低,易受基质干扰,因此样品溶液制备过程通常包括皂化、萃取、反相制备色谱净化等步骤,最后采用正相色谱紫外检测法进行分析,整个过程耗时费力,极大影响了分析效率,且目前尚无较好的解决方案。而结合两种或两种以上不同分离模式的二维或多维色谱分离在复杂样品分析中已有较多应用[8-12]。本文首次采用在线二维液相色谱法(2D-LC),将样品的净化及分析过程在线完成,样品经提取后,直接进样分析,测定了维生素AD药物制剂中的维生素A、D及前维生素D的含量,提高了方法的准确性和实际样品的分析效率。
1实验部分
1.1仪器、试剂与材料
三元液相色谱(DGLC)系统(Thermo Fisher,USA),配置包括6通道真空脱气机SRD3600、双梯度分析型色谱泵(DGP3600)、自动进样器(WPS3000TSL)、二极管阵列检测器(DAD3000)、柱温箱(TCC-3000,配1个2位置六通阀和1个2位置10通阀),变色龙色谱管理软件(Chromeleon 7.2 SR1)、Acclaim 120 C8色谱柱(150 mm×3.0 mm,3 μm)和Accucore polar premium色谱柱(150 mm×3.0 mm,2.6 μm)。
维生素D3、维生素D2(纯度≥95%,HPLC级,中国药品生物制品检定所)供含量测定用;全反式维生素A乙酸酯(All-trans retinol acetate,纯度>99%,Acros Organics公司)。KOH(分析纯)和抗坏血酸(纯度≥99.7%,分析纯)购自国药集团化学试剂有限公司;乙腈、甲醇(色谱纯,Fisher公司);去离子水(18.2 MΩ·cm)由Millipore纯水机制得;维生素AD滴剂市售,维生素AD乳剂由上海市兽药饲料检验所提供。
1.2样品制备
取维生素AD滴剂内容物适量,精密称定,置于25 mL 棕色容量瓶中,加适量无水乙醇,超声(400 W,40 kHz) 处理30 min,冷却,加无水乙醇至刻度,摇匀,过滤,取续滤液即得。
1.3标准溶液的配制
取适量维生素D3和维生素A标准品,精密称定,加甲醇溶解并制成浓度分别为0.1 mg/mL和0.5 mg/mL的标准储备液。
1.4系统适用性溶液制备
取维生素D3标准储备溶液1.0 mL,置于具塞玻璃容器中,通氮后密封,置于90 ℃水浴中避光加热1 h,取出迅速冷却,精密加入甲醇并定容至10 mL容量瓶中,摇匀,置于1 cm 具塞石英吸收池中,在2 支8 W 主波长分别为254 nm 和365 nm 的紫外灯下,将石英吸收池斜放45°,并距灯管5~6 cm,照射5 min,使溶液中含有前维生素D3、反式维生素D3、维生素D3和速甾醇D3。此溶液为系统适用性试验用溶液。
1.5仪器条件
DGLC系统的右泵作为一维分析泵,以Acclaim 120 C8柱(150 mm×3.0 mm,3 μm)为一维分析柱,梯度洗脱,流速0.5 mL/min;以DGLC的左泵作为二维分析泵,Accucore polar premium柱(150 mm×3.0 mm,2.6 μm)为二维分析柱,梯度洗脱,流速0.6 mL/min,柱温35 ℃,流动相均为乙腈(A)、甲醇(B)和水(C);二极管阵列检测器的检测波长分别为264 nm(维生素D)和325 nm(维生素A醋酸酯);进样体积5 μL;收集定量环(Loop环)的体积为500 μL。系统流路连接见图3,梯度洗脱程序及阀切换时间见表1。
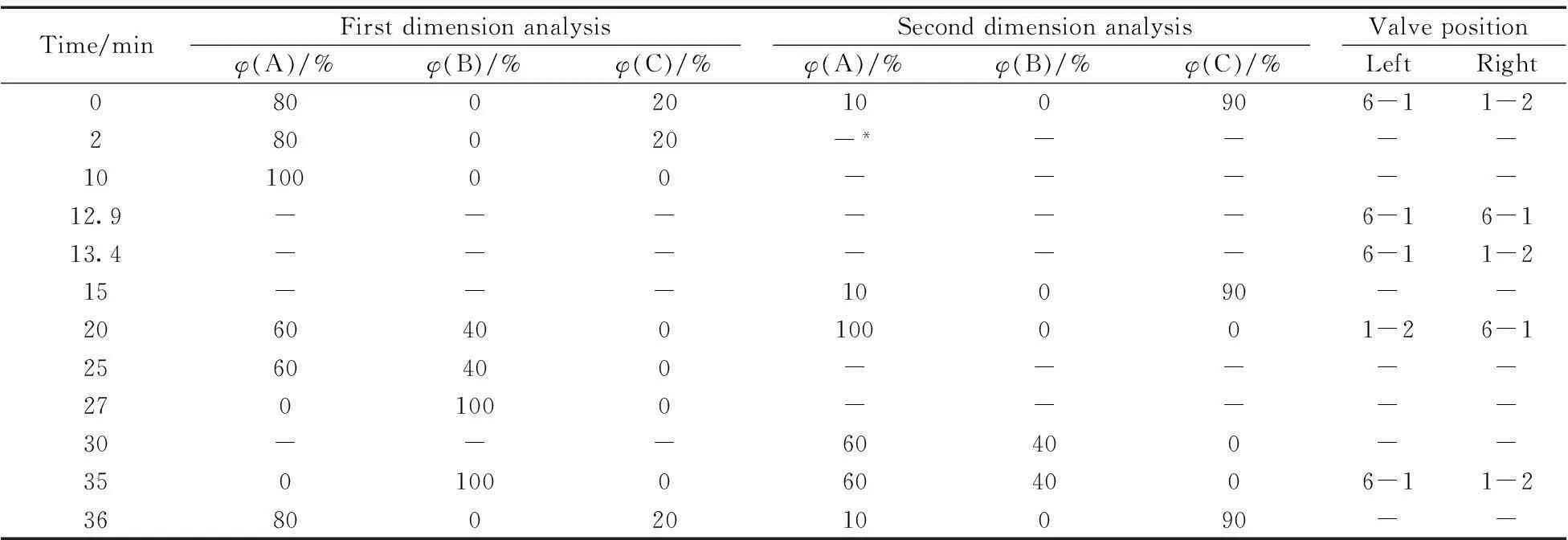
表1 一维分离和二维分离的梯度洗脱程序
*no data
在初始阶段,左阀1-6,右阀1-2,一维色谱柱完成维生素A的定量和维生素D的净化,同时二维色谱柱用初始流动相平衡;在转移阶段,左阀1-6,右阀1-2,一维色谱将含有维生素D及前维生素D的馏分转移至Loop环中;在二维分析阶段,左阀1-2,右阀1-2,左泵以含有高水的流动相将Loop中的样品带入二维色谱柱进行分析,实现维生素D和前维生素D的定量分析。
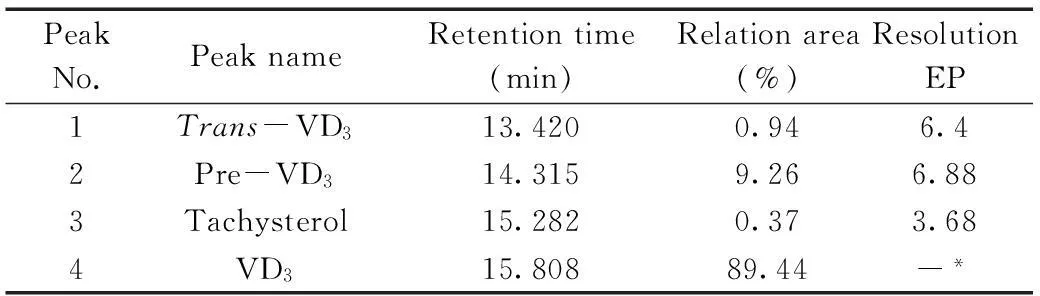
表2 系统适用性结果
*no data
2结果与讨论
2.1系统适应性试验
2010版药典二部附录VD的测定方法[6]中要求维生素D与速甾醇、前维生素D和反式维生素D的分离度大于1.0,维生素D、前维生素D、速甾醇和反式维生素D为同分异构体,分子量均为384.34,用正相色谱法以正己烷-异丙醇或戊醇作为流动相进行分析,能够将维生素D(VD)、前维生素D(前VD)及其非活性形式分离,但正相色谱法系统平衡慢,且重现性较差;反相色谱法能够分离维生素D2和D3,但对样品的前处理要求较高[13]。基于方法耐用性考虑,本文拟采用反相色谱法进行分析。分别尝试采用Acclaim C8,Acclaim C18,Accucore polar premium(一种极性嵌合的C18柱),Acclaim C30及Hypersil PAH等色谱柱对系统适应性试验样品进行分离。结果显示,Accucore polar premium色谱柱可实现各异构体基线分离,且各异构体的分离度均大于2,满足系统适应实验要求,结果见表2。其中各色谱峰定位的主要依据为:对比加热和光照后样品的色谱图(图4),VD加热会产生前VD,光照又会产生反式VD和速甾醇,因此可通过对比谱图定位前VD;参考UV吸收谱图和相对保留时间,文献[14]中VD、前VD、反式VD和速甾醇的最大吸收分别为265,265,275,279 nm,本实验各峰吸收分别为265,262,274.9,281.4 nm,UV吸收和相对保留时间也与文献报道基本一致;通过LC-MS结果,采用APCI源,结果4个色谱峰的m/z均为385.3[M+H]+,表明各峰的分子量均为384.3。综上结果实现了对色谱峰的定位。
2.2二维色谱分离方法分析
在前期实验中已成功构建了婴幼儿配方奶粉中维生素A、D和E的在线二维色谱分析方法[15],与奶粉基质样品不同,维生素AD制剂通过加鱼肝油或精炼食用植物油(在0 ℃左右脱去固体脂肪)溶解和调整浓度,并加稳定剂适量制成,在储存和制备过程中会产生前维生素D,其含量甚微,分离及定量易受基质干扰。因此药典方法通常利用反相制备色谱实现VD(包括前维生素D)与其他基质干扰物的分离净化,再利用正相色谱对维生素D及其前维生素D进行定量。本文尝试采用反相色谱净化结合反相色谱分析的在线二维色谱法对药品中VA和VD进行同时定量分析,由“2.1”系统适应性试验结果可知,Accucore polar premium能实现维生素D、前维生素D及其非活性的光热异构体分离,完全满足系统适应性试验要求,可作为第二维的分析柱使用,可对VD和前VD进行定量分析。在第一维净化色谱柱选择上,C8柱对脂溶性物质具有较小的疏水作用力,便于将脂溶性较强的基质干扰成分洗脱除去,且C8柱与Accucore polar premium柱分离机理能构成一定的正交性(根据Snyder等[16]疏水减法模型,两根色谱柱的正交因子(Fs)为65),可提升系统分离能力。由图5~6分离结果可知,前VD3和VD3在第二维色谱柱上实现了基线分离,且峰对称性良好,完全满足定量要求。
2.3线性关系、定量下限、精密度与重现性
分别精密量取维生素D3、维生素A的标准储备溶液适量,配制成系列混合标准溶液,按照优化的色谱条件进样分析。以各目标物的浓度为横坐标,对应峰面积为纵坐标,做线性回归。维生素D及维生素A分别在0.02~50.0、0.1~250 mg/L范围内线性关系良好,相关系数(r)均大于0.999。其中维生素D和维生素A的定量下限(S/N=10)分别为0.015 mg/L和0.04 mg/L。
精密度考察采用混合标准溶液连续进样6次,测得维生素D、A保留时间的相对标准偏差(RSD)分别为0.07%和0.14%,峰面积的RSD分别为0.48%和0.19%,表明该方法连续进样的精密度较好。
取维生素AD滴剂样品6份,按“1.2”方法制备样品溶液,测得维生素A和D3在6份样品中含量的RSD分别为0.58%和1.2%,表明该方法的重现性较好。
2.4前维生素D校正因子的测定
取浓度为0.1 mg/mL的维生素D储备液1 mL置于10 mL容量瓶中,加甲醇定容,摇匀,制成浓度为10 μg/mL的标准品溶液,进样分析,计算得维生素D的响应因子f1=C1/A1。另精密量取维生素D标准品储备溶液2份,每份1 mL,置于棕色顶空瓶中,按照2010版药典二部附录VD的测定方法[6]测定前VD的响应因子f2=(C1-f1A1)/A2。式中C1为f1测定项下维生素D标准品溶液的浓度(μg/mL);f1为维生素D的校正因子;A1为混合对照品溶液所得色谱图中维生素D的峰面积值;A2为混合对照品溶液所得色谱图中前维生素D的峰面积值。经计算得维生素D的响应因子f1为3.37,两次测定得到前维生素D的响应因子f2的平均值为9.31。
2.5回收率考察
精密称取维生素AD滴剂样品3份,分别按照高、中和低3个浓度加入维生素A和D3,涡旋混匀后,按照“1.2”方法制备样品溶液,在最佳色谱条件下进样分析,结果见表3。维生素D3的回收率为90.0%~98.9%,平均回收率为93.8%,平均RSD为1.1%,满足定量要求;维生素A的回收率为106.0%~109.6%,平均回收率为108.1%,平均RSD为0.77%。回收率结果均偏高,分析原因可能为采用本方法的一维反相分离条件未能实现全反式VA和13-顺式异构体的拆分所致,但采用本法可完成对VA总量的测定。

表3 维生素AD滴剂中维生素A和D3的加标回收率与相对标准偏差(n=3)
2.6实际样品的测定
取维生素AD滴剂及乳剂,按照“1.2”方法制备样品溶液,在最佳色谱条件下进样分析,计算维生素D 及前维生素D 折算成维生素D 后的总浓度(Ci):Ci=f1Ai1+f2Ai2。其中Ai1为维生素D的峰面积,Ai2为前维生素D的峰面积。
维生素AD滴剂中维生素A的标示量为1 500 IU/粒(450 μg/粒),结果测得量为1 722.4 IU/粒(516.73 μg/粒),满足药典标准要求(90%~120%);维生素D3的标示量为500 IU/粒(12.5 μg/粒),测得量为604.3 IU/粒(15.11 μg/粒),也满足药典规定的标准(>85%);维生素AD乳剂(兽药)中维生素A的标示量为5 000 IU/g,测得量仅为4 177.33 IU/g;维生素D的标示量为500 IU/g(12.5 μg/g),而维生素D3的测得量仅为26.12 IU/g(0.65 μg/g),样品中主要含维生素D2,其含量以维生素D3计算,约为9.5 μg/g。从测定结果可知,维持AD的含量均不满足标准要求,作为兽药维生素AD乳剂,其质量存在一定问题,后期还需要收集大量样品进行检测,并与标准方法测定结果进行比较,一方面考察本法的准确性,另一方面可对维生素AD乳剂的整体质量状况进行评价。
3结论
本文基于在线二维液相色谱技术建立了维生素AD制剂中维生素A和D的测定方法,系统适应性实验结果表明,本方法可满足维生素D的测定要求,利用一维色谱柱可完成维生素A总量的测定和维生素D的净化,利用二维色谱柱可完成维生素D2、维生素D3、前维生素D及其他光化异构体的分离,可准确对药物中前维生素D和维生素D进行定量分析。本方法的线性关系、准确度和精密度较好,采用优化的在线二维系统连接设计,一次进样可完成维生素A和D的定量测定,大大提高了实际样品的分析效率,可进行推广应用。
参考文献:
[1]Coates P M,Betz J M,Blackman M R,Cragg G M,Levine M,Mos J,White J D.EncyclopediaofDietarySupplements.2nd ed.Informa Healthcare,London and New York,2010:778-790.
[2]D’Ambrosio D N,Clugston R D,Blaner W S.Nutrients,2011,3(1):63-103.
[3]Holick M F.NewEngl.J.Med.,2007,357:266-281.
[4]Holick M F,Binkley N C,Bischoff-Ferrari H A,Gordon C M,Hanley D A,Heaney R P,Hassan Murad M,Weaver C M.TheJ.Clin.Endocrinol.Metab.,2011,96:1911-1930.
[5]Lu Z R,Chen T C,Holick M F.ActaPharm.Sin.(陆志仁,Chen T C,Holick M F.药学学报),1992,27(5):369-372 .
[6]Chinese Pharmacopoeia Commission.ChinesePharmacopoeiaPartⅡ:Appendix ⅦK(中国药典委员会.中国药典二部附录ⅦK),2010.
[7]United States Pharmacopoeia Convention.TheUnitedStatesPharmacopoeia35-TheNationalFormulary30.Baltimore:Port City Press,2012,581:227-230.
[8]Hu L H,Chen X G,Kong L,Su X Y,Ye M L,Zou H F.J.Chromatogr.A,2005,1092(2):191-198.
[9]Tian H Z,Xu J,Xu Y,Guan Y F.J.Chromatogr.A,2006,1137(1):42-48.
[10]Yao C L,Yang W Z,Wu W Y,Da J,Hou J J,Zhang J X,Zhang Y H,Jin Y,Yang M,Jiang B H,Liu X,Guo D A.J.Chromatogr.A,2015,1402 :71-81.
[11]Zhang Y H,Zhang D W,Meng Z Q,Ye M L.J.Instrum.Anal.(张艳海,张大伟,孟兆青,叶明立.分析测试学报),2013,32(3):320-325.
[12]Jin G W,Ding J J,Chen X,Yan J Y,Guo Z M,Zhang X L,Liang X M.J.Instrum.Anal.(金高娃,丁俊杰,陈雪,闫竞宇,郭志谋,张秀莉,梁鑫淼.分析测试学报),2014,33(2):133-137.
[13]Perales S,Alegría A,Barberá R,Farré R.FoodSci.Technol.Int.,2005,11(6):451-462.
[14]Wang S,Zheng F,Ding L.J.ChinaPharm.Univ.(王尚,郑枫,丁黎.中国药科大学学报),2012,43(1) :55-59.
[15]Zhang Y H,Qibule H S,Jin Y,Wang J,Ma W L.Chin.J.Chromatogr.(张艳海,其布勒哈斯,金燕,王佳,马文丽.色谱),2015,33(3):291-297.
[16]Snyder L R,Dolan J W,Carr P W.J.Chromatogr.A,2004,1060:77-116.
Simultaneous Determination of Vitamins A,D in Vitamin A and D Pharmaceutical by Online Two-dimensional Reverse-phase Liquid ChromatographyZHANG Yan-hai1,ZHANG Da-wei2,CAO Ying3,JIN Yan1*
(1.Thermo Fisher Scientific(China) Company,Shanghai201206,China;2.Heilongjiang Agricultural Reclamation
General Hospital,Harbin150088,China;3.Shanghai Animal Disease Control Center,Shanghai201103,China)
Abstract:A rapid method for the simultaneous determination of fat-soluble vitamins A and D in vitamin A and D pharmaceutical was developed using online two-dimensional liquid chromatography(2D-LC).A type of polar embedded C18was selected as the second dimension separating column according to system suitability testing requirement.C8was chosen as first dimension separating column because fat-soluble substance was rich in matrix and a better orthogonality could meet with polar embedded C18according to hydrophobic subtraction model.Sample solution after extracted with methanol without further purification was injected into liquid chromatography directly.The purification of vitamin D and quantification of vitamins A acetate were accomplished simultaneously in one dimensional separation using the right pump of Dual Gradient LC(DGLC) with methanol-acetonitrile-water as mobile phase.Vitamin D and pre-vitamin D were separated and quantified in two dimensional column by using the left pump of DGLC.The eluted target from the first dimensional column(1-D column) was collected by a 500 μL loop and then taken into the second dimensional column(2-D column) by the left pump of DGLC with high aqueous mobile phase.The cutting window could be confirmed by the retention time of target in one dimensional separation.Detection wavelengths of 325 nm and 264 nm were set at the diode-array detector.Vitamin A,vitamin D and pre vitamin D were quantified simultaneously and automatically in one injection by the external standard method.The results showed that the good linearities(r>0.999) for vitamin A and vitamin D could be obtained in the range of 0.1-250 mg/L and 0.02-50.0 mg/L,respectively.The recoveries of vitamin D ranged from 89.9% to 98.9%.The RSDs for precision and reproducibility are 0.48% and 1.2%,respectively.All the validating results indicated that vitamins A and D in pharmaceutical could be quantified rapidly and accurately by this method.
Key words:two-dimensional liquid chromatography(2D-LC);online separation;vitamin D;vitamin A;pre vitamin D;vitamin A and D drops
中图分类号:O657.72;O629.4
文献标识码:A
文章编号:1004-4957(2016)01-0028-07
doi:10.3969/j.issn.1004-4957.2016.01.005
通讯作者:*金燕,硕士,高级工程师,研究方向:色谱及色谱-质谱联用技术及其应用,Tel:021-69654588,E-mail:jinyanwc@sina.com
收稿日期:2015-06-24;修回日期:2015-07-15

