用HPLC-MS/MS法检测大鼠乳腺微透析液中环磷酰胺的浓度
胡霜霜,刘春生,童卫杭,曹 淼,吴 城,彭 珑,王 丹(第二炮兵总医院药学部,北京 100088)
·论著·
用HPLC-MS/MS法检测大鼠乳腺微透析液中环磷酰胺的浓度
胡霜霜,刘春生,童卫杭,曹淼,吴城,彭珑,王丹*(第二炮兵总医院药学部,北京 100088)
[摘要]目的:建立HPLC-MS/MS法检测大鼠乳腺微透析液中环磷酰胺的浓度。方法: 采用Cosmosil-C(18)色谱柱(150 mm×4.6 mm,5 μm),流动相:A相为0.1%甲酸溶液,B相为乙腈,0~1 min A∶B=70∶30,1~1.5 min A∶B=60∶40,1.5~5.5 min A∶B=40∶60,5.5~8 min A∶B=70∶30,梯度洗脱8 min,流速为1 ml/min。正离子多反应检测(MRM)方式进行检测,监测离子对:环磷酰胺m/z 261.3→140.1,内标安替比林m/z 189.2→104.0。结果:环磷酰胺的线性范围为0.05~10 μg/ml,最低定量限为0.05 μg/ml。日间和日内RSD均<15%,准确度和稳定性实验结果均符合生物样品的测定要求。结论:本方法灵敏度高,操作简便,适用于微透析样品中环磷酰胺的浓度测定。
[关键词]环磷酰胺;含量测定;微透析;色谱法,高效液相;质谱法
[Pharm Care Res,2015,15(3): 205-207]
环磷酰胺(cyclophosphamide)是临床上最常用的一种烷化剂类抗肿瘤药,广泛用于治疗恶性淋巴瘤、乳腺癌、卵巢癌、宫颈癌等,具有一定的化疗效果[1]。环磷酰胺是一个典型的前体药物,体外无活性,在肝中被细胞色素P450氧化酶氧化,生成活化型的磷酞胺氮芥发挥抗肿瘤作用,属细胞周期非特异性药物。目前,国内环磷酰胺血浆浓度的测定方法主要是GC法和HPLC法,但耗时较长,检测限偏高。此外,血药浓度结果不能准确反映靶标部位的治疗情况。微透析技术是近年发展起来的一种新型活体靶标取样技术[2]。本研究旨在建立HPLC-MS/MS法测定大鼠乳腺微透析液中环磷酰胺的浓度。
1材料
1.1仪器3200Q-Trap 型液相色谱-串联质谱仪,配有电喷雾离子化源(ESI)和Analyst 1.5.1数据处理软件(美国Applied Biosystem 公司);Agilent 1100高效液相色谱仪(美国Agilent公司);XH-C 涡旋混合器(中国金坛市白塔新宝仪器厂);CP225D分析天平(精度0.01 mg,德国Sartorius公司)。
微透析系统包括CMA150型动物保温垫、CMA402型微量注射泵、MAB 85型低温样品收集器、CMA30 型线性微透析探针(分子截留值6 kU,透析膜长1 cm),均购自美国CMA公司。
1.2试剂环磷酰胺对照品(批号100234-200502)和安替比林对照品(批号100506-200301,中国食品药品检定研究院);注射用环磷酰胺(规格0.2 g/支,进口批号H20110407,百特国际有限公司);乙腈、甲醇、甲酸均为色谱纯;水为无菌去离子水;复方氯化钠注射液(又名林格氏液,华润双鹤药业股份有限公司);水合氯醛(解放军第三O六医院生产);Veet脱毛膏(法国Veet公司)。
1.3实验动物SD大鼠2只,体重(200±10) g,雌性,购自北京维通利华实验动物技术有限公司,实验动物许可证号:SCXK(京)2012-0001。
2方法和结果
2.1色谱条件Cosmosil-C18色谱柱(150 mm×4.6 mm,5 μm);流动相:A相为0.1%甲酸水,B相为乙腈,0~1 min A∶B=70∶30,1~1.5 min A∶B=60∶40,1.5~5.5 min A∶B=40∶60,5.5~8 min A∶B=70∶30,梯度洗脱8 min;流速:1.0 ml/min,分流比1∶1;柱温:30 ℃;进样量:2 μl。
2.2质谱条件离子源:ESI源,正离子模式检测;离子喷射电压:4500 V;离子源温度:500 ℃;源内气体1(GS1,N2)压力:241.4 kPa;气体2(GS2,N2)压力:241.4 kPa;气帘气体(N2)压力:69 kPa;扫描方式:多反应监测(MRM);碰撞气(N2)压力:Medium;环磷酰胺、安替比林解簇电压(DP)分别为48、57 V;碰撞能量(CE)分别为27、22 eV;环磷酰胺、安替比林用于定量分析的离子对分别为m/z261.3→140.1、189.2→104.0。
2.3溶液的配制(1)环磷酰胺储备液的配制精密称取10 mg环磷酰胺对照品,置于10 ml容量瓶中,加入乙腈溶解,定容至刻度,配制成浓度为1 mg/ml的环磷酰胺储备液。(2)内标溶液的配制精密称取10 mg安替比林对照品,置于10 ml容量瓶中,加入乙腈溶解,定容至刻度,配制成1 mg/ml储备液,再用乙腈稀释成1 μg/ml的安替比林内标溶液。
2.4标准曲线及质控样品的制备吸取适量环磷酰胺储备液,用空白透析液(将探针植入大鼠乳腺组织,以林格氏液灌流,收集到的液体)稀释成浓度为0.05、0.1、0.5、1、2、5、10 μg/ml的系列对照品溶液。依次精密吸取各浓度的环磷酰胺对照品溶液20 μl,加入内标溶液10 μl,混合涡旋10 s。吸取适量环磷酰胺储备液,用空白透析液稀释,按上述方法操作,制备含环磷酰胺浓度为0.1、0.8、8.0 μg/ml的质控样品。
2.5微透析样品收集及处理
2.5.1探针体外校正以林格氏液冲洗探针后,将线性微透析探针浸入装有100 ml林格氏液的微透析反应瓶中,分别以不用浓度的药物(cin,1.0、4.0、8.0 μg/ml)作为灌流液,其他条件不变,收集的样品在所建立的HPLC-MS/MS条件下测定透析液中药物浓度(cout)。通过减量法计算环磷酰胺的体外探针回收率,R=(cin-cout)/cin,结果为(53.32±1.23)%。
2.5.2微透析样品收集大鼠用水合氯醛按体重(0.4 ml/100 g,ip)麻醉,腹部朝上固定于保温垫上,使其体温保持在37.5 ℃。用脱毛膏去除胸部毛,15 min后,暴露大鼠乳头,用直尺准确量取探针透析膜进出的长度。将线性微透析探针用18 G穿刺针引导平行植入乳腺组织后,抽回引导针并将探针留于组织中,然后将探针与微透析装置相连。以2 μl/ml的流速向其中泵入林格氏液作为灌流液,排除气泡并冲洗管路30 min,再以1.0 μl/ml的流速向微透析探针中泵入林格氏液,平衡1 h后,收集空白透析液。将注射用环磷酰胺用生理盐水溶解,尾静脉注射给药,一次性给予0.20 mg/g。以冷冻样品收集器连续收集透析液,采样间隔30 min,温度4 ℃,持续采样2 h。样品处理:精密量取透析液样品20 μl,加入内标溶液10 μl,涡旋10 s,进样2 μl。
2.6方法学考察
2.6.1专属性考察空白透析液、环磷酰胺及内标加入空白透析液的色谱图、组织透析液色谱图见图1。结果显示,内源性物质不干扰测定。
2.6.2线性关系考察取环磷酰胺储备液,用空白透析液稀释成0.05、0.1、0.5、1、2、5、10 μg/ml系列溶液,分别量取20 μl,加内标溶液10 μl,混合涡旋10 s,进样2 μl,进行HPLC-MS/MS分析。
以待测物浓度(X)为横坐标,以待测物与内标物的峰面积比(Y)为纵坐标进行线性回归,得环磷酰胺回归方程为Y=0.982X+0.012,r=0.999 2。结果表明,环磷酰胺在0.05~10 μg/ml范围内线性关系良好,检测限为2 ng/ml。
2.6.3精密度和准确度实验按2.4项下方法制备环磷酰胺浓度分别为0.5、4.5、8 μg/ml的低、中、高浓度质控样品,每个浓度5份,随行标准曲线回归方程计算浓度,并计算日内精密度和准确度。重复操作,连续测定3 d,考察方法的日间精密度和准确度,准确度=(平均值-理论值)/理论值×100%,结果见表1,表明此方法的精密度和准确度符合要求。
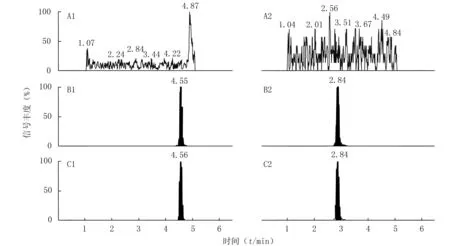
图1 HPLC-MS/MS法测定大鼠乳腺微透析液中环磷酰胺(1)和内标安替比林(2)的典型谱图Figure 1 The typical photograms of cyclophosphamide(1) and internal standard antipyrine(2) in rat breast microdialysis fluid by HPLC-MS/MS methodA:空白透析液;B:空白透析液+环磷酰胺对照品(0.1 μg/ml)+内标安替比林(1.0 μg/ml);C:微透析液样品;A1、B1、C1:环磷酰胺;A2、B2、C2:安替比林
2.6.4稳定性实验按2.4项下方法制备环磷酰胺浓度分别为0.5、4.5、8 μg/ml的低、中、高浓度质控样品,每个浓度各3个样品,分别在4 ℃、室温条件下放置10 h,-20 ℃反复冻融2次后,测试其稳定性。结果显示,测定值与理论值的RSD均<15%,表明透析样品在上述条件下均较稳定。
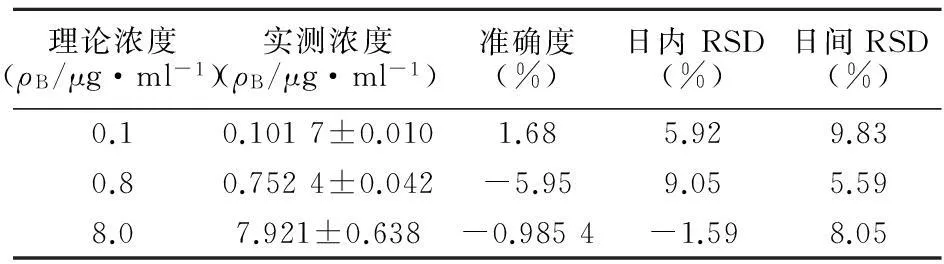
表 1 微透析样品中环磷酰胺的精密度和准确度实验结果
3讨论
3.1检测方法的选择环磷酰胺能溶于水,但溶解度不大,完全溶解需时间长,且其水溶液不稳定,对光和热敏感[3],因此,环磷酰胺的水溶液需现配现用。目前国内主要使用HPLC、GC等方法测定血浆中环磷酰胺的浓度,存在耗时较长、灵敏度不高等不足。本研究采用HPLC-MS/MS法检测环磷酰胺的浓度,由于环磷酰胺极性较大,所以在流动相洗脱时,需使用高比例的水相洗脱。本研究以梯度洗脱方式,采用正离子模式检测,可使环磷酰胺出峰较好,信号稳定。
3.2微透析样品的选择微透析技术可监测靶部位组织细胞外的游离药物浓度[4],因此,监测组织中药物的浓度比传统血药浓度的定量结果更具预测性[5]。文献报道,环磷酰胺普遍应用于乳腺癌联合治疗方案中,在乳腺癌化疗过程中占据着不可忽视的地位[1]。因此,本研究采用HPLC-MS/MS法检测乳腺微透析液中环磷酰胺的药物浓度,方法专属性强,检测限低,检测时间短,可在8 min内快速检测出乳腺中环磷酰胺的药物浓度,提供了一种快速有效监测环磷酰胺药物浓度的方法。
【参考文献】
[1]刘红光,佘键涛,康颖,等.循环应用低剂量环磷酰胺联合白细胞介素-2对乳腺癌荷瘤小鼠调节性T细胞及生存期影响[J].中南医学科学杂志,2013,41(4):353-356.
Liu HongGuang, She JianTao, KangYing,etal. Influence of cyclical administration with low-dose cyclophosphamide and interleukin-2 on regulatory T cells of murine breast cancer model and its life span[J].Med Sci J Central South China,2013,41(4):353-356.In Chinese with English abstract.
[2]王丹,刘春生,吕进,等.双位点微透析-HPLC联用平台的构建与评价[J].药学服务与研究,2015,15(2):123-125,154.
Wang Dan,Liu ChunSheng,Lü Jin,etal.Construction and evaluation of the on-line platform of double-site microdialysis combined with HPLC method[J].Pharm Care Res,2015,15(2):123-125,154.In Chinese with English abstract.
[3]Schuetze S M,Zhao L,Chugh R,etal.Results of a phase Ⅱ study of sirolimus and cyclophosphamide in patients with advanced sarcoma[J]. Eur J Cancer,2012,48(9):1347-1353.
[4]Li YanJun,Peris J,Zhong Li,etal. Microdialysis as a tool in local pharmacodynamics[J]. AAPS J, 2006,8(2):E222-E235.
[5]Darvesh A S,Carroll R T,Geldenhuys W J,etal.Invivobrain microdialysis: advances in neuropsychopharmacology and drug discovery[J]. Expert Opin Drug Discov,2011,6(2):109-127.
[修回日期]2015-06-06
[本文编辑]阳凌燕
Determination of cyclophosphamide in rat breast microdialysis fluid by HPLC-MS/MS method
HU ShuangShuang,LIU ChunSheng,TONG WeiHang,CAO Miao,WU Cheng,PENG Long,WANG Dan*
(Department of Pharmacy,Second Artillery General Hospital of PLA,Beijing 100088,China)
[ABSTRACT]Objective: To establish a HPLC-MS/MS method for the determination of cyclophosphamide concentration in rat breast microdialysis fluid.Methods:The analysis was performed on Cosmosil-C(18 )column(150 mm×4.6 mm,5 μm). The mobile phase was composed of 0.1% formic acid solution(A)-acetonitrile(B) in gradient elution at a flow rate of 1 ml/min,0-1 min A∶B=70∶30,1-1.5 min A∶B=60∶40,1.5-5.5 min A∶B=40∶60,5.5-8 min A∶B=70∶30.Selected positive ion multiple reaction monitoring(MRM) of m/z 261.3→140.1(cyclophosphamide) and m/z 189.2→104.0(internal standard antipyrine) was performed.Results:Calibration curves were linear over the range of 0.05-10 μg/ml for cyclophosphamide,the lowest detection limit was 0.05 μg/ml.Intra- and inter-day precisions were less than 15%.The results of accuracy and stability tests all met the requirements for the determination of biological samples. Conclusion:This method is sensitive and easy for operation,and could be used for the determination of cyclophosphamide in microdialysis samples.
[KEY WORDS]cyclophosphamide;content determination;microdialysis;chromatography,high performance liquid;mass spectrometry
[收稿日期]2014-12-11
DOI:10.5428/pcar20150314
[中图分类号]R927.2
[文献标志码]A
[文章编号]1671-2838(2015)03-0205-03
作者简介胡霜霜(女),硕士生,药师.E-mail:huss2008@126.com*通信作者(Corresponding author):王丹,E-mail:wdyy_618@sina.com
基金项目国家自然科学青年基金(81301662),中国博士后科学基金(2013M532151)

