鱼蛋白肽钙的分级及肽与钙的结合性能研究
范露,刘茹,熊善柏,*
(1.华中农业大学食品科技学院,湖北武汉430070;2.华中农业大学楚天学院食品与生物科技学院,湖北武汉430205;3.国家大宗淡水鱼加工技术研发分中心(武汉),湖北武汉430070)
鱼蛋白肽钙的分级及肽与钙的结合性能研究
范露1,2,刘茹1,3,熊善柏1,3,*
(1.华中农业大学食品科技学院,湖北武汉430070;2.华中农业大学楚天学院食品与生物科技学院,湖北武汉430205;3.国家大宗淡水鱼加工技术研发分中心(武汉),湖北武汉430070)
以白鲢采肉后的鱼骨为原料制备鱼蛋白肽钙,用无水乙醇分级分离得到6个级分:水不溶性级分CA、50%、60%、70%、80%、90%乙醇不溶性级分CB、CC、CD、CE、CF,采用红外分析法和葡聚糖凝胶色谱法等手段比较了各级分间的差异。结果表明:各级分中均含有一定量的肽和钙,6个级分可以归为3类:CA得率最高,水溶性最差,钙通过化学键与分子量较大的肽结合;CB、CC相似,得率最低,钙通过化学键与小肽或氨基酸结合;而CD、CE和CF三者相似,水溶性好,钙呈游离态,通过物理吸附作用与鱼蛋白肽结合。
鱼蛋白肽钙;分级;结合性能;红外分析法;葡聚糖凝胶色谱法
钙是人体中含量最多的矿质元素,具有构成骨骼和牙齿、维持神经肌肉正常活动、参与凝血等多项功能,对人体非常重要,而我国膳食结构以素食为主,含钙少,吸收差,因此补钙非常必要,通过改善膳食结构增加乳类摄入可以增加钙的摄入,但必要时必须通过钙制剂来补充机体钙质。
钙制剂经历了无机钙、有机酸钙和螯合钙3个阶段,氨基酸螯合钙和蛋白肽螯合钙以其稳定性好、吸收率高等特点备受关注[1]。氨基酸螯合钙研究较多,关于制备、结构鉴定、特性及应用等均有不少报道[2-4]。蛋白肽螯合钙多是以富含蛋白的原料通过水解制取多肽,再与钙盐反应制得螯合钙。而以蛋白水解产物为原料制备螯合物时,蛋白水解物本身就是一个复杂的体系,因此钙与肽的结合可能存在多种方式。杨燊[5]、夏松养[6]等采用酶水解南海低值鱼蛋白制备多肽复合物并制得多肽-钙螯合物,通过红外光谱分析推测钙离子与羧基以共价键的方式结合,并采用0%、50%和80%的乙醇对产物进行分级,结果表明未经乙醇沉淀的级分抗氧化活性最强;祝德义[7]研究了酶法水解动物皮制得的胶原多肽与Ca2+的结合行为,通过紫外光谱、红外光谱、扫描电镜等手段对结合产物进行初步表征,表明胶原多肽和Ca2+有一定的结合能力,且结合反应比较复杂,既有配位结合,又有离子键结合,还有吸附作用;Bao等[8]采用透析、凝胶色谱及红外对大豆水解液和钙离子生成的可溶性多肽钙进行研究,发现分子量在14.4 KDa和8 KDa~9 KDa的多肽与钙离子的结合能力最强,且钙与多肽的结合能力与羧基基团的含量线性相关。Jung等[9]在pH2.2醋酸环境下用胃蛋白酶水解鱼骨架,采用超滤和亲和色谱法分离出与钙离子亲和力最高的多肽,通过串联质谱仪分析得到与钙螯合程度最高的小肽分子序列,其与钙的结合能力与酪蛋白磷酸肽相当。
鱼骨是鱼糜制品加工中产生的主要下脚料,就常用的鲢鱼而言,在加工过程中鱼骨约占鱼体总重的10%,鱼头和鱼骨一起达到了40%[10],占整个下脚料的2/3[11]。鱼骨中不仅含有大量的钙磷,还含有丰富的蛋白质,将鱼骨加工制备鱼蛋白肽钙制剂可大大提高其附加值。本研究通过对鱼蛋白肽钙不同级分之间的比较,探寻各级分间的差异,为进一步研究其性质和应用提供依据。
1 材料与方法
1.1 材料与试剂
白鲢购于华中农业大学集贸市场;复合蛋白酶(6.49万U/g):诺维信天津公司生产;其他化学试剂均为分析纯。
1.2 仪器与设备
HH-6型数显恒温水浴锅:常州国华电器有限公司;DHG-9240A型电热恒温鼓风干燥箱:上海精宏实验设备有限公司;DJ550-A型绞肉机:沈阳市厨房设备厂;Avanti J-26型高速离心机:美国贝克曼公司;UV-2600型紫外可见分光光度计:Unico;NEXUS 470 FTIR型红外光谱仪:美国Nicolet公司。
1.3 方法
1.3.1 鱼蛋白肽钙的制备及分级

采用不同浓度乙醇梯度沉淀将反应产物分为6个级分。反应结束后,于5 000 r/min离心10 min,所得沉淀记为CA,上清液继续补充加入无水乙醇至体系乙醇浓度50%,于5 000 r/min离心10 min,所得沉淀记为CB,依次往前一次离心上清液中加入无水乙醇,使体系乙醇浓度分别达到60%、70%、80%、90%,离心所得沉淀依次为CC、CD、CE和CF。CA~CF各级分质量占合成产物总质量的比例即为该级分相对得率。反应前的鱼蛋白肽记为C0。
1.3.2 肽含量的测定
微量凯氏定氮法[12]。
1.3.3 钙含量的测定
GB/T-6436-2002 EDTA络合滴定法。
1.3.4 溶解率的测定
参考胡莉莉的方法[13]。
1.3.5 红外光谱分析
将样品于105℃烘干后与KBr在远红外快速干燥器下于玛瑙研钵中研细混匀,压片,在NEXUS-470型傅立叶变换红外光谱仪进行红外扫描。扫描范围4 000cm-1-400cm-1,仪器分辨率4cm-1,扫描次数32次。
1.3.6 肽钙分布测定
将样品配制成10 mg/mL的溶液,经0.45 μm的微孔滤膜过滤,用Sephadex G-25凝胶过滤层析,收集洗脱液,检测每管样品在280 nm下的吸光值,同时用1.3.3法测定每管中的钙含量,并以每次洗脱收集到的第1管的钙含量为基准,后续每管中的钙含量与第1管钙含量的比值即为钙相对含量。层析条件:上样量3 mL,洗脱液为0.02%迭氮化钠-0.9%氯化钠溶液,采用部分收集器收集,4.8 mL/管,6管/h。
1.3.7 数据处理
采用SAS和Excel软件进行处理。
2 结果与分析
试验所制备的鱼蛋白肽钙各级分经50℃烘干后均呈淡黄色晶体状,无异味,其中级分CD、CE和CF易吸潮结块。
2.1 鱼蛋白肽钙的基本组成
鱼蛋白肽钙分级后各级分的相对得率如表1所示。

表1 鱼蛋白肽钙各级分肽和钙含量(n=3,平均值±标准差)Table 1Content of peptide and calcium for every components(n=3,means±SD)
由表1可知,产物中级分CA所占比例最大,CD、CE和CF次之,级分CB和CC最少。在鱼蛋白肽钙分级过程中,未加乙醇时水不溶性成分沉淀下来,得到级分CA;实验过程中发现,乙醇浓度由0%增加到40%时,所沉淀产物极少,当乙醇浓度达50%时,部分产物被分离出来,即级分CB;乙醇浓度继续提高至60%时,此阶段获得的产物CC很少,所占比例最小;继续增大乙醇浓度至70%、80%、90%,醇不溶性成分逐渐被沉淀。
各级分的肽含量、钙含量及肽钙比例亦有差异。级分CA、CB、CC的肽含量较低,钙含量较高,肽钙比例小;级分CD、CE、CF肽含量较高,钙含量较低,肽钙比例较大。
2.2 鱼蛋白肽钙的溶解性
溶解性是钙制剂的一项重要质量指标。鱼蛋白肽钙各级分溶解率结果如图1所示。
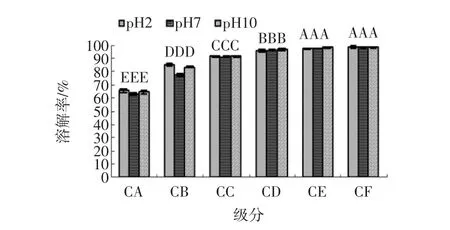
图1 鱼蛋白肽钙各级分溶解率(n=3)Fig.1 Ratio of dissolution for every components(n=3)
由图1可知,级分CA溶解性最差,级分CE和CF溶解性最好,在pH2、pH7和pH10中均几乎完全溶解。在分级过程中,随着体系乙醇浓度的增大,水溶性差的产物先沉淀,水溶性好的产物后沉淀,因此各级分溶解率随沉淀时所用乙醇浓度的增大而增大。此外,级分CA和CB的溶解率受pH影响较大。
2.3 鱼蛋白肽钙的红外光谱分析
图2是鱼蛋白肽和反应后鱼蛋白肽钙各级分红外光谱图。

图2 鱼蛋白肽钙各级分红外光谱图Fig.2 Infrared spectroscopy spectra of every components
反应前的鱼蛋白肽(C0)的谱图中位于3 300 cm-1吸收峰为蛋白质的N-H伸缩振动引起;位于1 660 cm-1吸收峰是由C=O伸缩振动引起,属于酰胺Ⅰ带;1590cm-1吸收峰为N-H面内弯曲产生,属于酰胺Ⅱ带,但部分为酰胺Ⅰ带所掩盖;1 410 cm-1伯酰胺C-N伸缩振动吸收峰,也称为酰胺Ⅲ带[7,14-16]。
与鱼蛋白肽C0相比,鱼蛋白肽钙各级分与之差异大小不一,从CA、CB、CC、CD、CE至CF,各级分与C0的差异逐渐缩小。加入Ca2+后,3 300 cm-1的N-H伸缩振动峰均有所加强;酰胺I带由1 660 cm-1红移至1 500 cm-1~1 400 cm-1不等;另外1 100 cm-1左右较弱的锯齿形吸收峰强度增大,CA最为明显,变为一光滑强峰,此峰为-NH2的面内摇摆振动,同时900 m-1左右的一个小吸收峰在CA、CB、CC中较明显,为N-H的面外弯曲振动,证明了CA中Ca2+与鱼蛋白肽结合紧密,其次是CB和CC。级分CD、CE和CF的红外图谱的峰形及峰强度与鱼蛋白肽C0较相似,推测其中钙与肽的相互作用可能比较微弱。
2.4 鱼蛋白肽钙的肽钙分布
鱼蛋白肽钙的肽钙分布结果见图3。
由图3肽钙分布图可知,根据肽与钙的相对出峰位置,6个级分的肽钙分布可归为3类:第一类是级分CA[图3(c)],该级分中钙的分布明显不同于游离钙[图3(a)],峰形尖而窄,出峰时间稍早于游离钙,且其尖峰恰好与肽的第一个峰重合,说明该级分中钙与大分子量肽段紧密结合,印证了红外分析结果;第二类包括CB[图3(d)]和CC[图3(e)]两个级分,该级分的钙出峰时间较晚,钙的峰值在肽的峰值之后,可能是钙与小肽或氨基酸结合在一起,而这些小肽或氨基酸在280 nm处并无吸收;第三类包括级分CD[图3(f)]、CE [图3(g)]和CF[图3(h)],这3个级分中虽然钙峰与肽峰部分重叠,但其中钙的峰形和出峰时间与游离钙[图3(a)]很相近,推断其中的钙与肽或氨基酸未形成化学键,而是以游离态存在,钙仅通过物理吸附作用

图3 鱼蛋白肽钙各级分肽钙分布图Fig.3 Peptide and calcium distribution of every components
而聚集在肽周围,结合力较弱,在凝胶色谱中二者分离开来,因此高浓度的乙醇沉淀下来的产物可能是肽和游离钙的混合物,这恰好解释了CD、CE和CF 3个级分的红外图谱与未经反应的鱼蛋白肽相差不大的原因。
3 结论
采用无水乙醇对鱼蛋白肽钙进行分级可获得CA、CB、CC、CD、CE和CF 6个级分,通过对各级分的相对得率、基本组成、水溶性、红外光谱分析和肽钙分布等的比较,发现各级分中均含有一定量的肽和钙,6个级分可归为3类:水不溶性的CA得率最高,水溶性最差,钙通过化学键与分子量较大的肽紧密结合;不溶于50%和60%乙醇的CB、CC相似,得率最低,钙通过化学键与小肽或氨基酸紧密结合;而不溶于70%、80%和90%乙醇的CD、CE和CF三者相似,水溶性好,钙呈游离态,通过物理吸附与鱼蛋白肽结合。本研究可为蛋白肽钙的分离和纯化提供依据。
[1]李翠芹,何腊平,仇保权.氨基酸螯合钙的研究进展[J].食品研究与开发,2011,32(10):162-164
[2]郭艳.水解米渣蛋白及制备氨基酸螯合钙的工艺研究[D].成都:四川大学,2006
[3]朱迎春.畜禽骨的综合利用及复合氨基酸螯合钙的开发研制[D].太原:山西农业大学,2005
[4]白建,朱迎春,梁锐萍,等.新型氨基酸螯合钙的研制[J].畜牧兽医科技信息,2005(11):75-76
[5]杨燊,邓尚贵,秦小明.低值鱼蛋白多肽-钙螯合物的制备和抗氧化、抗菌活性研究[J].食品科学,2008,29(1):202-206
[6]夏松养,谢超,霍建聪,等.鱼蛋白酶水解物的钙螯合修饰及其功能活性[J].水产学报,2008,32(3):471-477
[7]祝德义,李彦春,靳丽强,等.胶原多肽与钙结合性能的研究[J].中国皮革,2005,34(3):26-29
[8]Bao X L,Lv Y,Yang B C,et al.A study of the soluble complexes formed during clacium binding by soy-bean protein hydrolysates[J]. Food Chemistry,2008(10):1750-3841
[9]Won-Kyo Jung,Se-Kwon Kim.Calcium-binding peptide derived from pepsinolytic hydrolysates of hoki(Johnius belengerii)frame[J]. European Food Research and Technology,2007,224(6):763-767
[10]王建中,邓仁芳,朱瑞龙,等.淡水鱼鱼头与鱼骨的利用[J].食品科学,1994(2):47-50
[11]龚钢明,顾慧,蔡宝国.鱼类加工下脚料的资源化与利用途径[J].中国资源综合利用,2003(7):23-24
[12]张水华.食品分析[M].北京:中国轻工业出版社,2004:68-71
[13]胡莉莉,张正茂,郭蕾,等.球磨条件对水溶性大米淀粉理化特性的影响[J].食品科技,2007(8):94-97
[14]周元臻,魏永锋,张维平.壳聚糖-Ca(II)配位聚合物的合成及其性能表征[J].食品科学,2003,24(1):36-39
[15]谢晶曦,常俊标,王绪明.红外光谱在有机化学和药物化学中的应用(修正版)[M].北京:科学出版社,2001:298-321
[16]吴瑾光.近代傅里叶变换红外光谱技术及应用(下卷)[M].北京:科学技术文献出版社,1993:193-201
Studies on Classification of Fish Protein Peptides-calcium and Combination between Peptide and Calcium
FAN Lu1,2,LIU Ru1,3,XIONG Shan-bai1,3,*
(1.College of Food Science and Technology,Huazhong Agricultural University,Wuhan 430070,Hubei,China;2.College of Food and Biology Science and Technology,Chutian College,Huazhong Agricultural University,Wuhan 430205,Hubei,China;3.National R&D Branch Center For Conventional Freshwater Fish Processing(Wuhan),Wuhan 430070,Hubei,China)
Fish protein peptides-calcium was prepared from silver carp bone.It was divided into six components:deposit after reaction component CA,deposit in 50%,60%,70%,80%and 90%alcohol solution called CB,CC,CD,CE and CF,respectively.Meanwhile,the differences of the components were inspected with the method of IR and Sephadex.Both peptide and calcium existed in every components.And the six components can be cataloged as three kinds.The CA possessed highest yield and the poorest water-soluble capacity.Ca2+was combined with polypeptide by chemical bond in CA.The yield of CB and CC was the lowest. Ca2+was combined with micromolecular peptide or amino acid by chemical bond in CB and CC.The other components(CD,CE and CF)possessed the highest water-soluble capacity.Ca2+existed in free state or was combined with peptide by physical adsorption.
fish protein peptides-calcium;classification;combination;infrared spectroscopy;sephadex chromatography
2013-12-24
10.3969/j.issn.1005-6521.2015.02.002
现代农业产业技术体系建设专项资金(CARS-46-23)
范露(1982—),女(汉),讲师,硕士,研究方向:食品大分子提取及应用。
*通信作者:熊善柏(1963—),男(汉),教授,硕士,研究方向:水产品加工及贮藏工程。

