猪皮胶原肽-锌螯合物的制备工艺研究
吴家劲,边智杰,朱悦,张学涛,庞荔丹,高鹏
(山东中医药大学 药学院,山东 济南 250355)
猪皮为猪科动物的皮肤,可药食两用。在工业应用中,由于猪皮存在必需氨基酸的构成欠缺、人体条件下难消化、蛋白质生物效价低等缺点[1],除一部分应用于皮革生产外,猪皮原料只有20%转化为成品,其他大部分都变成了固体废弃物,这极大地浪费了资源,并且严重污染环境[2]。猪皮蛋白质含量丰富,降解后形成的胶原多肽,不仅具有较高的消化吸收性,还有保护胃黏膜以及降血压、抗溃疡、提高骨骼强度、促进皮肤胶原代谢等生理功能[3]。
锌是人体必需的微量元素之一,对人体健康状况有重要的调控作用,被医学和营养学界誉为“智能元素”[4]。锌与小肽螯合形成的小肽螯合锌具有特殊的单环螯合结构,与氨基酸螯合锌相比,小肽螯合锌更利于吸收,且稳定性更强,具有良好的补锌、抗菌、抗氧化以及提高机体免疫力的效果[5-7],极大提高了生物学效价。
目前肽-锌螯合物的研究大多集中在水产动物蛋白与锌的螯合物上,主要有牡蛎肽锌螯合物[8]、罗非鱼鳞胶原肽锌螯合物[9]、克氏原螯虾壳肽锌螯合物[10]、细点圆趾蟹肉酶解肽锌螯合物[11]、鲢鱼蛋白小肽锌螯合物[12]等,但是对猪皮胶原肽螯合锌的研究较少。
本研究以猪皮为原料,采用响应面法对猪皮胶原肽(以下简称猪皮肽)和硫酸锌的螯合工艺进行考察优化,旨在进行猪皮的深入开发研究,为今后的猪皮高值化加工利用提供理论基础。
1 仪器与材料
1.1 试验仪器
PHB-4型pH计(上海雷磁仪器有限公司);HH-2型数显恒温水浴锅(上海力辰邦西仪器科技公司);RE-52型旋转蒸发器(上海亚荣科技有限公司);FC5513型高速离心机(上海奥豪斯离心机有限公司);JB-2型恒温磁力搅拌器(上海雷磁仪器有限公司);HX-10型真空冷冻干燥机(上海圣科仪器有限公司);UV-1780紫外可见分光光度计(日本岛津仪器有限公司)。
1.2 试验材料
新鲜猪皮(济南金锣肉食厂);碱性蛋白酶(2000 U/mg)、菠萝蛋白酶(2000 U/mg)(上海佛森生物科技有限公司);牛血清白蛋白(上海源叶生物科技有限公司);其他试剂均为国产分析纯。
2 试验方法
2.1 猪皮肽的制备
猪皮肽的制备方法参照文献[13]。
2.1.1 去杂
取新鲜猪皮,刮去皮下杂质,-10 ℃冷冻24 h,剪刀剪成碎块(D≤2 mm、L≤1 cm)。
2.1.2 脱脂
取猪皮碎块,加入5倍量(即猪皮碎块质量的5倍)且质量分数为0.3%的氢氧化钠溶液脱脂8 h,滤去碱液,水洗至近中性,得脱脂猪皮。
2.1.3 酶解
脱脂猪皮匀浆8 min,加8倍量水加热煮沸15 min,冷却至55 ℃,转移至旋转蒸发器,加入脱脂猪皮质量1%的碱性蛋白酶,55 ℃保温酶解1 h,后加入1%菠萝蛋白酶,55 ℃保温酶解3 h,酶解液加热煮沸15 min灭酶,过滤,滤液冷藏约12 h,离心,取上清液减压浓缩,冷冻干燥后即得猪皮酶解原液冻干粉。
2.2 酶解原液冻干粉肽含量的测定
采用福林酚比色法[14],以牛血清白蛋白溶液为对照品,记录对照品浓度和吸光度,数据进行线性回归分析,计算冻干粉中的胶原肽质量分数。标准曲线为Y=16.883X+0.229 6(R2=0.993 8),计算得猪皮肽的质量分数为66.92%。
2.3 螯合工艺
螯合工艺为:新鲜猪皮→猪皮酶解液→猪皮肽→测肽含量→调pH→加一定比例硫酸锌→恒温持续搅拌螯合→无水乙醇沉淀→离心→定温减压干燥→肽锌螯合物。
2.4 猪皮肽-锌螯合单因素试验




2.5 猪皮肽-锌螯合响应面试验设计
在单因素试验基础上,使用Design-Expert.V8.0.6.1软件,进行4因素3水平的响应面分析试验,以螯合率为指标,考察猪皮肽-锌质量比(x1)、螯合pH(x2)、螯合温度(x3)、螯合时间(x4)对螯合工艺的影响。响应面试验因素水平编码见表1。

表1 响应面试验因素水平编码表Table 1 Response surface method factor level
2.6 螯合率的测定
采用乙二胺四乙酸(EDTA)络合滴定法[15]。称取一定量的猪皮肽螯合锌粉末,置于100 mL烧杯中,加50 mL水和数滴6 mol/L的盐酸,超声至溶解完全,冷却定容至100 mL,取10 mL于三角瓶,加入10 mL NH3-NH4Cl( pH=10)缓冲液,铬黑T指示剂2~3滴,用0.02 mol/L Na2EDTA溶液滴定至由酒红色变为蓝色,记录滴定消耗毫升数,每份样品溶液平行测定3次,取平均值,计算锌离子螯合率。

(1)

(2)
式中:M1为小肽螯合锌中锌离子的质量;c为EDTA标准溶液浓度,mol/L;V0为空白试验消耗Na2EDTA的体积,mL;V1为测定时平均消耗Na2EDTA的体积,mL。
3 结果与分析
3.1 单因素试验结果分析
3.1.1 螯合温度对螯合率的影响
由图1可知,温度升高,螯合率先增加后减小;0~50 ℃时,两者呈正相关关系,最适温度在50 ℃附近,此时螯合率最大;大于50 ℃,温度升高,螯合率随之减小,可能因温度偏高,致使部分螯合物结构稳定性[16]变差,部分螯合物分解使螯合率有所下降,所以最佳螯合温度为50 ℃。

图1 螯合温度对螯合率的影响Fig. 1 Effect of temperature on chelating rate
3.1.2 螯合时间对螯合率的影响
由图2可知,随着反应的进行,螯合率先迅速增大后趋于不变。在0~50 min范围内,肽锌反应物浓度和接触面积都比较大,所以前期反应速度较快;但随着反应物浓度的下降,反应逐渐接近饱和,所以反应后期螯合率趋于不再增加,说明50 min时螯合反应已基本完成。在螯合时间为50 min时,螯合率趋于平稳,可作为最佳螯合时间。

图2 螯合时间对螯合率的影响Fig. 2 Effect of time on chelating rate
3.1.3 螯合pH对螯合率的影响
由图3可知,pH增大,螯合率随之先上升后下降。pH<7.0时,螯合率随pH增大一直增加,在pH=7.0时,螯合率最大。当pH>7.0时,锌离子会发生沉淀,导致游离的锌离子减少,因此螯合率随pH增大一直减小。由此可见,肽锌螯合物的等电点可能在pH=7.0附近,此时酸碱对螯合物的影响较小[17],所以最佳螯合pH为7.0。

图3 螯合pH对螯合率的影响Fig. 3 Effect of pH on chelating rate
3.1.4 猪皮肽-锌质量比对螯合率的影响

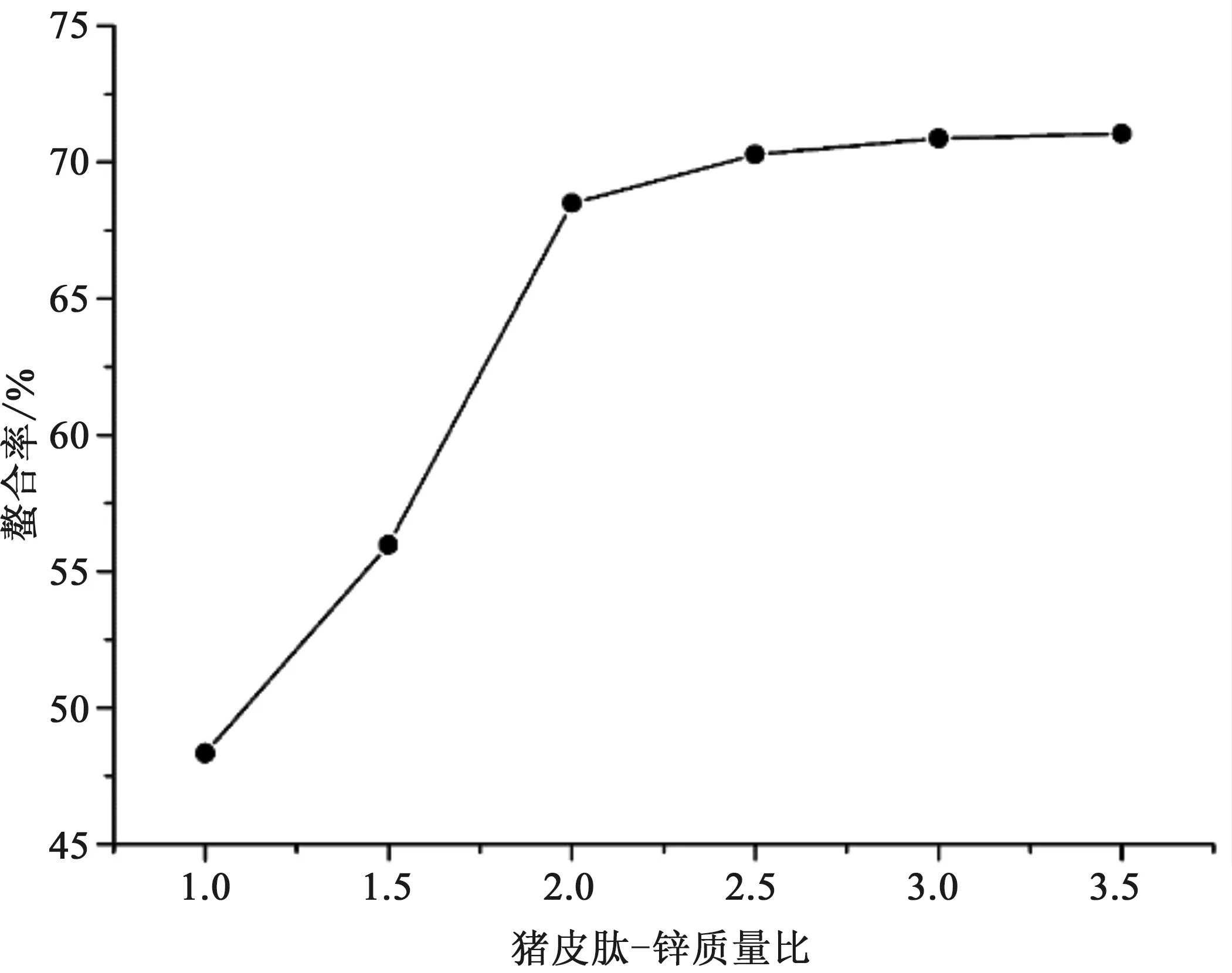
图4 猪皮肽-锌质量比对螯合率的影响Fig. 4 Effect of mass ratio of pigskin peptide and zinc on chelating rate
3.2 猪皮肽-锌螯合工艺响应面优化试验
3.2.1 响应面试验结果与方差分析
根据 Box-Benhnken试验设计原理,以肽锌螯合率为响应指标,以螯合肽-锌质量比(x1)、pH(x2)、温度(x3)、时间(x4)为响应变量,进行响应面优化试验,响应面组合试验设计及结果见表2,方差分析见表3。
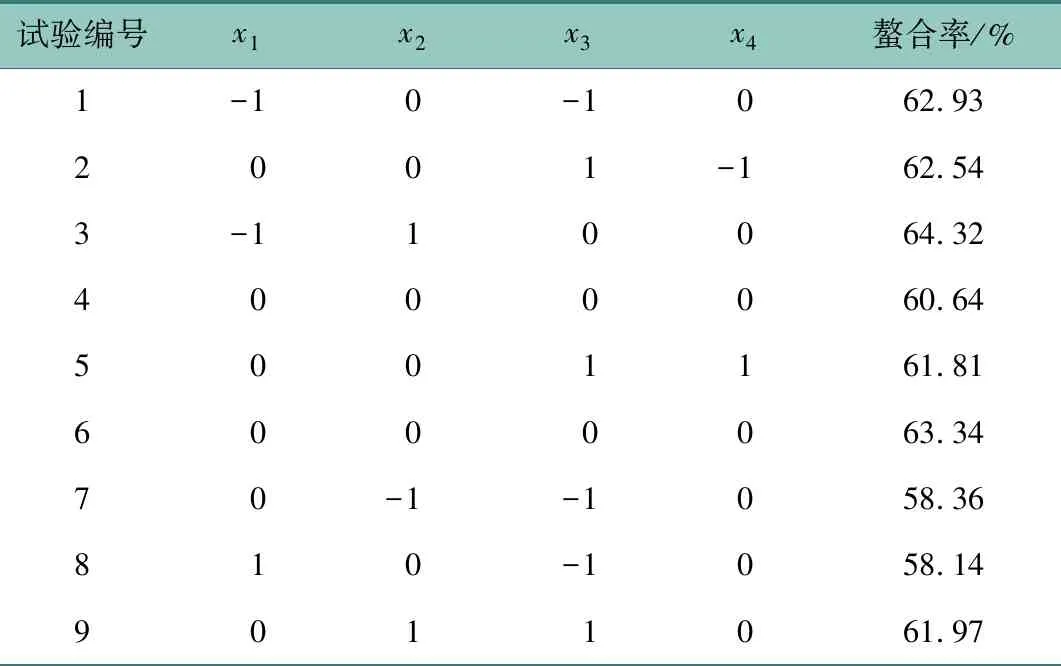
表2 响应面组合设计试验及结果Table 2 Design and result of response surface method combination

续表2

表3 回归模型方差分析结果Table 3 Variance analysis results of regression model
注:P<0.05,表明差异显著;P<0.01,表明差异极其显著。
4个因素与指标螯合率之间的响应面回归模型为:y=69.32+4.30x1-4.19x2+2.98x3+2.26x4-2.18x1x2+0.28x1x3+0.35x1x4+0.44x2x3-0.39x2x4+0.45x3x4-9.22x12-9.15x22-6.34x32-4.31x42。
由表3可知,模型P<0.000 1,表示该模型极显著,失拟项P=0.073 1>0.05差异不显著,回归模型无失拟因素。模型R2=0.964 2,证明响应面回归模型与实际试验拟合度较高,模型预测值与试验实际测量值相关性较好,各因素与响应值螯合率之间存在显著的线性关系,可用于猪皮胶原肽-锌螯合工艺的分析预测。各因素中一次项x1、x2、x3、x4均为显著影响(P<0.05),其中猪皮肽-锌质量比和pH对螯合率的影响最为显著,各因素对螯合率影响程度由大到小的顺序为:猪皮肽-锌质量比,pH,温度,时间。二次项x12、x22为极显著影响(P<0.000 1),二次项x32、x42为显著影响(P<0.05),交互项x1x2、x1x3、x1x4、x2x3、x2x4、x3x4的交互作用对螯合率的影响不是很显著。
3.2.2 响应面分析

图5 各因素对螯合率影响的响应曲面Fig. 5 The response surface for the chelating rate affected by various factors



由图5(d)可知,螯合pH与螯合温度两因素有较强的交互作用,螯合pH对螯合率的影响显著。螯合pH对响应值的影响大于螯合温度。随着螯合pH和螯合温度的增加,螯合率逐渐增大然后减小。这与肽-锌螯合物的等电点和稳定性有关,pH大于或小于7.0都不利于猪皮胶原肽-锌螯合物的生成。所以当螯合pH 7.0,螯合温度50 ℃时,螯合率达到最大值。
由图5(e)可知,螯合pH与螯合时间两因素有一定的交互作用,螯合pH对螯合率的影响较显著。螯合pH对响应值的影响大于螯合时间。随着螯合pH和螯合时间的增加,螯合率逐渐增大然后减小,这与肽-锌螯合物的等电点和螯合过程中水分的蒸发有关。当螯合pH 7.0,螯合时间50 min时,螯合率达到最大值
由图5(f)可知,螯合温度与螯合时间两因素交互作用不显著,对螯合率的影响作用较小。螯合温度对响应值的影响大于螯合时间。随着螯合温度和螯合时间的增加,螯合率逐渐增大然后减小,这与肽-锌螯合物的稳定性和螯合过程中水分的蒸发有关。当螯合温度50 ℃,螯合时间50 min时,螯合率达到最大值。
综合图5(a~f)可知,猪皮肽-锌质量比和螯合pH对螯合率的影响最为显著,螯合时间和温度对螯合率的影响相比较小,猪皮肽-锌质量比和pH过高或过低都会导致螯合率降低,这与方差分析结果一致,表明模型显著可行。
3.3 最佳螯合工艺验证试验
4 结论

致谢:本文在山东中医药大学创新训练平台上完成。感谢山东中医药大学的支持与帮助,感谢姜珊和王常噒的指导。

