基于粉末X射线衍射技术的固体制剂晶型定性分析*
杨世颖,邢逞,张丽,孙加琳,杜冠华,吕扬
(北京协和医学院&中国医学科学院药物研究所1.晶型药物北京市重点实验室;2.药物靶点研究与新药筛选北京市重点实验室,北京 100050)
现代化学药物发展经历了由多组分用药到单一组分用药、由低化学纯度到高化学纯度、由消旋体到手性药物的发展历程。目前,即便在药学家确保了化学药物的成分物质、化学纯度、结构手性等诸多因素后,仍可发现药品存在的临床疗效作用与药品质量间的差异。近年来,大量研究逐渐认识到药用的晶型物质状态变化是导致其差异的重要因素之一[1-3]。因此,对固体药物的多晶型研究与对药品的晶型质量控制越来越受到国内外制药企业、药政管理机构、药品检验机构的重视。药物制剂是药物发挥临床治疗作用的载体,因此对于固体制剂中的原料药晶型的质量控制成为不可忽视的重要技术环节。我国现行的《化学药物制剂研究基本技术指导原则》中就明确指出晶型药物的药物制剂应避免对其原料药晶型产生影响改变[4]。
目前用于原料药的晶型检测分析技术有多种,包括单晶X射线衍射、粉末X射线衍射、差示扫描量热、热重分析、红外光谱、拉曼光谱、固态核磁、显微分析等[5-8],均为基于单一化学成分的药物不同晶型状态的检测分析表征方法。但是固体制剂属复杂的多组分物质,若要实现固体制剂中的原料药晶型鉴别,对检测技术和方法的要求更加苛刻和困难。已有的文献报道对该方面研究也鲜少涉及[9-11]。
笔者采用粉末X射线衍射技术[13-14],基于物相分析方法,其衍射图谱依赖于样品的物质组成与各个成分含量的叠加关系;选择尼莫地平、罗红霉素2个药物品种,建立适用于固体制剂中晶型原料药的晶型有效鉴别分析方法,突破人们对固体制剂中原料药的晶型状态鉴别的技术难题,为晶型药物的质量控制提供关键技术支撑。
1 仪器与试药
1.1 仪器及条件 D/max-2550型粉末X射线衍射仪(日本理学Rigaku);实验条件设置:CuKα辐射,石墨单色器,管压 40 kV,管流 150 mA,2 θ扫描范围 3 ~80°,扫描速度 8°·min-1,步长 0.02°,发散狭缝 DS=1°,防散射狭缝 SS=1°,接收狭缝 RS=0.15mm。XS-105型十万分之一电子天平[瑞士梅特勒-托利多仪器(上海)有限公司];感量0.01 mg。
1.2 试药 研究用样品均为国家药典委员会与山东省药品检验所协助征集,包括5个生产厂家的尼莫地平、6个生产厂家的罗红霉素不同批号固体制剂及相应空白辅料样品。尼莫地平与罗红霉素试验样品信息见表1~2。
2 方法与结果
2.1 物相分析原理 任何一种物质在特定波长X射线照射下,都会给出特有的衍射指纹图谱,图谱衍射峰强度与物质成分质量成正比,根据粉末X射线衍射原理,对于单相物质,其衍射强度可以以公式(1)表示。
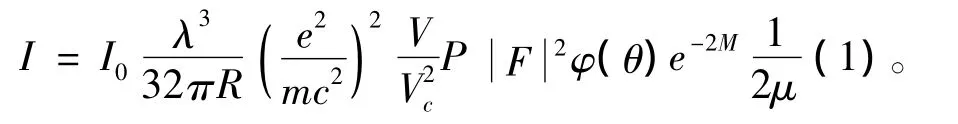
式中I0为入射X射线的强度,λ为入射X射线的波长,R为试样到观测点之间的距离,V为被照射晶体的体积,Vc为单位晶胞体积,P为多重性因子,F为结构因子,μ为线性吸收系数,φ(θ)为角因子,e-2M为温度因子。
粉末X射线衍射属物相分析方法,对于多组分物质,其衍射强度与各组分的衍射强度及其质量分数相关,多组分物质的衍射图谱是由所含各单组分物质衍射图谱的物理叠加而成[14-15]。
2.2 制剂样品的晶型分析 药物固体制剂是由药物原料与空白辅料按照处方比例混合而成的多相物质,属复杂成分体系。根据粉末X射线衍射物相分析原理,固体制剂样品在某个特定的2 θ或d值位置的衍射峰强度值是原料药与多种辅料的贡献之和,即I固体制剂=I原料药+I空白辅料。
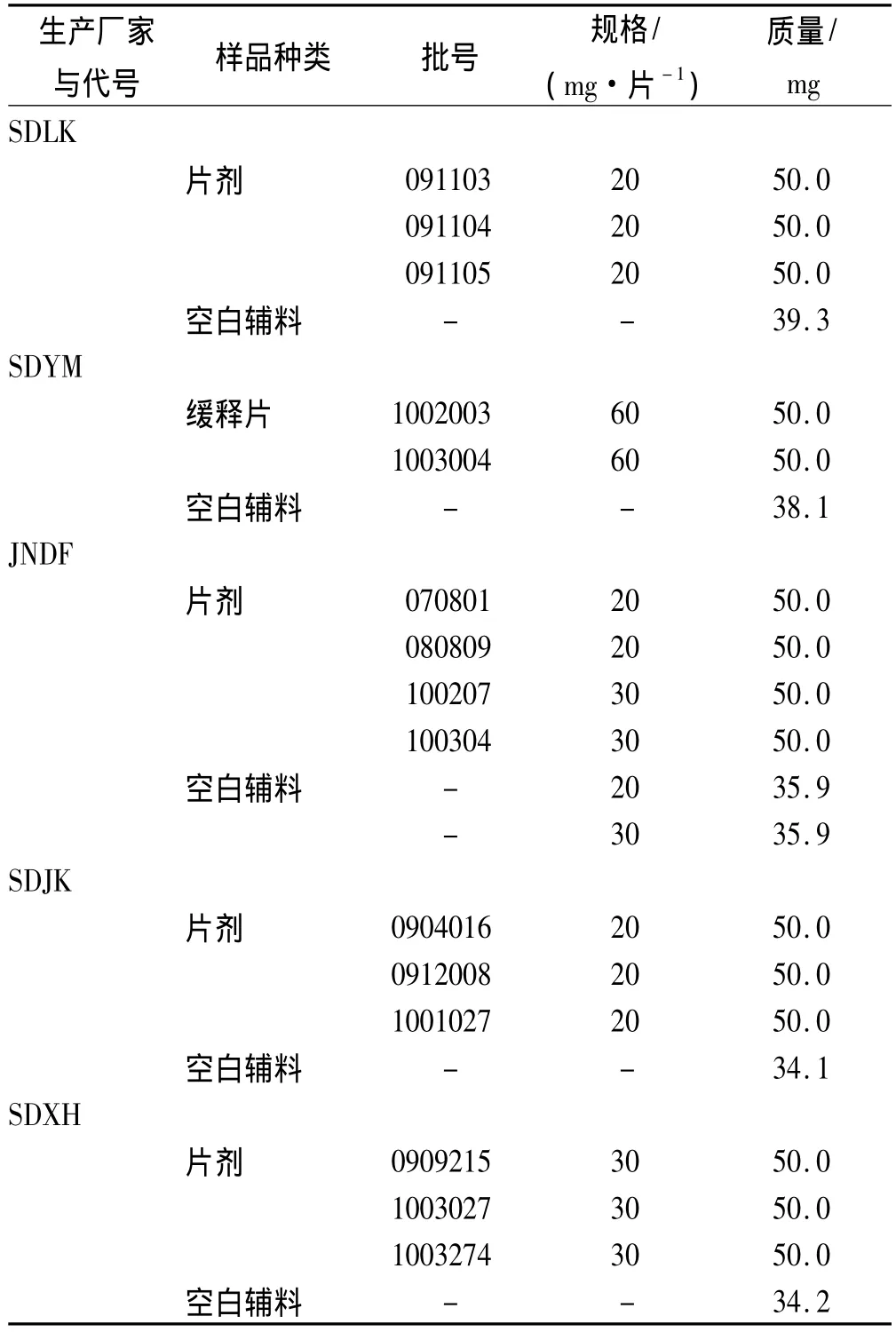
表1 尼莫地平实验样品信息Tab.1 Information of nimodipine samples
因此,若要获得原料药晶型的单相物质存在状态,需消除空白辅料等多相物质的干扰。笔者依据上述原理,建立了粉末X射线衍射固体制剂晶型分析的定性鉴别方法,通过定量检测和空白辅料物相扣除技术,从而获得固体制剂中的原料药晶型物质状态图谱数据,并与晶型标准图谱比对。
建立实验方法的具体步骤:
步骤1:实验样品质量计算。晶型原料量、空白辅料量及固体制剂量分别以a、b、c表示,则以固体制剂按照50 mg进样量,根据处方制剂配比计算实验用晶型原料量(a)与空白辅料量(b):空白辅料量(b)=固体制剂量(c)-晶型原料量(a)(2)。其中,晶型原料量(a)=固体制剂量(c)×制剂规格/制剂质量。
步骤2:实验样品制备与称量。实验样品均经研磨过100目筛[筛孔内径(150±6.6)μm]待用,其中固体制剂应首先去除包衣或胶囊壳后再进行研磨过筛。
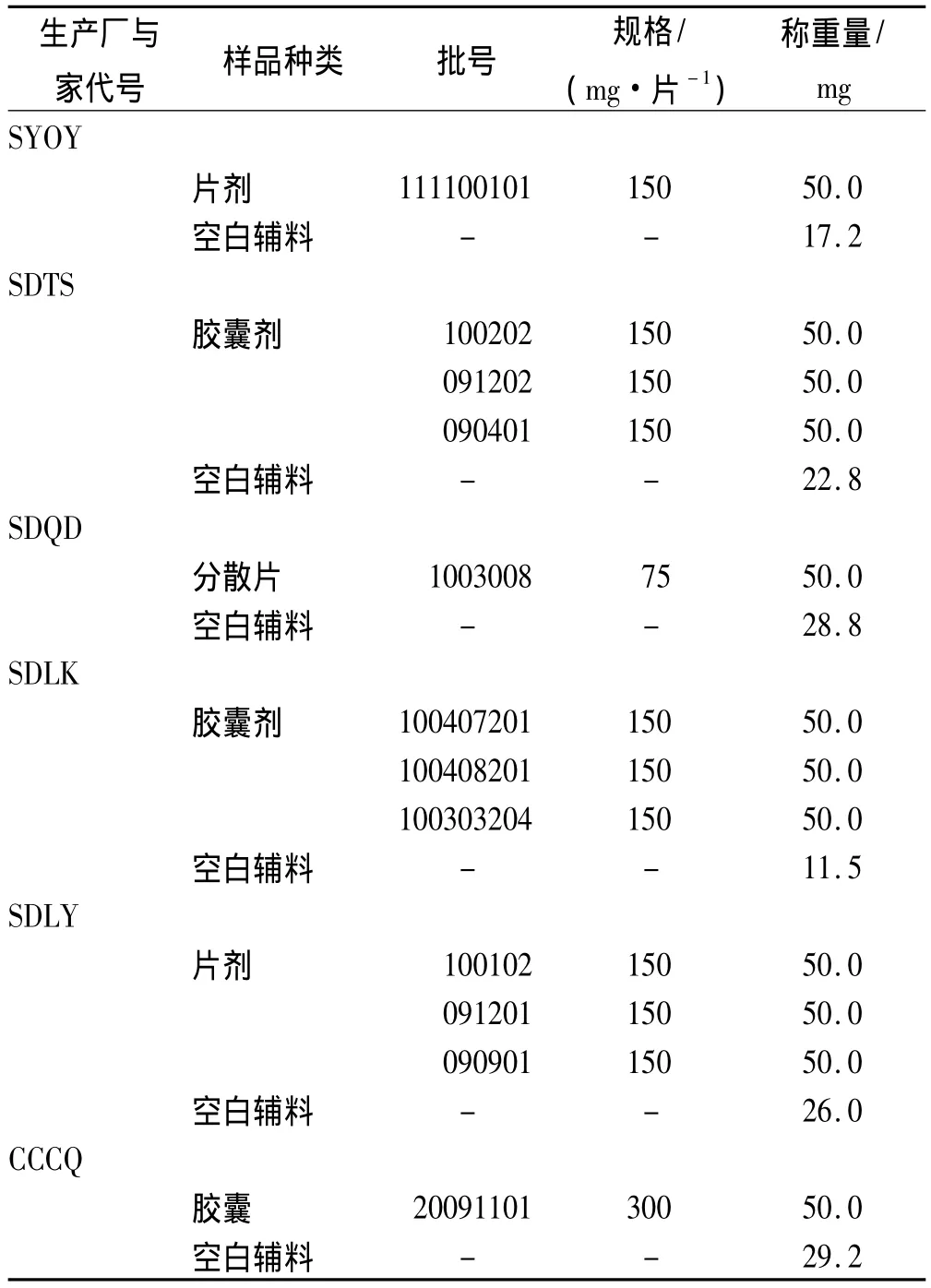
表2 罗红霉素实验样品信息Tab.2 Information of roxithromycin samples
本文定量称取:①晶型原料对照品50 mg,②固体制剂样品50 mg,③ 按步骤1中的式(2)定量称取空白辅料量,作为待测样品。样品实际称重量见表1,2。
步骤3:衍射实验。分别摄取各待测样品的粉末X射线衍射图谱。
步骤4:制剂中原料的晶型图谱计算。采用Origin软件,用固体制剂衍射图谱数据扣除空白辅料衍射图谱数据后计算获得制剂中原料药晶型的粉末X射线衍射图谱。罗红霉素样品晶型定性分析过程实例见图1。
步骤5:将步骤4获得制剂中原料药晶型的衍射图谱与原料药晶型对照图谱进行比对实现定性鉴别目的。
2.3 制剂晶型分析结果 ①尼莫地平:对5个厂家生产的15批尼莫地平固体制剂样品进行研究,分析其固体制剂中原料药的晶型物质存在状态,图2所示为尼莫地平晶型标准图谱与15批尼莫地平固体制剂中原料药的晶型状态图谱。尼莫地平不同批次固体制剂样品的晶型分析结果见表3。
结果表明,国产15批尼莫地平固体制剂样品中原料药分别以晶A型与晶B型两种状态存在,其中3个企业(SDLK-091104、SDYM-1003004、SDJK-0912008)生产的尼莫地平药品中原料药主成分为晶A型;两个企业(SDLK-091103和SDYM-1002003)生产的尼莫地平药品中原料药呈晶A型与晶B型混晶状态;其余批次尼莫地平样品,其原料药主成分为晶B型。
(2)罗红霉素:对6个厂家生产的12批罗红霉素固体制剂样品进行研究,分析其固体制剂中原料药的晶型物质存在状态,图3所示为罗红霉素晶型标准图谱与不同批次罗红霉素固体制剂中原料药的晶型状态图谱。罗红霉素不同批次固体制剂样品的晶型分析结果见表4。
结果表明,被测的12批罗红霉素固体制剂样品中的原料药亦存在两种晶型状态,其中一个生产企业(CCCQ-20091101)罗红霉素药品中原料药为晶B型,其他制剂样品中原料药晶型物质状态均为晶A型。
2.4 晶型对生物学影响 采用大鼠固体给药方式,评价尼莫地平和罗红霉素各2种晶型样品在大鼠体内的吸收特征,以阐明不同晶型状态对药物生物学的影响。图4为大鼠经固体分别给予尼莫地平和罗红霉素不同晶型成分后的体内血药浓度曲线。
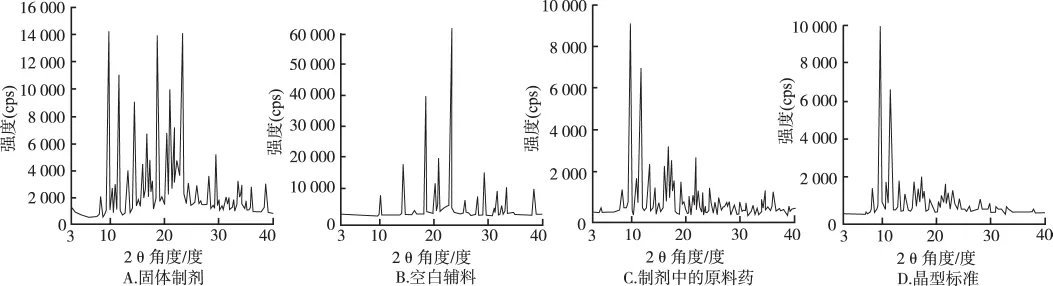
图1 罗红霉素SDQD-1003008批样品的晶型定性分析过程Fig.1 Qualitative analysis process of polymorphs in roxithromycin of batch of SDQD-1003008
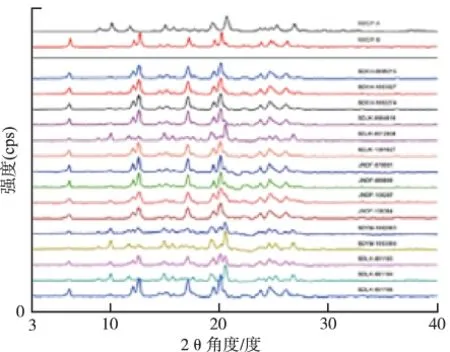
图2 不同批次尼莫地平固体制剂中原料药的晶型状态图谱Fig.2 Powder X Ray Diffraction patterns of active pharmaceutical ingredients in different batches of nimodipine as solid preparations
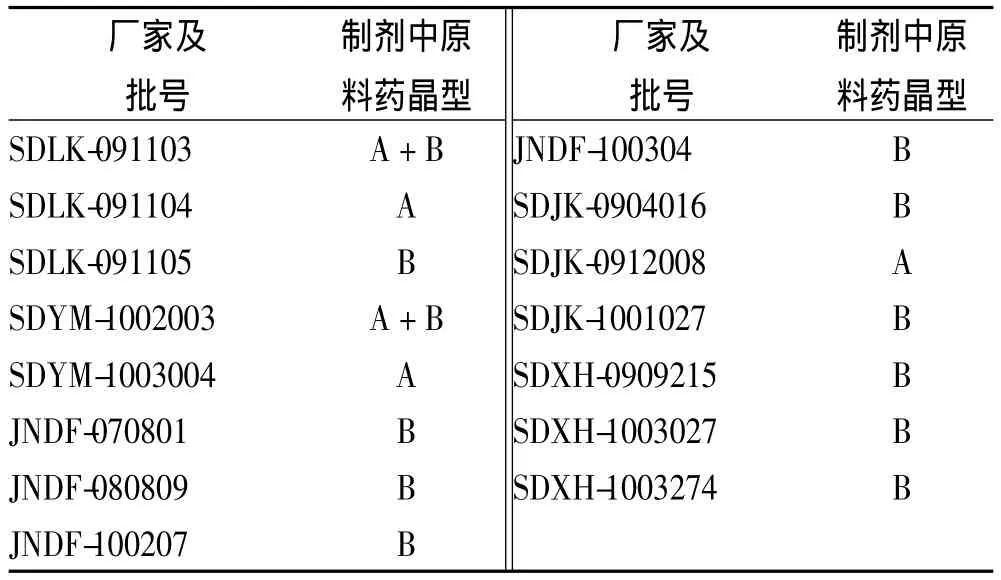
表3 尼莫地平固体制剂样品的晶型分析结果Tab.3 Analysis results of polymorphs of nimodipine samples as solid preparations
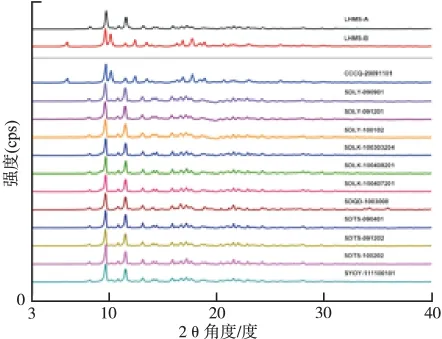
图3 不同批次罗红霉素固体制剂中原料药的晶型状态图谱Fig.3 Powder X Ray Diffraction patterns of active pharmaceutical ingredients in different batches of roxithromycin as solid preparations
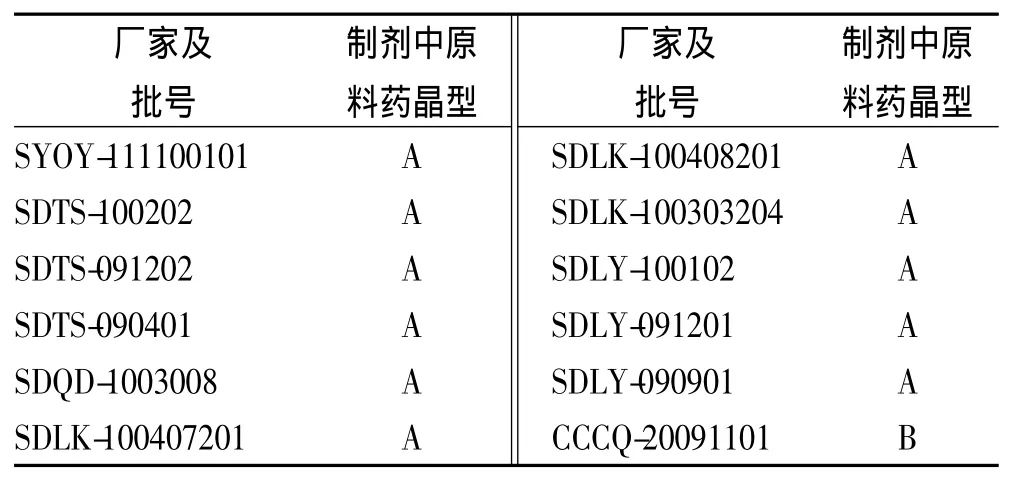
表4 罗红霉素固体制剂样品的晶型分析结果Tab.4 Analysis results of polymorphs of roxithromycin samples as solid preparations
整体动物生物学实验结果表明,尼莫地平和罗红霉素2种晶型在体内的生物吸收均存在显著差异,若使用其不同晶型物质作为药用晶型成分,则会导致其药品在临床应用中的治疗作用存在差异。
3 讨论
由于固体制剂组成成分复杂,如何实现对制剂中原料的晶型状态鉴别,一直是困扰国际药学的技术难题。
笔者在本实验中采用现代粉末X射线衍射分析技术,使用物相分析方法,以上市药品作为研究对象,成功实现了药品制剂中原料晶型状态的定性鉴别分析目的。
通过对5个厂家生产的15批尼莫地平固体制剂样品研究发现,制剂中使用的原料药晶型有三种,即晶A型、晶B型、晶A型+晶B型的混晶。通过对6个厂家生产的12批罗红霉素固体制剂样品研究发现,制剂中使用的原料药晶型有两种,即晶A型、晶B型。
研究发现,国产同一制药企业生产的不同批次产品的晶型状态不同,不同制药企业生产的同一品种晶型物质状态亦不同,说明已上市药品的晶型质量不可控。
整体动物生物学实验结果表明,尼莫地平和罗红霉素使用的晶型物质状态不同,可以导致药品临床治疗作用差异。
本研究提示,已经上市的药品若存在多晶型现象,应增加对其晶型质量控制标准和方法,否则药品的质量和临床作用将无法控制。
笔者对《中华人民共和国药典》2010年版收载的化学药物研究发现,百余个品种存在多晶型现象而无晶型质控要求,药物的多晶型现象及晶型质量控制已经成为制约我国药品质量不可忽视的重要科学问题,亟待解决。
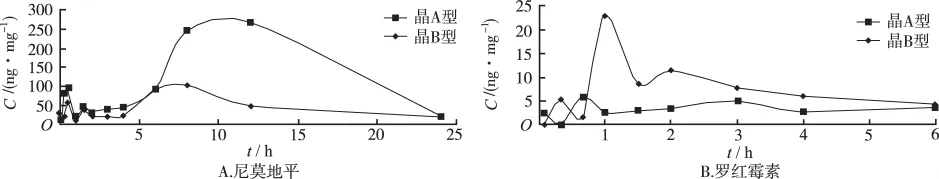
图4 尼莫地平与罗红霉素不同晶型在大鼠体内的血药浓度曲线Fig.4 Plasma concentration-time curves of polymorhps of nimodipine and roxithromycin in rats
(志谢:感谢国家药典委员会张慧燕、韩鹏和山东省食品药品检验研究院谢元超、刘广祯在样品征集过程中所做的贡献!)
[1]吕扬,杜冠华.晶型药物[M].北京:人民卫生出版社,2009:2-7.
[2]胡帆,赵睿,张丽,等.盐酸伐昔洛韦多晶型的溶解性质与药动学研究[J].医药导报,2012,31(11):1396-1400.
[3]吴媛媛,靳桂民,杜冠华,等.左氧氟沙星4种晶型的大鼠体内药动学研究[J].医药导报,2014,33(11):1407-1411.
[4]杜冠华,吕扬.固体化学药物的优势药物晶型[J].中国药学杂志,2010,45(1):1115-1120.
[5]冒莉,郑启泰,吕扬.固体药物多晶型的研究进展[J].天然产物研究与开发,2005,17(3):371-375.
[6]陈桂良,李君婵,彭兴盛,等.药物晶型及其质量控制[J].药物分析杂志,2012,32(8):1503-1508.
[7]BRITTAIN H G.Polymorphism in Pharmaceutical Solids[M].New York:Marcel Dekker,1999:227-278.
[8]马乐伟,杜葳,赵春顺.药物晶型定量分析方法的研究进展[J].药学学报,2011,46(8):896-903.
[9]吕丽娟,陈华,鲁靖睿,等.托伐普坦的晶型研究[J].现代药物与临床,2013,28(6):832-837.
[10]龚俊波,王琦,董伟兵,等.药物晶型转化与控制的研究进展[J].化工学报,2013,64(2):385-392.
[11]张娜,黄海伟,林兰,等.心血管系统治疗药物的晶型研究进展[J].现代药物与临床,2013,29(6):690-694.
[12]谢晓霞,杨建云,肖炳坤,等.X射线衍射法研究药物多晶型应用进展[J].现代科学仪器,2013,(2):8-12.
[13]常颖,郑启泰,吕扬.X射线衍射分析技术在药物研究中的应用[J].物理,2007,36(6):452-459.
[14]黄继武,李周.多晶材料X射线衍射-实验原理、方法与应用[M].北京:冶金工业出版社,2012:95-96.
[15]贾春晓.仪器分析[M].郑州:河南科学技术出版社,2009:294-295.

