205例药品不良反应报告分析
翟爱华 张 白 王 琦
济南市第五人民医院药剂科,山东 济南 250022
药品具有双重性,既可“治”病也可“致”病,既有治疗作用也有不良反应。药品不良反应(ADR)是指合格药品在正常用法用量下出现的与用药目的无关的有害反应[1]。为了解济南市第五人民医院(以下简称“我院”)ADR发生的特点和规律,探讨ADR发生机制,预防和减少ADR的发生,保证患者用药安全,现对我院2013年上报国家药品不良反应监测网的ADR患者进行回顾性分析,现报道如下:
1 资料与方法
通过国家药品不良反应监测系统检索我院2013年1~12月上报的ADR患者205例,对患者的年龄及性别、涉及药品、给药途径、ADR累及器官或系统等情况采用Excel和手工筛选方式进行回顾性统计、分析。
2 结果
2.1 发生ADR的患者性别与年龄分布
205例ADR报告中,男51例(24.88%),女154例(75.12%);年龄最小2个月,最大92岁。发生ADR患者年龄与性别分布见表1。
2.2 引起ADR的给药途径分布
205例ADR报告中,引起ADR的主要给药途径为静脉给药,共188例(91.71%);其次为口服给药11例(5.36%)。引起ADR的该药途径分布见表2。

表1 发生药品不良反应患者的年龄与性别分布(例)

表2 引起药品不良反应的给药途径分布
2.3 ADR涉及的药品种类分布
引起ADR的可疑药物按照其药理作用进行分类,总共包含12类、65个品种,其中,抗感染药物包括13个品种,居首位(20.00%);抗感染药物同时居ADR上报例数首位,共计80例(39.02%)。各类药物品种数及ADR上报例数统计见表3。

表3 药品不良反应涉及药物品种数及上报例数
2.4 ADR涉及药品分布
ADR发生例数以大环内酯类药物阿奇霉素最多,涉及药品排序前10位分布情况见表4。
2.5 ADR累及器官或系统及其临床表现
我院上报的205例ADR中,所累及系统共10类,以皮肤及附件损害最多见,共57例,占27.81%。见表5。
2.6 ADR类别分布
205例ADR中,按照严重程度分为一般和严重两类,其中“已知一般”的类型最多,共162例,占79.02%。见表6。

表4 药品不良反应涉及药品排序情况
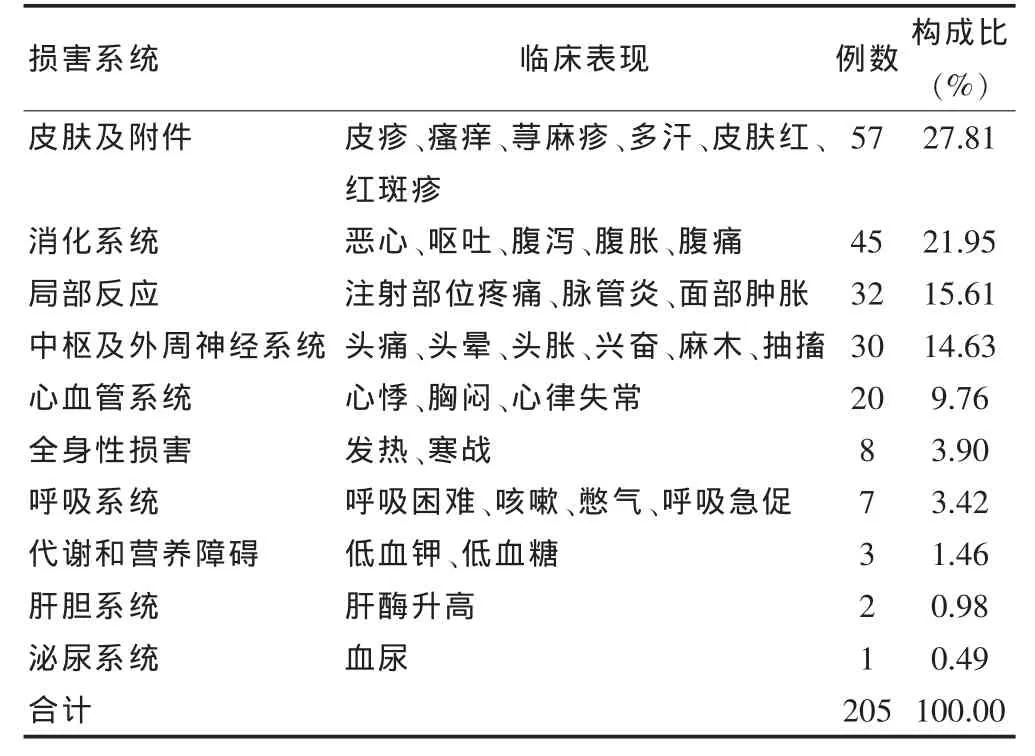
表5 药品不良反应累及器官或系统及其临床表现

表6 药品不良反应类别分布
2.7 ADR上报人群的职业分布
205例ADR中,上报人群的职业共有三类,其中主要是医师,占86.83%。见表7。

表7 药品不良反应上报人群的职业分布
3 讨论
3.1 ADR与患者年龄、性别的关系
在我院上报的205例ADR病例中,女性154例(75.12%),明显高于男性患者,与有关报道相一致[2-3]。ADR与性别的相关性迄今为止没有明确的解释。女性一般体重较男性轻,肌肉较男性少,用药量相同时作用强度可能与男性有差异,这可能是产生差异的基础。ADR在任何年龄段都可发生,但发生的比率、严重程度并不相同,从结果表1可以看出60岁及以上老年人发生ADR的比例最高,共88例,占42.93%。分析原因为:①药动学:老年人代谢功能降低,肝、肾和肠胃等器官和(或)系统功能衰退,药物容易在体内蓄积而发生ADR[4];老年人肌肉萎缩,全身含水量减少,脂肪组织中药物浓度升高[5];老年人血浆蛋白含量降低,结合药物减少,游离型药物在血浆和组织中浓度增加使不良反应发生率增加[6]。②药效学改变:衰老导致许多系统对某些药物的敏感性增加,引起不良反应的增加,尤以神经系统为最。③联合用药:老年人常同时罹患多种疾病,接受多种药物治疗。据报道,50%以上的老年患者同时服用4~6种药物,现已确认老年人ADR的发生率与用药品种呈正相关[7]。④老年人记忆力差,用药依从性差。以上提示对于老年人用药应谨慎,在尽量减少用药品种的基础上做到合理的联合用药,并注意调整剂量,同时对老年患者应做好用药监护。
3.2 ADR与给药途径的关系
由结果表2可见,在205例ADR患者中,由静脉滴注所致ADR最多,为188例,占91.71%。由此可知静脉滴注是引起ADR的最主要途径,这与以往报道相符[8]。出现这种情况的原因为:①我院ADR报告多来源于住院患者,静脉给药是目前我国临床最广泛的给药途径,80%以上的住院患者接受输液治疗。②静脉给药药物直接进入血液,没有吸收过程,作用迅速强烈,血药浓度较高,对机体刺激较大,而且药物的渗透压、pH、微粒、内毒素等都很容易引发不良反应[9]。③溶媒选择不当可引起ADR。溶媒选择的合理性对药物的稳定性具有十分重要的作用,溶媒种类很多,各自具备不同的特点。《中国药典》规定葡萄糖注射液的 pH为3.2~5.5,0.9%氯化钠注射液的 pH为 4.5~7.0。pH对药物稳定性影响极大,pH改变可影响溶解度、稳定性及药效。有报道指出,pH相差一个单位,[H+]相差10倍[10]。因此,应根据药物的理化性质来选择合适的溶媒以避免沉淀、变质和不溶性微粒的产生。需要注意的是,有些药物的包装中配有专用溶剂,对于这些药物中配备的专用溶剂不可随便丢弃,或擅自用其他溶剂替代;有些注射用无菌粉末说明书规定的初始溶媒与输液用的溶媒并不一致。④溶媒用量的多少可影响药物的浓度引起ADR。溶媒量过大会使药物浓度降低,降低药效,同时输注时间延长,不稳定因素增加,不良反应发生概率增大;溶媒量过小,药物不能全部溶解而产生浑浊或生成沉淀,药物浓度过大产生局部刺激引起不良反应。⑤静脉滴速过快是诱发注射剂ADR的因素之一[11]。滴注速度过快可使循环血量急剧增加,加重心脏负担,引起心力衰竭和肺水肿,特别是小儿、老年、胸部外伤、心力衰竭的患者更易发生,可成为致命的严重反应。输注速度过快,还可导致药物的血药浓度升高过快,超出安全范围产生毒性作用,特别是一些治疗指数窄、毒性作用大的药物及中药注射剂[12]。因此,在用药时应遵循能口服不肌注、能肌注不输液的原则,根据患者病情的严重程度,患者的年龄、体质以及药物的药代药动学特点选择合理的给药途径。
3.3 涉及药品种类
由结果表3可见,在205例ADR患者中,共涉及药物65种,其中以抗感染药物上报例数最多,共80例,占39.02%,与其他文献报道[13-14]基本一致,说明抗菌药物ADR发生率居于所有药物的首位[15]。ADR发生率与药物使用频率密切相关,而抗感染药物是临床应用最广泛的一类药物,几乎涉及临床所有科室,并且无指征用药、选用药物级别过高、用药疗程过长、联合用药过多等不合理用药现象较为严重,这也导致了不良反应发生的增多。
由结果表4可见,引起ADR的抗感染药物中大环内酯类药物阿奇霉素最多,共42例,占20.49%。符颖等[16]研究也证明大环内酯类药物易引起不良反应。阿奇霉素是一种新型的半合成大环内酯类抗菌药物,口服后吸收迅速、生物利用度高、体内分布广泛、细胞内游离浓度高、血消除半衰期长(35~48 h),具有抗菌、破胞和免疫调节的作用,可用于多种感染。阿奇霉素不需做皮试,故在临床使用较广。针对阿奇霉素在临床中的广泛滥用现象,在纽约召开的第20届美国急诊医学会(AAEM)年会上,不止一位专家呼吁停止将大环内酯类的阿奇霉素用于各种常见感染的治疗。国外研究显示,与阿莫西林相比,阿奇霉素用药5 d内,患者死亡和心律失常风险明显增加[17]。我院上报阿奇霉素引起的不良反应多表现为胃肠道反应、静脉刺激等,没有严重不良反应发生。有研究认为,阿奇霉素静脉给药更易引起严重不良反应,而口服给药不良反应发生率较低[18]。提示在制订给药方案时应严格按照阿奇霉素的抗菌谱及适应证用药,尽可能采用口服给药,静脉给药时控制药液的终浓度和滴注速度,一般终浓度不超过2.0 mg/mL;当浓度为1.0 mg/mL时,滴注时间为3 h,当浓度为2.0 mg/mL时,滴注时间为1 h。对于首次静脉给药的患者,在开始输注时应缓慢滴注并注意密切观察,如无异常可改为正常滴速。
3.4 ADR累及器官及临床表现
由结果表5可见,205例ADR累及器官或系统以皮肤及附件损害最多,共57例,占27.81%,主要表现为变态反应所致的皮疹、瘙痒、荨麻疹等;其次是消化系统症状,共45例,占21.95%,主要表现为恶心、呕吐、腹泻、腹胀、腹痛,这与有关文献报道相一致[19-23]。究其原因可能是皮肤性状改变较直观,易于观察;消化系统反应患者较易感觉,不需相关检验即可判断。ADR所累及的皮肤及附件损害和消化系统反应症状均比较轻,一般不需特殊处理停药后可自行缓解。
3.5 ADR的上报人群职业
在我国,医疗机构既是ADR发生的主要场所,也是ADR报告的最主要来源,自愿呈报是我国目前采取的主要监测方法。由结果表7可见,205例ADR病例中由医师上报的最多,占86.83%,由护士上报的最少,仅占0.49%。事实上,护士执行医嘱、落实各项治疗计划,是药物治疗的主要实施者,更易发现ADR。因此,在护理人员中开展ADR培训十分必要。护理人员应了解所使用药品的作用与不良反应,判断所用药与患者的病情是否相符并经常深入病房,观察了解患者的生命体征、皮肤及黏膜等变化,注意偶发反应,一旦发现应及时向医师报告,必要时采取停用和其他紧急处理措施,认真填写《药品不良反应/事件》报告表,减少漏报现象的发生。
综上所述,ADR的发生在患者的年龄、药品种类、给药方式和累及器官及临床表现方面具有一定的规律性,医师在用药前应当详细询问患者既往用药史、过敏史,严格按照药品的适应证选用药物,注意用法用量,尽量减少联合用药和静脉给药;护士在给药过程中应注意观察患者情况,控制静脉给药速度,一旦发生不良反应及时报告医师,及时处置;临床药师应做好用药监护,特别关注老人、小儿及肝肾功能不全的特殊患者,同时应做好ADR监测的宣传和培训。总之,ADR监测工作开展情况是衡量医疗机构医疗质量、管理水平和人员素质状况的重要标准之一[24],医护人员应重视ADR监测和报告工作,提高合理用药水平,尽量减少ADR的发生。
[1]康琪,梁萍,宋民宪.药品不良反应定义中“正常”的界定[J].中药与临床,2013,4(1):50-52.
[2]慕尚真.226例药品不良反应报告分析[J].中国医院用药评价与分析,2014,14(5):448-451.
[3]陆惠平,严晓沁,顾正平,等.我院340例药品不良反应的回顾性分析[J].中国药房,2012,23(22):2084-2086.
[4]秦庆芳,陆卫英.2010-2012年1237例中成药致不良反应报告分析[J].中国医院用药评价与分析,2014,14(3):262-264.
[5]孙淑娟,袭燕.抗菌药物治疗学[M].北京:人民卫生出版社,2008:105.
[6]罗健东,肖顺汉.临床药理学[M].北京:科学出版社,2008:87-89.
[7]施志云.老年人药物不良反应与用药原则[J].中国误诊学杂志,2008,8(30):7551-7552.
[8]胡伟,慈静.2011-2012年420例药品不良反应报告分析[J].中国医院用药评价与分析,2014,14(3):257-259.
[9]赵喜荣,张占铎,郝晓菁.2010年我院160例药品不良反应报告分析[J].中国药业,2012,21(2):56-57.
[10]张必奎.输液治疗用药的合理使用[M].北京:人民卫生出版社,2012:21-23.
[11]何贞忠.湖南省永江县人民医院2011~2013年住院患者ADR监测与分析[J].中国医院用药评价与分析,2014,14(5):454-458.
[12]田慧,王瑞芳.合理调控滴注速度在临床中的重要性[J].时珍国医国药,2008,19(10):2544-2546.
[13]李亚骞,黄玲梅,官真水.成都市双流县第一人民医院2012-2013年药品不良反应分析[J].中国医院用药评价与分析,2014,14(7):637-639.
[14]刘振胜,杜静,刘华强,等.146例严重药品不良反应报告分析[J].药学研究,2014,33(9):554-556.
[15]袁穗蓉.164例抗菌药物不良反应分析报告[J].中国医药导报,2010,7(7):111-112.
[16]符颖,麦丽珍,欧慧玉.279例药品不良反应报告回顾性分析[J].现代预防医学,2012,39(9):2192-2197.
[17]Rao GA,Mann JR,Shoaibi A,et al.Azithromycin and levofloxacin use and increased risk of cardiac arrhythmia and death[J].Ann Fam Med,2014,12(2):121-127.
[18]王兆丽,刘屹,王艳霞.阿奇霉素不良反应研究[J].中国医药导报,2009,6(5):114-116.
[19]杨永.抗菌药物不良反应56例报告分析[J].中国医药科学,2013,3(22):145-146.
[20]许辉.某基层医院2007~2012年药物不良反应分析[J].中国当代医药,2013,20(32):92-93,95
[21]何伟珍,吴丽兰,应小飞,等.浙江丽水2004年501例药品不良反应报告分析[J].中国药房,2005,16(10):774-775.
[22]王书芬,李震.某院105例抗菌药物不良反应报告分析[J].中国医药科学,2013,3(2):151-152,154.
[23]潘建华,韩莹旻,何晶等.219例抗菌药物不良反应分析[J].中国当代医药,2013,20(4):152-153.
[24]谢金洲.药品不良反应与监测[M].北京:中国医药科技出版社,2004:324.

