小檗碱对多囊卵巢综合征大鼠代谢及生殖作用的研究*
王娜梅
(河南中医学院第三临床医学院,河南郑州450008)
·论著·
小檗碱对多囊卵巢综合征大鼠代谢及生殖作用的研究*
王娜梅
(河南中医学院第三临床医学院,河南郑州450008)
目的探讨小檗碱对多囊卵巢综合征(PCOS)大鼠代谢及生殖的作用。方法采用皮下注射脱氢表雄酮(DHEA)造模法建立PCOS大鼠模型,将大鼠随机分为正常对照组、模型对照组、二甲双胍组和小檗碱组,分别给予相应药物连续灌胃28 d。用电子精密天平测量脂肪湿重,计算脂体比;全自动生化分析仪测定大鼠血清胆固醇及三酰甘油水平;口服葡萄糖耐量试验(OGTT)测定血糖;计算稳态模型胰岛素抵抗指数(HOMAIR)。行阴道涂片、苏木精-伊红染色法(HE)观察动情周期;用酶联免疫吸附测定法(ELISA)检测促卵泡生成素(FSH)、促黄体生成素(LH)、睾酮(T)、胰岛素(INS)水平;行卵巢组织HE染色,光镜下观察卵巢组织形态学变化。结果与正常对照组比较,模型对照组大鼠体内脂肪湿重及脂体比增加,血清胆固醇水平明显升高,糖耐量异常,空腹胰岛素及HOMA-IR明显升高,失去规律的动情周期,血清FSH、LH、T水平升高,卵巢呈多囊样改变。小檗碱和二甲双胍可不同程度地改变PCOS大鼠上述病理改变,小檗碱在降低血清胆固醇及脂肪湿重、脂体比方面明显优于二甲双胍。结论小檗碱可改善PCOS大鼠糖、脂代谢异常,降低LH、T水平,恢复大鼠动情周期,改善卵巢形态学结构。
多囊卵巢综合征;小檗碱;糖脂代谢;雄激素
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是最常见的妇科内分泌疾病之一,临床上以雄激素过高的临床或生化表现、持续无排卵、卵巢多囊改变为特征,常伴胰岛素抵抗(insulin resistance,IR)和肥胖[1]。改善IR和降低雄激素治疗常使患者恢复规律的月经周期和排卵。小檗碱是黄连的主要成分之一,在一千多年中药史上一直被用于治疗糖尿病。小檗碱具有明显的降糖和降血脂作用,可明显降低2型糖尿病患者的血糖、血脂水平,疗效肯定。除降糖作用外,近年研究发现小檗碱对雄激素合成亦具有明显作用[2-3]。小檗碱具有降糖、降脂及降雄激素作用,与PCOS的病理改变吻合,为此本研究应用小檗碱对PCOS大鼠模型进行干预治疗,观察其对模式大鼠生殖和代谢的调节作用,为小檗碱的临床应用提供基础研究依据,现报道如下。
1 材料与方法
1.1材料
1.1.1 实验动物选用23 d龄雌性SD清洁级大鼠60只,体重(50±20)g,由河南省动物实验中心提供,大鼠许可证号:SCXK(豫)2010-0002。采用独立通风笼饲养,喂食标准饲料。
1.1.2 主要药物与试剂脱氢表雄酮(dehydroepiandrosterone,DHEA)购自湖北芳通药业有限公司(批号:20120518),盐酸二甲双胍购自中美上海施贵宝制药有限公司(批号:1207097),盐酸小檗碱片购自成都锦华药业有限责任公司(批号:121014),注射用大豆油购自中航(铁岭)药业有限公司(批号:y12080204-3-01),大鼠胰岛素(Insulin,INS)酶联免疫吸附测定法(enzyme-linked immunosorbent assay,ELISA)检测试剂盒(批号∶2013032154)、大鼠睾酮(Testosterone,T)ELISA检测试剂盒(批号∶2013050428)、大鼠促黄体生成素(Luteinizing hormone,LH)ELISA检测试剂盒(批号∶201306012)及大鼠促卵泡生成素(follicle stimulating hormone,FSH)ELISA检测试剂盒(批号:2013060742)购自美国R&D公司,50%葡萄糖注射液购自河南润弘制药股份有限公司(批号:1208081)。
1.2方法
1.2.1 动物分组及造模方法60只雌性SD大鼠随机分为正常对照组(15只)和模型组(45只)。模型组每日颈背部皮下注射DHEA 6 mg/100 g+0.2 ml注射用大豆油,连续20 d;正常对照组每日颈背部皮下注射0.2 ml注射用大豆油,连续20 d,制作PCOS动物模型。造模结束后连续2个性周期(每个性周期4 d)阴道上皮细胞涂片,阴道上皮细胞持续角化,提示无排卵大鼠模型制作成功。
1.2.2 给药方法造模成功后将模型组大鼠随机分为模型对照组、小檗碱组和二甲双胍组,每组15只,每天上午8:00分别给予0.5%羧甲基纤维素钠溶液、盐酸小檗碱片300 mg/kg(溶于0.5%羧甲基纤维素钠溶液)、盐酸二甲双胍200 mg/kg(溶于0.5%羧甲基纤维素钠溶液)灌胃。正常对照组15只大鼠给予0.5%羧甲基纤维素钠溶液灌胃。灌胃期间大鼠死亡4只(其中模型对照组死亡2只,二甲双胍组及小檗碱组各死亡1只)。连续灌胃28 d后,行口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)测定大鼠各时间血糖值,行阴道涂片观察各组大鼠动情周期变化,于动情间期处死大鼠,留取血清待测,留取卵巢组织,4%多聚甲醛固定待测。
1.2.3 观察内容及方法①动情周期:连续2个周期阴道脱落细胞涂片、苏木精-伊红染色(hematoxylineosin staining,HE)观察大鼠动情周期;②OGTT试验:大鼠禁食、不禁水12 h,以3 g/kg剂量灌服50%葡萄糖溶液,尾尖取血,血糖仪测定大鼠灌糖后0、30、60及120 min的血糖值;③大鼠体重、体内脂肪湿重及脂体比:分别用电子体重测量仪和电子精密天平测量,计算脂肪湿重(脂肪湿重=卵巢周围脂肪+肾周围脂肪+肠系膜周围脂肪)和脂体比(脂体比=脂肪湿重/体重);④血脂测定:应用美国贝克曼库尔特有限公司生产的AU5800型全自动生化分析仪测定血清胆固醇及三酰甘油水平;⑤ELISA法检测大鼠血清INS、FSH、LH及T水平,计算LH/FSH值;⑥计算稳态模型胰岛素抵抗指数(homeostasis model assessment-insulinresistance,HOMA-IR):HOMA-IR=空腹血糖(mmol/L)×空腹胰岛素(mIU/L)/22.5;⑦HE染色观察大鼠卵巢形态学变化:取大鼠卵巢组织,去除卵巢表面的脂肪组织,4%多聚甲醛溶液固定,酒精逐级脱水,浸蜡包埋,5μm切片,HE染色,光镜观察卵巢组织形态学变化。
1.3统计学方法
采用SPSS 13.0统计软件进行数据分析,计量资料以均数±标准差(±s)表示,符合正态分布计量资料多组间比较用单因素方差分析,不符合正态分布的采用对数法或倒数法转换为正态资料后进行统计分析,P<0.05为差异有统计学意义。
2 结果
2.1各组大鼠代谢相关指标的变化
2.1.1 各组大鼠体重、脂肪湿重、脂体比比较与正常对照组比较,模型对照组体内脂肪湿重及脂体比显著增加(P=0.004和0.048)。与模型对照组比较,二甲双胍组体内脂肪湿重明显降低(P=0.024),小檗碱组脂肪湿重及脂体比显著降低(P=0.002和0.033)。小檗碱组体重较模型对照组有降低趋势,但各组大鼠体重比较差异无统计学意义。见表1。
2.1.2 各组大鼠血脂水平比较与正常对照组比较,模型对照组大鼠血清胆固醇水平明显升高(P=0.006)。与模型对照组比较,小檗碱组血清胆固醇水平明显降低(P=0.033),二甲双胍组血清胆固醇水平有降低趋势。各组血清三酰甘油水平比较差异无统计学意义。见表2。
2.1.3 各组大鼠OGTT血糖比较与正常对照组比较,模型对照组大鼠OGTT试验0、30和120 min血糖值明显升高(P=0.000),说明大鼠存在糖耐量异常。与模型对照组比较,二甲双胍组及小檗碱组OGTT试验各时间血糖值显著降低(P=0.000和0.008)。见图1。
2.1.4 各组大鼠空腹胰岛素及HOMA-IR比较与正常对照组比较,模型对照组大鼠空腹胰岛素及HOMA-IR明显升高(P=0.000),说明大鼠存在胰岛素抵抗。与模型对照组比较,二甲双胍组和小檗碱组的空腹胰岛素、HOMA-IR水平显著降低(P=0.000)。与二甲双胍组比较,小檗碱组空腹胰岛素及HOMA-IR水平显著升高(P=0.038和0.007)。见表3。
2.2各组大鼠生殖相关指标的变化
2.2.1 各组大鼠动情周期的变化连续2个周期的阴道涂片结果显示,正常对照组大鼠有规律的动情周期(4~5 d);模型对照组大鼠动情周期延长至8~9 d或无明显的动情周期,提示无排卵;经小檗碱及二甲双胍灌胃治疗后大鼠恢复规律的动情周期。
2.2.2 各组大鼠性血清FSH、LH、T水平及LH/FSH比较与正常对照组比较,模型对照组血清FSH、LH、T水平显著升高(P=0.000)。与模型对照组比较,二甲双胍组及小檗碱组FSH、LH、T水平显著降低(二甲双胍组P=0.000;小檗碱组P=0.000、0.007和0.000);小檗碱组LH及T水平较二甲双胍组明显升高(P=0.017和0.000)。各组LH/FSH值比较差异无统计学意义。见表4。
2.2.3 各组大鼠卵巢HE染色光镜下的形态学变化正常对照组卵巢组织内可见各级卵泡及多个黄体组织,卵泡内卵丘、卵母细胞清晰可见,颗粒细胞呈多层(8~9层);模型对照组卵巢组织内可见较多呈囊性扩张的卵泡,囊状卵泡内卵母细胞或放射冠消失,可见多个囊泡,颗粒细胞层数较少(2~3层)、排列疏松,正常形态的各级细胞少见,黄体数目较少;二甲双胍组卵巢组织内可见极少数囊泡,各级卵泡细胞数量增多,颗粒细胞及黄体数目增多,细胞排列紧密;小檗碱组卵巢组织内可见少数囊泡、各个发育阶段的卵泡及较多黄体组织,卵泡内颗粒细胞层数较模型组对照明显增多,排列整齐;二甲双胍组及小檗碱组卵巢组织中各级卵泡及黄体数目较模型对照组明显增多。见图2。
表1 各组大鼠体重、脂肪湿重、脂体比比较(±s)
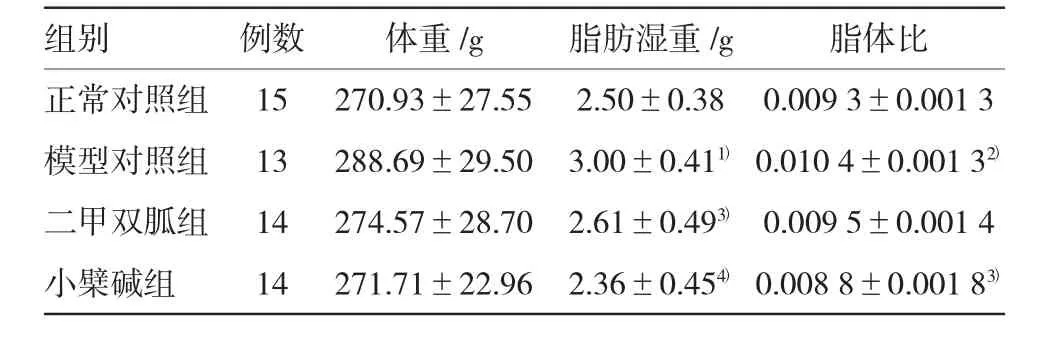
表1 各组大鼠体重、脂肪湿重、脂体比比较(±s)
注:1)与正常对照组比较,P<0.01;2)与正常对照组比较,P<0.05;3)与模型对照组比较,P<0.05;4)与模型对照组比较,P<0.01
组别例数体重/g脂肪湿重/g脂体比正常对照组15270.93±27.552.50±0.380.009 3±0.001 3模型对照组13288.69±29.503.00±0.411)0.010 4±0.001 32)二甲双胍组14274.57±28.702.61±0.493)0.009 5±0.001 4小檗碱组14271.71±22.962.36±0.454)0.008 8±0.001 83)
表2 各组大鼠血清胆固醇、三酰甘油比较(mmol/L±s)
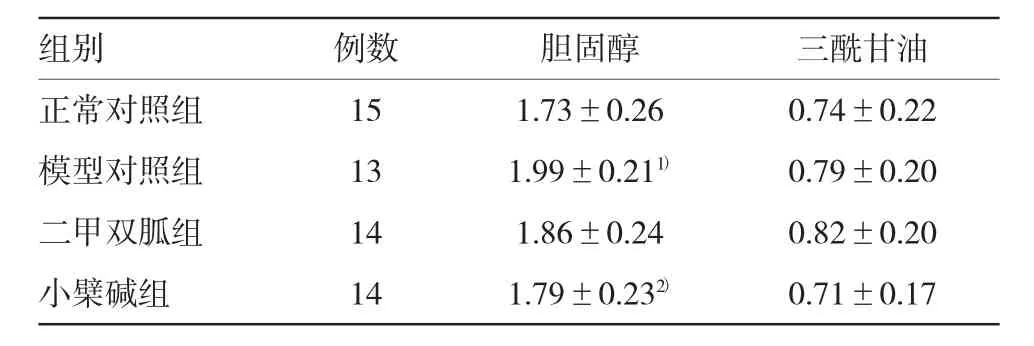
表2 各组大鼠血清胆固醇、三酰甘油比较(mmol/L±s)
注:1)与正常对照组比较,P<0.01;2)与模型对照组比较,P<0.01
组别例数胆固醇三酰甘油正常对照组151.73±0.260.74±0.22模型对照组131.99±0.211)0.79±0.20二甲双胍组141.86±0.240.82±0.20小檗碱组141.79±0.232)0.71±0.17

图1 各组大鼠OGTT血糖比较
表3 各组大鼠空腹胰岛素及HOMA-IR比较(±s)

表3 各组大鼠空腹胰岛素及HOMA-IR比较(±s)
注:1)与正常对照组比较,P<0.01;2)与模型对照组比较,P<0.01;3)与二甲双胍组比较,P<0.05;4)与二甲双胍组比较,P<0.01
组别例数空腹INS/(mU/L)HOMA-IR正常对照组159.44±2.052.19±0.46模型对照组1332.17±3.461)13.99±2.991)二甲双胍组149.93±2.412)2.21±0.522)小檗碱组1412.01±2.312)3)2.89±0.692)4)
表4 各组大鼠血清FSH、LH、T水平及LH/FSH比较(±s)

表4 各组大鼠血清FSH、LH、T水平及LH/FSH比较(±s)
注:1)与正常对照组比较,P<0.01;2)与模型对照组比较,P<0.01;3)与二甲双胍组比较,P<0.05;4)与二甲双胍组比较,P<0.01
组别例数FSH/(mIU/ml)LH/(mIU/ml)T/(pg/ml)LH/FSH正常对照组155.26±0.8319.55±2.10157.55±17.663.83±0.84模型对照组139.75±0.881)38.23±4.161)298.10±31.621)3.96±0.63二甲双胍组147.09±0.742)29.62±4.502)185.49±24.522)4.24±0.85小檗碱组147.58±1.072)32.94±3.202)3)225.20±19.152)4)4.40±0.54
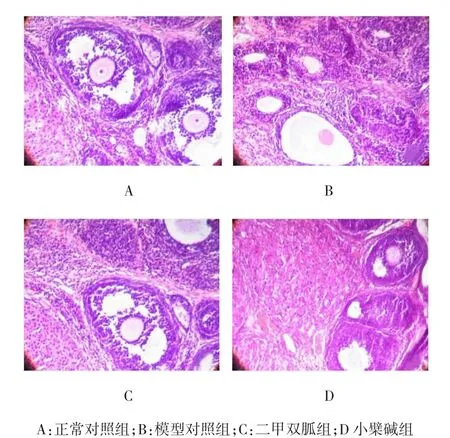
图2 各组大鼠卵巢组织切片(HE×200)
3 讨论
PCOS是常见的女性内分泌失调性疾病,病因不清,发病机制尚未阐明。临床上PCOS主要表现为糖、脂代谢异常和生殖功能障碍并存,长期发展可引起糖尿病、冠状动脉粥样硬化性心脏病、高血压、高血脂及子宫内膜癌等远期代谢并发症,严重影响妇女生殖健康和生活质量。PCOS患者的代谢异常主要表现为IR和高胰岛素血症;PCOS患者的生殖功能障碍主要表现为卵巢排卵功能障碍和雄激素分泌过多[4]。PCOS患者亦常常存在血脂代谢异常。一项临床回顾分析研究表明,PCOS患者IR的发生率为38.1%,血脂异常的发生率为24.7%,血脂异常与IR呈正相关。临床上可使用胰岛素增敏剂改善IR,从而改善PCOS患者的血脂代谢异常[5]。肥胖尤其是中心性肥胖及高雄激素血症,与PCOS血脂异常的发生亦密切相关。本研究结果显示,模型对照组大鼠动情周期延长或无明显的动情周期,呈无排卵状态;血清FSH、LH、T水平升高,呈高雄激素、高LH水平状态;卵巢呈多囊样变;模型对照组大鼠存在糖耐量异常,空腹胰岛素及HOMA-IR明显高于正常对照组;模型对照组大鼠血清胆固醇水平明显升高,体内脂肪湿重及脂体比较正常对照组显著增加,提示大鼠存在IR、脂代谢异常及生殖功能障碍。说明本模型是研究PCOS生殖及代谢异常的较理想的动物模型。
目前PCOS治疗以药物治疗为主,并提倡生活方式的调整,如控制饮食、运动及减轻体重。鉴于IR在PCOS发病中的重要作用,临床上给予IR的PCOS患者胰岛素增敏剂。改善IR后,常常可使患者雄激素水平下降,月经周期好转甚至正常,排卵率增加。本研究中二甲双胍显示较好的改善PCOS大鼠糖耐量异常、降低胰岛素、改善大鼠IR及降低大鼠LH、T水平的作用,并可恢复大鼠动情周期,改善卵巢多囊状态。目前临床应用的胰岛素增敏剂主要有双胍类和噻唑烷二酮类。两者的疗效确切,但是不良反应重且价格较贵,不利于患者长期应用。因此,寻找一种针对PCOS治疗的安全、经济、有效的药物是临床亟待解决的问题。
小檗碱是从传统中药黄连根茎中提取的异喹啉类生物碱,属季铵类化合物。近年来研究表明,小檗碱除具有传统的抗菌消炎的作用外,还能够改善IR,降低血糖,降血脂,增加胰岛素敏感性而用于2型糖尿病的治疗,且无明显不良反应。小檗碱的作用特点和二甲双胍类似,属胰岛素增敏剂,临床可用于糖耐量异常和轻度高血糖患者。相关实验研究中,小檗碱可明显降低链脲佐菌素诱导的糖尿病大鼠空腹血糖水平,改善糖耐量异常,降低血清胆固醇及三酰甘油水平[6]。最近一项临床研究表明,小檗碱可明显降低PCOS患者空腹血糖、空腹胰岛素水平,增强胰岛素敏感性,并且可明显减低PCOS患者血脂水平[7]。也有研究表明,小檗碱能显著改善PCOS患者的向心性肥胖,调节血脂,减轻体重,改善高胰岛素血症,增加胰岛素敏感性,并可改善慢性炎症[8-9]。在本研究中,PCOS大鼠经灌胃治疗后,小檗碱可明显降低模型大鼠体内脂肪湿重,降低脂体比,降低大鼠血清胆固醇水平,改善大鼠糖耐量异常状态,降低空腹胰岛素水平,改善大鼠IR,显示较好的降脂、降糖作用。其降糖作用与二甲双胍组相似,但其降低空腹胰岛素及胰岛素抵抗指数效果稍逊于二甲双胍,而其降低血清胆固醇、脂肪湿重及脂体比作用明显优于二甲双胍。小檗碱降糖机制目前仍不清楚,可能是通过活化腺苷酸活化蛋白激酶信号分子起降糖作用,也可能是通过调节胰岛素信号通路上的关键分子,包括胰岛素受体底物1、磷脂酰肌醇3激酶P85亚基、蛋白激酶B、葡萄糖转运蛋白4等而起到降糖作用[10-11]。有研究表明,小檗碱通过调节胰岛素受体的表达而降血糖,该调节是蛋白激酶C依赖性的[12]。
除降糖作用外,近年研究发现,小檗碱对雄激素合成亦具有明显降低作用。小檗碱可逆转地塞米松诱导的胰岛素抵抗卵泡膜细胞雄激素合成的增加及葡萄糖摄取的减弱[13]。小檗碱对雄激素受体信号通路有抑制作用[14]。本研究中,小檗碱可明显降低PCOS大鼠血清T水平,进一步在动物身上体现小檗碱的降雄激素作用。除降雄激素作用外,本研究显示,小檗碱对PCOS大鼠高LH水平亦有明显降低作用,可改善大鼠内分泌失调状态。小檗碱治疗后,经2个周期阴道涂片发现大鼠恢复规律的动情周期,在卵巢形态学改变方面黄体数目增多,各级卵泡数目增多,囊泡数目减少,可能是小檗碱改善大鼠糖脂代谢异常、改善高雄激素、IR等异常内分泌状态,使大鼠整体内分泌功能趋于正常,从而卵巢形态学趋于正常,使大鼠恢复规律的动情周期及排卵。
综上所述,小檗碱可改善PCOS大鼠糖脂代谢异常,降低T及LH水平,改善大鼠内分泌失调状态及卵巢形态学结构,使大鼠恢复规律的动情周期,从而使大鼠生殖功能趋于正常。由于实验条件的限制,其作用的相关分子机制有待进一步研究。
[1]谢幸,苟文丽.妇产科学[M].北京∶人民卫生出版社,2013∶358.
[2]王秀秀,李威,刘逸超,等.小檗碱对胰岛素抵抗卵巢甾体激素体外合成和代谢的调控作用[J].中国中西医结合杂志,2010,30(2)∶161-166.
[3]李慕白,高敬书,寇丽辉,等.小檗碱对胰岛素抵抗多囊卵巢综合征患者激素水平的调节作用[J].中国妇幼保健,2015,30(11)∶1718-1720.
[4]吴效科.多囊卵巢综合征可能是原发性卵泡病[J].中国实用妇科与产科杂志,2007,23(9)∶660-663.
[5]洪宇,刘雯,赵晓苗,等.多囊卵巢综合征患者的血脂代谢异常及与胰岛素抵抗的关系分析[J].实用妇产科杂志,2012,28(3)∶230-233.
[6]CHEN Y,WANG Y,ZHANG J,et al.Berberine improves glucose homeostasis in streptozotocin-induced diabetic rats in association with multiple factors of insulin resistance[J].ISRN Endocrinol,2011,DOI∶10.5402/2011/519371.
[7]WEI W,ZHAO H,WANG A,et al.A clinical study on the short-term effect of berberine in comparison to metformin on the metabolic characteristics of women with polycystic ovary syndrome[J].Eur J Endocrinol,2012,166(1)∶99-105.
[8]刘成丽,王丽丽,曲凤占,等.右归丸联合小檗碱对多囊卵巢综合征胰岛素抵抗的研究[J].现代生物医学进展,2015,15(20)∶3943-3945.
[9]邓海云,魏巍,关源源.小檗碱治疗多囊卵巢综合征伴胰岛素抵抗的研究[J].天津医药,2012,40(10)∶1009-1011.
[10]CICERO AF,TARTAGNI E.Antidiabetic properties of berberine∶from cellular pharmacology to clinical effects[J].Hosp Pract,2012,40(2)∶56-63.
[11]LIU LZ,CHEUNG SC,LAN LL,et al.Berberine modulates insulin signaling transduction in insulin-resistant cells[J].Mol Cell Endocrinol,2010,317(1/2)∶148-153.
[12]KONG WJ,ZHANG H,SONG DQ,et al.Berberine reduces insulin resistance through protein kinase C-dependent up-regulation of insulin receptor expression[J].Metabolism,2009,58(1)∶109-119.
[13]ZHAO L,LI W,HAN F,et al.Berberine reduces insulin resistance induced by dexamethasone in theca cells in vitro[J].Fertil Steril,2011,95(1)∶461-463.
[14]LI J,CAO B,LIU X,et al.Berberine suppresses androgen receptor signaling in prostate cancer[J].Mol Cancer Ther,2011,10(8)∶1346-1356.
(童颖丹 编辑)
Effect of Berberine on metabolism and reproduction in rats with polycystic ovarian syndrome*
Na-mei WANG
(The Third Affiliated Hospital,Henan College of Traditional Chinese Medicine,Zhengzhou,Henan 450008,P.R.China)
【Objective】To study the effect of Berberine on metabolism and reproduction in rats with polycystic ovarian syndrome(PCOS).【Methods】PCOS rat model was established by subcutaneous injection of DHEA.Rats were randomly divided into 4 groups:normal control group,model control group,Metformin group and Berberine group.Wet weight of fat in the four groups was measured with electronic precision balance.Serum cholesterol and triglyceride levels were detected by automatic biochemical analyzer,and blood glucose was detected using oral glucose tolerance test(OGTT).Estrous cycles were observed by vaginal smear and HE staining method.Follicle stimulating hormone(FSH),luteinizing hormone(LH),testosterone(T)and insulin levels were detected by ELISA.Ovarian morphology was observed using HE staining and light microscopy.【Results】Compared with the normal control group,the wet weight of fat in the model control group significantly increased.Cholesterol,fasting insulin,HOMA-IR,FSH,LH and T levels of the model control group were markedly higher than those of the normal control group.Rats in the model control group had polycystic ovaries,abnormal glucose tolerance and irregular estrus cycles.Berberine and Metformin ameliorated the above pathological changes of PCOS rats to different degree.Berberine had better effects on lowering serum cholesterol and body fat than Metformin.【Conclusions】Berberine can improve glucose and lipid metabolism,reduce LH and T levels,restore estrus cycle and improve ovarian morphology in PCOS rats.
polycystic ovarian syndrome;Berberine;glucose and lipid metabolism;androgen
R711.75;R271.9
A
1005-8982(2015)35-0013-05
2015-06-15
河南中医学院博士科研基金(No:BSJJ2010-32)

