“测定空气中氧气的含量”实验的改进和反思
张洁+宋守娟
摘要:基于现行鲁教版九年级化学课本中“测定空气中氧气的含量”实验,对药品要求较高,实验条件较难控制,实验成功率低的问题,通过限定药品用量、更换药品、改进装置、兴趣实验开发的方法探索,改进了实验,提高了实验效率,并能启发学生敢于质疑,培养实验动手能力及探究精神。
关键词:空气中氧气含量测定;实验改进;初中化学实验
文章编号:1005–6629(2015)4–0050–03 中图分类号:G633.8 文献标识码:B
现行鲁教版九年级化学课本中“测定空气中氧气的含量”实验,用图1装置和铜粉来进行实验。实验趣味性强,以此为载体引导学生设计和实施实验,进行误差分析,能有效训练学生的发散性思维能力,提高学生学习化学的兴趣。
可是在实验时,我们发现存在如下问题:
(1)实验室里久置的铜粉不是呈亮紫红色,而是呈褐色。
(2)用新制的铜粉做实验,发现加热时玻璃管里的铜粉表面生成一层黑色固体,停止加热,黑色固体又慢慢变成砖红色,且结成硬块粘附在玻璃管内壁上。
(3)实验所用时间长,完成一次实验约需15分钟。
(4)经过20多次实验,实验相对误差平均值大于25%,有的实验甚至不能成功。
基于上述几方面的问题,以期寻找更好的实验方法,获得更好的实验效果,我们进行如下的探索和改进。
1 通过限定药品用量化解弊端
1.1 探索与分析
查阅资料得知,铜粉质软,研磨加工困难,在潮湿空气中容易氧化变质成氧化铜,需要采用氮气保护、真空包装。我校实验室里的铜粉属于超细铜粉,因无法采用氮气保护或真空保存,久置后部分铜粉变质生成氧化铜,所以颜色呈褐色。
红色的含铜元素的固体物质有铜和氧化亚铜。向少量加热新制铜粉所得的砖红色固体中加入稀盐酸,发现有少量气泡放出,溶液变为浅黄色,有少许白色沉淀生成,试管底部有红色固体沉积。通常情况下铜不与稀盐酸反应,我们猜想红色固体中可能含有氧化亚铜。氧化亚铜与稀盐酸发生歧化反应,生成铜和氯化铜。用氢气还原砖红色固体,得到亮紫红色固体,也证明砖红色固体中含有氧化亚铜。
1.2 改进方法
经过分析和反思,根据密闭容器内氧气的体积计算所需铜粉的质量,实验时让铜粉稍过量(装置中封闭空气65mL,理论上需铜粉0.074g,实际实验时在玻璃管中放入铜粉0.2g)。加热铜粉,在加热过程中,不断缓慢推拉注射器的活塞,让铜粉与氧气充分反应。停止加热后,将注射器内的气体全部推出,让气体先储存到气球里,待装置冷却至室温时,再将气球里的气体缓慢全部挤出,使注射器的活塞后退,直到活塞稳定。如果使用的玻璃管和注射器容积较大,密闭容器内封闭空气较多,需铜粉质量较大时,应将铜粉薄薄地平铺在玻璃管中,以免铜粉堆积使热量聚集导致氧化铜分解,也避免反应不充分造成浪费。
1.3 改进效果
限制铜粉用量之后,生成的黑色固体没有再变成砖红色,经过10次实验测得相对误差平均值为17%,实验误差有所减小。但玻璃管与气球连接口容易漏气;对气球的要求也比较高,用弹性好张力大、厚薄适当的气球较好,如5cm长的圆形橡胶玩具气球;将气球里的气体往玻璃管中挤时需十分仔细;作为学生探究实验,实验误差仍然较大,且耗时长(约需10分钟)。
2 通过更换药品使实验现象更明显
2.1 实验探究
红磷在氧气中容易燃烧,反应充分,生成白烟,易散热,我们用红磷代替铜粉进行实验。根据氧气的体积计算所需红磷的质量(理论上需要0.0144g),实际实验时每次用0.3g。进行4组对比实验,测得氧气体积分数数据如下:
2.2 注意事项
用红磷替换铜粉进行实验,因为红磷易燃,作为学生探究实验有一定的危险性。需在教师的指导下进行,同时注意以下几点:
(1)认真检查装置气密性;
(2)准确测量玻璃管的体积,准确读出玻璃管和注射器内封闭空气的总体积;
(3)实验中不断缓慢推动注射器的活塞,不断轻轻挤压气球,使氧气充分参与反应;
(4)读数前,气球里的气体需全部挤压到玻璃管中,待装置冷却到室温再读数;
(5)由于红磷燃烧产生白烟放热,需硬质玻璃管;气球应选择弹性好张力大的,如大3号圆形橡胶玩具气球;
(6)红磷用量需根据氧气质量计算得出,不要过量太多,以免造成污染与浪费。红磷易燃,使用时一定注意不要撒到外面,用剩的红磷要统一回收。
2.3 改进效果
将铜粉换成红磷进行实验和现行教材的用铜粉实验相比较,实验误差小(4次实验相对误差平均值约为8.1%);且只需稍稍加热玻璃管,红磷即可燃烧,生成白烟,反应迅速且充分,现象明显,容易操作;白烟分散附着于玻璃管内壁迅速散热,实验时间缩短(每次实验约需6分钟),实验的成功率比较高,教学中更有说服力和可行性。
3 通过改变装置提高实验成功率
为了避免气球易爆易漏气且不易将其中气体全部挤出的缺点,我们从学生的创新实验中寻找灵感,改用下图装置进行实验。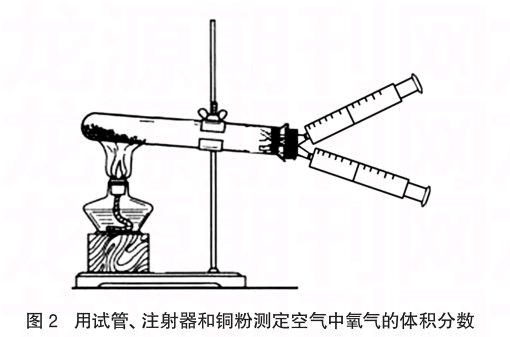
3.1 改进方法
在一支50mL的试管中装入约0.2g的新制铜粉,平铺均匀,用橡皮塞将试管密封(塞约占试管容积1/50),在橡皮塞上插两支注射器,注射器中密封约16mL空气,试管与注射器中共有65mL空气。将试管固定在铁架台上,并用酒精灯加热试管,同时缓慢交替推动注射器的活塞,直到铜粉颜色不再变化。停止加热,用吹风机使试管迅速冷却至室温,读数,注射器中剩余气体约3mL,从而得出结论,氧气约占空气体积的1/5。
3.2 注意事项
(1)检查图2装置的气密性,在试管和注射器内共预留空气65mL。
(2)预先根据氧气体积计算与其恰好完全反应时所需铜粉质量约为0.074g。为使氧气全部参加反应,在试管中平铺约0.2g新制的铜粉。
(3)给铜粉加热,并且不断缓慢地推动注射器的活塞(玻璃注射器效果更好),直到固体全部变成黑色,停止加热。
(4)待装置冷却到室温时读数。
(5)进行数据分析,注射器内减少的空气体积约为13mL,是空气体积(65mL)的1/5。
3.3 改进效果
该装置用另一支注射器代替气球,气密性好,交替推动注射器活塞容易进行气体交换,避免了气球挤压时易爆、易失去弹性的缺点,且注射器可以多次使用,不易损坏。本实验操作简单,实验现象明显,实验时间短(4分钟),实验误差小,实验成功率高,实验效果更好。
4 通过增加趣味性激发实验兴趣
在实际课堂教学中,为增加教学的趣味性,还可以从老师同学设计的趣味实验中寻找灵感,启发学生做一些趣味实验来测定氧气的体积分数。
4.1 实验方法
用图3装置和热帖(暖宝宝)中的药品进行实验,以期对学生有所启发。在注射器中封闭约2mL热帖中的固体,预留15mL空气,把注射器前端开口用橡皮塞塞住,不断轻轻晃动注射器,固体与注射器内的氧气充分反应,大约5分钟后,注射器内的气体减少约3mL,说明氧气约占空气体积的1/5。
4.2 实验效果
本实验取材于生活中的用品,在实验中仔细观察,可以明显看到注射器的活塞向下移动,气体体积逐渐减少,实验趣味性强。经10次实验,相对误差平均值小于5%,实验过程简单,易于操作,实验现象明显,便于学生在家自主完成实验。
综上所述,我们撰写本文的目的,就是要告诉学生解决一个问题可以有多种思路,一种思路又可以有多种方法。同时启发学生自主设计、进行实验,在不断的设计、实验、反思中完善方法,形成理念,进而培养学生的创新意识和探究精神。
参考文献:
[1]范广,张引莉,孙家娟.氧化铜与氧化亚铜稳定性的热力学讨论[J].广州化工,2012,40(10):162~163.
[2]毕华林.义务教育教科书·化学(九年级)(全一册)[M].济南:山东教育出版社,2013:79.
[3]张升晖,杨春海.化学实验[M].北京:中国计量出版社,2007.

