选择性铵离子交换MCM-49分子筛的酸性及催化性能研究*
赵 飞,高伟东,姜文静,暴 跃,张 钰**
(1.吉林化工学院 材料科学与工程学院,吉林 吉林 132022;2.中国石油吉林石化公司 乙烯厂,吉林 吉林 132021)
MCM-49分子筛是1993年Bennett[1]报道的具有MWW层状结构的微孔分子筛,3套独立的孔道体系构成其分子筛骨架:一是层间超笼孔系(0.71 nm×0.71 nm×1.82 nm);二是层内二维正弦网状孔道(0.40 nm×0.59 nm);三是密布于晶体外表面杯状半笼结构(0.70 nm×0.71 nm×0.71 nm)。MCM-49分子筛具有较大的外比表面积,正弦孔道对分子扩散有较强的限域作用,同时层间超笼可为大分子过渡态提供空间,在催化反应中表现出优异的择形性能和稳定性[2-4],被广泛应用于异构化、催化裂化、烷基化等反应过程[5-9]。在苯与丙烯烷基化合成异丙苯的反应中,Corma等的研究表明,烷基化反应主要发生在MCM-49分子筛外表面的十二元环孔穴,而层间正弦孔道和超笼处易发生丙烯齐聚,不仅降低了原料丙烯的利用率和产物选择性,更是分子筛积碳及失活的主要原因[10-11]。因而,研究有效的方法既保留MCM-49分子筛外表面酸性位,又能够适当抑制内表面酸中心,对提高该反应的丙烯利用率、提高选择性、抑制积碳将会有积极作用。在现有固体酸酸性调变方法中,脱铝改性、磷酸改性、稀土离子改性等方法不能对分子筛内、外表面进行选择性调变[8-9],而采用大分子有机物虽能够选择性地中毒分子筛外表面,却对分子筛内表面酸性起不到调变作用。以过量的氯化钠溶液处理MCM-49分子筛的内、外表面酸中心,然后以四丙基溴化铵(TPABr)选择性交换MCM-49,使酸中心主要分布于HMCM-49外表面,对其苯与丙烯液相烷基化催化性能进行了对比研究。
1 实验部分
1.1 试剂与仪器
偏铝酸钠:AR,上海江浦化学制品厂;硅溶胶:LUDOX AS-30,青岛海洋化工厂;六亚甲基亚胺(HMI):AR,江西射阳化工厂;TPABr:AR,百灵威化学技术公司;硝酸铵:AR,天津化学试剂二厂;丙烯:聚合级,光明气体公司;苯:AR,天津化学试剂二厂。
均相水热合成反应釜:JXF-8,烟台松岭化工有限公司;电热恒温鼓风干燥器:DHG-9240A,上海一恒仪器公司;马弗炉:SX-5-12,天津泰斯特仪器设备有限公司;高压固定床微型反应器:FINEREACTOR-4100C,浙江泛泰仪器设备有限公司;转靶X射线衍射仪:Shimadzu XRD-6000;气相色谱仪:Shimadzu GC-14B,日本岛津公司;红外光谱仪:Nicolet Impact 410,美国尼高力公司;扫描电子显微镜:Hitachi X-65,日本日立公司。
1.2 催化剂制备
1.2.1 MCM-49制备
采用动态水热合成方法,以偏铝酸钠为铝源,硅溶胶为硅源,HMI为模板剂制备MCM-49分子筛[n(SiO2)∶n(Al2O3)=12.5][8],晶化温度175 ℃,晶化时间72 h。将晶化产物过滤、洗涤至中性后烘干12 h,并于空气气氛中以3 ℃/min的速度升温至540 ℃,并恒温焙烧6 h,制得NaMCM-49分子筛。在85 ℃下,将焙烧后的NaMCM-49与1 mol/L NH4NO3水溶液进行铵离子交换,经过滤、洗涤、干燥后在空气气氛下3 ℃/min升温至540 ℃恒温焙烧6 h,得HMCM-49(NH4NO3)。
1.2.2 选择性铵离子交换MCM-49分子筛的制备
将NaMCM-49与1.0 mol/L NaCl水溶液在50 ℃下离子交换3次,共计12 h,经过滤、洗涤至中性后于120 ℃干燥过夜,焙烧后得Na-NaMCM-49。将Na-NaMCM-49与质量分数35%的TPABr水溶液在一定温度下离子交换4 h,然后过滤、洗涤、干燥过夜。所得样品在空气气氛下于100 ℃恒温2 h,以1 ℃/min升温至540 ℃并恒温6 h,所得样品标记为HMCM-49(TPABr-交换温度-交换次数),分别得到HMCM-49(TPABr-333K-1)、HMCM-49(TPABr-333K-2)和HMCM-49(TPABr-298K-1)。
1.3 催化剂评价
采用高压固定床反应器进行苯与丙烯液相烷基化反应催化性能评价。催化剂颗粒度为0.25~0.425 mm,填装量为1.5 g,原料流向为上进下出,反应系统压力保持在3.5 MPa。首先向反应器中进入苯,待反应管被苯液所充满,系统温度、压力达到设计值后,原料丙烯经加压液化后由泵计量加入反应器,反应产物经冷阱收集。产物分析在Shimadzu GC-14B气相色谱仪上进行,采用氢火焰检测器,采用面积归一化法对产物进行定量计算,校正因子通过实验测定。采用丙烯转化率、异丙苯选择性和烷基化产物总选择性说明催化剂的催化性能。其中,异丙苯选择性代表异丙苯占烷基化产物(异丙苯、二异丙苯和三异丙苯)的摩尔分数(以丙烯为基准计算),烷基化产物总选择性代表异丙苯、二异丙苯和三异丙苯3者所消耗的丙烯占所有消耗丙烯的产物的摩尔分数。
1.4 催化剂表征
采用日本岛津Shimadzu XRD-6000型转靶X射线衍射仪对样品进行物相分析,Cu Ka 靶(λ=0.154 2 nm),管电压40 kV,管电流30 mA。采用Hitachi X-65扫描电子显微镜对样品形貌进行表征。利用原位吸附-红外测试装置进行氘代乙腈吸附-红外光谱测试,过程如下:将样品自撑片置入红外样品池,在350 ℃下真空处理1 h,室温吸附氘代乙腈并真空处理1 h后,采用Nicolet Impact 410型红外光谱仪进行红外光谱测试。采用动态程序升温脱附装置进行NH3-TPD测试,过程如下:将催化剂样品50 mg置于氩气流下550 ℃吹扫1 h,降温至100 ℃吸附氨气0.5 h后脱附1 h,然后以10 ℃/min的速度程序升温至600 ℃脱附。
2 结果与讨论
2.1 物相和结构表征
NaMCM-49分子筛在焙烧前和焙烧后的XRD谱图见图1。
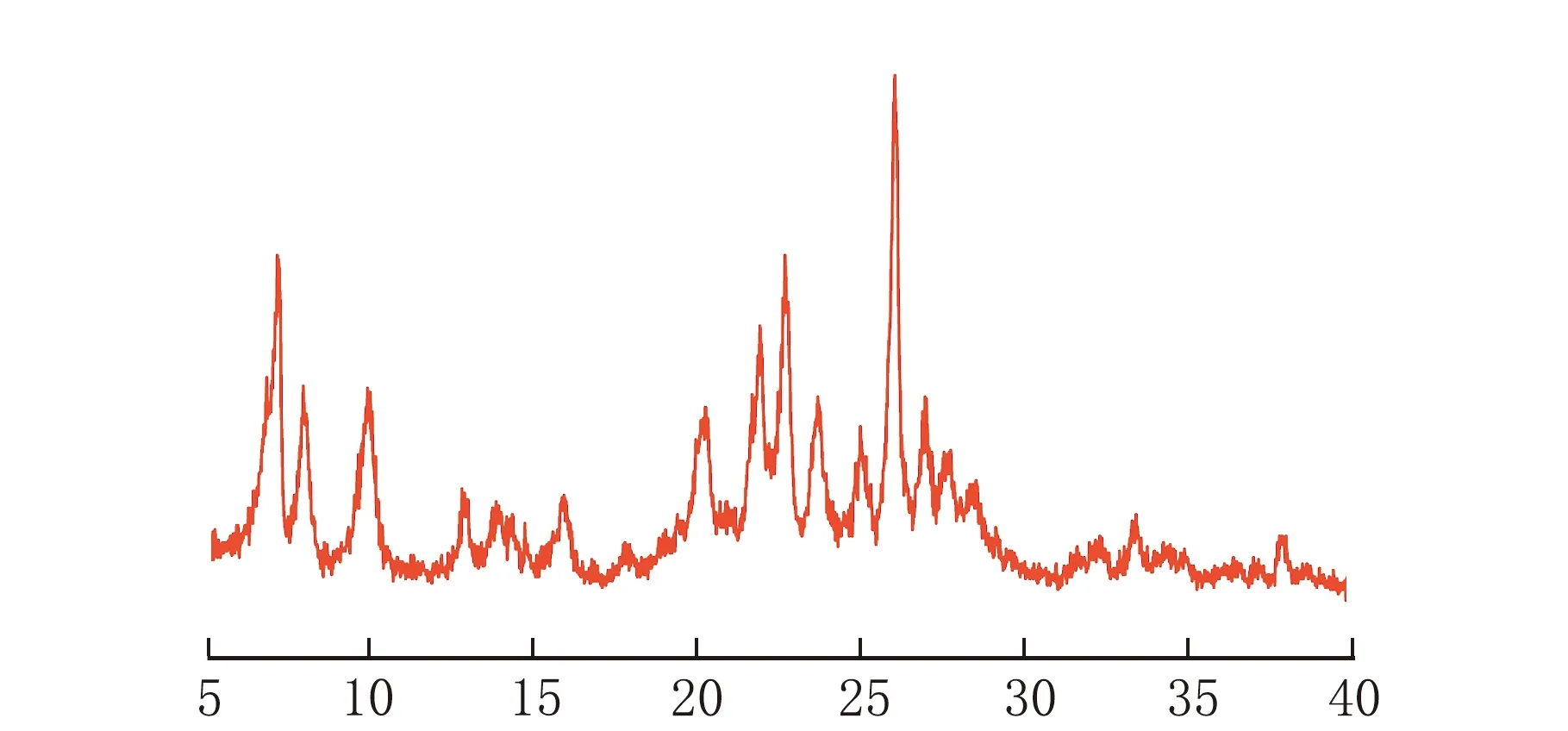
2θ/(°)a 焙烧前
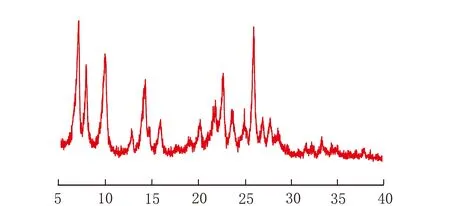
2θ/(°)b 焙烧后图1 NaMCM-49分子筛的X射线衍射图谱
由图1可见,衍射峰的峰位和相对强度均与文献报道相一致[12],与焙烧前样品相比,焙烧后的NaMCM-49在15°附近的衍射峰强度明显增高,表明所制备的是高纯度、高结晶度的MCM-49分子筛。
NaMCM-49分子筛的扫描电镜照片见图2。
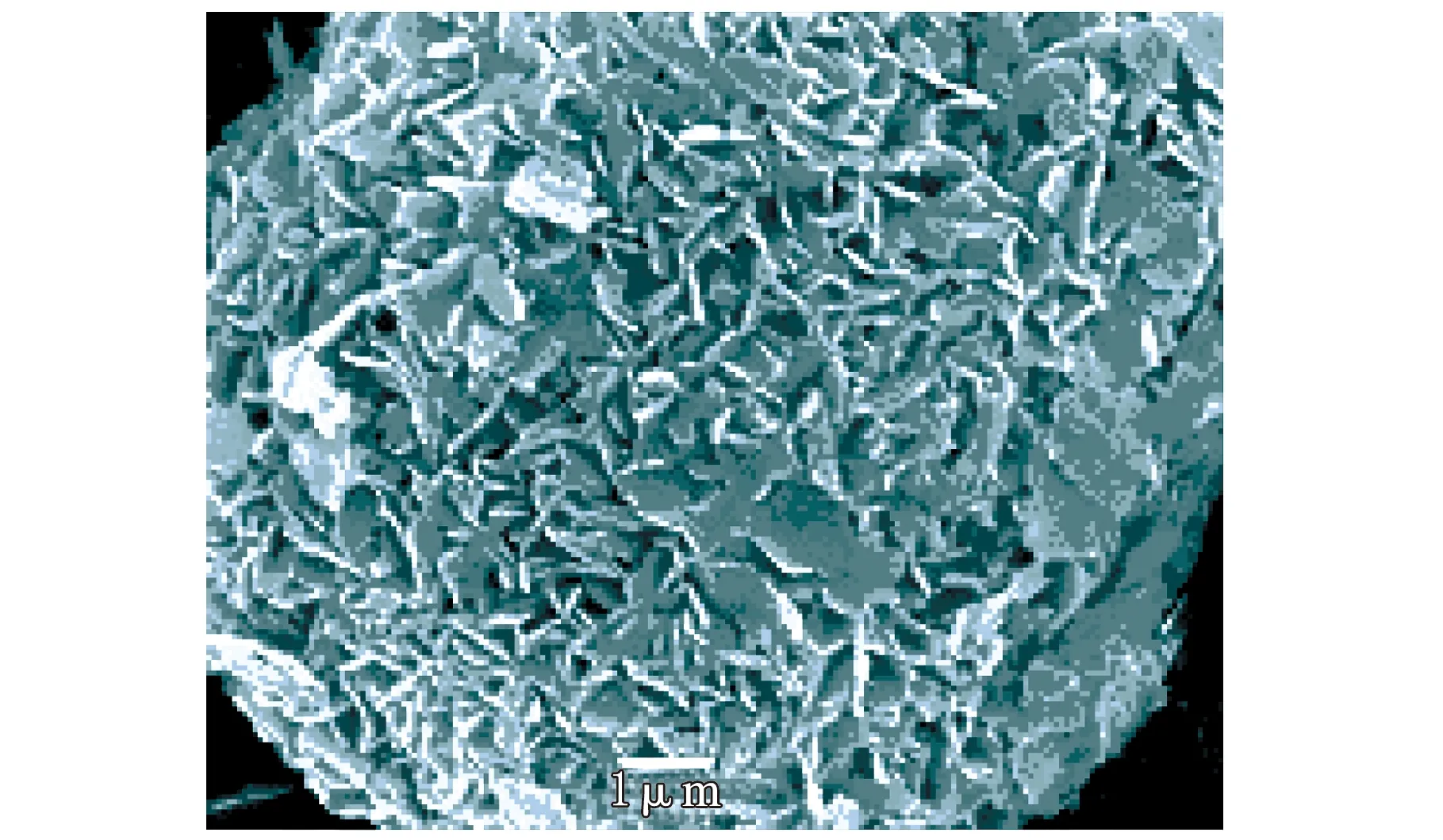
图2 焙烧前NaMCM-49分子筛的扫描电镜照片
由图2可见,NaMCM-49分子筛为椭圆形薄层片状晶体,延晶片的x轴、y轴方向尺寸约为500 nm,延晶片z轴方向尺寸约80~110 nm。
2.2 NH3-TPD酸性表征
HMCM-49(NH4NO3)、Na-NaMCM-49和HMCM-49(TPABr)的NH3-TPD曲线见图3。
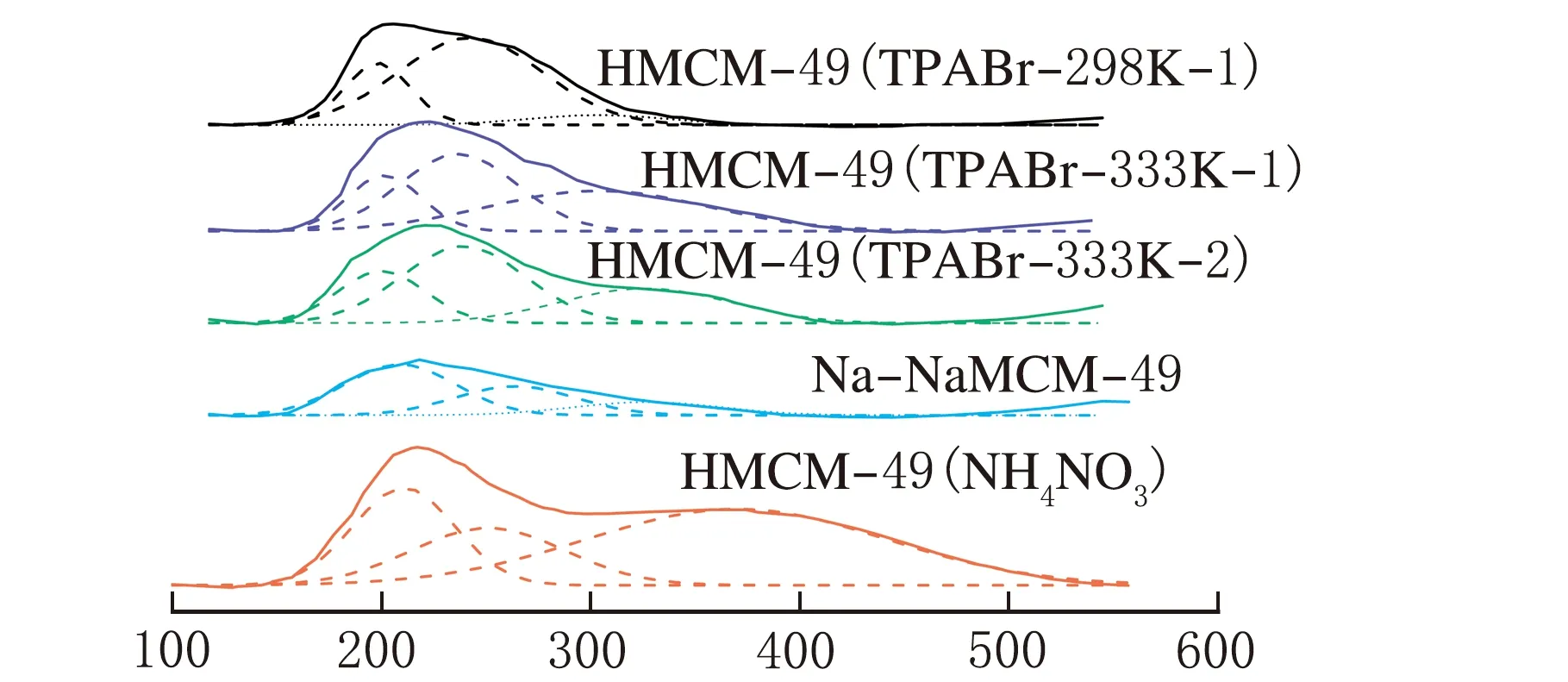
t/℃图3 HMCM-49分子筛的氨程序升温脱附曲线
程序升温脱附曲线的2个峰分别代表弱酸位氨的脱附和强酸位氨的脱附。实验中发现,增加硝酸铵的交换次数和交换时间并不能进一步增加NH3-TPD曲线的脱附峰面积。在该实验条件下,硝酸铵与分子筛内、外表面的离子交换反应充分进行。
实验中采用氯化钠溶液与NaMCM-49分子筛多次离子交换获得了Na-NaMCM-49。由Na-NaMCM-49的NH3-TPD曲线可见,脱附峰总面积很小,强酸位基本没有脱附峰出现,仅存在少量弱酸脱附峰,说明Na-NaMCM-49上绝大部分酸中心被钝化。将Na-NaMCM-49与TPABr离子交换后获得了HMCM-49(TPABr)。与Na-NaMCM-49相比,HMCM-49(TPABr-333K-2)的氨脱附峰总面积明显增加,说明TPABr离子交换有效进行。HMCM-49(TPABr-333K-2)的NH3-TPD曲线上弱酸中心的脱附峰面积与HMCM-49(NH4NO3) 基本相当,强酸中心的脱附峰面积则明显低于HMCM-49(NH4NO3),分子筛总酸量降低了近50%,酸强度基本不变。随着离子交换温度的提高和交换次数的增加,HMCM-49(TPABr)的总酸量和强酸中心酸量持续增加。
2.3 氘代乙腈-红外光谱测试酸性表征
采用氘代乙腈吸附-红外光谱测试研究了HMCM-49(NH4NO3)、Na-NaMCM-49和HMCM-49(TPABr-333K-2)上B酸和L酸的酸量(见图4),并利用高斯拟合进行定量计算。氘代乙腈是比较敏锐的探针小分子,容易扩散进入分子筛内部微孔,被广泛应用于微孔固体酸酸性的表征[13-16]。在氘代乙腈吸附-红外光谱谱图中,与强L酸位(Al—OH)相结合的C≡N峰出现在2 323 cm-1处,2 299 cm-1处代表C≡N结合在分子筛B酸位的(Si—OH—Al)谱峰,而硅羟基(Si—OH)和C—2H的谱峰分别出现在2 285和2 255 cm-1处。
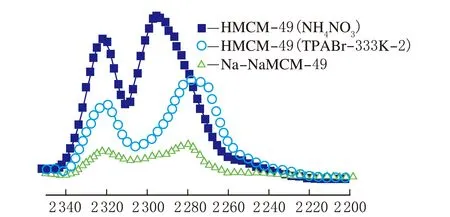
σ/cm-1图4 HMCM-49分子筛的氘代乙腈吸附-红外光谱谱图
由图4可见,Na-NaMCM-49呈现出极低的L酸和弱B酸酸量,这与NH3-TPD表征结果一致,进一步证明钠离子交换对MCM-49分子筛的酸中心起到钝化作用。与Na-NaMCM49相比,HMCM-49(TPABr-333K-2)红外谱图上代表强L酸,弱B酸(硅羟基)和硅铝桥羟基的峰面积明显增加。高斯拟合计算结果表明,HMCM-49(TPABr-333K-2)的L酸量和B酸量分别为HMCM-49(NH4NO3)的51%和44%。考虑到Na-NaMCM49上残存的B酸峰面积,经计算分布在MCM-49分子筛外表面的B酸中心约占总B酸中心的12.6%,该结果与文献报道的MCM-22分子筛的数据相接近。
上述酸性表征结果表明,采用TPABr为铵化剂,通过调整离子交换温度、交换时间和交换次数,制备出了酸中心主要分布在分子筛外表面且具有不同强酸酸量的HMCM-49(TPABr)催化材料。
2.4 HMCM-49分子筛催化性能
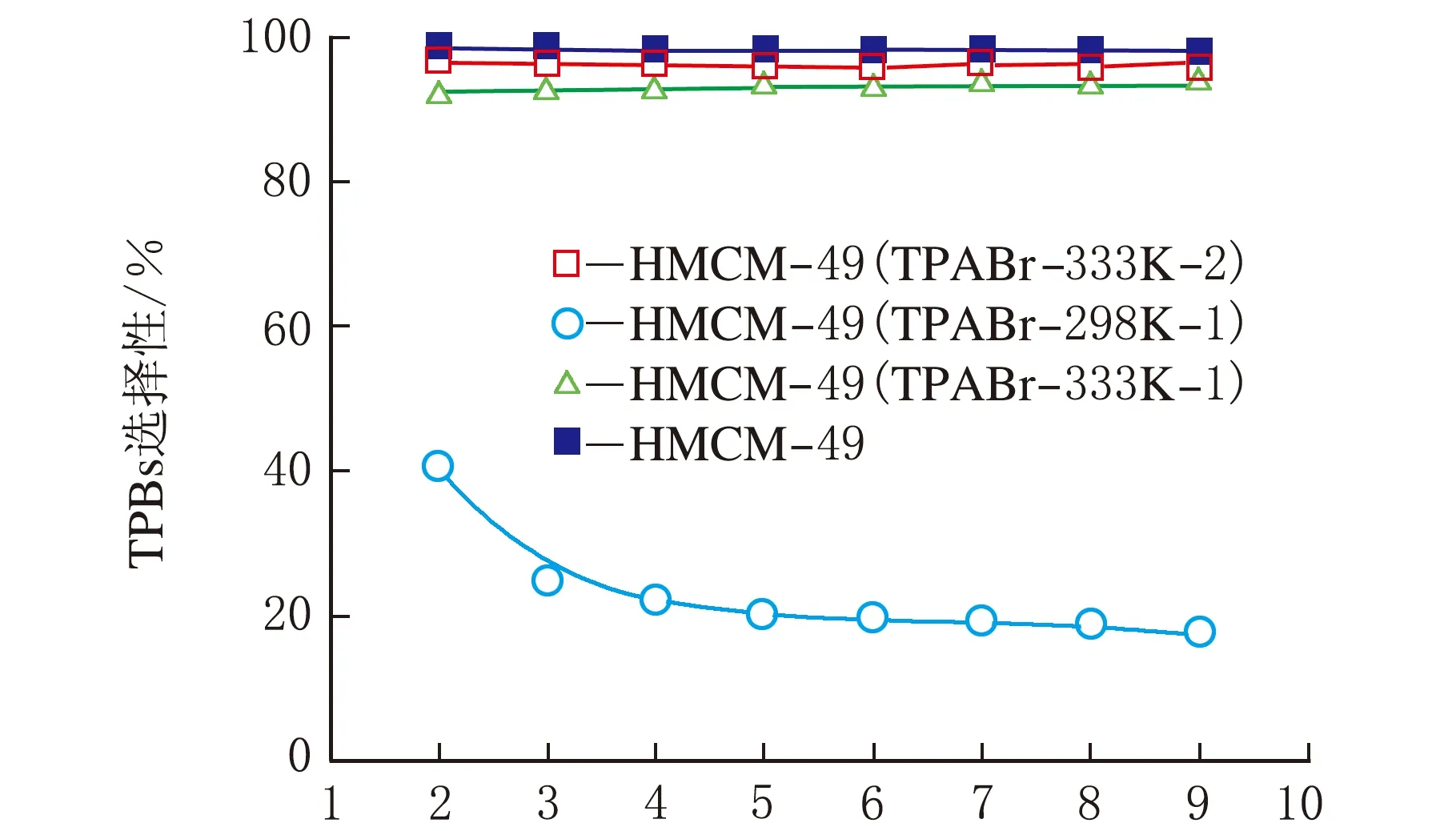
在烷基化反应温度为140 ℃、反应压力3.5 MPa、n(苯)∶n(丙烯)=6、丙烯空速为1.3 h-1、反应时间9 h的条件下,研究了HMCM-49分子筛催化苯与丙烯液相烷基化反应催化性能。HMCM-49(NH4NO3)和HMCM-49(TPABr)分子筛的催化活性、选择性及其随反应时间的变化情况见表1和图5。
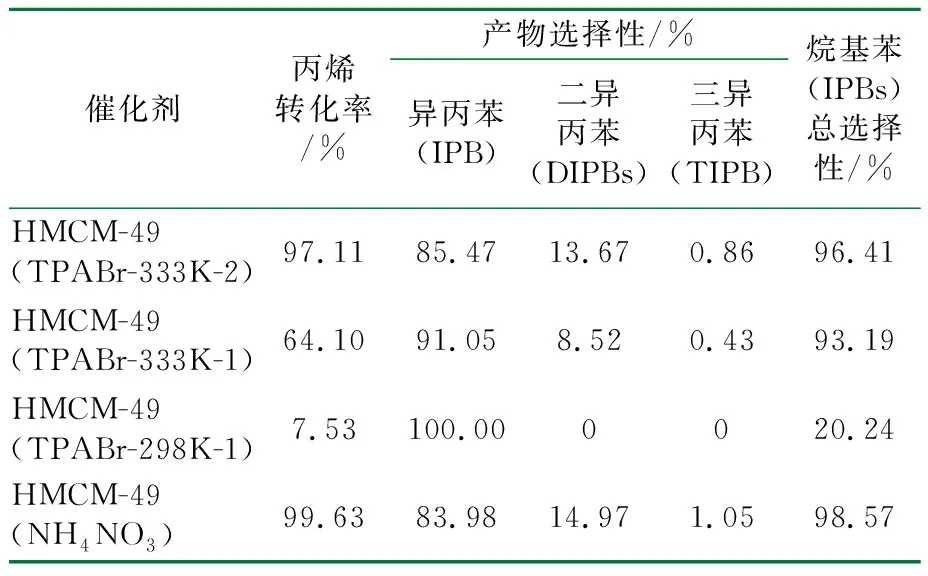
表1 HMCM-49催化活性及选择性数据
在催化活性方面,HMCM-49(NH4NO3)丙烯转化率较高,达到99.63%。HMCM-49(TPABr)3个样品的丙烯转化率存在明显差异。HMCM-49(TPABr-333K-2)的丙烯转化率与HMCM-49(NH4NO3)相比降低了2.5%,达到97.11%。HMCM-49(TPABr-333K-1)的丙烯转化率为64.1%,而HMCM-49(TPABr-298K-1)的丙烯转化率仅为7.53%。
在催化选择性方面,HMCM-49(NH4NO3)分子筛的烷基化产物总选择性达到98.57%,异丙苯选择性为83.98%(以丙烯为基准计算)。与之相比,HMCM-49(TPABr-333K-2)的烷基化产物总选择性为96.41%,异丙苯选择性为85.47%,略高于HMCM-49(NH4NO3)。HMCM-49(TPABr-298K-1)的烷基化产物总选择性则约为20%,这可能是由于其有效强酸中心不足,大量丙烯无法发生烷基化反应而转化为丙烯低聚物。
对比酸性表征结果可见,在NH3-TPD曲线上各分子筛样品的弱酸中心酸量没有明显差异,而强酸酸量符合HMCM-49(NH4NO3)>HMCM-49(TPABr-333K-2)>HMCM-49(TPABr-333K-1)>>HMCM-49(TPABr-298K-1)的规律,与催化活性规律相一致,这说明苯与丙烯液相烷基化反应主要发生在强酸中心。虽然HMCM-49(TPABr-333K-2)的强酸量明显低于HMCM-49(NH4NO3),但两者催化活性却基本相当,说明二者的有效强酸中心酸量基本相当。由于TPABr的分子动力学直径远远大于MCM-49分子筛层间十元环窗口直径,所形成的酸中心应主要分布于分子筛外表面的十二元环孔穴及孔口。上述结果表明外表面的强酸中心是苯与丙烯液相烷基化反应的有效活性位,TPABr选择性离子交换方法抑制了内表面酸中心的同时保留了外表面有效强酸中心。另外,对比HMCM-49(TPABr)的NH3-TPD曲线强酸脱附峰面积和图5中相应样品的丙烯转化率,发现苯与丙烯液相烷基化催化活性与外表面强酸中心酸量之间存在一定的对应关系。
t/h
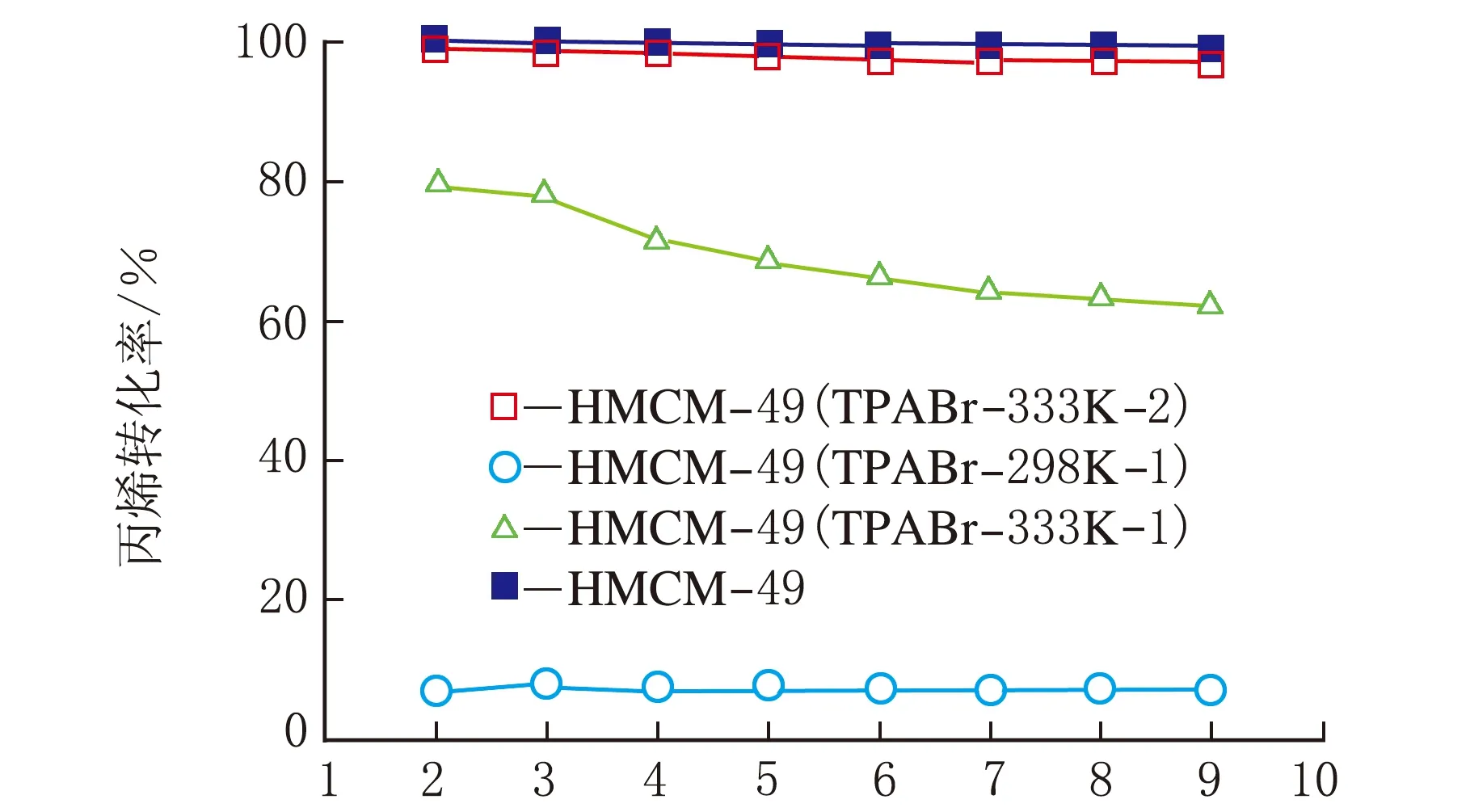
t/h图5 HMCM-49分子筛催化性能对比
3 结 论
采用动态水热合成方法制备出高纯度、高结晶度的纳米MCM-49分子筛,采用TPABr选择性地交换MCM-49分子筛外表面的钠离子,制备出酸中心主要分布在外表面的HMCM-49(TPABr)。采用NH3-TPD和乙腈吸附-红外光谱测试对分别以硝酸铵和TPABr制备的HMCM-49的酸性质进行了研究,考察了HMCM-49分子筛催化苯与丙烯液相烷基化反应的催化活性和选择性。结果如下。
(1) 氯化钠溶液处理结合TPABr选择性离子交换的方法抑制了内表面酸中心的同时保留了外表面有效强酸中心,调整TPABr离子交换条件,可以获得酸中心主要分布在外表面并具有不同强酸酸量的HMCM-49(TPABr)催化材料;
(2) 外表面的强酸位是苯与丙烯液相烷基化反应的有效活性位,苯与丙烯液相烷基化催化活性与外表面强酸中心酸量之间存在一定的对应关系;
(3) TPABr选择性离子交换制备的HMCM-49(TPABr)具有较好的催化性。在反应温度140 ℃,n(苯)∶n(丙烯)=6的条件下,丙烯转化率略低于HMCM-49(NH4NO3),异丙苯选择性达到85.47%,略高于HMCM-49(NH4NO3)。
[ 参 考 文 献 ]
[1] Bennett J M,Chang C D,Lawton S L,et al.Synthetic porous crystalline MCM-49,its synthesis and use:US,5236575[P].1993-08-17.
[2] Leonowicz M E,Lawton J A,Lawton S L,et al.MCM-22:a molecular sieve with two independent multidimensional channel systems [J].Science,1994,264:1910-1913.
[3] Lawton S L,Lenowicz M E,Partrideg R D,et al.Twelve-ring pockets on the external surface of MCM-22 crystals [J].Micropor Mesopor Mater,1998,23:109-117.
[4] Lawton S L,Fung A S,Kennedy G J,et al.Zeolite MCM-49:a three-dimensional MCM-22 analogue synthesized by in situ crystallization [J].J Phys Chem,1996,100:3788-3798.
[5] Eller Karsten,Kummer Rudolf.Preparation of amines from olefins on zeolites of the MCM-49 or MCM-56 type:US,5840988[P].1998-11-24.
[6] Cheng Jane C,Huang Tracy J.Process for the alkylation of benzene-rich reformate using MCM-49:US,5545788 [P].1996-08-13.
[7] Brown Stephen H,Crane Robert A,Caul Lorenzo De.Ethyl acetate synthesis from ethylene and acetic acid using solid acid catalysts:US,5973193[P].1999-10-26.
[8] 张钰,吴淑杰,杨胥微,等.脱铝MCM-49分子筛酸性及苯与丙烯液相烷基化性能研究[J].高等学校化学学报,2007,28(7):1319-1324.
[9] 张钰,王丽霞,吴淑杰,等.磷酸修饰MCM-49分子筛的结构、酸性及苯与丙烯烷基化反应性能研究[J].高等学校化学学报,2007,28(9):1726-1730.
[10] Corma A,Martinez-Soria V,Schnoeveld E.Alkylation of benzene with short-chain olefins over MCM-22 zeolite:catalytic behaviour and kinetic mechanism [J].Journal of Catalysis,2000,192:163-173.
[11] Du H,Olson D H.Surface acidic properties of a HMCM-22 zeolite:collidine poisoning and hydrocarbon adsorption studies [J].J Phys Chem B,2002,106:395-402.
[12] Rubin Mae K,Chu Pochen.Composition of synthetic porous crystalline material,its synthesis and use:US,4954325 [P].1990-09-04.
[13] Sobalik Z,Tvaruzkova Z,Wichterlova B,et al.Acodic and catalytic properties of Mo/MCM-22 in methane aromatization:an FTIR study [J].Applied Catalysis A:General,2003,253:271-282.
[14] Wichterlova B,Tvaruzkova Z,Sobalik Z,et al.Determination and properties of acid sites in H-ferrierite:a comparison of ferrierite and MFI structure [J].Microporous and Mesoporous Materials,1998,24:223-233.
[16] Wu Peng,Kan Qiubin,Wang Dongyang,et al.The synthesis of Mo/H-MCM-36 catalyst and its catalytic behavior in methane non-oxidative aromatization [J].Catalysis Communications,2005,6(7):449-454.

