一种新型1,8-萘酰亚胺衍生物的合成及光谱性能研究*
张聿平,陆林华,徐冬梅
(苏州大学 材料与化学化工学部,江苏 苏州 215123)
1,8-萘酰亚胺及其衍生物因具有色泽鲜艳、荧光强烈、荧光量子效率高、光稳定性和热稳定性好、分子易于修饰等优点,而成为一类备受关注的功能材料,被广泛用于荧光染料和荧光增白剂[1]、荧光探针和传感器[2]以及光电材料[3]。
pH值在生命体系和生理活动以及工农业生产和环境等领域都起着重要的作用,其监测和控制意义重大[4]。1,8-萘酰亚胺衍生物是一个典型的光诱导电子转移(PET) 体系,可以在其结构的4-位或5-位上引入不同的烷胺基调节PET过程,从而改变其对pH值的响应性[5-6]。在温和的条件下将2-(2-羟乙基氨基)乙氨基引入到1,8-萘酰亚胺的4-位上,合成了一种新型的化合物N-正丁基-4-(2-(2-羟乙基氨基)乙氨基)-1,8-萘酰亚胺(ABN),并研究了其光物理性能及其光物理性能对pH值的响应性。
1 实验部分
1.1 试剂与仪器
4-溴-1,8-萘酐(BNA):分析纯,辽阳联港染料化工有限公司;羟乙基乙二胺(AEEA):质量分数>99%,苏州联胜化学有限公司;正丁胺(BA)、乙腈、乙醇、四氢呋喃(THF)、甲醇、N,N-二甲基甲酰胺(DMF)、乙酸乙酯、氯仿、石油醚、氢氧化钠、硼酸、磷酸、乙酸:分析纯,国药集团上海试剂有限公司。
Agilent 1200/6220型质谱仪:美国Agilent公司;UNITY INOVA 400型核磁共振谱仪:美国Varian 公司;Magna-550型傅立叶变换红外光谱仪:美国Nicolet 公司:U-3900 紫外-可见光谱仪:美国Perkine Elmer公司;Fluoromax-4荧光光谱仪:法国HORIBA Jobin Yvon 公司;Mettler-Toledo FE20 pH 计:美国Mettler-Toledo 公司;X-6型显微熔点测定仪:北京泰克仪器有限公司。
1.2 ABN的合成
N-正丁基-4-溴-1,8-萘酰亚胺(BrBN) 的合成[7]。n(BNA)∶n(BA) =1∶1.5,在三口烧瓶中,将BNA溶于乙醇,通氮气,加热并搅拌,当温度达到50 ℃时逐滴加入BA,滴毕升温至80 ℃,恒温反应24 h。减压除去溶剂,用去离子水洗涤,得黄色固体粗产品,用乙醇重结晶得黄白色针状晶体BrBN,收率为86.5%,熔点为102~104 ℃。
ABN的合成。n(BrBN)∶n(AEEA)=1∶11,在三口烧瓶中,将BrBN溶于乙醇,通氮气,加热并搅拌至溶液透明后,逐滴加入AEEA,滴毕升温至80 ℃,恒温反应24 h。减压除去溶剂,得黄色固体粗产品,用乙酸乙酯和石油醚[V(乙酸乙酯)∶V(石油醚)=1∶4]重结晶,再经硅胶柱层析,洗脱剂为甲醇和氯仿[V(甲醇)∶V(氯仿)=2∶5],得黄色固体产物ABN,收率为58.6%。
合成原理见图1。
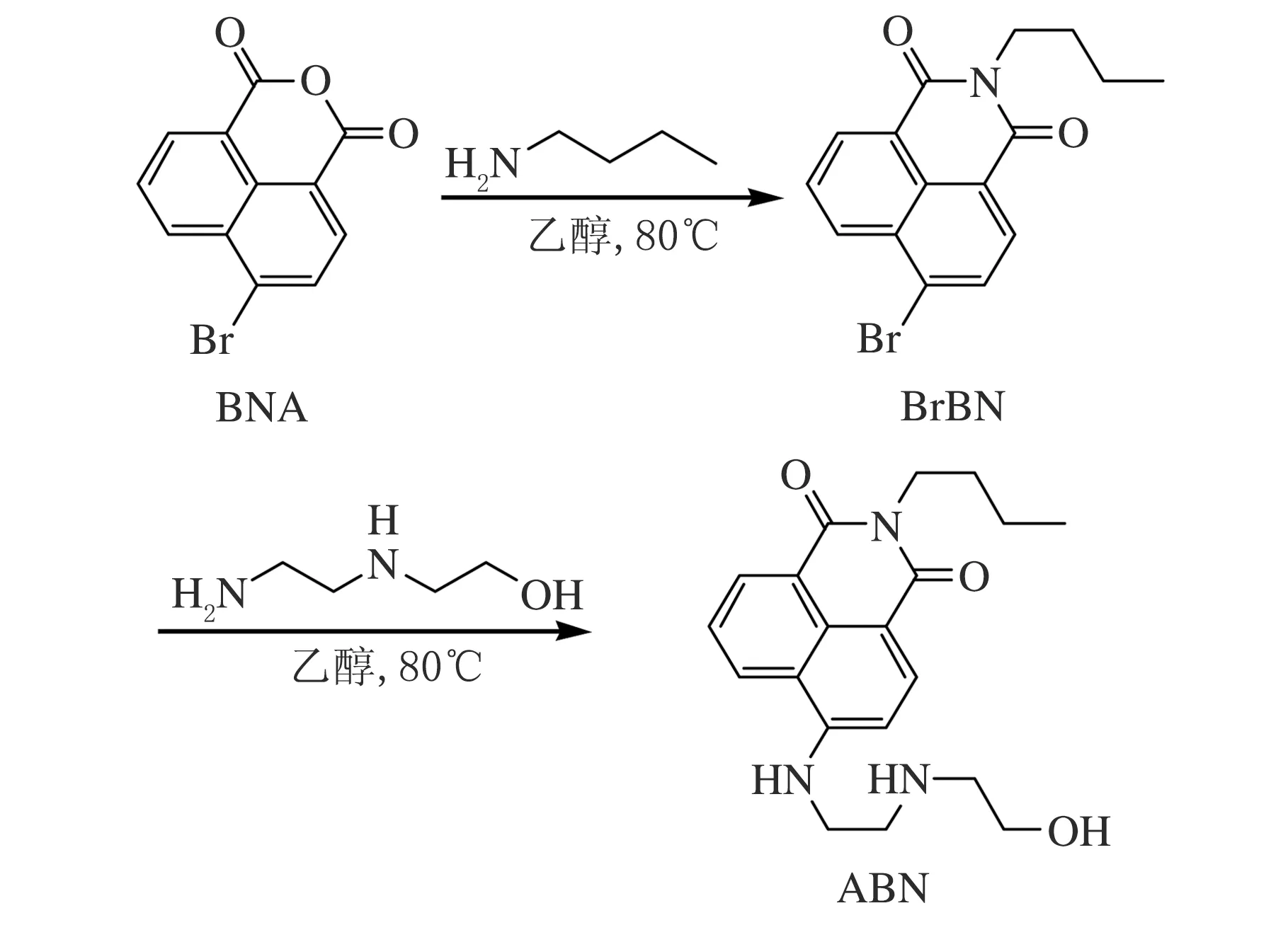
图1 合成原理图
2 结果与讨论
2.1 ABN的结构表征
2.1.1 红外光谱
ABN的红外光谱图见图2。
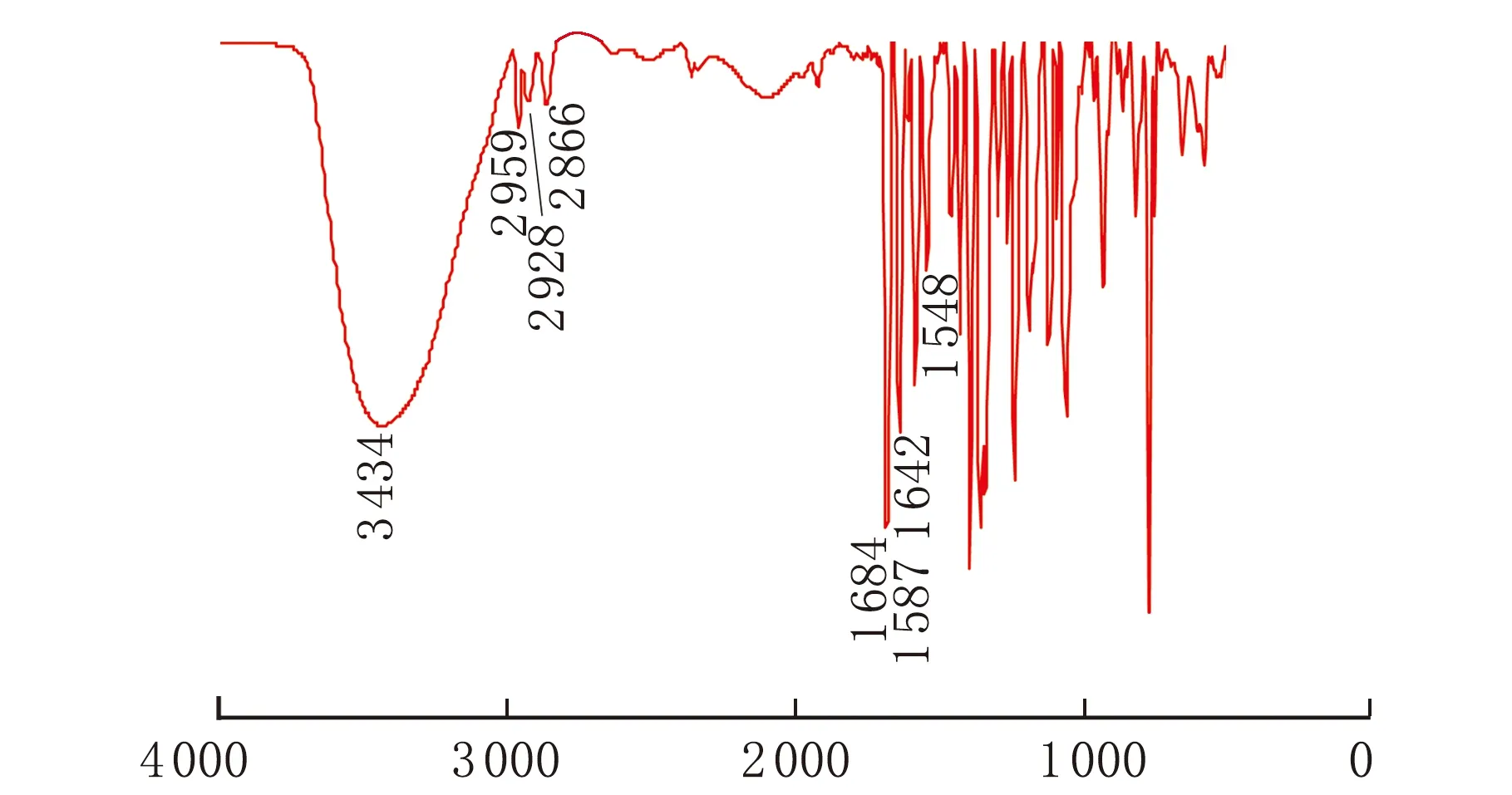
σ/cm-1图2 ABN的FTIR谱图

2.1.2 核磁共振
ABN的1H-NMR谱图(DMSO-d6)见图3。从图3中可看出,ABN中各种氢的化学位移(δ/×10-6):0.85~0.96(a;3H;CH3;t),1.27~1.40(b;2H;CH2CH2CH2CH3;m),1.50~1.65(c;2H;CH2CH2CH2CH3;m),2.64~2.72(h;2H;NHCH2CH2OH;m),2.86~2.94(f;2H;ArNHCH2CH2NH;m),3.43~3.52(d;2H;CH2CH2CH2CH3;t;e;2H;ArNHCH2CH2NH;m),3.95~4.08(i;2H;NHCH2CH2OH;m),4.55~5.59(j;1H;OH;或g;1H;CH2NHCH2;s),6.80~6.88(m;1H;ArH;d),7.65~7.80(o;1H;ArH;n;1H;ArNHCH2CH2NH;m),8.24~8.29(l;1H;ArH;d),8.40~8.48(k;1H;ArH;d),8.65~8.75(p;1H;ArH;d)。其中化学位移δ=2.50处的质子峰归属于溶剂DMSO-d6,δ=3.33处的质子峰归属于DMSO-d6中的H2O。
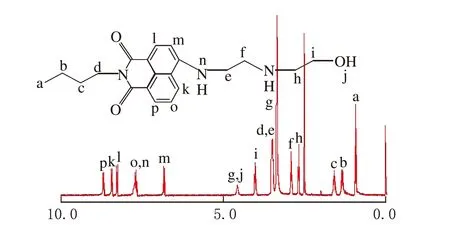
δ/×10-6图3 ABN的1H-NMR谱图(DMSO-d6为溶剂,400 MHz)
2.1.3 质谱
ABN的质谱图见图4。
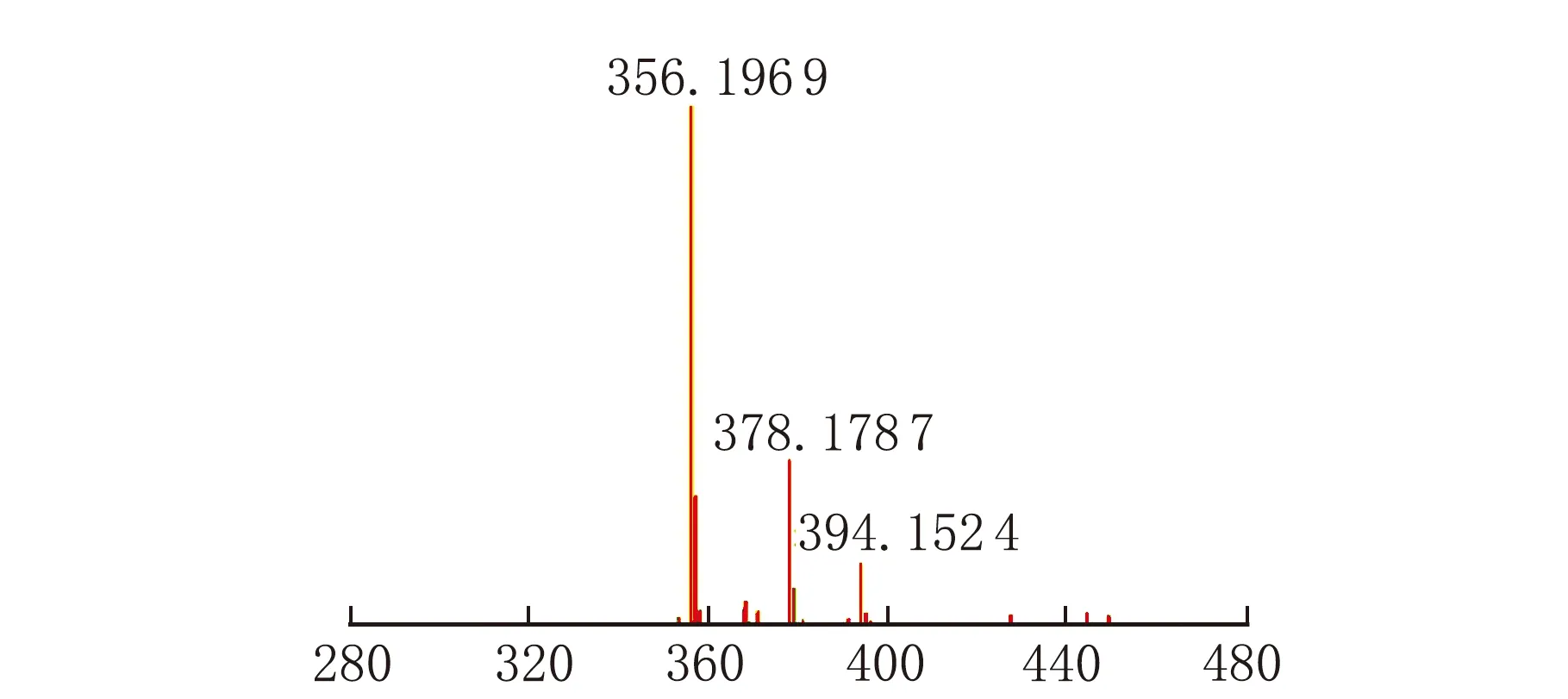
m/z图4 ABN的质谱图
图4中m/z=356.196 9、378.178 7和394.152 4分别对应于[M+H]+、[M+Na]+和[M+K]+分子离子峰。红外光谱、核磁和质谱分析结果证明成功合成了ABN。
2.2 ABN的光物理性能
2.2.1 ABN的吸收和发射光谱
选择不同溶剂配制浓度为5.0×10-5mol/L的ABN溶液,测定紫外-可见吸收光谱和荧光发射光谱,结果见图5和图6。
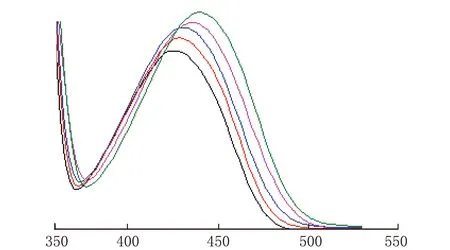
λ/nm图5 溶剂对ABN溶液紫外-可见吸收光谱的影响.
由上至下溶剂依次为DMF、CH3OH、CH3CN、THF、CH3COOCH2CH3。
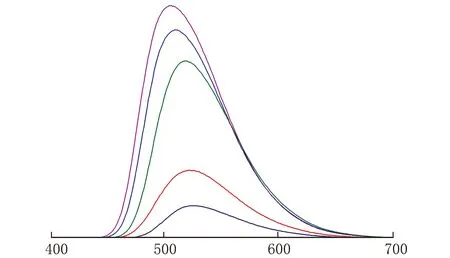
λ/nm图6 溶剂对ABN荧光光谱的影响
由上至下溶剂依次为CH3COOCH2CH3、THF、CH3CN、CH3OH、DMF,λex=433 nm,狭缝宽度5 nm。
由图5、图6可见,随着溶剂极性的增加,ABN溶液最大吸收波长和荧光波长红移,符合一般萘酰亚胺衍生物的光谱变化规律。溶剂对荧光光谱的影响大于对吸收光谱的影响。极性溶剂使荧光大大减弱,说明该分子从激发态返回基态时容易将能量转移给极性溶剂分子而以非辐射形式释放,即表现为荧光猝灭。
2.2.2 ABN的甲醇和DMF溶液的光物理性能
详细考察了ABN在甲醇和DMF中的光物理性能,结果见表1。由表1可见,在甲醇和DMF中,ABN的最大吸收波长分别为436 和440 nm(对应摩尔消光系数为1.20×104和1.25×104L/mol·cm),最大荧光波长为522和527 nm(对应荧光量子效率为0.509和0.073)。在DMF中荧光量子效率较小,可能是ABN分子与溶剂DMF分子之间作用较强,激发态的ABN分子把能量转移给DMF分子而以非辐射形式释放。

表1 ABN在甲醇和DMF中的光物理性能
荧光量子产率和斯托克斯位移用公式(1)和(2)计算。
(1)
(2)
其中,Фs和Фr为待测物质和参比物质的荧光量子产率;Ss和Sr为待测物质和参比物质的积分荧光强度;As和Ar为待测物质和参比物质在该激发波长的入射光的吸光度;nDs和nDr为溶解待测物质和参比物质的溶剂的折射率;λF和λA为待测物质的最大荧光波长和最大吸收波长。罗丹明B作为参比物质,在乙醇中Фr=0.97,nDr=1.361 0。
2.3 ABN荧光光谱的pH响应性
用不同pH值的Britton-Robinson缓冲溶液与ABN的DMF溶液配制不同pH值的ABN的DMF/Britton-Robinson缓冲溶液[V(DMF)∶V(Britton-Robinson缓冲溶液)=1∶99],测定荧光光谱,结果见图7。
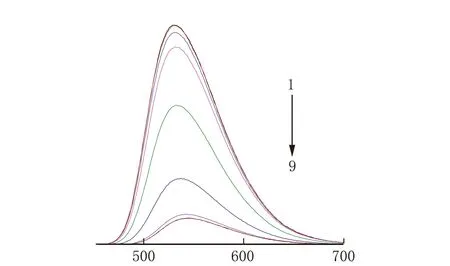
λ/nm1~9:pH=2.25,4.05,6.15,7.26,8.21,9.01,10.02,11.24图7 不同pH值的ABN溶液的荧光光谱
V(DMF)∶V(Britton-Robinson缓冲溶液)=1∶99,c(ABN)=5×10-5mol/L,λex=433 nm,狭缝宽度5 nm。
由图7可见,随着pH值的减小,ABN溶液的荧光强度逐渐增强。这是由于随着溶液酸性增大,ABN结构中(2-羟乙基)氨基(NHCH2CH2OH) 中的NH结合H+而给电子能力下降,向1,8-萘酰亚胺荧光团的PET过程减弱而导致荧光增强。pH值从11.24变化至2.25,荧光强度增强了8.6倍。在pH=6.73~9.61,ABN溶液的荧光强度与pH值呈良好的线性关系,线性方程为y= -2 059 940x+2.113 1×106,相关系数为0.957 77,说明ABN具备定量检测pH值的条件,是一个潜在的pH探针。由于所用溶剂DMF/Britton-Robinson缓冲溶液[V(DMF)∶V(Britton-Robinson缓冲溶液)=1∶99]中99%是水,而且线性pH范围在中性附近,因此ABN在环境和生命体系中pH值的检测方面有较好的应用前景。
3 结 论
(1) 在温和的条件下以中等收率合成了一种新型化合物:N-正丁基-4-(2-(2-羟乙基氨基)乙氨基)-1,8-萘酰亚胺(ABN)。通过红外光谱、核磁和质谱对ABN的结构进行了分析表征;
(2) 在乙酸乙酯、四氢呋喃、乙腈、甲醇、N,N-二甲基甲酰胺溶剂中,ABN的最大吸收波长分别为426、429、431、436和440 nm,最大荧光波长分别为506、510、519、522和527 nm。随着溶剂极性的增加,ABN溶液的吸收和发射光谱发生红移;
(3) ABN的荧光光谱具有较好的pH响应性:在接近全水的体系中,荧光强度随溶液酸性增强而增大,且在pH=6.73~9.61范围内,ABN溶液的最大荧光强度与pH值呈良好的线性关系,展现出ABN在环境和生命体系中pH值检测方面有较好的应用前景。
[ 参 考 文 献 ]
[1] 曹成波,朱艳丽,于学丽,等.萘酰亚胺类功能材料应用研究进展[J].精细与专用化学品,2007,15(3/4):6-10.
[2] Duke RM,Veale EB,Pfeffer FM,et al.Colorimetric and fluorescent anion sensors:an overview of recent developments in the use of 1,8-naphthalimide-based chemosensors[J].Chemical Society Reviews,2010,39:3936-3953.
[3] 袁忠义.苝酰亚胺和萘酰亚胺类有机半导体的设计、合成及性质研究[D].大连:大连理工大学,2010:4-14.
[4] Tan Y,Yu J,Gao J,et al.A fluorescent pH chemosensor for strongly acidic conditions based on the intramolecular charge transfer(ICT) effect[J].RSC Advances,2013,3:4872-4875.
[5] Bojinov VB,Simeonov DB,Georgiev Nikolai I.A novel blue fluorescent 4-(1,2,2,6,6-pentamethylpiperidin-4-yloxy)-1,8-naphthalimide pH chemosensor based on photoinduced electron transfer[J].Dyes and Pigments,2008,76(1):41-46.
[6] Xie J,Chen Y,Yang W,et al.Water soluble 1,8-naphthalimide fluorescent pH probes and their application to bioimagings[J].Journal of Photochemistry and Photobiology A:Chemistry,2011,223(2):111-118.
[7] 王建新,毕晨光,袁冰,等.荧光类非离子表面活性剂的设计与合成[J].石油化工,2006,35(5):464-468.

