磁性活性炭催化臭氧氧化降解水中甲基橙
任百祥,范晶莹,杨春维
(吉林师范大学 环境科学与工程学院,吉林 四平 136000)
材料与药剂
磁性活性炭催化臭氧氧化降解水中甲基橙
任百祥,范晶莹,杨春维
(吉林师范大学 环境科学与工程学院,吉林 四平 136000)
通过浸渍法制备了钕铁硼磁性活性炭(NdFeB/AC),采用SEM和VSM技术对其进行了表征,并将其作为非均相催化剂用于臭氧氧化降解水中甲基橙(MO)。表征结果显示:NdFeB/AC具有硬磁特性;当m(NdFeB)∶m(AC)=1∶2时,其比饱和磁化强度和比剩余磁化强度分别为15.9 A·m2/kg和6.0 A·m2/kg,矫顽力可达104.5 kA/m。实验结果表明:在NdFeB/AC投加量为3.0 g/L、初始溶液pH为5.0、初始MO质量浓度为20 mg/L、臭氧质量浓度为15.0 mg/L、室温的条件下反应40 min,MO降解率达93.9%,显著优于投加AC的64.4%;AC和NdFeB/ AC催化臭氧氧化降解MO的反应过程均遵循一级动力学规律,且NdFeB/AC的反应速率常数为AC的近3倍。
钕;铁;硼;磁性活性炭;非均相催化剂;臭氧;甲基橙
染料废水是一种高色度、强毒性、难处理的化学工业废水[1]。而其中的偶氮染料废水,由于具有污染物结构复杂、稳定性强、可生物降解性差等特点,使得传统的生物法对其处理效果不佳[2]。因此,高级氧化技术在该类废水的处理中受到重视。在众多高级氧化工艺中,臭氧氧化因其高效、二次污染小、工艺条件相对温和稳定等特点,逐渐引起注意[3-4]。臭氧具有高还原电位,尤其在碱性条件下,可分解产生强氧化性的羟基自由基,把难降解的大分子有机物氧化降解成低毒或无毒的小分子物质,从而提高废水的可生化性或直接将有机物降解矿化[5-6]。但单纯的臭氧氧化反应速率较慢,不能适应当今工业废水的处理要求[7],故催化臭氧氧化的开发应运而生[8]。
与均相催化剂相比,非均相催化剂因易分离、活性离子溶出少、反应速率快等特点而受到肯定[9]。活性炭(AC)作为一种非均相催化剂具有价格便宜、易获得、催化效果较好等优势,在有机废水的臭氧氧化处理领域受到关注[10]。但作为催化剂的粉末状活性炭具有回收困难的问题,故工业推广价值不大。
本工作采用浸渍法将具有较高磁性能的钕铁硼(NdFeB)永磁体粉末负载于颗粒状AC上,以实现磁性分离,并将其作为非均相催化剂用于臭氧氧化降解水中甲基橙(MO)。
1 实验部分
1.1 试剂、材料和仪器
MO、NaOH、硫酸、盐酸、CaCl2:分析纯。
AC:颗粒状,粒径0.3~2.0 mm,椰壳基;NdFeB:粉末状,粒径37~40 μm。
7407型振动样品磁强计:LakeShore公司;S-570型扫描电子显微镜:日立公司;UV-265型紫外-可见分光光度计:岛津公司;CH-Y30G型臭氧发生器:广州创环臭氧电气设备有限公司。
1.2 磁性AC的制备
AC的预处理:称取一定量的AC颗粒,于30%(w)的盐酸中浸泡24 h,取出,用去离子水洗至中性,于50 ℃下烘干备用。
分别称取一定量的NdFeB和预处理后的AC于烧杯中,加入0.1 mol/L的CaCl2溶液,中速搅拌(150 r/min)10 min;再加入10%(w)的硫酸调节pH以保持酸性,搅拌条件下浸渍10 min;外加磁场进行磁性分离,将分离出的颗粒物于50 ℃下干燥,制得磁性AC(NdFeB/AC)。
1.3 实验装置及方法
实验装置的示意图见图1。实验装置由臭氧发生器、三相流化床反应器(自制,有机玻璃材质,双层圆柱状,外柱半径60 mm,内柱半径40 mm,有效容积750 mL)、气体吸收装置3部分组成。反应器运行时,由臭氧发生器产生的气态臭氧经过流量计和三相流化床内管底端的曝气头进入反应器内管,并在反应器内柱中扩散,使催化剂与反应液在反应器内循环流动,臭氧流量由气体流量计控制。

图1 实验装置的示意图
用5%(w)的NaOH溶液或盐酸调节MO溶液的pH,取一定量的催化剂放入装有MO溶液的反应器中,通入臭氧后(产气量维持在10 g/h,臭氧质量浓度为15.0 mg/L,)开始计时,反应温度为室温((25±1)℃),每隔5 min取样,共反应40 min。
1.4 分析方法
采用SEM技术观察催化剂的微观形貌,采用振动样品磁强计(VSM)测定NdFeB/AC的磁滞回线,采用紫外-可见分光光度计测定MO溶液于波长510 nm处的吸光度,计算MO的质量浓度和降解率。
2 结果与讨论
2.1 NdFeB/AC的表征
2.1.1 SEM照片
AC和NdFeB/AC的SEM照片见图2。

图2 AC和NdFeB/AC的SEM照片
由图2可见:在未负载NdFeB磁粉前,AC表面虽不平整,但总体平滑,有较大比表面积;但在负载NdFeB后,表面的颗粒明显增多,且具有较丰富的蜂窝状结构。这表明,通过浸渍可将NdFeB磁粉负载于AC表面,使AC表面发生变化,比表面积增大。
2.1.2 磁滞回线
NdFeB/AC的磁滞回线见图3。由图3可见,AC负载NdFeB后表现出硬磁性材料的典型磁滞回线形态,说明该材料具备了硬磁性,因而更易通过外加磁场的方法进行分离。
2.1.3 m(NdFeB)∶m(AC)对NdFeB/AC磁性的影响
m(NdFeB)∶m(AC)对NdFeB/AC磁性的影响见图4。由图4可见,当m(NdFeB)∶m(AC)=1∶2时,NdFeB/AC具有较高的磁性,比剩余磁化强度和矫顽力分别达到6.0 A·m2/kg和104.5 kA/m的最高值,比饱和磁化强度也达到15.9 A·m2/kg的次高值。因此,选择m(NdFeB)∶m(AC)=1∶2的 NdFeB/AC作为催化剂进行后续实验。由图4还可见,m(NdFeB)∶m(AC)=1∶2的NdFeB/AC经过40 min的反应后,其比饱和磁化强度和比剩余磁化强度仍可达9.7 A·m2/kg和2.3 A·m2/kg,矫顽力为22.5 kA/m,可用磁性分离的方法轻松实现催化剂和溶液的分离。
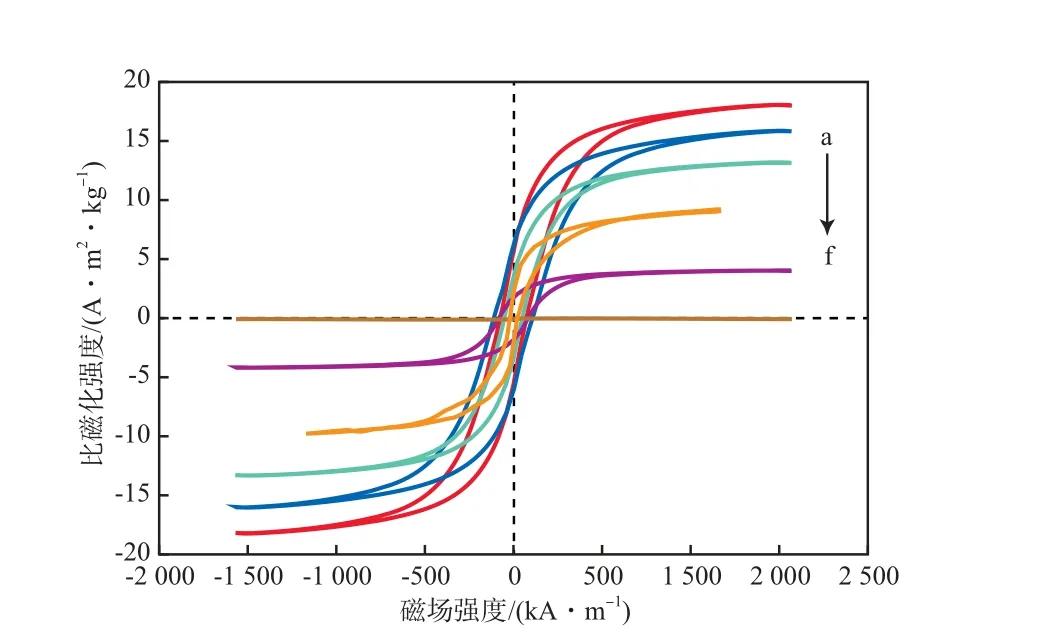
图3 NdFeB/AC的磁滞回线

图4 m(NdFeB)∶m(AC)对NdFeB/AC磁性的影响
2.2 MO的催化臭氧氧化降解
2.2.1 单因素实验
2.2.1.1 NdFeB/AC投加量
在初始溶液pH为5.0、初始MO质量浓度为20 mg/L的条件下,NdFeB/AC投加量对MO降解率的影响见图5。由图5可见:随NdFeB/AC投加量的增加,MO降解率呈上升趋势;当投加量为0.8 g/L时降解率仅为63.9%,而投加量增至3.0 g/L时降解率迅速升至93.9%;继续增加投加量至4.0 g/L,降解率变化不大。这主要是因为:非均相催化剂主要的催化活性点位位于催化剂表面,随催化剂投加量的增加,活性点位也相应增加,与水相中有机物及臭氧的接触几率就大,有助于有机污染物的氧化降解;但当催化剂增加到一定浓度时,反应的主要制约因素由活性点位的数量变为有机相和臭氧扩散至活性点位的阻力,故催化反应效率受催化剂浓度的影响不大。综上所述,选择NdFeB/AC投加量为3.0 g/L较适宜。
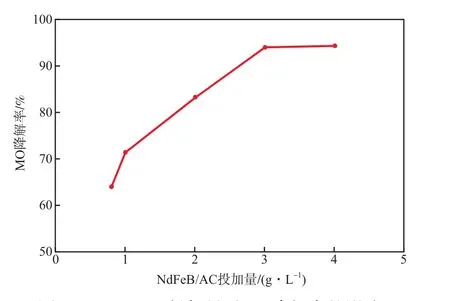
图5 NdFeB/AC投加量对MO降解率的影响
2.2.1.2 初始溶液pH
在NdFeB/AC投加量为3.0 g/L、初始MO质量浓度为20 mg/L的条件下,初始溶液pH对MO降解率的影响见图6。由图6可见,在偏酸性条件下MO的降解效果更理想。这主要是因为:MO在酸性条件下由偶氮结构转变为醌式结构,与偶氮结构相比醌式结构更易被自由基攻击而发生降解。由图5还可见,pH=3.0与pH=5.0时的降解率差别不大。考虑到调节pH所需的药剂成本,选择pH=5.0较适宜。

图6 初始溶液pH对MO降解率的影响
2.2.1.3 初始MO质量浓度
在NdFeB/AC投加量为3.0 g/L、初始溶液pH为5.0的条件下,初始MO质量浓度对MO降解率的影响见图7。

图7 初始MO质量浓度对MO降解率的影响
由图7可见,随初始MO质量浓度的增加,降解率总体呈缓慢下降趋势。这主要是因为:随MO浓度的升高,MO扩散到催化剂活性点位的能力提高,故反应初期的反应效率较高,加之臭氧不断通入以维持氧化剂的投入,因而使得高浓度的MO也具有较高的降解率;但因底物浓度高,其中间产物也会被吸附到活性点位发生反应,因而阻碍了新的MO降解,导致降解率下降。考虑到初始MO质量浓度为20 mg/L与10 mg/L时的降解效果差别较小,而底物浓度为10 mg/L的2倍,故选取20 mg/L进行后续实验。
2.2.2 NdFeB/AC与AC的催化效果对比
在上述优化条件下,NdFeB/AC与AC的催化效果对比见图8。由图8可见:投加催化剂对MO的氧化降解具有明显的促进作用,且NdFeB/AC的催化能力显著优于同等粒径的非磁性AC;反应40 min时,单纯臭氧氧化的MO质量浓度由20 mg/L降至约13 mg/L,而投加AC作为催化剂时约为7 mg/ L,MO降解率由37.0%大幅提升至64.4%;投加NdFeB/AC时,MO质量浓度降至约1 mg/L,降解率高达93.9%。由图8还可见:未通入臭氧仅投加NdFeB/AC或AC时,AC对MO有一定的吸附效果,但效果有限;而NdFeB/AC对MO的吸附很弱,可忽略。这主要是因为AC的部分孔洞与通道被负载的NdFeB阻塞,导致吸附效果变差。

图8 NdFeB/AC与AC的催化效果对比
2.2.3 反应动力学
按式(1)对优化条件下AC与NdFeB/AC催化臭氧氧化降解MO反应过程的实验数据进行拟合。拟合结果为:AC与NdFeB/AC催化反应的k值分别为0.025,0.070 min-1,相关系数分别为0.9999和0.9959。拟合结果表明:反应过程均遵循一级动力学规律;NdFeB/AC催化反应的k值是AC的近3倍,说明NdFeB/AC具有较好的催化臭氧氧化降解水中有机污染物的能力。

式中:t为反应时间,min,ρ0和ρ分别为初始和t时刻的MO质量浓度,mg/L;k为反应动力学常数,min-1。
3 结论
a)通过浸渍法制备了具有硬磁特性的NdFeB/ AC。当m(NdFeB)∶m(AC)=1∶2时,其比饱和磁化强度和比剩余磁化强度分别为15.9 A·m2/kg和6.0 A·m2/kg,矫顽力可达104.5 kA/m。反应后的NdFeB/AC仍具强磁性,可用磁性分离的方法轻松实现催化剂和溶液的分离。
b)通过浸渍法可将NdFeB磁粉负载于AC表面,形成蜂窝状表面结构,从而提高其比表面积。
c)在NdFeB/AC投加量为3.0 g/L、初始溶液pH为5.0、初始MO质量浓度为20 mg/L、臭氧质量浓度为15.0 mg/L、室温的条件下反应40 min,MO降解率达93.9%,显著优于投加AC的64.4%。
d)AC和NdFeB/AC作为非均相催化剂催化臭氧氧化降解MO的反应过程均遵循一级动力学规律,且NdFeB/AC的反应速率常数为AC的近3倍。
[1] 马丹丹,文晨,季民. 微电解-铁碳内电解耦合预处理高浓度染料废水[J]. 化工进展,2013,32(1):205 - 208.
[2] 倪可,王利平,李祥梅,等. 负载型金属催化剂的制备及印染废水的催化氧化处理[J]. 化工环保,2014,34(2):176 - 180.
[3] 宁军,陈立伟,蔡天明. 臭氧催化氧化降解苯胺的机理[J]. 环境工程学报,2013,7(2):551 - 556.
[4] 雷利荣,李友明. 臭氧及催化臭氧氧化法处理制浆废水的研究进展[J]. 中国造纸,2013,32(5):55 -61.
[5] 尚会建,周艳丽,赵彦,等. 活性炭催化臭氧氧化处理低浓度氨氮废水[J]. 化工环保,2012,32(5):405 - 408.
[6] 王佳裕,戴启洲,鱼杰,等. 活性炭催化臭氧氧化扑热息痛的机制研究[J]. 环境科学,2013,34(4):1402 - 1410.
[7] 杨德敏,袁建梅,吴小娟,等. 多相催化臭氧化技术处理钻井废水的试验研究[J]. 工业水处理,2013,33(7):58 - 61.
[8] 赵俊娜,李再兴,刘艳芳,等. Mn/γ-Al2O3催化剂的制备及头孢合成废水的催化臭氧氧化法深度处理[J]. 化工环保,2014,34(5):475 - 480.
[9] 雷利荣,李友明,马黎明. 活性炭、氧化铝及其负载二氧化钛催化臭氧处理制浆废水[J]. 华南理工大学学报:自然科学版,2012,40(2):149 - 155.
[10] 董淑福. 多相催化臭氧氧化法处理印染废水的研究[J]. 工业水处理,2013,33(4):58 - 60.
(编辑 魏京华)
一种TiO2光催化涂层的制备方法及用途
该专利涉及一种TiO2光催化涂层的制备方法及用途。通过电沉积有机硅烷凝胶-溶胶前驱体溶液的方法,先在泡沫金属基体上制得一层惰性多孔的、结合力强的纳米SiO2中间层薄膜,然后负载锐钛矿型纳米TiO2涂层,最终制得具有较高光催化活性的复合涂层材料,用于光催化降解空气或污水中的有机污染物。以电沉积法制备的SiO2中间层克服了以往浸涂法制备的SiO2中间层存在的膜厚度不高、多孔性不够、TiO2负载量低、与基体结合力差等缺陷,且中间层厚度可调,与基体结合力更好,增大负载量的同时增强了与后续负载涂层的结合力,大幅提高了光催化活性。该专利方法操作简单,成本较低,光催化涂层的重复利用率高,有望大规模应用于工业化生产。/CN 104588021 A,2015-04-29
一种紫外光催化降解有机污染物的催化剂及其制备方法
该专利涉及一种紫外光催化降解有机污染物的催化剂及其制备方法。将钛酸四丁酯、乙酸、甲醇和聚乙烯吡咯烷酮倒入锥形瓶中,搅拌得到溶胶,经静电纺丝得到纳米纤维膜,煅烧得到TiO2纳米纤维;将其置于硝酸银溶液中搅拌还原,紫外光照射得到Ag-TiO2催化剂。该专利克服了采用单一TiO2作光催化剂时存在的禁带宽度窄、电子转移速率慢、电子-空穴复合速率快的问题,提高了光催化降解有机污染物的效率。用静电纺丝得到的TiO2纳米纤维催化剂降低了光生电子-空穴的复合速率,提高了转移速率和催化降解效率。该方法操作简便,反应条件温和。/CN 104588004 A,2015-04-29
Degradation of Methyl Orange in Water by Catalytic Ozone Oxidation with Magnetic Activated Carbon
Ren Baixiang,Fan Jingying,Yang Chunwei
(College of Environmental Science and Engineering,Jilin Normal University,Siping Jilin 136000,China)
The neodymium-iron-boron-based magnetic activated carbon (NdFeB/AC) was prepared by dipping method and characterized by SEM and VSM technology. And it was used as a heterogeneous catalyst for ozone oxidation of methyl orange (MO) in water. The characterization results indicate that:NdFeB/AC is hard magnetic;When m(NdFeB)∶m(AC)=1∶2,its specific saturation magnetization,specific remanent magnetization and coercive force are 15.9 A·m2/kg,6.0 A·m2/kg and 104.5 kA/m respectively. The experimental results show that:Under the conditions of NdFeB/AC dosage 3.0 g/L,initial solution pH 5.0,initial MO mass concentration 20 mg/L,ozone mass concentration 15.0 mg/L,room temperature and reaction time 40 min,the MO degradation rate can reach 93.9%,which is signif i cantly better than 64.4% of that with AC as catalyst;The degradation process of catalytic ozone oxidation with AC and NdFeB/AC both follows the fi rst order dynamic law,and the reaction rate constant with NdFeB/AC is nearly 3 times as much as that with AC.
neodymium;iron;boron;magnetic activated carbon;heterogeneous catalyst;ozone;methyl orange
X788
A
1006-1878(2015)04-0409-05
2015 - 02 - 27;
2015 - 04 - 21。
任百祥(1964—),男,吉林省农安县人,硕士,教授,电话 0434 - 3292207,电邮 renbx6438@sina.com。联系人:杨春维,电话 13694001403,电邮 chunwei_yang@jlnu.edu.cn。
吉林省科技厅自然科学基金项目(20140101215JC);吉林省科技厅重点科技攻关项目(20150204049SF);吉林省科技发展计划项目(201205076);工业生态与环境工程教育部重点实验室开放基金项目(KLIEEE-13-07)。

