离子液体辅助合成Nd掺杂TiO2的可见光催化性能
宋永强,张秀玲,2,底兰波,2
(1. 大连大学 物理科学与技术学院,辽宁 大连 116622;2. 大连大学 特种加工与功能材料制备辽宁省教育厅重点实验室,辽宁 大连 116622)
离子液体辅助合成Nd掺杂TiO2的可见光催化性能
宋永强1,张秀玲1,2,底兰波1,2
(1. 大连大学 物理科学与技术学院,辽宁 大连 116622;2. 大连大学 特种加工与功能材料制备辽宁省教育厅重点实验室,辽宁 大连 116622)
在离子液体1-丁基-3-甲基咪唑四氟化硼([C4MIM]BF4)的辅助下,采用溶胶-凝胶法制备了Nd掺杂TiO2光催化剂(Nd-TiO2(IL))。实验结果表明:在加入[C4MIM]BF4、n(Nd)∶n(TiO2)=2.5%的条件下制得的Nd-TiO2(IL)(记作2.5%Nd-TiO2(IL))的光催化性能最好;在初始亚甲基蓝质量浓度10 mg/L、2.5%Nd-TiO2(IL)加入量1 g/L的条件下,光催化反应180 min,亚甲基蓝降解率为84%,2.5%Nd-TiO2(IL)光催化降解亚甲基蓝的表观速率常数为0.0109 min-1。表征结果显示:Nd的掺杂抑制了TiO2晶粒长大,增大了TiO2的比表面积,2.5%Nd-TiO2(IL)的比表面积为80.77 m2/g;[C4MIM]BF4的加入提高了TiO2的晶化度;Nd以Nd3+的形式,通过晶格取代方式进入TiO2晶格。
钕掺杂; 二氧化钛; 离子液体; 光催化剂;可见光催化
自1977年TiO2首次被Frank和Bard用于光解水以来,其在工业废水处理和空气净化等领域的研究受到越来越广泛的关注[1-3]。但锐钛矿相TiO2的带隙较宽,只有在波长小于或等于紫外光波长的电磁波辐射下才具有光催化活性。在太阳光谱中紫外光仅占5%,这极大地限制了TiO2光催化剂在实际中的应用。采用掺杂和染料敏化等技术可降低TiO2带隙能、提高TiO2的可见光利用率[4]。目前,金属掺杂技术包括过渡金属掺杂和稀土金属掺杂两种方法。其中,过渡金属掺杂能使TiO2产生掺杂能级,从而捕捉电子和空穴,使具有较低能量的可见光可以激发TiO2中的电子。但在溶液中过渡金属掺杂的TiO2的量子产生率低于1%[5],导致TiO2的可见光催化效率降低。具有4f电子结构的稀土离子可以产生多电子组态,通过稀土掺杂可拓展TiO2的光吸收波段,提高其可见光催化活性[6-7]。离子液体因具有界面张力低和成核率高等优点,广泛应用于介孔材料的制备[8-9]。目前,以离子液体辅助制备Nd掺杂TiO2光催化剂的研究还鲜有报道。
本工作以Nd(NO3)3为Nd源,在离子液体1-丁基-3-甲基咪唑四氟化硼([C4MIM]BF4)的辅助下,采用溶胶-凝胶法制备了Nd掺杂TiO2光催化剂(Nd-TiO2(IL))。采用紫外-可见漫反射吸收光谱、XRD、比表面积分析和TEM等技术对Nd-TiO2(IL)进行了表征。通过XPS谱图对Nd-TiO2(IL)的光催化机理进行了分析。
1 实验部分
1.1 试剂和仪器
钛酸四丁酯、无水乙醇、Nd(NO3)3、冰醋酸、亚甲基蓝:分析纯。
[C4MIM]BF4: 纯度大于99%,中国科学院兰州化学物理研究所。
PLS-SXE300型氙灯:功率300 W,滤光片波长大于420 nm,北京泊菲莱公司;721型分光光度计:上海菁华科技仪器有限公司;Gary100型紫外-可见分光光度计:美国瓦里安公司;DX-2700型X射线衍射分析仪:丹东浩源公司;NOVA 2200e型比表面积及孔径分析仪:美国康塔仪器公司;Tecnai G2Spirit型透射电子显微镜:荷兰FEI公司;ESCALAB250型多功能表面分析系统:ThermoVG公司。
1.2 光催化剂的制备
在磁力搅拌下将10 mL钛酸四丁酯溶于30 mL无水乙醇中,得溶液A;将一定量浓度为0.1 mol/ L的Nd(NO3)3溶液加入到30 mL无水乙醇、10 mL冰醋酸、10 mL蒸馏水和1.5 mL [C4MIM]BF4组成的混合溶液中,在室温下充分搅拌30 min,得溶液B。将溶液A以0.02 mL/s的速率滴加到溶液B中,搅拌4 h,得溶胶。在室温下放置24 h后,在100 ℃下干燥4 h,最后在马弗炉中于500 ℃下热处理2 h,研磨成粉末,得到Nd-TiO2(IL)。
当Nd(NO3)3溶液的加入量分别为2.90,5.80,7.25,8.70 mL时,分别得到n(Nd)∶n(TiO2)=1.0%,2.0%,2.5%,3.0%的Nd-TiO2(IL),记作1.0%Nd-TiO2(IL),2.0%Nd-TiO2(IL),2.5%Nd-TiO2(IL),3.0%Nd-TiO2(IL)。未加入Nd(NO3)3溶液时的试样记作TiO2(IL)。在Nd(NO3)3溶液的加入量为7.25 mL、未加入[C4MIM]BF4时得到的试样记作2.5%Nd-TiO2。
1.3 光催化反应
以亚甲基蓝溶液作为模拟污染物,评价催化剂的光催化性能。以功率为300 W的氙灯为可见光源,光源距液面的垂直距离为20 mm。首先,在室温下将100 mL质量浓度为10 mg/L的亚甲基蓝溶液及加入量为1 g/L的光催化剂放入反应器中,暗箱静置30 min,达到吸附平衡后开启氙灯,进行光催化反应,每隔30 min取样,离心后进行分析。
1.4 分析方法
采用分光光度计在波长664 nm处测定反应前后亚甲基蓝溶液的吸光度。亚甲基蓝溶液的吸光度和质量浓度在低浓度范围内遵循Lambert-Beer定律,线性关系良好[7]。
通过对TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO23种试样进行表征,考察[C4MIM]BF4和Nd掺杂对TiO2可见光催化性能的影响。采用紫外-可见分光光度计,以硫酸钡为标准参比,对试样进行紫外-可见漫反射吸收光谱分析,扫描范围为200~800 nm;采用X射线衍射仪分析试样的相组成,Cu Kα射线,管电压40 kV,管电流30 mA;采用比表面积及孔径分析仪测定试样的比表面积;采用透射电子显微镜观察试样的形貌。采用多功能表面分析系统对试样的XPS能谱进行分析。
2 结果与讨论
2.1 光催化剂种类对亚甲基蓝降解率的影响
在光催化反应时间为180 min的条件下,光催化剂种类对亚甲基蓝降解率的影响见图1。由图1可见:随Nd(NO3)3溶液加入量的增加,Nd-TiO2(IL)的光催化效果先增大后减小;以2.5%Nd-TiO2(IL)为光催化剂时的亚甲基蓝降解率最高,降解率为84%;以2.5%Nd-TiO2为光催化剂,亚甲基蓝降解率最低。
2.2 光催化剂种类对亚甲基蓝降解速率的影响
不同光催化剂降解亚甲基蓝的降解速率拟合曲线见图2。图中:t为光催化反应时间,min;ρ0为初始亚甲基蓝质量浓度,mg/L;ρt为反应为t时刻的亚甲基蓝质量浓度,mg/L。由图2可见,不同光催化剂降解亚甲基蓝的ln(ρ0/ρt)与t均呈良好的线性关系,说明Nd-TiO2(IL)降解亚甲基蓝的反应为一级反应,这与Katsumata等[10]对亚甲基蓝光催化降解反应的研究结果一致。表观速率常数的计算结果表明,随Nd(NO3)3溶液加入量的增加,表观速率常数先增大后减小,以2.5%Nd-TiO2(IL)为光催化剂时的表观速率常数最大,为0.0109 min-1。

图1 光催化剂种类对亚甲基蓝降解率的影响

图2 不同光催化剂降解亚甲基蓝的降解速率拟合曲线
2.3 紫外-可见漫反射吸收光谱表征结果
TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的紫外-可见漫反射吸收光谱图见图3。由图3可见:TiO2(IL)在可见光区域的光吸收很弱;2.5%Nd-TiO2在可见光部分出现很多吸收峰(527,586,683,762,807 nm),说明Nd掺杂具有敏化TiO2的作用[11];2.5%Nd-TiO2(IL)在可见光部分整体吸收增强,但无明显的吸收峰,说明[C4MIM]BF4和Nd掺杂的共同作用提高了TiO2在可见光区的光吸收强度,使2.5%Nd-TiO2(IL)在可见光下具有较高的光催化活性,同时,[C4MIM]BF4的加入降低了Nd自身电子结构敏化TiO2的效应。

图3 TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的紫外-可见漫反射吸收光谱图
2.4 XRD表征结果
TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的XRD谱图见图4。由图4可见:2θ=25.1o,37.7o,48.1o,54.0o,55.1o,62.8o,75.2o处对应锐钛矿相TiO2的(101),(004),(200),(105),(211),(204),(215)晶面的衍射峰,与标准卡片JCPDS 89-4921一致[12];2.5%Nd-TiO2(IL)(101)晶面的衍射峰强度大于2.5%Nd-TiO2,说明[C4MIM]BF4的加入提高了TiO2的晶化度;2.5%Nd-TiO2(IL)(101)晶面的衍射峰强度较TiO2(IL)弱,说明Nd的掺杂抑制了TiO2晶粒的增长。
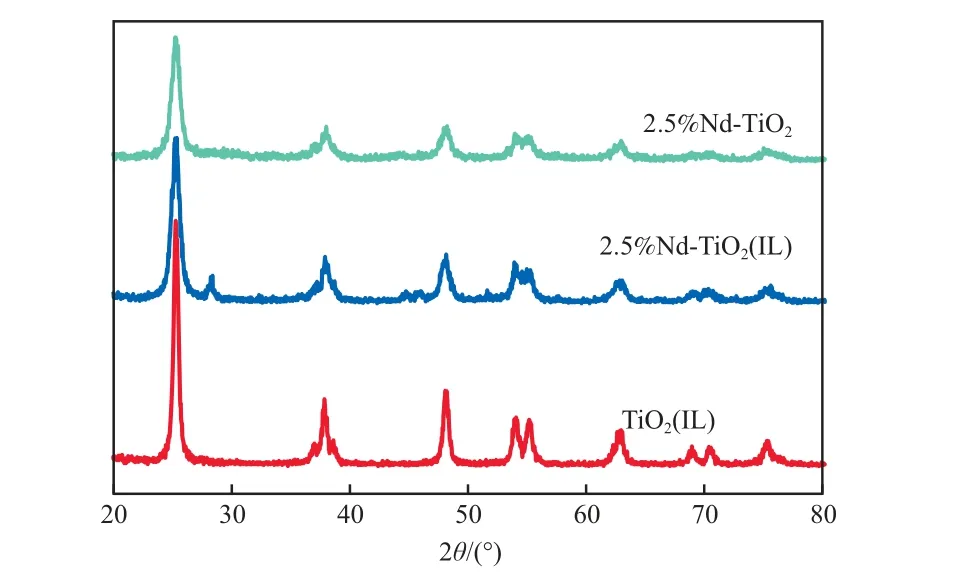
图4 TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的XRD谱图
2.5 比表面积分析结果
TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的结构参数见表1。由表1可见:Nd的掺杂有利于TiO2比表面积的增加和粒径的减小;2.5%Nd-TiO2(IL)的比表面积为80.77 m2/g,远高于TiO2(IL)的比表面积(51.60 m2/g);[C4MIM]BF4的加入使得TiO2的孔体积与孔径增大。
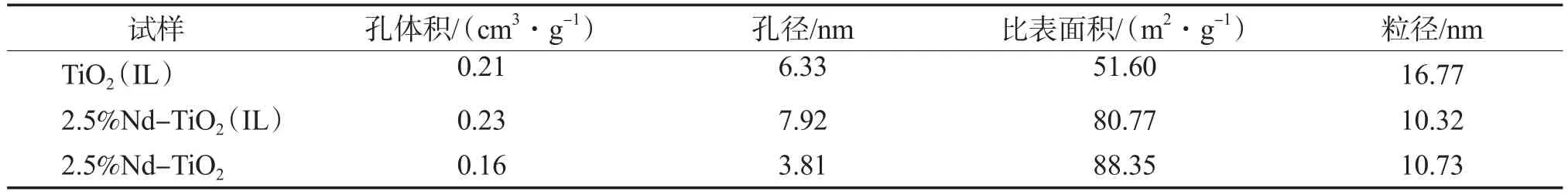
表1 TiO2(IL),2.5%Nd-TiO2(IL),2.5%Nd-TiO2的结构参数
2.6 TEM表征结果
2.5%Nd-TiO2(IL)和2.5%Nd-TiO2的TEM照片见图5。由图5可见,2.5%Nd-TiO2(IL)和2.5%Nd-TiO2的粒径均约为10 nm,但2.5%Nd-TiO2(IL)的晶形优于2.5%Nd-TiO2,说明[C4MIM]BF4能提高TiO2的晶化度。

图52.5%Nd-TiO2(IL)和2.5%Nd-TiO2的TEM照片
2.7 Nd掺杂TiO2光催化的机理分析
2.5%Nd-TiO2(IL)的XPS能谱图见图6。由图6可见:在Nd 4d的高分辨XPS能谱中,2.5%Nd-TiO2(IL)的Nd 4d峰值为122.6 eV,与金属Nd0的峰值(118.0 eV)相比,向高位移动了4.6 eV,这是由于Nd的电子密度减小所致,说明金属Nd以Nd3+的形式掺杂在TiO2晶格中[13];在Ti 2p的高分辨XPS能谱中,结合能为458.7 eV和464.5 eV 的峰分别对应Ti的2p3/2和2p1/2的特征峰,这与Ti4+的特征峰一致,说明Ti是以四价的形式存在于TiO2的晶格中;在O 1s的高分辨XPS能谱中,结合能为530.2 eV的峰对应O2-存在于TiO2中形成的Ti—O键的特征峰,结合能为531.8 eV的峰是O与H结合形成的—OH的特征峰[14]。上述分析表明,Nd3+以晶格取代方式进入TiO2晶格,降低了TiO2的带隙能,使得TiO2发生红移,光催化性能得到提高。对于具有较宽带隙的半导体材料,在氧化还原过程中电子与空穴的结合是光催化活性降低的主要原因。Nd的掺杂可诱导产生间隙氧缺陷和取代氧缺陷,这些缺陷在捕捉电荷、阻止电子与空穴结合的过程中起到了重要作用[15]。
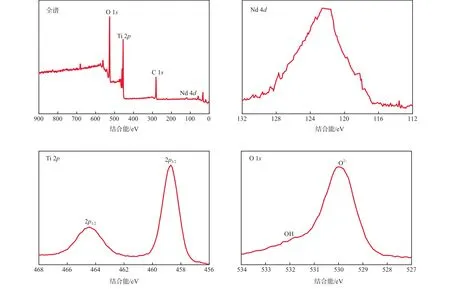
图62.5%Nd-TiO2(IL)的XPS能谱图
3 结论
a) 以钛酸四丁酯和Nd(NO3)3为原料,在离子液体[C4MIM]BF4的辅助下,通过溶胶-凝胶法制备了一系列Nd-TiO2(IL)。其中,2.5%Nd-TiO2(IL)(n(Nd)∶n(TiO2)=2.5%)的光催化性能最好。在初始亚甲基蓝质量浓度为10 mg/L、2.5%Nd-TiO2(IL)加入量为1 g/L的条件下,光催化反应180 min,亚甲基蓝降解率为84%。2.5%Nd-TiO2(IL)光催化降解亚甲基蓝的表观速率常数为0.0109 min-1。
b) 采用紫外-可见漫反射吸收光谱、XRD、比表面积分析和TEM等技术对光催化剂进行表征。表征结果显示:Nd的掺杂抑制了TiO2晶粒长大,增大了TiO2的比表面积,2.5%Nd-TiO2(IL)的比表面积为80.77 m2/g,远高于TiO2(IL)的比表面积(51.60 m2/g);[C4MIM]BF4的加入提高了TiO2的晶化度;Nd掺杂和[C4MIM]BF4的共同作用提高了TiO2在可见光区的光吸收强度,使2.5%Nd-TiO2(IL)具有较高的可见光催化活性。
c) XPS分析结果表明,Nd以Nd3+的形式,通过晶格取代方式进入TiO2晶格。Nd的掺杂降低了TiO2的带隙能,使TiO2的光催化活性得到提高。
[1] Su Yaling,Deng Yirong,Zhao Lu,et al. Photocatalytic Degradation of Microcystin-LR Using TiO2Nanotubes Under Irradiation with UV and Natural Sunlight[J]. Chin Sci Bull,2013,58(10):1156 - 1161.
[2] Zheng Qing,Zhou Baoxue,Bai Jing,et al. Self-Organized TiO2Nanotube Array Sensor for the Determination of Chemical Oxygen Demand[J]. Adv Mater,2008,20(5):1044 - 1049.
[3] 董业硕,费学宁,池勇志,等. 可见光响应易回收TiO2催化剂研究进展[J]. 化工环保,2012,32(3):231 - 236.
[4] Biswas S K,Pathak A,Pramanik N K,et al. Codoped Cr and W Rutile Nanosized Powders Obtained by Pyrolysis of Triethanolamine Complexes[J]. Ceram Int,2008,34(8):1875 - 1883.
[5] Litter M I,Navio J A. Photocatalytic Properties of Iron-Doped Titania Semiconductors[J]. J Photochem Photobiol,A,1996,(3):171 - 181.
[6] Damian W,Michal M,Michalina K,et al. Influence of Nd-Doping on Photocatalytic Properties of TiO2Nanoparticles and Thin Film Coatings[J]. Int J Photoen,2014,2014:463034.
[7] 黄凤萍,张双,王帅,等. 稀土Nd掺杂纳米TiO2的制备及光催化活性探讨[J]. 硅酸盐通报,2014,33(7):1643 - 1648.
[8] 王凯,张丽娟,徐志坚,等. pH对离子液体辅助水热制备介孔二氧化钛结构的影响[J]. 无机材料学报,2014,29(2):131 - 136.
[9] Han C C,Lin Y P,Ho S Y,et al. Effect of Ionic Liquid-Templated Mesoporous Anatase TiO2on Performance of Dye-Sensitized Solar Cell[J]. J Phys D:Appl Phys,2010,43(3):035102.
[10] Katsumata H,Ssda M,Nakaoka Y,et al. Photocatalytic Degradation of Diuron in Aqueous Solution by Platinized TiO2[J]. J Hazard Mater,2009,171(1/2/3):1081 - 1087.
[11] 何春萍. 钕掺杂纳米二氧化钛光催化活性研究[J].吉林化工学院学报,2007,24(3):27 - 29.
[12] Choi E H,Hong S I,Moon D J. Preparation of Thermally Stable Mesostructured Nano-Sized TiO2Particles by Modified Sol-Gel Method Using Ionic Liquid[J]. Catal Lett,2008,123(1/2):84 - 89.
[13] Khalid N R,Ahmed E,Hong Zhanglian,et al. Graphene Modif i ed Nd/TiO2Photocatalyst for Methyl Orange Degradation Under Visible Light Irradiation[J]. Ceram Int,2013,39(4):3569 - 3575.
[14] Sun Jian,Liu Shouxin. Preparation of Lanthanum-Doped TiO2Film and its Application for Gaseous Toluene Removal[J]. J Inorg Mater,2010,25(9):928 - 934.
[15] 赵真,宋季岭,郑佳红,等. 钕掺杂氧化锌粉末的光性能和光催化性能[J].中国有色金属学报:英文版,2014,24(5):1434 - 1439.
(编辑 王 馨)
Visible-Light Photocatalytic Activity of Nd-Doped TiO2Synthesized with Ionic-Liquid Assistance
Song Yongqiang1,Zhang Xiuling1,2,Di Lanbo1,2
(1. College of Physical Science and Technology,Dalian University,Dalian Liaoning 116622,China;2. Key Laboratory for Non-traditional & Functional Materials Preparation of Education Department of Liaoning Province,Dalian University,Dalian Liaoning 116622,China)
The Nd doped TiO2photocatalyst (Nd-TiO2(IL)) was prepared by sol-gel method with assistance of ionic liquid[C4MIM]BF4. The experimental results show that: The photocatalyst prepared under the conditions of [C4MIM]BF4addition and n(Nd)∶n(TiO2)=2.5% (2.5%Nd-TiO2(IL)) has the highest photocatalytic activity;When the initial mass concentration of methylene blue is 10 mg/L,the 2.5%Nd-TiO2(IL) dosage is 1 g/L and the reaction time is 180 min,the degradation rate of methylene blue is 84%,the apparent rate constant on 2.5%Nd-TiO2(IL) is 0.0109 min-1. The characterization results show that: The doped Nd inhibits the growth of TiO2nanoparticles and increases the surface area of TiO2,the surface area of IL-2.5%Nd/TiO2is 80.77 m2/g;The crystallinity of TiO2is increased with the addition of[C4MIM]BF4;Nd3+enters into the TiO2lattice by lattice substitution.
neodymium doping;titanium dioxide;ionic liquid;photocatalyst;visible-light photocatalysis
O649.1
A
1006-1878(2015)04-0344-05
2015 - 04 - 06;
2015 - 05 - 13。
宋永强(1993—),男,河南省鹤壁市人,大学生,电话 0411 - 87402712,电邮 yongqiangsong@sina.com。联系人:底兰波,电话 0411 - 87402712,电邮dilanbo@163.com。
国家自然科学基金项目(21173028);辽宁省高等学校优秀科技人才支持计划项目(LR2012042);大连市金州新区科技创新主体支持计划培育专项(KJCX-ZTPY-2014-0001)。

