临床合用那格列奈对氟伐他汀药代动力学的影响*
朱慧婷 徐召飞
(江西省儿童医院,江西 南昌330006)
氟伐他汀(Fluvastatin)是第一个全化学合成的HMG-CoA还原酶抑制剂,竞争性抑制胆固醇的生物合成,降低肝细胞内胆固醇的含量,刺激低密度脂蛋白(LDL)受体的合成,并加速从血浆中清除LDL-C,以达到降低血脂的作用[1-2]。那格列奈(Nateglinide)属非磺脲类促胰岛素分泌剂,用于治疗2型糖尿病的新型口服降血糖药,该药起效迅速、持续作用时间短,降糖效果佳,不良反应少且轻[3]。临床治疗中调节血脂药物、降血糖联合应用情况非常普遍,了解联合用药可能存在的药物相互作用,对临床用药的安全性具有重要意义。本文通过研究氟伐他汀、那格列奈合用对氟伐他汀药代动力学特征的影响,为临床合理用药提供理论依据。
1 材料与方法
1.1 试药和试剂
氟伐他汀钠胶囊(来适可)由北京诺华制药有限公司生产(规格:40mg/粒,批号:20141022);那格列奈片(唐力)由北京诺华制药有限公司生产(规格:120mg/片;批号:20140215);甲醇(色谱纯),乙酸乙酯,Merck公司生产;其余试剂均为市售分析纯。
1.2 仪器
岛津LCMS-2010EV高效液相色谱—质谱联用仪;CBM-20A 系统控制器;LC-20AB 双泵;SIL-20A自动进样器;CTO-20A柱温箱;电磁切换阀;LCMSsolution色谱工作站;XW-80A旋涡混匀器;N-EVAP 112干浴氮吹仪;Anke LXJ-Ⅱ大容量多管离心机;Sigma 3K30台式超高速冷冻离心机。
1.3 色谱及质谱条件
分 析 柱 Shim-Pack ODS C18(250mm ×2.0mm 5m);流动相:甲醇-0.1%醋酸溶液(60∶40v/v),流速0.2ml·min-1,柱温:35℃;选择性离子检测(SIM);电喷雾离子化(ESI);离子极性:负离子;检测对象:氟伐他汀,钠,m/z:410.2;瑞舒伐他汀,m/z:480;雾化气流速1.5L·min-1;干燥气流量:4.0L·min-1,检测电压1.60kV;曲形脱溶剂装置温度:250℃;加热块温度:200℃。
1.4 血浆样品的处理过程
取血浆0.5ml,精密加入15μl内标(瑞舒伐他汀,10μg/ml),再加100μl 0.1mol·L-1冰醋酸溶液,混匀后加5.0ml乙酸乙酯,振荡5min,4500 r/min离心10min,取上清液4.0ml,置50℃干浴锅中氮气挥干,以0.1ml甲醇溶解残渣,再经18000 rpm离心10min后,取10μl进样,用峰面积进行定量LC-MS分析。
1.5 试验设计
本试验采用随机、开放、单周期,平行试验设计,试验经过伦理委员审批通过,试验前所有受试者均签署知情同意书,24名男性受试者随机分为两组,年龄为20~40岁,体重指数19~24kg/m2,体重相差不超过10kg;无药物过敏史,无影响药物吸收的消化系统疾病,无影响药物代谢的肝、肾功能不全等疾病,经体格检查,心电图、血常规、尿常规、肾功能及肝功能实验室检查合格,受试前2周内未服过任何药物,试验结束后3d体检复查相关检查,考察其安全性。单药组和合用组分别空腹同时口服氟伐他汀钠胶囊(来适可)40mg,氟伐他汀钠胶囊40mg和那格列奈片(唐力)120mg,于服药前(0h)及服药后0.25,0.5,0.75,1.0,1.5,2.0,2.5,3.0,4.0,6.0,8.0 和12.0h分 别采集上肢静脉血4ml至肝素化试管中,以3000r/min离心10min,分离出血浆置-20℃冷冻保存。离心分离血浆。血浆按照“1.4”项下方法操作,进行LCMS分析,测得的平均血药浓度-时间曲线。
1.6 药代动力学评价和数据分析
所有计量资料均采用¯x±s表示,根据氟伐他汀钠血药浓度,绘制血药浓度-时间曲线,采用中国药理学会数学药理专业委员会DAS2.0统计计算软件进行数据处理,计算单用氟伐他汀钠胶囊及其合用那格列奈片后的药代动力学参数。
2 结果
2.1 受试者的人口学特征
两组受试者基线时在人口学特征组间比较,组间差异无统计学意义P>0.05,表明两组均衡,具有良好的可比性。详见表1。
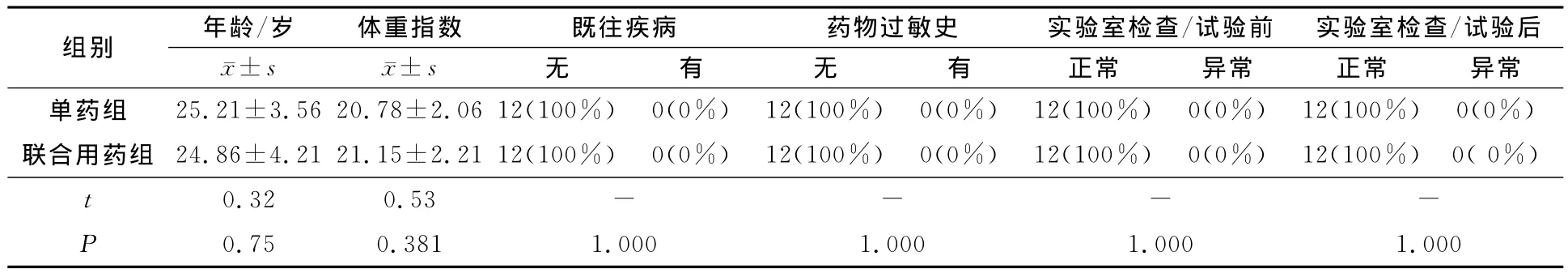
表1 两组受试者一般资料比较(n=12)
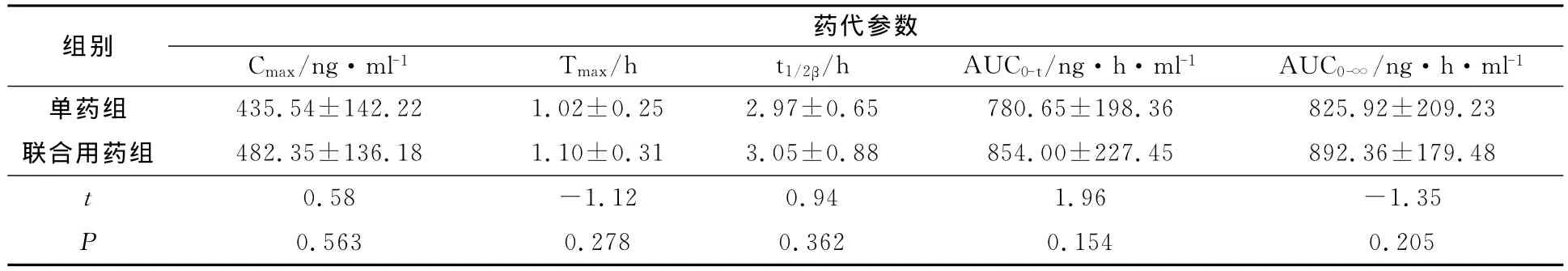
表2 单用和联合用药后主要药代动力学参数(¯x±s)
2.2 药代动力学参数
24例受试者全部的按方案要求完成临床试验全部内容,单用组和联用组所得血药浓度数据结果经DAS2.0处理后,主要药代动力学参数见表2,两组的 Cmax、Tmax、AUC0-t、AUC0-∞、t1/2β分别经t检验均无统计学差异(P>0.05)。
2.3 血药浓度—时间曲线
24例受试者单药组氟伐他汀钠胶囊及联合应用那格列奈片后不同时间点血浆中盐酸氟伐他汀的血药浓度—时间曲线。见图1。
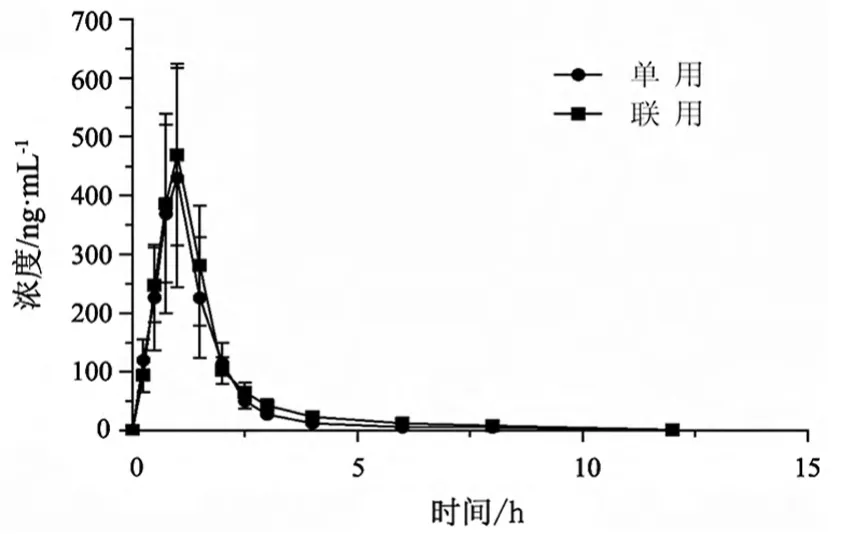
图1 单用及联用后氟伐他汀平均血药浓度—时间曲线
3 讨论
随着我国人口老龄化的进展和环境的复杂化,同时合并多种疾病的患者与日俱增,临床最为常见多为同时合并有高血压、高血脂和高血糖的“三高”患者,此类患者的临床治疗多数情况下需要合并应用调节血脂药物、降血糖以及其他药物治疗,药物的联合应用带来的可能是更多的药物相互作用,从而影响治疗效果,甚至产生严重的不良反应。有研究表明,部分降血脂药物与降血糖药或其它药物可能发生药物相互作用,不同的个体服用同等剂量氟伐他汀时,表现出显著的疗效差异,此类个体差异的存在可能与OATP1B1及CYP2C9遗传多态性对其转运代谢的影响有一定关系[4]。如患者联合应用OATP1B1转运受体或肝药酶CYP2C9底物的药物,服用常规剂量的氟伐他汀,可能会引起作用靶点药物浓度积聚或降低,从而产生不良反应或毒性,需通过调整给药剂量,达到相应的降血脂治疗。而有研究文献报道OATP1B1为那格列奈从血液中转运入肝细胞的主要转运体,其肝摄取作用对那格列奈的代谢也有很大影响[5]。基于那格列奈与氟伐他汀均是OATB1B1的底物[6],是转运其进入肝细胞的主要载体,并且两种药物均由细胞色素P450酶CYP2C9进行肝脏代谢[7-8]。有研究表明氟伐他汀的常规剂量为20~40mg/d,不同的个体服用同等剂量氟伐他汀时,表现出显著的疗效差异,Cmax及 AUC相差分别可达5~7倍[9],存在如此大的个体差异可能与OATP1B1及CYP2C9遗传多态性对其转运代谢的影响有一定关系,也可能与合用其它药物产生基于竞争抑制药物转运体OATP1B1和细胞色素P450酶CYP2C9的作用而导致。因此是在氟伐他汀临床治疗中药物联合应用治疗中需要考虑的重要因素。
本文围绕氟伐他汀与那格列奈的合用是否存在药物相互作用而致氟伐他汀体内药代动力学的改变,建立了专属性强、特异性高的血浆样品中氟伐他汀HPLC-MS的检测方法,结果显示氟伐他汀单用和与那格列奈片联合应用后,两组受试者耐受性良好,无不良事件的发生,安全性均较好。氟伐他汀人体药代动力学特征与单次用药相比较未有明显改变,主要药代动力学参数(Cmax、Tmax、AUC0-t、AUC0-∞、t1/2β)两组比较无显著差异(P>0.05),采用本研究建立的HPLC-MS的检测方法获得的氟伐他汀药代动力学参数与相关研究报告结果基本一致[10]。虽然大量药代动力学研究发现氟伐他汀与那格列奈体内药物代谢过程可能受细胞色素P450酶和肝细胞主要转运体的影响,因此,同类药物合同时应考虑竞争或抑制作用的发生,但本研究结果证实单次给药联合应用该两种药物并未发现存在明显的相互竞争或抑制作用,氟伐他汀体内过程两组受试者基本一致,本文结果可为氟伐他汀和那格列奈片的临床联合应用提供可靠的理论依据和用药参考。本研究主要从单次给药考察两药合用后药代动力学方面的相互作用,样本量依据生物等效性和药代动力学相关指导原则实施,共选择24例受试者,例数可能较少,但所求得药代动力学数据结果应无有较大差异,所得结果与相关文献报道的结果也基本相符。此外,多次给药后是否存在同样的结果尚待进一步研究发现。
[1] Zhao S,Wang F,Yang K,et al.Efficacy and safety of fluvastatin extended-release tablets in Chinese patients with hyperlipidemia:a multi-center,randomized,double-blind,double dummy,active-controlled,parallel-group study[J].Zhonghua Nei Ke Za Zhi,2014,53(6):455-459.
[2] 葛琳.氟伐他汀与曲美他嗪联合治疗不稳定型心绞痛疗效观察[J].济宁医学院学报,2008,31(3):219-220.
[3] 顾晨晨,徐朝晖,阮克锋,等.2型糖尿病治疗药物那格列奈的研究进展[J].中国新药与临床杂志,2014,32(2):81-85.
[4] Chauvin B,Drouot S,Barrail-Tran A,et al.Drug-drug interactions between HMG-CoA reductase inhibitors(statins)and antiviral protease inhibitors[J].Clin Pharmacokinet,2013,52(10):815-831.
[5] Takanohashi T,Kubo S,Arisaka H,et al.Contribution of organic anion transporting polypeptide(OATP)1B1and OATP1B3to hepatic uptake of nateglinide,and the prediction of drug-drug interactions via these transporters[J].J Pharm Pharmacol,2012;64(2):199-206.
[6] Sharma P,Butters C J,Smith V,et al.Prediction of the in vivo OATP1B1-mediated drug-drug interaction potential of an investigational drug against a range of statins[J].Eur J Pharm Sci,2012,47(1):244-255.
[7] Buzková H,PechandováK,Danzig V,et al.Lipid-lowering effect of fluvastatin in relation to cytochrome P450 2C9variant alleles frequently distributed in the Czech population[J].Med Sci Monit,2012,18(8):512-517.
[8] 李宝群,万丽娟,程艳芬,等.SLO1B1和CYP2C9联合突变对那格列奈降血糖效果的影响[J].实用医学杂志,2010,26(13):2311-2313.
[9] 周权,阮邹荣,袁虹,等.反相高效液相色谱法测定人血浆中氟伐他汀浓度及其药动学研究应用[J].中国药学杂志,2006,41(12):1651-1653.
[10]杨林,丁莉坤,高晓华,等.LC-MS法测定人血浆氟伐他汀浓度[J].中国新药杂志2013,22(2):215-218.

