高效液相色谱法测定橙皮苷磷脂复合物中橙皮苷含量
张 卿,管海燕,金 竹,卢来春
(中国人民解放军第三军医大学大坪医院野战外科研究所药剂科,重庆 400042)
高效液相色谱法测定橙皮苷磷脂复合物中橙皮苷含量
张 卿,管海燕,金 竹,卢来春
(中国人民解放军第三军医大学大坪医院野战外科研究所药剂科,重庆 400042)
目的 建立测定橙皮苷磷脂复合物中橙皮苷含量的高效液相色谱(HPLC)法。方法 色谱柱为Diamonsil C18柱(250 mm×4.6 mm,5 m),流动相为乙腈-0.5%醋酸水溶液(25∶75),流速为1.0 mL/min,检测波长283 nm,柱温30℃,进样量20 L。结果 橙皮苷进样质量浓度在5.19~103.73 g/mL(r=0.999 5)范围内与峰面积线性关系良好,平均回收率为101.02%(RSD=1.30%),橙皮苷磷脂复合物中橙皮苷的平均含量为282.5 g/mg。结论 该法准确可靠、重复性好,可用于橙皮苷磷脂复合物的含量测定。
橙皮苷;磷脂复合物;高效液相色谱法;含量测定
橙皮苷是橙皮素与芸香糖形成的糖苷,为二氢黄酮衍生物,呈头发样针状晶体,白色或苍白色,熔点258~262℃,广泛存在于豆科、唇形花科、蝶形花科、芸香科、柑橘属植物中,具有抗炎、抗氧化、抗菌、抗癌、调节免疫力、防辐射、保护心血管系统等药理活性[1]。但其水溶性和脂溶性差,口服绝对生物利用度低[2]。口服给药是大多数药物最好的给药途径,可以提高患者的顺应性,且经济、安全,但许多有前景的脂溶性或水难溶性药物生物利用度低[3]。因此,选用合适的载体和制剂技术改善其理化性质,提高与胃肠道黏膜的亲和性和透过性等,是促进其口服吸收的有效途径[4]。将中药活性成分与磷脂制成磷脂复合物后,可明显增加中药活性成分的吸收,提高其生物利用度,增强其药理效应[5]。为此,本研究中制备了橙皮苷磷脂复合物,并建立了测定其含量的高效液相色谱(HPLC)法。
1 仪器与试药
1200型高效液相色谱仪(安捷伦公司);sartorius BT 25S型电子分析天平(赛多利斯科学仪器有限公司);磁力搅拌器(上海江星仪器有限公司);FD-1C型冷冻干燥机(北京德天佑科技发展有限公司)。橙皮苷原料药(含量为95.5%,批号为20131214),橙皮苷标准品(含量为98.79%,批号为20130413),均购自大连美仑生物技术有限公司;大豆卵磷脂(上海太伟药业有限公司);甲醇、乙腈为色谱纯;水为双蒸水;其余试剂为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-0.5%醋酸水溶液(25∶75);检测波长:283 nm;柱温:30℃;流速:1.0 mL/min;进样量:20 μL。
2.2 样品制备[6]
取处方量的橙皮苷和大豆卵磷脂,加入二甲亚砜(DMSO)-甲醇混合溶液作为反应溶剂,50℃下搅拌1 h,-80℃预冻,然后冷冻干燥除去反应溶剂,即得到橙皮苷磷脂复合物。经红外光谱(IR)、差示扫描量热(DSC)分析,证明该复合物是橙皮苷和磷脂通过物理作用结合在一起的。
2.3 方法学考察
专属性考察:称取橙皮苷对照品,精密称定,溶于DMSO-甲醇混合溶液10 mL,再取上述溶液0.5 mL,溶于甲醇10 mL制成质量浓度为97.9 mg/L的对照品溶液。同样方法制备处方量的大豆卵磷脂溶液和橙皮苷磷脂复合物溶液,按拟订色谱条件进样测定。结果显示,大豆卵磷脂不干扰橙皮苷的测定,符合系统适用性要求,色谱图见图1。
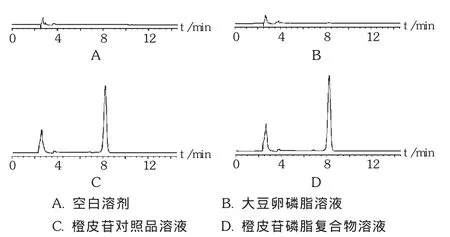
图1 高效液相色谱图
线性关系考察:称取 10.5 mg橙皮苷标准品,精密称定,置100 mL容量瓶内,加甲醇溶解并定容,得橙皮苷贮备液。精密吸取橙皮苷贮备液,置10 mL容量瓶中,加甲醇定容,分别制得质量浓度为5.2,10.4,20.8,41.5,51.9,83.0,103.7 μg/mL的系列溶液。取上述系列溶液,分别按拟订色谱条件进样测定,记录色谱图。以进样质量浓度为横坐标、橙皮苷峰面积为纵坐标进行线性回归,得回归方程 Y=23.12 X-1.89(r=0.999 5)。结果表明,橙皮苷进样质量浓度在5.19~103.73 μg/mL范围内与峰面积线性关系良好。
精密度试验:取质量浓度为51.9 μg/mL的橙皮苷贮备液,按拟订色谱条件连续进样 5次,测定峰面积。结果的 RSD= 0.23%(n=5),表明仪器精密度良好。
重复性试验:取同一批号样品,平行制备6份供试品溶液,按拟订色谱条件进样测定,记录峰面积。结果的 RSD为1.59%(n=6),表明方法重复性良好。
回收试验:取约12,15,18 mg的橙皮苷标准品,精密称定,置100 mL容量瓶中,加入处方量的大豆卵磷脂,用DMSO-甲醇混合溶液溶解并定容。分别按拟订色谱条件进样测定,以外标法计算。结果见表1。

表1 橙皮苷回收试验结果(n=9)
2.4 样品含量测定
精密称取橙皮苷磷脂复合物(相当于橙皮苷30 mg),置10 mL容量瓶中,加DMSO-甲醇混合溶液溶解并定容,12 000 r/min离心10 min,精密量取0.5 mL续滤液置10 mL容量瓶中,加入甲醇定容,作为供试品溶液。按拟订色谱条件进样测定,以外标法计算含量。取样品3批,制备成供试品溶液,进样分析,记录峰面积,计算橙皮苷的含量。结果3批样品中橙皮苷的平均含量为282.5 μg/mg。
3 讨论
参照2010年版《中国药典(一部)》橙皮苷的含量测定方法,其流动相为甲醇-醋酸-水(35∶4∶61),结果分离度不好。分别比较了甲醇-0.5%醋酸水溶液、乙腈-0.5%醋酸水溶液、乙腈-5 mmol/L醋酸铵溶液的分离效果,结果表明,以乙腈-0.5%醋酸水溶液为流动相时分离度、峰形、理论板数较好。根据出峰时间调整流动相比例,最终选择乙腈-0.5%醋酸水溶液(25∶75)作为流动相。
本试验中建立了测定橙皮苷磷脂复合物中橙皮苷含量的HPLC法,在拟订色谱条件下,辅料、溶剂对测定无干扰,结果准确,方法重复性好,可有效控制该制剂的质量,为进一步研制橙皮苷口服制剂奠定了基础。
[1]钱俊臻,王伯初.橙皮苷的药理作用研究进展[J].天然产物研究与开发,2010,22(1):176-180.
[2]凡小燕,李 俊,王 雯,等.橙皮苷自微乳在大鼠小肠的吸收动力学[J].安徽医科大学学报,2011,46(8):754-758.
[3]Pinnamaneni S,Das NG,Das SK.Formulation approaches for orally administered poorly soluble drugs[J].Pharmazie,2002,57(5):291-300.
[4]江 波,印春华.提高难溶性药物口服生物利用度的方法[J].中国医药工业杂志,2002,33(7):358-362.
[5]孙 燕,高 尔,王汝琴.中药活性成分磷脂复合物研究进展[J].医学综述,2007,13(11):875-877.
[6]张 颖,李 楠,王彩云,等.HPLC测定鲑鱼降钙素磷脂复合物的含量[J].华西药学杂志,2013,28(6):623-625.
Determination of Hesperidin Content in Hesperidin-Phospholipid Complex by HPLC
Zhang Qing,Guan Haiyan,Jin Zhu,Lu Laichun (Department of Pharmacy,Research Institute of Field Surgery,Daping Hospital of Third Military University,Chongqing,China 400042)
Objective To establish a HPLC method for the content determination of hesperidin-phospholipid complex.M ethods The chromatographic separation was performed on a Diamonsil C18column(250 mm×4.6 mm,5 μm)with a mobile phase of acetonitrile-0.5% acetic acid aqueous solution(25∶75).The flow rate was 1.0 mL/min and the detection wavelength was 283 nm.The column temperature was maintained at 30℃ and the inject volume was 20 μL.Results Hesperidin in the range of 5.19-103.73 μg/mLshowed the good linear relation(r=0.999 5).The average recovery rate was 101.02%(RSD=1.30%).The average content of hesperidin contained in hesperidin-phospholipid complex was 282.5 μg/mg.Conclusion The established method in this study is accurate,reliable and reproducible,and can be used for the content determination of hesperidin-phospholipid complex.
hesperidin;phospholipid complex;HPLC;content determination
张卿,硕士研究生,药师,主要从事中西药物新型给药系统研究,(电话)023-68757098(电子信箱)zhangqingzq023@163.com;卢来春,博士研究生,副主任药师,主要从事创新药物及制剂的研究,本文通讯作者,(电话)023-68757091(电子信箱)lulaicq@163.com。
2014-11-13)
重庆市卫生局中医药科技项目,项目编号:ZY20132058。
R284.1;R282.71
A
1006-4931(2015)13-0030-02

