龙蛭胶囊质量控制*
王捷,刘伟,叶勇,何成章,陆华,程道海,黎渊弘
(1.广西医科大学制药厂,南宁 530021;2.广西医科大学药学院,南宁 530021;3.广西医科大学第一附属医院药剂科,南宁 530021)
龙蛭胶囊由地龙、菲牛蛭、川芎和红花等提取物蚓激酶、菲牛蛭素、阿魏酸、红花黄色素等组成,有抗凝和纤溶双重作用,临床用于防治血栓疾病[1-2]。该药通过多成分的协同、整合,多种作用靶点起到防治血栓的目的。为控制质量,现以纤维蛋白平板法测定纤溶活性,用全自动血凝仪测定该药体外抗凝效应,用薄层色谱(thin-layer chromatography,TLC)法鉴别阿魏酸、羟基红花黄色素A,高效液相色谱(high performance liquid chromatography,HPLC)法测定阿魏酸和羟基红花黄色素A含量等,利于该药质量控制。
1 仪器与材料
1.1 仪器 Waters515高效液相色谱仪(沃特世科技上海有限公司);N2000色谱数据工作站(浙江大学智能信息工程有限公司);BP211D电子天平(德国Sartorius,精密度:0.01 mg);UV-2100双光束紫外可见分光光度计(北京瑞利分析仪器公司);LDZ4-0.8自动平衡微型离心机(北京医用离心机厂);B11241-89B电热恒温水浴箱(北京医疗设备厂);ACL-Advace全自动血凝仪(美国IL公司生产);ZF-20C暗箱式紫外分析仪(上海宝山顾村电子仪器厂);BZ500S-M7超声器(必能信超声上海有限公司);OLYMPUS SP-800数码照相机。
1.2 试药 龙蛭胶囊(广西医科大学第一附属医院研制,批号:20100901,20101001,20101101);注射用尿激酶(广东天普生物化学制药有限公司,批号:20110105);阿魏酸对照品(中国食品药品检定研究院,批号:110773-201313,含量:99.6%);羟基红花黄色素A对照品(中国食品药品检定研究院,批号:111637-200503,含量:98%);甲醇:色谱纯;水为双蒸水;其他试剂均为分析纯。
1.3 动物 家兔,体质量2.0~2.5 kg,动物雌雄兼用,均由广西医科大学实验动物中心提供,动物合格证号:SCXK(桂)2009-0002。
2 方法与结果
2.1 性状 本品为胶囊,除去囊壳后显灰黄棕色至棕褐色粉末,味微腥,微苦。
2.2 纤溶活性检测[3-4]
2.2.1 纤溶活性定性检测 采用纤维蛋白平板法(标准平板和加热平板)。按需在平板上打直径3 mm小孔,每孔加不同浓度的尿激酶或龙蛭胶囊10μL(含龙蛭胶囊内容物3 mg),置37℃保温18 h后取出观察。结果:龙蛭胶囊在普通平板和加热平板上都能溶解纤维蛋白(溶圈直径20 mm),而尿激酶在普通平板上有较强的纤溶作用,在加热平板上则无纤溶作用(无溶圈),也说明龙蛭胶囊纤溶机制与尿激酶不同,是以直接纤溶为主。
2.2.2 纤溶活性定量检测 配制 1000,500,250,125,62.5,31.25 U·mL-16个浓度的尿激酶标准系列,37℃保温18 h,用游标卡尺测量最大和最小直径,以标准品两直径乘积对标准品活力单位双对数作图绘制标准曲线。以样品乘积查标准曲线得活力单位。Y=0.348X+0.552,r=0.951。结果龙蛭胶囊纤溶活性为73 U·g-1。统计学处理:所有实验数据以均数±标准差()表示,用方差分析q检验,t检验进行统计学处理,P<0.05为差异有统计学意义。
2.3 抗凝效应
2.3.1 贫血小板血浆的制备 家兔由颈动脉抽血,用3.8%枸橼酸钠抗凝,血液与抗凝剂之比为9∶1,4000 r·min-1离心 15 min,(离心机半径 r=12 cm)取上清液即为贫血小板血浆。
2.3.2 体外法 取龙蛭胶囊600 mg溶于0.9%氯化钠溶液至 2.5mL,以 4000 r·min-1离心 10 min,得上清液 1.75mL(约342 g·L-1生药),分别取上清液 1,0.5,0.25mL(对照组给予 0.9%氯化钠溶液),分别加入用由上述所制备的贫血小板血浆9,9.5,9.75mL3个不同稀释浓度,每一稀释浓度取100μL,然后按活化部分凝血酶时间(activated partial thromboplastin time,APTT)、凝血酶原时间(prothrombin time,PT)、凝血酶时间(thrombin time,TT)试剂盒说明,在美国IL公司ACL-Advace全自动血凝仪上进行测定。结果龙蛭胶囊体内外APTT、PT、TT显著延长(P<0.01)。见表1。
2.4 TLC 鉴别
2.4.1 阿魏酸薄层鉴别 取本品内容物细粉1 g,加稀盐酸30mL,超声处理10 min,滤过,滤液用乙醚(40mL,20mL)提取2次,合并乙醚液,挥干,残渣加乙酸乙酯0.5mL使溶解,作为供试品溶液。另取阿魏酸对照品适量,加乙酸乙酯制成每毫升含阿魏酸0.5 mg的溶液,作为对照品溶液。另称取阴性样品(缺川芎提取物)1 g,同法处理,得阴性对照溶液。照薄层色谱法(《中华人民共和国药典》2010年版一部附录ⅥB)实验,吸取上述两种溶液各5μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-三氯甲烷-冰醋酸(12∶4∶1)为展开剂,10℃以下展开,取出,晾干,于荧光灯(365nm)下观察。结果供试品溶液色谱中,在与对照品溶液色谱相应位置上显1个相同颜色明亮荧光斑点。阴性对照溶液色谱中,在与对照品溶液色谱相应位置上,无荧光斑点,见图1。
2.4.2 红花黄色素薄层鉴别 取本品内容物2 g,加80%甲醇溶液30mL,密塞,超声处理30 min,滤过,蒸干,残渣加丙酮1mL使溶解,滤过,滤液作为供试品溶液。另取羟基红花黄色素A对照品适量,加丙酮制成每毫升含羟基红花黄色素A0.2 mg的溶液,作为对照品溶液。另称取阴性样品(缺红花提取物)2 g,同法处理,得阴性对照溶液。照薄层色谱法(《中华人民共和国药典》2010年版一部附录ⅥB)实验,吸取上述两种溶液各5μL,分别点于同一硅胶H薄层板上,以乙酸乙酯-甲酸-水-甲醇(7∶2∶3∶0.4)为展开剂,展开,取出,晾干,日光下观察。结果供试品溶液色谱中,在与对照品溶液色谱相应位置上显1个相同颜色斑点。阴性对照溶液色谱中,在与对照品溶液色谱相应位置上,无斑点,见图2。
表1 4组家兔APTT、PT、TT的检测值Tab.1 Result of APTT,PT,TT of four groups of rabbits t·s-1,

表1 4组家兔APTT、PT、TT的检测值Tab.1 Result of APTT,PT,TT of four groups of rabbits t·s-1,
与对照组比较,*1 P<0.01Compared with control group,*1 P <0.01
组别 家兔/只 浓度/(g·L-1)APTT PT TT龙蛭胶囊大剂量组 10 34.2 188.20 ±57.12*1 21.20 ±1.03*1 19.00 ±0.66*1中剂量组 10 17.1 134.20 ±13.19*1 13.50 ±0.70*1 17.12 ±0.64*1小剂量组 10 8.5 106.10 ±48.8*1 10.90 ±0.56*1 6.80 ±0.63*1对照组 10 …55.00 ±4.13 9.40 ±0.84 13.00 ±1.00

图1 龙蛭胶囊中阿魏酸TLC图1~3.供试品;4.阴性对照品;5.阿魏酸对照品Fig.1 TLC of ferulic acid in longzhi capsule1 -3.sample;4.negative control;5.ferulic acid reference
2.5 HPLC法测定阿魏酸含量
2.5.1 色谱条件与系统适用性 采用 Kromasil C18(4.6 mm ×200 mm,5μm)色谱柱,流动相:水-冰醋酸-甲醇(65∶1∶35),流速:1.0mL·min-1,检测波长:320nm,柱温:25℃,进样量:10μL,理论板数按阿魏酸峰计算应不低于5000。在上述色谱条件下测定,结果阿魏酸保留时间为14.2 min,阴性样品对测定无干扰,见图3。
2.5.2 阿魏酸对照品溶液 精密称取阿魏酸对照品16.67 mg,置50mL棕色量瓶中,加甲醇溶解后定容,摇匀,即得贮备液。精密量取贮备液1.5mL,置25mL棕色量瓶中,加甲醇稀释至刻度,摇匀即得浓度为20μg·mL-1的阿魏酸对照品溶液。
2.5.3 供试品溶液制备 取龙蛭胶囊内容物细粉约2.5 g,精密称定,置具塞锥形瓶中,精密加入乙酸乙酯100mL,超声处理(功率100 W,频率40 kHz)30 min,冷却补足减失质量,滤过。精密量取续滤液5mL,蒸干,残渣加适量甲醇溶解,后转置10mL棕色量瓶中,加甲醇稀释定容至刻度,摇匀,即得。

图2 龙蛭胶囊中红花黄色素TLC图1~3.供试品;4.阴性对照品;5.羟基红花黄色素A对照品Fig.2 TLC of hydroxysafflor yellow A in longzhi capsule1 - 3.sample;4.negative control;5.hydroxysafflor yellow A reference

图3 阿魏酸的HPLC色谱图A.阴性对照品;B.阿魏酸对照品;C.供试品;1.阿魏酸Fig.3 HPLC chromatogram of ferulic acidA.negative control;B.ferulic acid reference;C.sample;1.ferulic acid
2.5.4 阴性对照溶液制备 按处方比例,取除川芎提取物外其他药,制得阴性样品,按“2.5.3”项制备即得。
2.5.5 线性关系考察 精密吸取阿魏酸对照品溶液2,5,10,15,20μL,注入高效液相色谱仪,按上述色谱条件依次测定峰面积。以进样量为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程:Y=9.90×106X-7.05 ×104,r=0.9999。结果表明阿魏酸在进样量0.04 ~0.40μg 范围内呈良好线性关系。
2.5.6 精密度实验 精密吸取同浓度阿魏酸对照品溶液,按上述色谱条件,进样10μL,平行测定6次,测定峰面积,计算RSD为1.06%(n=6),结果可见精密度良好。
2.5.7 稳定性实验 精密吸取同一供试品溶液,间隔不同时间测定,在 0,2,4,6,8 h 各进样 10μL,测定峰面积,计算含量,RSD为1.7%,结果表明供试品溶液在8 h内稳定。
2.5.8 重复性实验 精密称取同批龙蛭胶囊内容物6 份,按“2.5.3”项制备供试品溶液,分别进样 10μL,按上述色谱条件测定阿魏酸峰面积,计算含量,结果RSD 为1.28%(n=6)。
2.5.9 加样回收率实验 精密称取同批龙蛭胶囊内容物(阿魏酸含量0.2006%)1.25 g,置具塞锥形瓶中,精密添加阿魏酸对照品溶液(0.3334 mg·mL-1)7.5mL,平行实验6份,测定相应峰面积,计算含量和回收率,结果阿魏酸平均加样回收率为99.32%,RSD为 1.20%,见表 2。

表2 阿魏酸加样回收率实验结果Tab.2 Results of recovery test of ferulic acid
2.5.10 样品含量测定 取龙蛭胶囊3批,分别按“2.5.3”项制备供试品溶液,精密吸取阿魏酸对照品溶液和供试品溶液各10μL,注入色谱仪,按上述色谱条件测定峰面积,按外标法计算阿魏酸含量,结果见表3。

表3 3批龙蛭胶囊中阿魏酸含量测定结果Tab.3 Results of determination of ferulic acid content of longzhi capsules (n=3)
2.6 HPLC法测定羟基红花黄色素A含量
2.6.1 色谱条件与系统适用性 采用 Kromasil C18(4.6 mm ×200 mm,5μm)色谱柱,流动相:甲醇-乙腈-0.8%磷酸(25∶2∶73),流速:1.0mL·min-1,检测波长:403nm,柱温:25 ℃,进样量:10μL,理论板数按羟基红花黄色素A峰计算应不低于3000。在上述色谱条件下测定,结果羟基红花黄色素A保留时间为38.6 min,阴性样品对测定无干扰,见图4。
2.6.2 羟基红花黄色素A对照品溶液 精密称取羟基红花黄色素A对照品12.5 mg,置25mL棕色量瓶中,加甲醇溶解后定容至刻度,摇匀,即得贮备液。精密量取贮备液5mL,置10mL棕色量瓶中,加甲醇稀释至刻度,摇匀即得浓度为(250μg·mL-1)羟基红花黄色素A对照品溶液。
2.6.3 供试品溶液制备 取龙蛭胶囊内容物细粉约2.5 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇溶液50mL,超声处理(功率100 W,频率40 kHz)30 min,冷却补足减失质量,滤过。精密量取续滤液25mL,浓缩至约5mL,转移至10mL棕色量瓶中,加甲醇稀释定容至刻度,摇匀,即得。

图4 羟基红花黄色素A的HPLC色谱图A.阴性对照品;B.羟基红花黄色素A对照品;C.供试品;1.羟基红花黄色素AFig.4 HPLC chromatogram of hydroxysafflor yellow AA.negative control;B.hydroxysafflor yellow A reference;C.sample;1.hydroxysafflor yellow A
2.6.4 阴性对照溶液制备 按处方比例,取除红花提取物外其他药,制得阴性样品,按“2.6.3”项制备即得。
2.6.5 线性关系考察 精密吸取羟基红花黄色素A对照品溶液 2,5,10,15,20μL,注入高效液相色谱仪,按上述色谱条件依次测定峰面积。以进样量(μg)为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,得回归方程:Y=4.67 ×105X+3.18 ×105,r=0.9998。结果表明羟基红花黄色素A在进样量0.5~5.0μg范围内呈良好线性关系。
2.6.6 精密度实验 精密吸取同浓度羟基红花黄色素A对照品溶液,按上述色谱条件,进样10μL,平行测定6次,测定峰面积,计算RSD为1.32%(n=6),结果可见精密度良好。
2.6.7 稳定性实验 精密吸取同一供试品溶液,间隔不同时间测定,在 0,2,4,6,8 h 各进样 10μL,测定峰面积,计算RSD为1.73%。结果表明供试品溶液在8 h内稳定。
2.6.8 重复性实验 精密称取同批龙蛭胶囊内容物6 份,按“2.6.3”项制备供试品溶液,分别进样 10μL,按上述色谱条件测定羟基红花黄色素A峰面积,计算含量,结果RSD为1.47%(n=6)。
2.6.9 加样回收率实验 精密称取同批龙蛭胶囊内容物(羟基红花黄色素A含量0.125%)2.5 g,置具塞锥形瓶中,精密添加羟基红花黄色素A对照品溶液(0.5 mg·mL-1)6.5mL,平行实验 6 份,测定相应峰面积,计算含量和回收率,结果羟基红花黄色素A平均加样回收率为99.14%,RSD为1.30%,见表4。
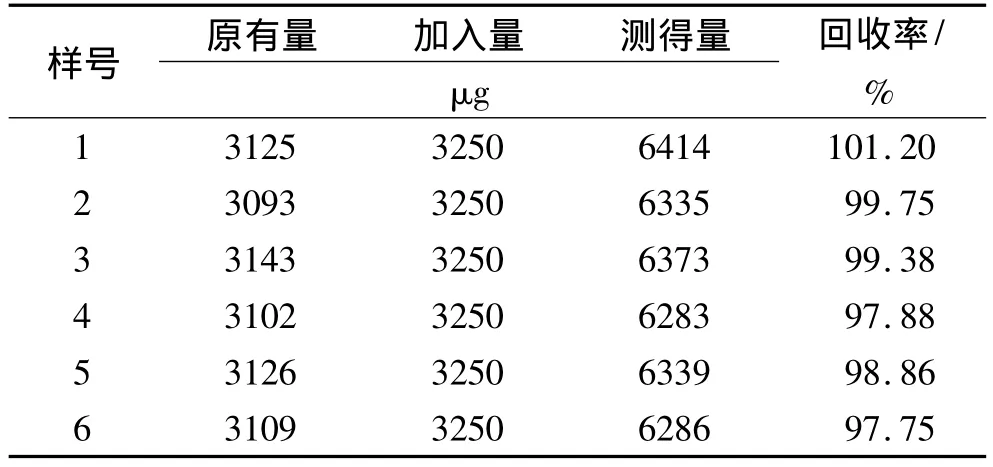
表4 羟基红花黄色素A加样回收率实验结果Tab.4 Determination results of ferulic acid content in three batches of longzhi capsules
2.6.10 样品含量测定 取龙蛭胶囊3批,分别按“2.6.3”项制备供试品溶液,精密吸取羟基红花黄色素A对照品溶液和供试品溶液各10μL,注入色谱仪,按上述色谱条件测定峰面积,按外标法计算羟基红花黄色素A含量,结果见表5。

表5 3批龙蛭胶囊中羟基红花黄色素A含量测定结果Tab.5 Determination results of hydroxysafflor yellow A content in three batches of longzhi capsules
3 讨论
血栓可引起血管狭窄、血液流通阻塞、部分器官缺血或栓塞,引发包括肺栓塞、急性心肌梗死、脑血栓和末梢动静脉血栓等疾病。心脑血管疾病已是世界上影响人类健康的最严重的疾病之一。治疗血栓药物分为抗血小板聚集药、抗凝血药和溶栓药三类,溶栓药物治疗是目前最有效的抗血栓治疗方法,但常出现免疫反应、出血等副作用,故研究和控制溶栓新药龙蛭胶囊质量将利于该药质量和疗效安全稳定,利于充分发挥该药疗效特色,也符合近年来国内医院制剂质量不断提升的趋势和定性定量要求[5-6]。
纤维蛋白平板法是目前国内外检测纤溶酶活性主要方法之一,有直接性、直观性等优点,广泛应用于纳豆激酶、蚓激酶、源于各种蛇毒纤溶酶活性及自然界其它新型纤溶酶筛选方法的鉴定和活力测定[7-9],故选用。普通纤维蛋白平板可检出纤溶酶活性和激酶活性,现用加热平板分辨这两种活性,将制备好的平板80℃加热30 min,检测可直接溶解纤维蛋白的纤溶酶活性,效果良好。
阿魏酸是该药的主要有效成分之一,可抑制血小板聚集、抗血栓形成、解除血管平滑肌痉挛、改善心肌缺血、抗炎止痛、抗氧化、提高膜稳定性、调节人体免疫功能等,占生药含量0.1% ~0.2%,是川芎根、茎中的一种芳香酸成分,溶于热水,乙醇和乙酸乙酯,稍溶于乙醚,难溶于苯和石油醚。用乙酸乙酯提取时,淀粉和糖类物质不会被提取[10-11],测定干扰少,故选用乙酸乙酯提取法。
该药所含的红花黄色素是中药菊科植物红花(Carthamus tinctorius L.)的干燥管状花的主要有效组分之一,由多种水溶性查尔酮成分的混合物组成,存在于红花的水溶性提取部位,其中羟基红花黄色素A含量最高,是红花主要效应物质,有抗脑缺血损伤、抗氧化、抗心肌损伤、对血小板的活性影响、抗凝、抗肿瘤等作用[12-14],现采用TLC法对该药中此成分加以鉴别,研究结果显示色谱效果好,相应斑点清晰。
[1]黎渊弘,钟小斌,戴曦,等.龙蛭胶囊体内外对动物血栓形成的影响和安全性实验[J].时珍国医国药,2012,23(1):133-134.
[2]黎渊弘,戴曦,钟小斌.龙蛭胶囊体内外对动物凝血、纤溶功能的影响[J].广西医科大学学报,2012,29(1):28-30.
[3]张彬,汪波,龚元,等.几种水蛭抗凝血物质提取及活性分析[J].中山大学学报:自然科学版,2012,51(4):92 -96.
[4]李华,陈陵霞,许瑞安.纤溶活性的药学测定方法研究[J].中国临床药理学与治疗学,2008,13(9):1066 -1070.
[5]王捷,龙禹,蒋英,等.不合理用药和干预[J].中国医药指南,2011,9(22):364 -366.
[6]王捷,辛丽娜,龙禹.肾复康胶囊中大黄素含量测定[J].中国药师,2009,12(4):474 -475.
[7]赵明,潘映红,王一丁.一种灵敏的体外溶栓活性检测方法薄层聚丙烯酰胺纤维蛋白胶板法的建立[J].中国药学杂志,2005,40(4):302 -304.
[8]张汉忠,董明华,张汉贞.水蛭活性物质体外抗凝及纤溶活性的研究[J].湖北中医学院学报,2002,4(2):31-32.
[9]葛勤,张恩娟,刘同华,等.地龙的化学成分及制剂质量研究概况[J].中国药业2004,13(3):69-71.
[10]范永春,杨光明,潘扬,等.川芎及其制剂质量控制的研究概况[J].时珍国医国药,2003,14(9):574 -575.
[11]蔡翠芳,唐星,李积军.川芎中阿魏酸的提取纯化工艺[J].沈阳药科大学学报,2008,25(1):70 -72.
[12]金鸣,高子淳,李金荣,等.大孔树脂柱色谱法制备红花黄色素和羟基红花黄色素 A[J].中草药,2004,35(1):25-28.
[13]姚苗苗,董仲才,任爱农.羟基红花黄色素A的研究进展[J].中南药学,2009,7(12):931 -934.
[14]臧宝霞,金鸣,李金荣.羟基红花黄色素A抗凝作用的研究[J].中草药,2007,38(5):741 -743.

