Acrysof IQ Toric人工晶状体矫正白内障患者角膜规则散光的临床观察
侯培莉,陆 燕,叶 芬,兰 文,黄振平
0 引 言
白内障手术已从单纯的复明手术转变为屈光手术,据统计白内障患者中,角膜散光>1.5D的患者占15%~29%[1],散光易导致患者视物疲劳、眼痛、视物模糊及重影等不适,严重影响患者的视觉质量。目前多种方法可矫正散光,例如角膜缘松解手术、手术后采用准分子激光手术等,虽然一定程度上可减轻患者的散光度数,提高视力,但由于此类方法预测性差,术后存在屈光回退,并且导致髙阶像差增高,因此临床上迫切需要一种更加有效的方法提高散光白内障患者的术后视觉质量。近年来,Acrysof IQ Toric IOL作为一种全新的矫正散光的非球面晶体应用于临床。本文对植入Acrysof IQ Toric IOL矫正角膜散光的白内障患者进行临床观察,分析该IOL矫正角膜散光的效果及其在囊袋内的稳定性。
1 资料与方法
1.1 研究对象 选择2012年10月至2013年3月在我院接受白内障超声乳化加IQ Toric IOL植入并完成随访3个月的白内障患者30例(34只眼),其中双眼4例,单眼26例;男13例,女17例;年龄43~89岁,平均(66.15±12.89)岁。病例纳入标准:确诊为年龄相关性白内障的患者,角膜散光为规则散光,散光度数1.0~6.0D,能够按时随访者。排除标准:角膜不规则散光及影响视力恢复的其他眼部疾病,如青光眼、葡萄膜炎、糖尿病视网膜病变、老年性黄斑变性及翼状胬肉等,曾有眼内手术史及屈光手术史者。
1.2 方法 术前人工晶状体度数计算采用A型超声波检测仪检测,选择SRK-T公式计算需植入人工晶状体球镜度数,球镜目标屈光度为0~-1.0D。柱镜度数及轴位通过Alcon公司在线计算器(Toric culator.com),结合球镜度数及术前角膜曲率及散光轴向,同时考虑手术切口位置及术源性散光,得到最佳轴位及最小预计残余散光。
术前半小时用复方托吡卡胺滴眼液充分散大瞳孔。患者取坐位,将裂隙灯光带转至水平位,裂隙灯通过角膜正中央,用标记笔在角膜缘 0°、90°、180°作3个标记,术中使用刻度盘在角膜缘标记人工晶状体轴位。所有标记及手术均由同一医师完成。手术方法:常规消毒、铺巾,开睑器开睑,盐酸奥布卡因滴眼液表面麻醉3次,行2.2 mm角膜缘透明切口,前房注入Discovisc粘弹剂,连续环形撕囊,撕囊口直径5~5.5 mm,水核分离和水核分层后,采用Alcon公司Infiniti超声乳化仪进行白内障超声乳化,吸除残余皮质,囊袋内注入粘弹剂,并植入IQ Toric IOL。吸除IOL后方粘弹剂,顺时针调整IOL位置到预定轴位,使人工晶状体标记点与预置轴位重合。轻压IOL光学部使其与后囊膜贴附,清除前房粘弹剂。水封闭透明角膜切口。术毕涂妥布霉素地塞米松眼膏,纱布遮盖。所有病例均无术中并发症,IOL植入顺利,未出现晶体袢折断、后囊破裂等并发症。
1.3 观察指标 术前UCVA及BCVA,术后1周、1个月、3个月UCVA采用国际标准远视力表结合主觉验光检查。角膜地形图仪观察角膜散光变化。术后1 d、1周、1个月、3个月散瞳后在裂隙灯显微镜下观察轴位变化。以术后1 d的轴位作为IOL轴位旋转的参照指标。
1.4 统计学分析 采用SPSS 17.0软件进行统计学分析。计量资料且呈正态分布者以均数±标准差()表示,采用两因素方差分析进行手术前后不同时间点的角膜散光、预计残余散光和术后残余散光的组间比较,其两两比较采用LSD检验。术后IOL轴位移动度的比较采用LSD检验。以P≤0.05为差异有统计学意义。
2 结 果
2.1 手术前后视力比较 白内障患者术前UCVA与术后1周、1个月、3个月的UCVA相比,差异有统计学意义(P<0.05);术前BCVA与术后1周、1个月、3个月的BCVA比较,差异均有统计学意义(P<0.05)。术后1周、术后1个月、3个月的UCVA均高于术前 BCVA,差异有统计学意义(P<0.01)。见表1。
表1 手术前后患者UCVA和BCVA的比较(,n=34)Figure 1 Comparison of preoperative and postoperative UCVA and BCVA(,n=34)
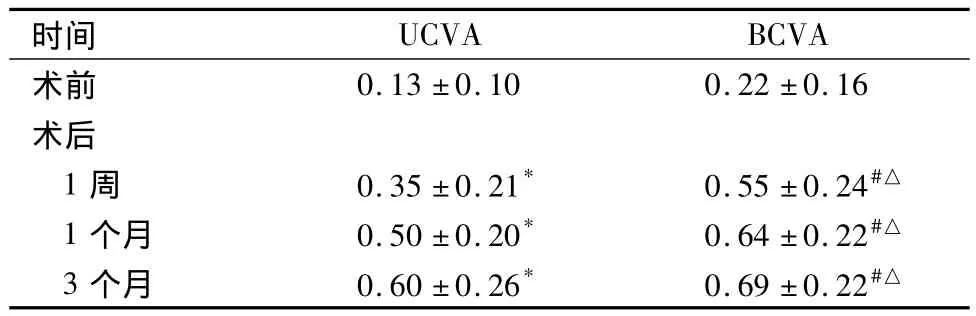
表1 手术前后患者UCVA和BCVA的比较(,n=34)Figure 1 Comparison of preoperative and postoperative UCVA and BCVA(,n=34)
与术前UCVA比较,*P<0.05;与术前BCVA比较,#P<0.05;与术后同时段UCVA比较,△P<0.01
时间UCVA BCVA术前0.13 ±0.10 0.22 ±0.16术后1 周 0.35 ±0.21* 0.55 ±0.24#△1 个月 0.50 ±0.20* 0.64 ±0.22#△3 个月 0.60 ±0.26* 0.69 ±0.22#△
2.2 屈光状态 术前角膜散光平均为(2.07±1.13)D,预计残余散光为(0.28 ±0.22)D。术后 1周、1 个月、3 个月残余散光分别为(0.26 ±0.13)D、(0.30 ±0.16)D、(0.34 ±0.29)D。术前角膜散光与术后1周、1个月、3个月残余散光相比差异具有统计学意义(P<0.01),术后1周、1个月、3个月残余散光与预计残余散光相比,差异均无统计学意义(P >0.05)。
2.3 术后IOL轴位移动度 术后1 d开始用裂隙灯显微镜测量IOL的轴位并进行记录。术后1周、1个月、3个月平均轴位移动度分别为:(3.17±1.83)°、(3.22 ±1.94)°、(3.57 ±1.69)°,术后 1 个月与术后1周比较,差异无统计学意义(P>0.05);术后3个月与术后1周比较,差异无统计学意义(P>0.05);术后1个月与术后3个月比较,差异无统计学意义(P>0.05)。术后3个月所有随访患者IOL轴位移动度均<10°。
2.4 并发症 所有患者在随访期间未发生继发性青光眼、眼内感染、瞳孔变形、虹膜粘连、黄斑水肿、前囊环收缩、后发性白内障等并发症。
3 讨 论
在白内障手术中有多种矫正角膜散光的方法,如选择在角膜曲率陡峭子午线上做透明角膜切口或者对侧做一松解切口,但均存在预测性差、矫正范围有限并且存在回退现象,容易受患者年龄、角膜切口位置及大小、角膜厚度等因素的影响,因此进行白内障手术时植入散光型人工晶状体具有良好的优势。Merdicate等[2]研究发现植入 Toric IOL后患者的UCVA好于角膜缘松解切开。刘荣和张红[3]研究发现Toric IOL能够有效地矫正角膜散光,并且具有较好的旋转稳定性。鲍先议等[4]研究高度角膜散光患者植入Toric IOL后的临床效果,结果显示高度数Toric IOL可矫正高度数的角膜散光,其预测性好,在囊袋中有可靠的稳定性。研究表明,IOL每移动1°就有3.3%的柱镜度数失效[5],IOL 移动超过 30°则柱镜的作用就完全消失。Watanabe等[6]使用ASOCT观察Toric IOL植入术后的旋转度,研究发现术后1周、1个月的旋转度较小,稳定性好。
Acrysof IQ Toric IOL是一片式疏水性丙烯酸酯IOL,前表面为非球面,后表面为环形曲面。其光学直径为6.0 mm,全长 13 mm,屈光指数为 1.55,目前国内有T2~T9这8种型号,对应的柱镜值分别为1.0、1.5、2.25、3.0、3.75、4.5、5.25、6.0,理论上可以矫正角膜平面 0.68D、1.03D、1.55D、2.06D、2.57 D、3.08D、3.6D、4.11D 的散光。我国目前常用的型号为T3、T4、T5。本文研究发现植入Acrysof IQ Toric IOL可以有效地矫正白内障患者的角膜散光,同时具有较好的预测性、安全性及稳定性。同时,此人工晶状体为非球面散光型人工晶状体,具有良好的术后视觉质量。术前准确测量IOL的度数对于Acrysof IQ Toric IOL植入术后的视觉质量起到至关重要的作用[7]。我们采用IOL-Master进行眼轴及IOL度数的测量,并使用角膜地形图进行角膜曲率测量,使得IOL度数的测量值更加精确。根据临床经验发现,植入Acrysof IQ Toric IOL后应特别注意要用I/A注吸头吸净IOL后方的粘弹剂,这样可有效地减少术后IOL在囊袋内的旋转,从而增加IOL的稳定性,使白内障患者术后的残余散光减少。另外,还要注意术前要充分散大瞳孔,对于一些如虹膜后粘连导致瞳孔难以散大的白内障患者,则要避免植入Acrysof IQ Toric IOL。
总之,IQ Toric IOL矫正散光效果好,具有较好的预测性及旋转稳定性,可作为白内障合并规则角膜散光患者的良好选择。正常人角膜存在正性球差,并保持相对稳定的状态。随着年龄的增长,晶状体的负性球差逐渐转为正性,使全眼的球差增加,导致暗视力差及对比敏感度下降等[8]。徐仁凤等[9]对白内障术后不同IOL的对比敏感度进行研究,结果发现非球面IOL组的对比敏感度较多焦点IOL、单焦点IOL高;研究显示非球面IOL可抵消球面像差,从而有效提高对比敏感度。IQ Toric IOL为非球面散光型IOL,不仅能够矫正角膜散光,还具有非球面IOL的特性,因此可抵消部分正性球差,使老年患者术后总球差降低,从而提高患者的视觉质量。由于本文随访病例数较少,随访时间相对较短,因此对IQ Toric IOL植入术后患者的远期临床效果及视觉质量仍有待于进一步随访。
[1]Fam HB,Lim KL.Meridional analysis for calculating the expected spherocylindrical refraction in eyeswith toric intraocular lenses[J].J Cataract Refract Surg,2007,33(12):2072-2076.
[2]Merdicate J,Iriqoven C,Ruiz M,et al.Toric intraocular lens versus opposite clear corneal incision to correct astigmatism in eyes having cataract surgery[J].J Cataract Refract Surg,2009,35(3):451-458.
[3]刘 荣,张 红.Toric人工晶状体矫正角膜散光的效果评价[J].眼科研究,2009,27(3):226-228.
[4]鲍先议,王 勇,叶应嘉,等.高度角膜散光白内障患者植入Toric IOL的临床观察[J].国际眼科杂志,2012,12(7):1316-1318.
[5]Viestenz A,Seitz B,Langenbucher A.Evaluating the eye's rotational stability during standard photography effect on determining the axial orientation of toric intraocular lenses[J].J Cataract Refract Surg,2005,31(3):557-561.
[6]Watanabe K,Negishi K,Torii H,et al.Simple and accurate alignment of toric intraocular lenses and evaluation of their rotation errors using anterior segment optical coherence tomography[J].Jpn J Ophthalmol,2012,56(1):31-37.
[7]李建昌,黄振平.人工晶体度数测量的研究现状[J].医学研究生学报,2009,22(11):1211-1216.
[8]Holladay JT,Piers PA,Koranyi G,et al.A new intraocular lens design to reduce spherical aberration of pseudophakic eyes[J].J Refract Surg,2002,18(6):683-691.
[9]徐仁凤,黄振平,杨丽萍.白内障术后不同人工晶状体对比敏感度的研究[J].医学研究生学报,2007,20(3):266-268.

