经皮椎体后凸成形术治疗老年压缩性骨折效果分析
陈乙瑞 骆 浩 冯世龙 魏 星 陈晓华重庆三峡中心医院骨一科,重庆 404000
老年骨质疏松导致椎体压缩性骨折是目前常见的脊柱疾病,严重影响老年人的生活质量。椎体压缩骨折后降低了伤椎节段的前中柱抗压强度,增加了后柱的压应力负荷,导致脊柱运动单元的强度和稳定性显著下降[1]。经皮椎体后凸成形术(percutaneous kyphoplasty,PKP)的生物力学研究证实压缩骨折的椎体经后凸成形后其伤椎节段的运动稳定性较成形前显著提高,可防止椎体的进一步塌陷和变形,缓解患者疼痛[2-4]。该术式目前已成为治疗老年骨质疏松性椎体压缩骨折的新途径,本研究采用PKP技术共治疗老年骨质疏松导致的椎体压缩骨折,效果满意,与之前运用的经皮椎体成形术 (pereutaneous vertebroplasty,PVP)相比,具有一定的优势,现报道分析如下:
1 资料与方法
1.1 一般资料
选择2011年3月~2013年2月重庆三峡中心医院骨一科治疗的因老年骨质疏松致椎体压缩骨折患者16例为研究组(PKP组),共20个椎体。其中男7例,女 9 例;年龄 52~86 岁,平均(72.0±3.5)岁;单椎体压缩 12 例,双椎体压缩 4 例;骨折部位:在 T12~L3、T12椎4例,L1椎体6例,L2椎体6例,L3椎体4例。其中老年骨质疏松所致新鲜压缩骨折4例,老年骨质疏松所致陈旧压缩骨折10例,乳腺癌致椎体转移瘤合并骨质疏松压缩骨折2例。
选择2010年3月~2011年2月老年骨质疏松导致椎体压缩骨折15例为对照组(PVP组),共20个椎体。男 7 例,女 8 例。年龄 51~87 岁,平均(71.0±3.8)岁;单椎体压缩10例,双椎体压缩5例;骨折部位:在T12~L3、T12椎 5例,L1椎体 7例,L2椎体 4例,L3椎体 4例。其中老年骨质疏松所致新鲜压缩骨折4例,老年骨质疏松所致陈旧压缩骨折9例,乳腺癌致椎体转移瘤合并骨质疏松压缩骨折2例。
临床表现:患者均有不同程度的胸腰背疼痛症状,伤椎处有明显的压痛和叩击痛,平卧时转侧翻身较困难,所有患者均无脊髓和神经刺激症状及体征。骨密度核扫描均提示中、重度骨质疏松,CT及MRI扫描显示所有椎体后壁完整,椎管内均无明显占位。两组性别、年龄、骨折椎体等一般资料比较,差异均无统计学意义(P > 0.05),具有可比性。
1.2 术前检查
所有患者术前行正侧位脊柱X线检查,陈旧骨折均作椎体过伸过屈位X片检查(以排除腰椎不稳所致活动性疼痛);患者均行MRI及CT扫描、骨密度测定。影像学检查重点在于观察椎体压缩程度,鉴别陈旧与新鲜骨折,判断椎体骨质疏松并伴有部分椎体高度丢失,椎体后缘及椎弓根是否完整,分析肿瘤侵犯范围以及脊髓受压情况。
术前检查还包括胸片、血常规、心电图、血糖,、凝血功能等检查。常规行双下肢血管彩超及D-二聚体检查以排除血栓形成,降低因血栓所致的肺栓塞。
1.3 手术方法及处理
1.3.1 对照组(PVP 组)
1.3.1.1 体位 常规俯卧位、胸腹部悬空。新鲜骨折采用通过手术台腰桥作用适当行过伸体位复位椎体。定位:C形臂透视下,正位确认伤椎椎弓根的位置,侧位确认椎弓根的方向,将穿刺点定位在椎弓根眼的外上方,用画线笔表定位标志,消毒铺巾。
1.3.1.2 麻醉 常规2%利多卡因局部麻醉。1例因疼痛及精神紧张不能耐受手术行全身麻醉。心率、血压和血氧饱和度监护,心肺功能较差者采用鼻导管给氧或面罩吸氧。
1.3.1.3 手术过程 消毒铺巾后,X线引导下由正位椎弓根的外上与矢状面成约15°夹角进行经皮穿刺。穿刺针通过椎弓根,深度达椎体前1/3。确认穿刺针位置良好后,去除针芯。调制骨水泥至黏稠状态,在正、侧位X线间断透视监控下用注射器接穿刺针注入伤椎。X线透视见骨水泥沿骨小梁间隙浸润。边缘毛刺状至骨皮质为止.若发现骨水泥浸润至椎体后缘或向椎体外渗漏则立即停止推注。骨水泥完全硬化后。拔出穿刺针。
1.3.2 研究组(PKP 组)
麻醉、体位、穿刺方法同PVP。具体过程如下:①定位针穿刺:在一侧椎弓根外侧取1 cm切口,于C形臂透视监控下,经椎弓根入路,穿刺针穿过切口,移除穿刺针针芯,让穿刺针导管盲端(无尖端不易损伤临近组织并在软组织内不易滑动)在腰椎置于横突的副突和峡部形成的“/”嵴的顶点,手感感觉针道远端在顶点位置,连续C形臂透视显示椎弓根外上缘,用穿刺针芯缓慢穿入椎体后缘,避免椎弓根内壁穿破,继续将针尖穿至椎体前中1/3处[5],以便球囊顺利置入伤椎。②建立工作通道:将2 mm的引导管沿穿刺针置入,再建立工作通道,直达椎体后壁。③置入球囊:通过工作通道将15 mm长的球囊置入,注入造影剂(泛影蒲氨有过敏发生,选择海三醇相对安全)。进入工作通道。扩张球囊:在扩张球囊的过程中,连续加压使球囊膨胀,当球囊接近上终板的位置即可,避免将球囊扩至最大容积量。一般15 mm的球囊能容纳4 mL,而20 mm的球囊能容纳6 mL。当球囊压力扩至300 Psi时,不能再加压。当球囊压力扩至不能下降时应停止加压。④注入硫酸钙或骨水泥:球囊扩张达到要求后,取出球囊,用硫酸钙或骨水泥4 mL,稀释搅拌至骨水泥呈黏糊状,逐渐注入(硫酸钙凝固时间短,仅需2 min即开始凝固,调制好后需立即注入)。注射骨水泥及硫酸钙全程于C形臂透视下,监视椎体内硫酸钙或骨水泥的弥散情况,当硫酸钙或骨水泥充满椎体到后壁或外渗时应停止推注,此时须间断转动穿刺针以防止针与所注入的骨水泥粘牢,2~3 min后待骨水泥已基本固化,可旋转穿刺针并拔出,可避免黏糊状的骨水泥沿针道向后渗漏。必要时进行双侧穿刺注射。本研究对于术前CT提示椎体侧壁和前壁有骨折的患者,为防止骨水泥渗漏至椎体边缘,在注入骨水泥时,先只注入0.5 mL,3~5 min后待注入的骨水泥在椎体内分布的大部分硬化后再注入剩下的骨水泥。这样可以防止骨水泥渗漏现象。术毕,正侧位摄片记录注射情况。同时,患者术后平卧6 h,吸氧并监测生命体征。骨水泥术中和术后影像资料见图1。
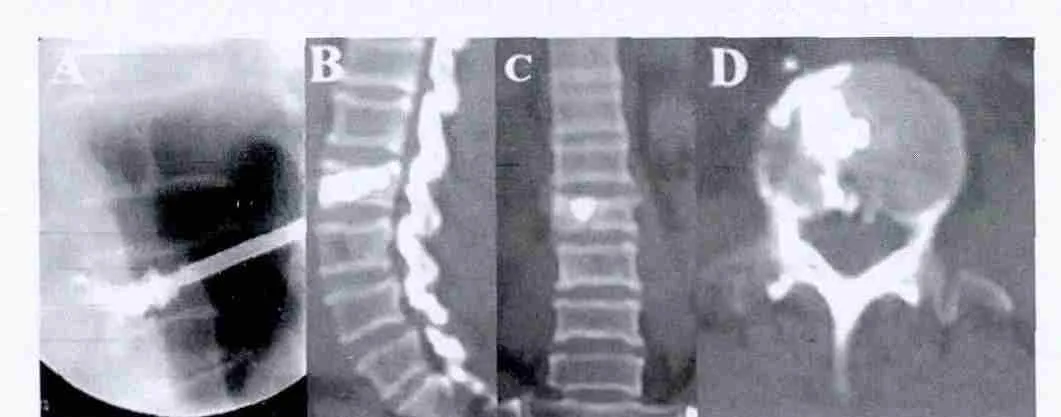
图1 术中术后骨水泥
1.3 疗效评定
1.3.1 疼痛评定
采用疼痛视觉模拟评分(VAS)[6]评价患者术前、术后48 h及随访时的疼痛情况。疼痛依据患者的主观感受,0分表示无疼痛,1~3分表示轻度疼痛,4~6分表示中度疼痛,7~9分表示重度疼痛,10分表示难忍受。
1.3.2 伤椎前柱恢复程度
拍摄脊柱侧位片,椎体前柱高度变化通过测量获取,比较百分率。
1.3.3 骨水泥或硫酸钙渗漏情况
通过CT结果统计渗漏例数,比较百分率。
1.4 统计学方法
采用统计软件SPSS 15.0对数据进行分析,计量资料以均数±标准差(±s)表示,两独立样本的计量资料采用t检验。计数资料以率表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组疼痛评分术前、术后及随访3个月比较
两组患者椎体操作全部成功,手术时间45~70 min,平均55 min/椎。术后患者疼痛明显改善,两组术后及随访时疼痛评分均低于术前,差异均有统计学意义(P<0.05);两组间各时段疼痛评分比较,差异均无统计学意义(P > 0.05)。 见表1。
表1 两组术前、术后及随访3个月时疼痛评分比较(分,±s)
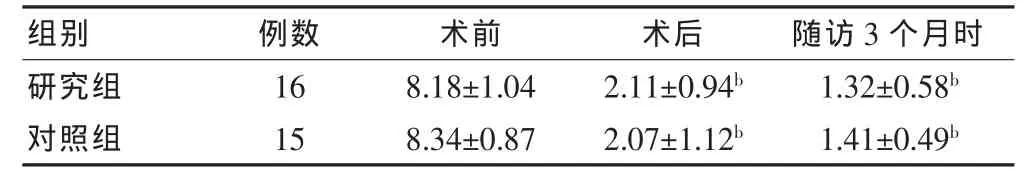
表1 两组术前、术后及随访3个月时疼痛评分比较(分,±s)
注:与组内术前比较,bP < 0.05
研究组对照组16 15 8.18±1.04 8.34±0.87 2.11±0.94b 2.07±1.12b 1.32±0.58b 1.41±0.49b组别 例数 术前 术后 随访3个月时
2.2 两组术后及随访3个月时前柱高度变化比较
卧床休息12~24 h后,戴腰围保护下活动,术后使用抗生素1~2 d,术后2~3 d摄X线正侧位片及CT扫描检查。研究组随访时前柱高度与术后比较轻微降低,而对照组几乎无变化。术后及随访3个月时两组间脊柱前柱高度变化差异有统计学意义(P<0.05)。见表2。
表2 两组术后及随访3个月时前柱高度变化比较(%,±s)

表2 两组术后及随访3个月时前柱高度变化比较(%,±s)
注:与对照组比较,cP < 0.05
研究组对照组16 15 57.0±6.2 59.0±7.3 82.0±12.5c 71.0±8.6 80.0±10.4c 71.0±8.8组别 例数 术前 术后 随访3个月时
2.3 两组术中骨水泥渗漏情况比较
术后复查时,研究组有1例患者出现1个椎体骨水泥渗漏,渗漏率为5.00%,对照组4例患者出现骨水泥渗漏,其中2例分别出现2个椎体,另外2例分别出现1个椎体渗漏,渗漏率为30.00%。两组比较,差异有统计学意义(P<0.05)。 见表3。
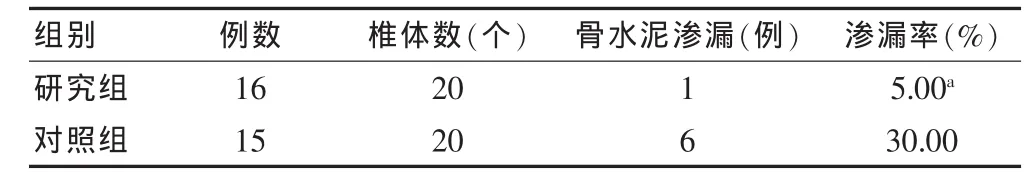
表3 两组术中骨水泥渗漏情况比较
3 讨论
老年骨质疏松导致的椎体压缩骨折,是临床中常见的疾病,其治疗分为保守治疗和手术治疗。保守治疗过去以卧床休息或口服止痛药物等为主,但长时间卧床可发生机体抵抗力下降及脏器功能障碍,易出现肺部、泌尿系感染、褥疮、血栓形成等并发症死亡概率高,还可导致骨质的大量丢失,致使疼痛加重[7]。此外,激素疗法、口服用钙剂等短期镇痛效果差,需长期服用才有一定效果。手术治疗以前的方法是采用各种内固定及减压来增强脊柱稳定性及恢复椎体高度为目的,但该手术创伤大,存在一定的手术风险,术后并发症多,直接影响患者的生活及生存质量。近年来,PKP技术的发展,使这一技术广泛的应用于临床,也取得了满意的疗效,获得同行的认可。尽管该术式缓解疼痛机制尚不清楚,但力学上稳定受累椎体似乎最有可能是缓解疼痛的机制[8]。研究表明经皮椎体后凸成形术不仅能很好地缓解患者的疼痛症状,还能将压缩的骨折椎体复位到一定的高度,矫正后凸畸形,而且其手术并发症少,比传统的经皮椎体成形术具有明显的优势[9]。PKP及PVP是在影像设备的监视下,利用微创技术将骨水泥等生物材料经皮肤及椎弓注入椎体,恢复椎体高度,增加病变椎体强度,防止椎体进一步塌陷和再骨折[10],解除疼痛并改善躯体功能[11]。1984年法国介入放射学家首先应用于椎体血管瘤的治疗[12],随后这类技术开始应用于骨质疏松椎体压缩骨折、椎体转移肿瘤等的治疗[13]。PKP技术是在PVP的基础上的一种可扩张的球囊,经皮经椎弓根将球囊置入椎体,加压球囊膨胀使椎体复位,并在椎体内形成空腔,填充骨水泥,矫正后突畸形,缓解疼痛,维持椎体稳定性,恢复椎体的高度,并且避免了骨水泥渗漏等并发症[14],临床效果满意。
[1]Alexandru D,So W.Evaluation and management of vertebral compression fractures[J].Perm J,2012,16(4):46-51.
[2]Galovich LA,Perez-Higueras A,Altonaga JR,et al.Biomechanical,histological and histomorphometric analyses of calcium phosphate cement compared to PMMA for vertebral augmentation in a validated animal model [J].Eur Spine J,2011,20(3):376-382.
[3]Marlin E,Nathoo N,Mendel E.Use of percutaneous kyphoplasty and vertebroplasty in spinal surgery[J].J Neurosurg Sci,2012,56(2):105-112.
[4]Smith ZA,Yang I,Gorgulho A,et al.Emerging techniques in the minimally invasive treatment and management of thoracic spine tumors[J].J Neurooncol,2012,107(3):443-455.
[5]Taylor RS,Taylor RJ,Fritzell P,et al.Balloon kyphoplasty and vertebroplasty for vertebral compression fractures:a comparative systematic review of efficacy and safety[J].Spine,2006,31:2747-2755
[6]龚泽辉,龙宝珠,夏樱丹,等.Mckenzie疗法用于腰椎间盘突出症患者的疗效观察[J].中国康复医学杂志,2012,27(6):562-563.
[7]杨丰建,林伟龙,朱炯,等.经皮椎体成形术和经皮椎体后凸成形术治疗骨质疏松性椎体压缩骨折[J].中国脊柱脊髓杂志,2011,21(1):50-54.
[8]Wink M,Stahl JP,Oertel M,et al.Treatment of pain from osteoporotic verbral collapse by percutaneous PMMA vertebroplasty[J].Acta Neurochir(Wien),2004,146(5):469-476.
[9]项良碧,周大鹏,田竟,等.椎体成形术在骨质疏松性椎体骨折治疗中的应用[J].安徽医学,2008,14(1):95-102.
[10]Perry A,Mahar A,Massie J,et al.Biomechanical evaluation of kyphoplasty with calcium sulfate cement in a cadaveric ostepoprotic vertebral compression fracture model[J].Spine J,2005,5(5):489-493.
[11]张友,冯世龙,熊小江,等.椎弓根螺钉内固定结合自固化硫酸钙灌注治疗胸腰椎骨折28例[J].第三军医大学学报,2009,31(10):987-989.
[12]刘锐,贾思明,张培勋.经皮椎体成形术治疗脊柱转移癌[J].中国骨与关节损伤杂志,2005,20(2):91-92.
[13]程军,关群,熊小江,等.椎弓根系统固定结合椎体成形术治疗胸腰椎骨折[J].中国骨与关节损伤杂志,2012,27(11):1016-1017.
[14]Kassamali RH,Ganeshan A,Hoey ET,et al.Pain management in spinal metastases:the role of percutaneous vertebral augmentation[J].Ann Oncol,2011,22(4):782-786.

