气管内滴入核仁素shRNA表达载体对脂多糖肺损伤大鼠肺泡巨噬细胞活化的影响
王 艺 徐剑铖 毛 梅 李秋梅 田 静 苏 磊
肺泡巨噬细胞(alveolar macrophages,AM))是肺部炎症反应的主要始动细胞,也是脂多糖(lipopolysacharide,LPS)的主要效应细胞,其表面表达有多种模式识别受体可以识别结合LPS,启动跨膜和细胞内信号传导,引起多种炎症介质和细胞因子如肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-6(interleukin-6,IL-6)的释放,从而导致过度炎症反应和急性肺损伤(acute lung injury,ALI)[1-3]。核仁素(nucleolin,由C23基因编码)是真核细胞核仁中含量最丰富的一种蛋白质,它是一种穿梭蛋白,可以自由穿梭于细胞核、细胞浆和细胞膜之间,具有多种生物学功能,参与了细胞周期的调节,并在病原微生物的感染和自身免疫系统疾病中也发挥一定的作用[4]。目前大量研究表明核仁素在单核-巨噬细胞系统膜表面广泛分布并且参与了LPS所致炎症反应[5-8]。我们前期的研究发现正常大鼠AM膜表面表达有核仁素,体外实验证实其参与了LPS的内化及对AM的激活,它可能是LPS的一种新的膜识别受体[9]。
本实验拟在体应用RNA干扰(RNA interference,RNAi)技术,通过气管滴入的方法转染针对核仁素的shRNA表达载体,干扰大鼠AM膜核仁素的表达,观察其对LPS所致ALI大鼠的保护作用,为阐明AM膜核仁素在LPS诱导ALI中的作用及机制提供实验依据。
材料与方法
一、试剂和动物
成年清洁级SD大鼠,体质量(200±20)g,购自第三军医大学实验动物中心。重组质粒pBS-U6.C23shRNA及对照质粒pBS-U6.ControlshRNA由美国Ambion公司合成,jetPEITM转染试剂购自法国Polyplus-transfection公司,LPS(E coli O55:B5)购自美国Sigma Invitrogen公司,大鼠TNF-α和IL-6 ELISA试剂盒购自晶美生物科技公司,抗鼠C23抗体、抗NF-κBp65抗体及PVDF膜购自SantaCruz公司,蛋白定量BCA法试剂盒和细胞膜、细胞核蛋白提取试剂盒均为碧云天生物技术公司产品。
二、实验动物分组
健康雄性SD大鼠40只,随机分为A组(空白对照组),B组(ALI组),C组(转染重组质粒pBS-U6.C23shRNA并ALI组),D组(转染对照质粒pBS-U6.ControlshRNA并ALI组),每组10只动物。
三、气管内滴注转染重组质粒
将100 μg的重组质粒pBS-U6.C23shRNA溶于300 μl的生理盐水中,将200 μg的jetPEITM 溶于300 μl生理盐水中,将二者混合迅速振荡混匀溶液(共600 μl),室温下孵育20 min后抽入无菌1 ml注射器,待转染。C组大鼠经2%戊巴比妥钠(40 mg/kg)腹腔注射麻醉后,仰卧位固定于鼠板上,消毒切开颈部皮肤,钝性分离出气管,将装有质粒DNA 1ml的注射器经两气管软骨环间隙穿刺进入气管,回抽无阻力并有空气则证明在气管内,将转染液体缓慢推入。推注完毕后,拔出注射器,立即将鼠板直立旋转,使气管内的液体均匀分布至两肺,最后消毒缝合切口,等待复苏。苏醒后的大鼠继续饲养待建立LPS致ALI的动物模型。同法,将D组大鼠经气管内滴入转染对照质粒pBS-U6.ControlshRNA 100 μg。
四、LPS致ALI模型建立
转染48 h后,B、C、D组大鼠经尾静脉缓慢注射LPS(E coli O55:B5)5 mg/kg,A组大鼠经尾静脉缓慢注射生理盐水,15 min注射完毕。观察大鼠自主呼吸,实验在注射LPS 4 h后结束。
五、观察指标及方法
各组动物致伤后4 h,做如下实验:①ELISA测定大鼠肺泡灌洗液(bronchoalveolar lavage fluid,BALF)中TNF-α及IL-6的含量:无菌条件下收集BALF,按TNF-α及IL-6 ELISA检测试剂盒说明书操作检测BALF中TNF-α及IL-6蛋白的浓度,用酶标仪在450 nm处测吸光值;②Western blot检测AM膜核仁素蛋白表达:BALF离心沉淀用膜蛋白提取试剂提取AM膜蛋白,用BCA法测定蛋白浓度,后分别加入5×SDS上样缓冲液,沸水煮5 min,离心后取上清液上样进行聚丙烯凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE),电转将蛋白条带转移到PVDF膜上,用含50 g/L脱脂奶粉的封闭液封闭2 h,一抗(兔抗大鼠C23多克隆抗体,稀释度1︰500)4 ℃孵育过夜,二抗(羊抗兔IgG/HRP,稀释度1︰1000)37 ℃孵育1 h,洗膜后用化学发光试剂显色;③EMSA检测NF-κB活性:提取大鼠AM核蛋白,将核提取物、生物素标记特异性探针和结合反应液等混合制成结合反应体系,聚丙烯酰胺凝胶电泳后转膜、化学发光反应,应用Quantity One图像分析软件测定各条带积分光密度值表示核提取物中NF-KB的活性,同时进行特异性与非特异性竞争试验;④左下肺组织固定后石蜡包埋,切片,HE染色,光镜观察。
五、统计学方法
结 果
一、肺组织病理学观察
大鼠肺组织病理变化,见图1。A组肺泡腔结构、完整,无明显病理变化,组间无显著差异;B组肺泡结构破坏明显,部分肺泡腔变小,肺泡间隔增厚,间质增生,可见较多的炎性细胞浸润;C组肺泡结构仍有破坏,但较B组损伤有减轻,部分肺泡壁增厚,肺间质增生减轻,浸润的炎性细胞减少,与B组相比炎症有减轻;而D组与B组病理变化无明显差异。

注:A:对照组; B:LPS处理组;C:LPS+pBS-U6.C23 shRNA组;D:LPS+pBS-U6.ControlshRNA组
二、AM膜核仁素蛋白表达
经LPS处理后,B组及D组的大鼠AM膜核仁素蛋白表达显著增加,与A组相比,组间有统计学意义(P<0.01);C组大鼠AM膜核仁素蛋白表达明显下调,与B组相比,组间差异有统计学意义(P<0.01);而D组与B组中的大鼠AM膜核仁素蛋白表达组间差异无统计意义(P>0.05),见图2。
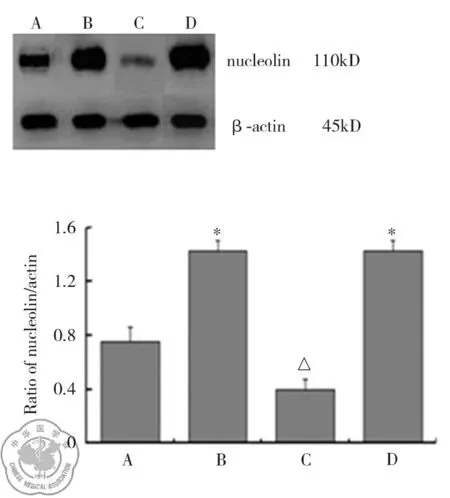
注:A:对照组; B:LPS处理组; C:LPS+pBS-U6.C23shRNA组;D:LPS+pBS-U6.ControlshRNA组;﹡P<0.01与对照组比较;△P<0.01 与LPS组比较
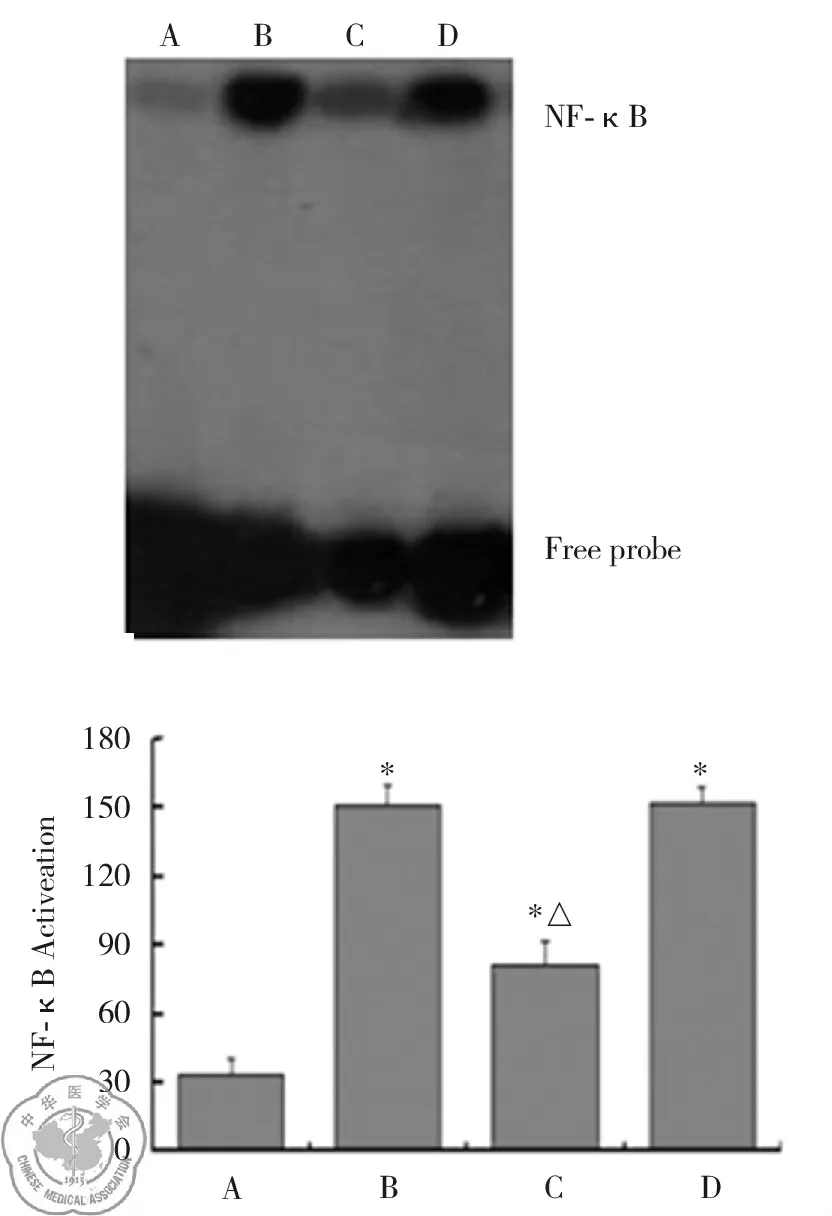
三、AM中NF-κB活性变化
对照组大鼠AM中NF-κB活性较弱,经LPS处理后,各组大鼠AM中NF-κB活性显著增加,与A组相比,组间差异非常明显(P<0.01)。C组大鼠AM中NF-κB活性明显降低,与B组比较,差异显著(P<0.05);而D组与B组比较,组间无明显差异(P>0.05),见图3。
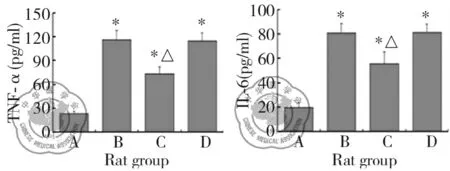
四、BALF中TNF-α 和IL-6的含量
经LPS诱导肺损伤后,显著增加了大鼠BALF中促炎因子TNF-α 和IL-6的表达,各组和A组相比差异显著(P<0.01);C组大鼠BALF中TNF-α 和IL-6的含量显著降低,与B组相比差异显著(P<0.01);而D组与B组相比,组间差异无统计学意义(P>0.05),见图4。
注:A:对照组;B:LPS处理组;C:LPS+pBS-U6.C23shRNA组;D:LPS+pBS-U6.ControlshRNA组;﹡P<0.01 与对照组比较;△P<0.05 与LPS组比较
注:A:对照组;B:LPS处理组;C:LPS+pBS-U6.C23shRNA组;D:LPS+pBS-U6.ControlshRNA组;﹡P<0.01 与对照组比较;△P<0.01 与LPS组比较
讨 论
AM是肺先天免疫系统中的前卫细胞,是接触抗原最早、机会最多的细胞,也是LPS的靶细胞。其表面多种膜受体和膜分子如CD14、Toll样受体(Toll-like receptor,TLR)、β2整合素(CD11/CD18)以及甘露糖受体(mannose receptor,CD206)等均参与了LPS的识别及信号传导,但阻断这些受体并不能完全抑制炎症因子的释放和减轻肺损伤,提示还有其他膜受体存在的可能性;并且LPS还可能与某些膜受体结合并被转运入细胞内,直接激活细胞内的信号传导[10]。因此,进一步明确LPS的膜结合受体及信号传导机制,有利于阐明LPS致ALI的发病机制及寻找新的治疗靶点。
核仁素以磷酸化的形式存在于细胞膜表面,已知它在单核-巨噬细胞膜表面有表达并且具有与糖蛋白中的多糖链结合的特性[11-14],依据这一特性同时由于LPS分子结构中含有O-侧链多糖,有学者提出单核巨噬细胞膜核仁素可能识别LPS而参与LPS所致炎症反应的假说。方立等[5]发现核仁素存在于人外周血单核细胞(THP-1)膜表面,抗核仁素抗体可以显著抑制LPS诱导的早期炎症介质TNF-α、IL-1β的表达与分泌。在内毒素血症小鼠的肺组织和RAW264.7 细胞炎症模型中,相对分子量为110×103的核仁素表达上调,相对分子量为80×103的核仁素片段表达减少,在核仁素过表达组LPS所致的IL -1β释放明显增加;而在核仁素低表达组LPS所致的IL -1β释放明显减少[6]。近来研究发现革兰氏阴性菌感染人THP-1单核细胞时伴有核仁素表达上调;LPS诱导小鼠RAW264.7巨噬细胞活化时伴有核仁素裂解片段的表达下调[7-8]。我们前期的实验发现大鼠AM膜核仁素在LPS的识别和信号传导过程中发挥重要作用,但其具体的结合机制和信号传导机制尚未明确[9]。
由于AM膜核仁素分子处于LPS信号识别和转导的上游环节,如果能减少膜核仁分子表达和或抑制膜核仁分子的生物学作用,则有可能从上游环节入手来阻断信号转导途径,避免产生过度的炎症反应,从而在LPS所致的ALI发病早期开展有效的抗炎治疗。我们采用RNA干扰技术,来沉默目的基因。基于ALI的器官特异性,我们选择了气管内滴入的方法转染pBS -U6C23shRNA质粒。实验结果证实了jetPEITM体内转染shRNA的高效性和安全性,与对照组相比,BALF中AM膜核仁素蛋白表达明显下降,干扰效率达到72%同时也说明通过气道转染的方法是安全可行的。实验中我们对比分析了各组大鼠BALF中的TNF-α和IL-6的蛋白水平,发现预先给予气管内转染pBS-U6C23shRNA质粒后,BALF中的TNF-α和IL-6蛋白表达水平均明显降低,NF-κB的活性也明显下降,进一步在体内实验中证实了RNA干扰对膜核仁素介导的LPS信号传导具有明显的阻断作用。其次,我们还发现气管内滴入的方法转染pBS-U6C23shRNA质粒后,一定程度上可以改善、缓解肺的病理损伤,说明核仁素RNA干扰在一定程度上减轻了肺损伤,减轻了肺部炎症,提示AM膜核仁素在LPS诱导的大鼠ALI的发病过程中起到一定作用。RNA干扰可以通过抑制AM膜核仁素表达,减少LPS内化入AM,降低NF-κB活性,减少分泌TNF-α和IL-6炎症因子,减轻肺损伤,因此,沉默核仁素基因有望成为防治LPS所致ALI的有效手段之一。
沉默核仁素基因可通过阻断AM信号通路来减轻炎症反应,从而可能对LPS所致的ALI起到保护作用。但由于本研究以实验动物作为载体,具有一定的局限性,尚需进一步的临床实验为防治LPS所致的ALI提供更有力的实验依据。
参 考 文 献
1 Tsushima K,King LS,Aggarwal NR,et al. Acute lung injury review[J]. Intern Med,2009,48(9): 621-630.
2 刘 涛,任成山. 炎症介质在急性肺损伤/急性呼吸窘迫综合征发病机制中的作用[J/CD]. 中华肺部疾病杂志:电子版,2013,6(3):265-269.
3 陈向军,马李杰,侯绍杰,等. 白藜芦醇对脂多糖诱导的急性肺损伤的保护作用[J/CD]. 中华肺部疾病杂志:电子版,2013,6(1):20-24.
4 Bartova E,Horakova AH,Uhlirova R,et al. Structure and epigenetics of nucleoli in comparison with non-nucleolar compartments[J]. J Histochem Cytochem,2010,58(5): 391-403.
5 方 立,王慷慨,蒋 磊,等. 膜表面核仁素对脂多糖所致TNF-α和IL-1β表达的影响[J]. 中南大学学报(医学版),2008,33(11): 999-1004.
6 张 彬,肖献忠,张文辉,等. 核仁素对LPS 诱导的白细胞介素1β释放的影响[J]. 中国病理生理杂志,2010,26(9): 1796-1800.
7 Saba JA,McComb ME,Potts DL,et al. Proteomic mapping of stimulus-specific signaling pathways involved in THP-1 cells exposed to Porphyromonas gingivalis or its purified components[J]. J Proteome Res,2007,6(6): 2211-2221.
8 Zhang X,Kuramitsu Y,Fujimoto M,et al. Proteomic analysis of macrophages stimulated by lipopolysaccharide: Lipopolysaccharide inhibits the cleavage of nucleophosmin[J]. Electrophoresis,2006,27(8): 1659-1668.
9 Wang Yi,Mao Mei,Xua Jian-cheng. Cell-surface Nucleolin is involved in Lipopolysaccharide internalization and signaling in alveolar macrophages[J]. Cell biology international,2011,35(7): 677-685.
10 Wang Yanyan,Yang Yang,Liu Xin,et al. Inhibition of clathrin/dynamin-dependent internalization interferes with LPS-mediated TRAM-TRIF-dependent signaling pathway[J]. Cell Immunol,2012,274(1-2): 121-129.
11 Hirano K,Miki Y,Hirai Y,et al. A multifunctional shuttling protein nucleolin is a macrophage receptor for apoptotic cells[J]. J Biol Chem ,2005,280(47): 39284-39293.
12 Miki Y,Tazawa T,Hirano K,et al.Clearance of oxidized erythrocytes by macrophages: involvement of caspases in the generation of clearance signal at band 3 glycoprotein[J]. Biochem Biophys Res Commun ,2007,363(1): 57-62.
13 Krantz S,Salazar R,Brandt R,et al. Purification and partial amino acid sequencing of a fructosyllysine-specific binding protein from cell membranes of the monocyte-like cell line U937[J]. Biochim Biophys Acta,1995,1266(1): 109-112.
14 Semenkovich CF,Ostlund RE Jr,Olson MO,et al. A protein partially expressed on the surface of HepG2 cells that binds lipoproteins specifically is nucleolin[J]. Biochemistry,1990,29(41): 9708-9713.
——一道江苏高考题的奥秘解读和拓展

