培美曲塞联合铂类一线治疗晚期非鳞非小细胞肺癌的临床观察
韡旻
上海交通大学附属胸科医院呼吸内科,上海 200030
培美曲塞联合铂类一线治疗晚期非鳞非小细胞肺癌的临床观察
陈文怡 王韡旻姜丽岩 施春雷 熊丽纹 储天晴 裴俊 顾爱琴
上海交通大学附属胸科医院呼吸内科,上海 200030
背景与目的:晚期肺癌一线化疗有效率仅30%~40%,本研究旨在探讨培美曲塞联合铂类药物(卡铂或顺铂)治疗晚期非鳞非小细胞肺癌(non-small cell lung cancer,NSCLC)的疗效及不良反应。方法:121例非鳞NSCLC患者,给予培美曲塞联合铂类化疗:培美曲塞500 mg/m2第1天,静脉滴注,卡铂300 mg/ m2,第1天,静脉滴注,每3周重复;或培美曲塞500 mg/m2,第1天,静脉滴注,顺铂70 mg/m2,第1天,静脉滴注,每3周重复。上述方案连用2~6个周期,至少2个周期评价疗效。主要观察终点是疾病控制率(disease control rate,DCR),其次是中位无进展生存时间(progression-free survival,PFS)、1年生存率和安全性。结果:全组可评价疗效121例,完全缓解(complete response,CR)1例,部分缓解(partial response,PR)44例,病情稳定(stable disease,SD)50例,疾病进展(progressive disease,PD)26例,客观有效率(objective response rate,ORR)为37.2%(45/121),DCR为78.5%(95/121),PFS为5.2个月(95%CI:4.4~6.0个月),1年生存率为59.0%。其中培美曲塞联合卡铂组ORR为38.3%(23/60),DCR为78.3%(47/60),PFS为5.1个月(95%CI:3.8~6.4个月),1年生存率55.2%;培美曲塞联合顺铂组ORR为36.1%(22/61),DCR为78.7%(48/61),PFS为6.2个月(95%CI:4.3~8.1个月),1年生存率为62.5%。两组之间的ORR、DCR、PFS和1年生存率差异无统计学意义(P>0.05)。主要不良反应为中性粒细胞和白细胞下降、乏力及胃肠道反应。结论:培美曲塞联合铂类药物一线治疗晚期非鳞NSCLC疗效确切,不良反应发生率低,耐受性较好。
培美曲塞;卡铂;顺铂;一线治疗;晚期非小细胞肺癌
支气管肺癌在我国最常见恶性肿瘤之一,其发病率逐年升高,死亡率己占各种癌症疾病之首。其中75%~80%的患者是非小细胞肺癌(non-small cell lung cancer,NSCLC),其中超过70%的患者在确诊时已经属于不适合手术切除的晚期患者[1]。晚期NSCLC患者治疗目前主要以铂类为基础的两药联合化疗方案[2]。培美曲塞作为一种新型多靶点抗叶酸药物,2008年9月美国FDA批准用于晚期非鳞NSCLC的一线治疗[3]。本研究回顾总结了2010年8月—2012年8月应用培美曲塞联合卡铂或顺铂治疗121例晚期非鳞NSCLC患者,现将结果报告如下。
1 资料和方法
1.1 一般资料
晚期非鳞NSCLC患者121例,男性61例,女性60例,年龄33~76岁,中位年龄59岁,ECOG评分0分13例,1分107例,2分1例,病理类型为腺癌113例,大细胞癌8例,ⅢB期23例,Ⅳ期98例。所有患者均经过病理学或细胞学证实;均有可测量的病灶,既往未接受任何化疗和放疗,均为初治患者且治疗前无化疗禁忌证。培美曲塞联合卡铂和培美曲塞联合顺铂之间基线资料比较差异无统计学意义(P>0.05,表1)。化疗期间血常规每周2次化验,每个化疗周期前给予肝肾功能、心电图检测,每2个周期行胸部CT扫描进行评价。
1.2 治疗方法
培美曲塞联合铂类(卡铂或顺铂)化疗:培美曲塞500 mg/m2,第1天,静脉滴注10 min,卡铂300 mg/m2或顺铂70 mg/m2,第1天,静脉滴注,每3周为1个周期。用药前一周开始给予口服含叶酸制剂400 μg/d,持续到治疗结束,用药前1周给予维生素B12针1 mg肌肉注射;用药前1天、当天和第2天每次口服地塞米松片4.5 mg,每日2次。

表1 培美曲塞联合卡铂/顺铂化疗患者临床一般资料(n=121)Tab. 1 Clinical characteristics of patient with pemetrexed combined with carboplatin/ cisplatin (n=121)
1.3 疗效和不良反应评定标准
疗效按照W H O实体瘤客观疗效评定标准(R E C I S T),分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)和进展(progressive disease,PD)。客观有效率(objective response rate,ORR)为CR+PR患者占全组患者的百分率;疾病控制率(disease control rate,DCR)为CR+PR+SD患者占全组患者的百分率。不良反应根据WHO关于抗癌药物毒性反应评定标准评价,分为0~4级。无进展生存时间(progression free survival,PFS)定义为从化疗开始至疾病进展或任何原因死亡的时间;总生存期(overall survival,OS)定义为从化疗开始至任何原因死亡的时间。随访至2013年8月31日,在随访截止时仍有存活的患者,按最后一次联络的日期计算。
1.4 统计学处理
采用SPSS 16.0统计学软件进行统计处理,组间患者一般情况比较采用χ2检验,生存分析采用Kaplan-Meier法,不同分组之间比较采用Logrank检验。P<0.05为差异有统计学意义。
2 结 果
2.1 临床疗效及生存时间
患者至少接受了2个周期的联合化疗。每完成2个周期的化疗就做疗效评价。4~6个周期后建议患者随访。化疗失败后或进展后部分患者给予了EGFR-TKI分子靶向治疗,部分给予二线化疗。
本研究121例患者中,CR 1例,PR 44例,SD 50例,PD 26例;ORR为37.2%(45/121);DCR为78.5%(95/121)。其中培美曲塞联合卡铂组60例中CR 1例,PR 22例,SD 24例,PD 13例;ORR为38.3%(23/60);DCR为78.3%(47/60)。而培美曲塞联合顺铂组共61例,CR 0例,PR 22例,SD 26例,PD 13例;ORR为36.1%(22/61);DCR为78.7%(48/61)。两组之间的ORR和DCR差异无统计学意义(P>0.05)。全组中位PFS为5.2个月(95%CI:4.4~6.0个月);1年生存率为59.0%。培美曲塞联合卡铂治疗组中位PFS为5.1个月(95%CI:3.8~6.4个月);1年生存率为55.2%。培美曲塞联合顺铂组中位PFS为6.2个月(95%CI:4.3~8.1个月);1年生存率为62.5%。两组PFS和1年生存率之间差异无统计学意义(P>0.05,表2)。

表2 培美曲塞联合铂类治疗非鳞NSCLC疗效比较(n=121)Tab. 2 The ef ficacy comparison of pemetrexed plus platinum in the treatment for non-squamous NSCLC (n=121)
2.2 不良反应
本研究患者共计完成治疗周期520个,中位周期数为4个(2~6个),所有患者至少完成2个周期的治疗。121例患者主要不良反应为骨髓抑制、乏力和胃肠道反应。白细胞减少发生率为29.8%(36/121),3/4级为8.3%(10/121);中性粒细胞减少发生率为36.4%(44/121),3/4级为10.7%(13/121);血小板减少9.1%(11/121), 3/4级为1.7%(2/121);恶心/呕吐发生率为23.1%(28/121),无3/4级发生。乏力发生率为18.2%(22/121)。培美曲塞联合卡铂治疗最常见不良反应是与化疗药物有关的血液学不良反应,3/4级血液学不良反应主要是中性粒细胞减少、白细胞减少和血小板减少。没有观察到因中性粒细胞减少导致发热需要使用抗生素治疗。最常见非血液学不良反应为恶心/呕吐、乏力和厌食。培美曲塞联合顺铂治疗的患者中,最常见化疗相关性3/4级血液学不良反应是中性粒细胞减少,其中4级中性粒细胞减少1例,3级中性粒细胞减少6例。最常见的药物相关性非血液学不良反应为恶心/呕吐,其次是乏力和厌食。两组均没有患者接受输血治疗,也无患者发生化疗相关性死亡。培美曲塞联合卡铂组的血小板减少发生率较培美曲塞联合顺铂组高,差异有统计学意义(χ2=5.028,P=0.03,表3)。
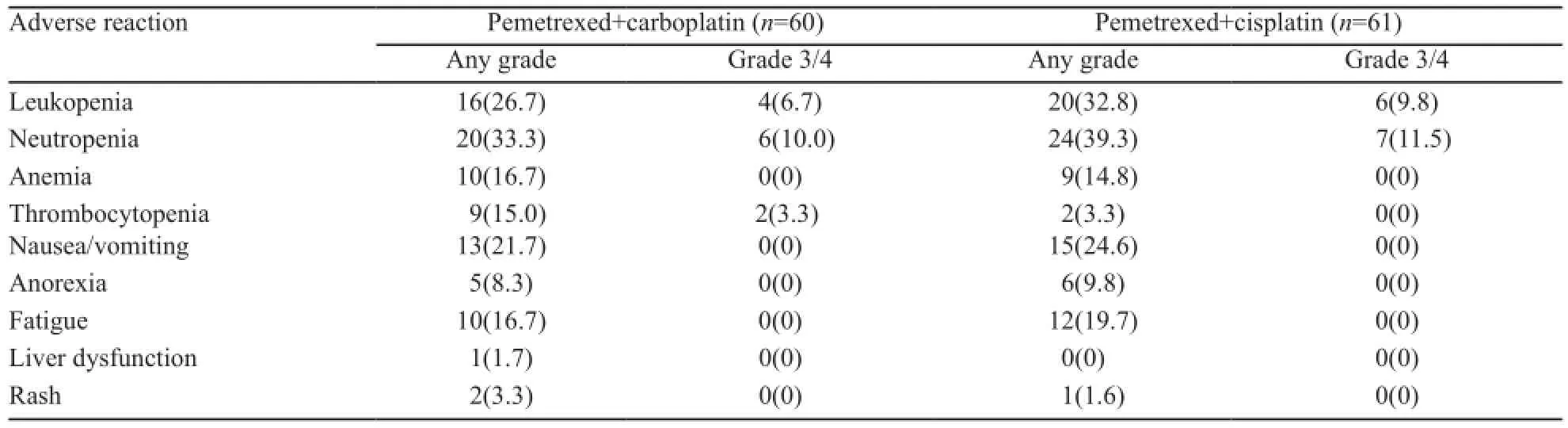
表3 培美曲塞联合铂类治疗非鳞NSCLC不良反应[n(%)]Tab. 3 The adverse effect of pemetrexed combined with platinum in the treatment for nonsquamous NSCLC
3 讨 论
培美曲塞是基于经典的抗代谢类药甲氨蝶呤和5-FU基础上研制的新一代抗代谢药,属于细胞周期特异性抗代谢药物,主要通过干扰细胞复制过程中叶酸代谢途径而发挥抗肿瘤作用。药物研究显示,培美曲塞能明显抑制胸苷酸合成酶、二氢叶酸还原酶和甘氨酰胺核苷甲酰基转移酶的活性,它们均为重要的叶酸依赖性辅酶,培美曲塞正是通过对这3个关键酶活性进行多靶点抑制,使得嘌呤和胸腺嘧啶核苷生物合成减少,进而抑制肿瘤细胞DNA的合成,特别是使肿瘤细胞停滞于DNA合成期(S期),促进肿瘤细胞凋亡,达到抗肿瘤的作用[4]。铂类是一种重金属化疗药物,属细胞周期非特异性药物,具有细胞毒性,可抑制癌细胞的DNA复制过程,并损伤其细胞膜上结构,有较强的广谱抗癌作用,是晚期NSCLC的一线联合化疗的基础药物[5]。Hanna等[6]进行的一项大规模、随机、对照Ⅲ期临床研究结果显示,单药培美曲塞与多西他赛二线治疗NSCLC后对比,无论有效率(9.1% vs 8.8%)、中位生存期(8.3个月 vs 7.9个月)还是1年生存率(29.7% vs 29.7%)差异均无统计学意义,但是中性粒细胞下降(5.3% vs 40.2%)、粒细胞缺少性发热(1.9% vs 12.7%)及脱发(6.4% vs 37.7%)等药物性不良反应在培美曲塞组显著降低。Scagliotti等[7]报告了一项Ⅲ期临床研究,共1 725例初治的ⅢB期或Ⅳ期NSCLC患者随机入组,分别接受培美曲塞联合顺铂和吉西他滨联合顺铂治疗。研究结果表明,培美曲塞联合顺铂近期疗效及生存期不差于吉西他滨联合顺铂,而前者3/4级血液学不良反应发生率较低。但病理亚组分析表明腺癌及大细胞癌患者接受培美曲塞联合顺铂其生存期优于吉西他滨联合顺铂。2008年9月30日美国食品和药物管理局(Food and Drug Administration,FDA)和批准培美曲塞联合顺铂作为局部晚期或转移性非鳞NSCLC的一线治疗方案。
顺铂是第一代铂类药物,需要水化,胃肠道反应较大;而卡铂是第二代铂类药物,不需要水化,胃肠道反应较小。本研究选择应用的卡铂、顺铂的剂量是标准的治疗剂量范围,临床根据患者的年龄、全身状况及合并症来决定应用卡铂还是顺铂。本研究全组患者ORR为37.2%,DCR为78.5%,中位PFS为5.2个月(95% CI:4.4~6.0个月),1年生存率为59.0%(95% CI:50.0%~68.0%)。化疗血液不良反应主要是3/4级中性粒细胞减少,没有因中性粒细胞减少引起发热和严重感染,给予粒细胞集落刺激因子治疗后都能恢复正常;非血液不良反应主要表现为1/2级胃肠道反应和乏力,与国内外文献报道基本相近,显示了培美曲塞对非鳞NSCLC有良好的临床获益率和较低的不良反应,改善了患者生活质量[8]。
本研究结果显示培美曲塞联合卡铂化疗,ORR为38.3%,DCR为78.3%;中位PFS为5.1个月(95%CI:3.8~6.4个月),1年生存率为55.2%。而培美曲塞联合顺铂化疗,ORR为36.1%,DCR为78.7%;中位PFS为6.2个月(95%CI:4.3~8.1个月),1年生存率为62.5%。两种含铂化疗方案ORR和1年生存率差异无统计学意义(P>0.05)。卡铂组血小板减少发生率高于顺铂组,差异有统计学意义(P<0.05),而非血液不良反应方面,卡铂和顺铂两者差异无统计学意义(P>0.05)。全组无肾功能损害和治疗相关性死亡。
综上所述,培美曲塞联合卡铂和(或)顺铂一线治疗晚期非鳞NSCLC可以获得较好的临床疗效,不良反应较轻,患者耐受性较好,值得在临床上推广应用。
[1] FERLAY J, SHIN H R, BRAY F, et al. Estimates of worldwide burden of cancer in 2008: GLOBOCAN 2008[J]. Int J Cancer, 2010, 127: 2893-2917.
[2] AZZOLI C G, BARKER S J R, TEMIN S, et al. American Society of Clinical Oncology Clinical Practice guideline update on chemotherapy for stage Ⅳ non-small-cell lung cancer[J]. J Clin Oncol, 2009, 27: 6251-6266.
[3] ZINNER R G, FOSSELLA F V, GLADISH G W, et al. PhaseⅡ study of pemetrexed in combination with carboplatin in the first-line treatment of advanced non-small cell lung cancer[J]. Cancer, 2005, 104: 2449-2456.
[4] JONES R J, TWELVES C J. Pemetrexed: a multitargeted antifolate (ALIMTA), LY-231514)[J]. Expert Rev Anticancer Ther, 2002, 2(1): 13-22.
[5] DELBALDO C, MICHIELS S, SYZ N, et al. Benefits of adding a drug to a single-agent or a 2-agent chemotherapy regimen in advanced non-small-cell lung cancer: a meta-analysis [J]. JAMA, 2004, 292: 470-484.
[6] HANNA N, SHEPHERD F A, FOSSELLA F V, et al. Randomized phase Ⅲ trial of pemetrxed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy[J]. J Clin Oncol, 2004, 22(9): 1589-1597.
[7] SCAGLIOTTI G V, PARIKH P, VOL PAWEL J, et al. Phase Ⅲ study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced stage non-small cell lung cancer[J]. J Clin Oncol, 2008, 26(21): 3543-3551.
[8] SCAGLIOTTI G V, PARK K, PATIL S, et al. Survival without toxicity for cisplatin plus pemetrexed versus cisplatin plus gemcitabine in chemonaive patients with advanced non-small cell lung cancer: a risk-benefit analysis of a large phase Ⅲstudy[J]. Euro J Cancer, 2009, 13: 2298-2303.
Clinical observation of efficacy and safety of pemetrexed plus platinum as the first-line chemotherapy with advanced non-squamous non-small cell lung cancer
CHEN Wen-yi, WANG Wei-min, JIANG
Li-yan, SHI Chun-lei, XIONG Li-wen, CHU Tian-qing, PEI Jun, GU Ai-qin
(Department of Respiratory Medicine, Shanghai Chest Hospital Af filiated to Shanghai Jiao Tong University, Shanghai 200030, China)
GU Ai-qin E-mail: guaiqin11@126.com
Background and purpose: The effective rate of first-line chemotherapy for advanced lung cancer is 30%-40%. The purpose of this study was to evaluate the ef ficacy and adverse effects of pemetrexed combined with carboplatin or cisplatin in the treatment of patients with advanced non-squamous non-small cell lung cancer (NSCLC). Methods: One hundrend and twenty-one patients with advanced non-squamous NSCLC were enrolled in this study and all of these patients had been con firmed with pathology or cytology. Among the 121 cases, 60 cases were male and 61 were female, the median age was 59 years, adnenocarcinoma in 113 patients and large cell carcinoma in 8 patients. Combination regimen: patients received pemetrexed 500 mg/m2on day 1 and carboplatin 300 mg/m2or cisplatin 70 mg/m2on day 1 by intravenous infusion, administrated every 3 weeks for 2 to 6 cycles. All patients who received 2 or more cycles could be evaluated. Disease control rate (DCR) was the primary end point; secondary end points included progression-free survival (PFS), 1-year survival rate and safety. Results: There was 1 case with complete response (CR), 44 cases achieved partial response (PR), 50 had stable disease (SD) and 26 cases had progressive disease (PD) in the overall cases. ORR and DCR were 37.2% (45/121) and 78.5% (95/121), respectively. The median PFS time was 5.2 months and 1-year survival rate was 59.0%. In pemetrexed combined with carboplatin group, the ORR and DCRwere 38.3% (23/60) and 78.3% (47/60), respectively; The median PFS was 5.1 months (95%CI: 3.8-6.4 month) and 1-year survival rate was 55.2%. The patients treated with pemetrexed plus cisplatin, the ORR and DCR were 36.1% (22/61) and 78.7% (48/61), respectively. Median PFS was 6.2 months (95%CI: 4.3-8.1 month) and 1-year survival rate was 62.5%. There were no statistical differences between carboplatin/pemetrexed and cisplatin/pemetrexed for both ORR, DCR, PFS and 1-year survival rate (P>0.05). The major adverse effects were leukopenia, neutropenia, fatigue and gastrointestinal reaction. Conclusion: Pemetrexed plus platinum chemotherapy could be considered as the firstline treatment option for advanced non-squamous NSCLC patients. Pemetrexed combined with carboplatin/ cisplatin regimen has ef ficacy with mild toxicity and better tolerability.
Pemetrexed; Carboplatin; Cisplatin; First-line chemothrepay; Advanced non–small cell lung cancer
10.3969/j.issn.1007-3969.2014.08.009
R734.2
A
1007-3639(2014)08-0610-05
2014-02-11
2014-06-20)
力比泰®获批晚期非鳞状非小细胞肺癌一线及继续维持治疗
顾爱琴 E-mail:guaiqin11@126.com
2014年6月21日,国家食品药品监督管理总局正式批准力比泰®(注射用培美曲塞二钠)作为局部晚期或转移性非鳞状细胞型非小细胞肺癌一线及继续维持治疗的新适应症。这2项适应症的获批得到多项临床研究数据的支持,其中包括力比泰®在中国的注册临床JMIL以及全球著名的JMDB和PARAMOUNT临床研究。数据显示:力比泰®的一线和继续维持治疗中能显著延长非鳞癌患者的总生存。
同济大学附属上海市肺科医院周彩存教授表示:“新适应症的获批,进一步证明了力比泰®在晚期非小细胞肺癌治疗领域的显著疗效。化疗是治疗晚期非小细胞肺癌的主要手段,而高效低毒的新型化疗药物不仅可使饱受疾病折磨的肺癌患者延长生命,还能提高他们的生存质量。”

