不同分离制备时间对凝血因子Ⅷ含量的影响探讨
尤榕,黄丽红,黄智君
(江西省血液中心,江西南昌330052)
·检验与临床·
不同分离制备时间对凝血因子Ⅷ含量的影响探讨
尤榕,黄丽红,黄智君
(江西省血液中心,江西南昌330052)
目的分析不同分离时间制备新鲜冰冻血浆(FFP)对凝血因子Ⅷ(简称Ⅷ因子)含量的影响。方法按不同分离制备时间(6~8h、9~12h、13~18h)分为3组,对3组新鲜冰冻血浆产品进行凝血因子Ⅷ含量检测。结果3组不同时间分离制备FFP的凝血因子Ⅷ含量采用单因素方差分析,F=35.07,P<0.05,有统计学意义;再进行两两比较,发现第1组vs第2组,P>0.05,无统计学意义;第1组vs第3组和第2组vs第3组,P<0.05,有统计学意义。结论实际采集、制备FFP全过程中,应严格把控各个环节上的关键点,加强对采血、分离制备、速冻的时间和贮存、运输、离心、速冻温度的控制;确保在12h内制备的FFP的凝血因子Ⅷ的质量,既满足临床输注的安全性和有效性,又能满足临床对FFP需求量。
新鲜冰冻血浆;分离制备时间;凝血Ⅷ因子含量
DOI∶10.3969/j.issn.1674-1129.2014.06.033
新鲜冰冻血浆(FFP)中凝血因子Ⅷ是血友病患者缺乏的凝血因子之一,对这种患者的止血凝血,Ⅷ因子具有不可替代的作用。而血液采集、贮存、运输、分离、制备、速冻等过程中各关键点,均会影响凝血Ⅷ因子的含量。
制备新鲜冰冻血浆,使用抗凝剂为CPD、CP2D、CPDA-1的血液应在8h内分离并速冻,而抗凝剂为ACD的血液则在6h内分离并速冻。当血液采集时间200ml>7min,或400ml>13min时,所采集的全血不可用于制备新鲜冰冻血浆。血浆中不稳定的凝血因子Ⅷ在体外半衰期为l2~24h[1],随着保存时间延长其活性逐渐降低,为了确保新鲜冰冻血浆质量、维持凝血因子Ⅷ稳定、提高临床疗效,应尽量缩短新鲜液体血浆在室温的停留时间[2],采集后的血液尽快置于2℃~6℃保存,在运输过程中保持2℃~10℃,离心分离温度控制在2℃~6℃。速冻是保存凝血因子Ⅷ的关键加工步骤,冷冻速率和血浆中心温度是2个关键参数,分离后应在60 min内将血浆中心温度降至-30℃以下快速冻结,在-18℃下保存有效期一年[3]。
FFP中含有全部的凝血因子,特别是不稳定的Ⅴ、Ⅷ因子,Ⅴ、Ⅷ凝血因子在凝血过程中具有极其重要的作用,在FFP制备过程中保护Ⅴ、Ⅷ因子活性,减少其活性损失,对临床血浆输注的效果具有重要意义,而影响V、Ⅷ凝血因子活性的主要因素是温度和时间[4]。在2012颁布新版《GB18469-2012全血及成分血质量要求》及第3版《临床输血》[5]中,FFP定义由原来在全血采集后6h(全血保养液为ACD)或8h(全血保养液为CPD、CPD-1)内,改为最好在6~8h内,但不超过18h分离出血浆并速冻呈固态的成分血。参考国外的相关标准[6],其中规定新鲜冰冻血浆(冷沉淀原料浆)的制备时间最长不宜超过18h。
FFP中不稳定凝血因子(V因子和Ⅷ因子)的含量多少是评价新鲜冰冻血浆质量的关键[7],因此笔者针对在近同等条件下进行采集、运输、分离条件、速冻、储存的血液,但在不同时间段进行分离制备FFP,检测其凝血因子Ⅷ含量,进行统计学分析,现报告如下。
1 材料与方法
1.1 对象及分组样本为2012年7月至2014年8月间自愿无偿献血者血液标本,全部采用抗凝剂CPDA-1配方,按不同时间段制备FFP样本共183份,分为3组,第1组:6~8h内分离制备,共94份样本;第2组:9~12h内分离制备,共42份样本;第3组:13~18h小时分离制备,共47份样本。
1.2 仪器与试剂仪器:为日本SYSMEX公司生产的CA-500全自动血凝分析仪;深圳普特公司产的LWS-3100W型低温工作台,Dometic公司生产的MBF21血浆速冻机,三洋低温冰箱。配套试剂:Ⅷ因子试剂、APTT试剂、氯化钙CaCl2试剂,均在有效期内使用。
1.3 方法按照《GB18469-2012全血及成分血质量要求》,FFP中凝血因子Ⅷ含量≥0.7IU/ml,对3组样本进行凝血因子Ⅷ含量检测。
1.4 统计学方法计量数据采用x±s表示,对三组Ⅷ因子含量进行单因素方差分析,进行两两比较,P<0.05为有统计学意义。
2 结果
不同分离制备时间对凝血因子Ⅷ含量的影响:在不同时间分离得到FFP的凝血Ⅷ因子含量,结果显示(见表1),采用单因素方差分析,F=35.07,P<0.05有差别,后进行两两比较,得出第1组vs第2组,P>0.05,无统计学差异,第1组vs第3组和第2组vs第3组,均P<0.05,有统计学差异。
表1 不同分离制备时间对Ⅷ因子含量的影响(±s)
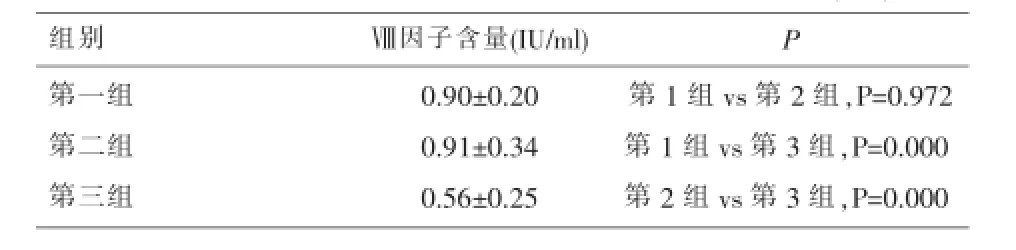
表1 不同分离制备时间对Ⅷ因子含量的影响(±s)
组别Ⅷ因子含量( I U / m l ) P第一组第二组第三组0 . 9 0 ± 0 . 2 0 0 . 9 1 ± 0 . 3 4 0 . 5 6 ± 0 . 2 5第1组v s第2组,P = 0 . 9 7 2第1组v s第3组,P = 0 . 0 0 0第2组v s第3组,P = 0 . 0 0 0
3 讨论
FFP含有V因子和Ⅷ因子等凝血因子,保持它们的生物活性,才能满足临床的要求。FFP主要用于治疗凝血因子缺乏引起的出血,是多种凝血因子缺乏性疾病的有效的治疗制品。常用于严重肝病患者、大量输血伴发凝血功能障碍、血浆置换、烧伤、DIC等,所以临床对FFP的需求量较大,根据本中心临床供血数据统计,2012年较2011年增涨8%,2013年较2012年增涨45.22%,但由于原制备时间的限制(6~8h),故原制备量较难满足临床需求。
现各血站在18h内分离制备FFP的凝血因子Ⅷ是否能达到国家标准,目前报道较少。本研究在对南昌地区不同时间段进行分离制备的FFP,按照分离制备时间的不同分为3个时间组(6~8h、9~12h、13~18h),对3组不同时间段凝血Ⅷ因子含量采用单因素方差分析,F=35.07,P<0.05有统计学差异,再进行两两比较,显示第1与第2组间差异无统计学意义,但第3组与第1组、第2组间均差异有统计学意义。分析结果显示,在6~12h内进行分离制备的FFP,其凝血因子Ⅷ含量基本符合国家标准,但13~18h分离制备的FFP的凝血因子Ⅷ含量,只有23.40%达到国家标准。说明当分离制备时间在13~18h,凝血因子Ⅷ受到影响而大部分失活,凝血因子Ⅷ在体外半衰期为8~12h,这是FⅧ:C活性丧失的主要原因[8],l2h后分离的冰冻血浆,不稳定凝血因子(特别是Ⅷ因子)会明显降低,而影响凝血活性[9],考虑FFP中的凝血因子易受血浆储存、运输等条件的影响而失活,从而导致血液疗效的降低[10]。提示在实际采集、制备FFP全过程中,应严格把控各个环节上的关键点,加强冷链对FFP整个制备过程的控制至关重要[11],以及对采血,分离制备、速冻的时间的控制,确保FFP中凝血因子Ⅷ的质量,符合国家标准。
通过对3组不同时间段凝血因子Ⅷ含量的分析研究,笔者认为制备FFP的分离时间可延长至12h,在确保FFP中凝血因子Ⅷ质量的同时,既保障临床输注的有效性和安全性,又满足临床对FFP的大量需求。
[1]杨江存,李芒会,于青,等.新鲜冰冻血浆融化后不同放置时间凝血因子的变化[J].中国输血杂志,2005,18(3)∶211-212.
[2]李锡兰,禹晓彬.探讨影响新鲜冰冻血浆FⅧ∶C的主要因素[J].实验与检验医学,2008,26(5)∶531.
[3]中华人民共和国卫生部.血站技术操作规程[S].2012∶6-10.
[4]赵宏祥,葛健民,程玉根.新鲜冰冻血浆制备凝血因子活性保护的探讨[J].中国现代医生,2007,45(2)∶16-17.
[5]付涌水.临床输血[M].第3版.北京∶人民卫生出版社,2013∶40.
[6]European Committee(Partial Agreement)on Blood Tran sfusion(CDP-TS).Guide to the preparation,use and quality assurance of blood components[S].16th Edition.2010.
[7]叶柱江,刘赴平.不同制备方法对新鲜冰冻血浆中凝血因子Ⅷ活性含量的影响[J].现代检验医学杂志,2009,24(3)∶108.
[8]胡丽华,曹奎杰,陈汉华,等.库存全血凝血因子Ⅷ改变的研究[J].临床血液杂志,2000,13(1)∶21-22.
[9]温秀明,胡劲辉,韦庆文,等.不同保存时间分享的血浆临床疗效研究[J].国际医药卫生导报,2006,12(7)∶19-21.
[10]王清云,陶黎岚.新鲜冰冻血浆中凝血因子检测结果与分析[J].淮海医药,2010,28(5)∶439.
[11]李静旗,张丽,宫本兰.冷链对新鲜冰冻血浆FⅧ活性的影响[J].临床输血与检验,2003,5(3)∶192-193.
R457.1+2,R554.1
A
1674-1129(2014)06-0735-02
2014-08-08;
2014-09-23)

