黑加仑果汁中花色苷的贮藏稳定性
赵玉红,贾琳娜,赵铁楠,高玉梅,张立钢
(1.东北林业大学林学院,黑龙江 哈尔滨 150040;2.林下经济资源研发与利用协同创新中心,黑龙江 哈尔滨 150040;3.东北农业大学食品学院,黑龙江 哈尔滨 150030)
黑加仑果汁中花色苷的贮藏稳定性
赵玉红1,2,贾琳娜1,赵铁楠1,高玉梅1,张立钢3,*
(1.东北林业大学林学院,黑龙江 哈尔滨 150040;2.林下经济资源研发与利用协同创新中心,黑龙江 哈尔滨 150040;3.东北农业大学食品学院,黑龙江 哈尔滨 150030)
以黑加仑果汁为原料,研究不同温度、不同可溶性固形物含量和抗氧化剂(抗坏血酸)存在条件下贮藏过程中果汁花色苷的化学稳定性、降解动力学及颜色变化。结果表明:果汁中花色苷在4 ℃、可溶性固形物含量9°Brix条件下较稳定,随着贮藏温度升高和可溶性固形物含量升高,花色苷残留率越低。贮藏过程中花色苷的降解符合一级反应动力学,反应速率常数k越大,半衰期t1/2越小,活化能Ea越低。添加50 mg/L抗坏血酸使果汁花色苷降解速率常数k明显增大,半衰期t1/2和降解活化能Ea明显减小,因此抗坏血酸对花色苷残留率的减少有促进作用。在贮藏过程中随着时间的推移,花色苷不断的减少,果汁发生褐变,亮度和红色度逐渐降低,黄色度逐渐增加,而且抗坏血酸对贮藏过程中花色苷的颜色变化具有促进作用。
黑加仑果汁;花色苷;化学稳定性;颜色变化;反应动力学
黑加仑,又名黑穗醋栗、黑豆果,为虎耳草目茶藨子科小型灌木,成熟果实为黑色小浆果,其主要种植区分布在黑龙江、吉林、辽宁、新疆等地[1]。黑加仑中总花青素含量为350 mg/100 g鲜果质量,是草莓的8.8 倍[2]。花色苷是花青素与糖以糖苷键结合而成的一类化合物[3],广泛存在于植物的花、果实、茎叶和根的细胞中。花色苷不但是天然食用色素,是国内外公认的替代人工合成食用色素的理想资源,而且具有美容、养颜、降脂、减肥和抗衰老等重要的生理功能[4]。但花色苷稳定性差,研究证明花色苷除受其结构影响外,还易受pH值、温度、光、氧、酶、抗坏血酸、糖及其降解产物、二氧化硫、氨基酸、酚酸、金属离子、加工方法等影响[5-9]。目前对天然花色苷化学结构与花色苷褪色机理的研究还不是很清楚,且稳定性受到多种因素的影响,不同因素作用下花色苷降解动力学也不尽相同,在食品工业中很难加以控制。因此对影响花色苷稳定性的各种因素的协同作用进行系统性的研究,并通过环境因素的协同作用,提高花色苷类色素在食品贮藏加工中的稳定性非常必要。
随着消费者口味需求的变化,越来越多的消费者对浆果果汁饮料情有独钟。在果汁饮料生产过程中,为了方便贮藏和运输,经常将果汁进行浓缩处理,因此,贮藏温度和浓缩后的不同可溶性固形物含量是影响贮藏稳定性的关键因素。虽然不同来源花色苷的热稳定性已受到国内外一些学者的关注,如郭庆启等[10-11]分别研究了树莓果汁和蓝靛果果汁中花色苷在50~80 ℃时的热降解动力学,降解过程符合一级动力学反应,随着温度的升高,活化能Ea和半衰期t1/2显著下降。但对浆果中花色苷尤其是黑加仑花色苷稳定性的研究还只限于分析加热过程中花色苷含量的变化和热降解动力学[12],关于其在不同可溶性固形物条件下,贮藏过程中的稳定性研究未见报道。添加抗氧化剂如抗坏血酸对贮藏过程中黑加仑果汁花色苷的含量变化和降解动力学的研究尚未见报道。果汁颜色是评价保质期和产品质量的重要指标[13],果汁中花色苷在不同条件下其颜色及其深浅也不尽相同,且花色苷是一类不稳定的物质,在生产和贮藏中容易发生化学变化,导致加工和贮藏过程中的颜色劣变,因此监测果汁颜色变化,可从另一侧面反映出其中花色苷稳定性变化,郭松年等[14]对石榴汁花色苷颜色变化进行了探讨,发现其颜色随时间和温度的升高,a值下降,b值上升,而针对黑加仑果汁及其浓缩汁在贮藏过程中颜色变化的研究尚未见报道。
本实验拟对黑加仑果汁在贮藏过程中受贮藏温度、果汁可溶性固形物含量、抗坏血酸影响引起的花色苷含量、降解动力学和颜色变化进行研究,探讨黑加仑果汁适宜的贮藏参数,为黑加仑果汁及其他浆果果汁的贮藏及应用提供理论依据。
1 材料与方法
1.1 材料与试剂
黑加仑冷冻鲜果 黑龙江哈尔滨市本色集团。
盐酸、磷酸氢二钠、磷酸二氢钠、氢氧化钠、醋酸钠、冰乙酸、氯化钾、抗坏血酸均为国产分析纯
1.2 仪器与设备
JA2003分析天平 上海飞科公司;榨汁机 荷兰Philips有限公司;H.H.S电热恒温水浴锅 沈阳莱柏利德有限公司;SZ-4旋转蒸发仪 沈阳莱柏利德有限公司;TDL-5W台式低速离心机 湖南星科科学仪器有限公司;PB-10 pH计 Sartorius仪器(北京)有限公司;TV-1810紫外-可见分光光度计 北京普析通用仪器有限责任公司;YP2001N台秤 上海精密科学仪器有限公司;BCD-215KS电冰箱 Haier有限公司;MQK-92手持式糖量计 上海米青科实业有限公司;ZR700数码相机日本卡西欧公司;密封干燥器 长春百奥生物仪器有限公司;DNP-9052电热恒温培养箱 嘉兴市中新医疗仪器有限公司。
1.3 方法
1.3.1 原料预处理
以黑加仑鲜果为原料,除去腐烂果实,将果实清洗后,进行破碎处理,用打浆机打碎后,过滤得到果汁,果汁用离心机离心,转速为4 000 r/min,离心时间设定5 min,得到原汁[15]。采用手持糖量计测定原汁可溶性固形物含量为9 °Brix、pH计测定原汁pH 2.9。
采用旋转蒸发仪将黑加仑果汁进行浓缩,实验条件下最大浓缩至可溶性固形物含量为40 °Brix,因此将原汁分别浓缩至可溶性固形物含量为20、30、40 °Brix。旋转蒸发的温度设定为45 ℃,真空度为1 Pa。
果汁的酸度pH 2.9,不利于果汁中微生物生长,在浓缩果汁中,一般性细菌难以忍受高含量的糖分和低pH值。一般果汁变质后会呈现混浊、产生酒精和有机酸变化,导致原有风味被破坏或产生一些不愉快的异味。在60 d密封贮藏过程中,感官评价上只出现颜色褐变并未产生浑浊和不愉快异味。
1.3.2 花色苷稳定性的分析
将黑加仑果汁(9 °Brix)和可溶性固形物含量为20、30、40 °Brix浓缩汁分装于容量为10 mL的带盖玻璃瓶中,密封,分别置于4、25、40 ℃条件下避光贮藏,每10 d测量花色苷的含量并记录颜色变化,每个样品平行3 组实验。
分别在黑加仑果汁(9 °Brix)和可溶性固形物含量为20、30、40 °Brix浓缩汁中添加50 mg/L抗坏血酸混合均匀[16],装入10 mL的带盖玻璃瓶中,密封,分别置于4、25、40 ℃条件下避光贮藏,每6 d测量花色苷的含量并记录颜色变化,每个样品平行3 组实验。
1.3.3 花色苷含量的测定
采用pH示差法[12,17],分别移取1 mL样液2 份,分别用pH 1.0、pH 4.5的缓冲液定容至10 mL。置于暗处平衡2 h,以空白样(取1 mL蒸馏水,分别用pH 1.0、pH 4.5的缓冲液定容至10 mL)作对照,用分光光度计分别在520 nm和700 nm波长处测定吸光度,用A700nm来消除样液混浊的影响。按式(1)计算花色苷含量(c)。
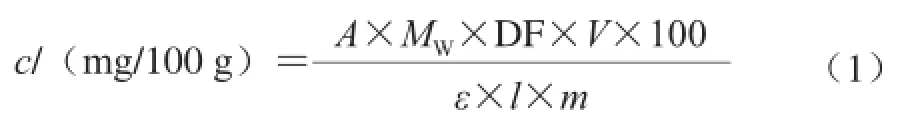
式(1)中:A为吸光度;ε为矢车菊花素-3-葡萄糖苷的消光系数,26 900;DF为稀释因子;MW为矢车菊花素-3-葡萄糖苷的分子摩尔质量,449.2 g/mol;V为最终体积/mL;m为样品质量/mg;l为光程,1cm;A=(A520nmpH 1.0-A700nmpH 1.0)-(A520nmpH 4.5-A700nmpH 4.5)。
1.3.4 反应动力学研究
反应动力学采用公式(2):

式(2)中:x0为初始含量;x为经过t时刻后黑加仑花色苷的含量,计算出黑加仑花色苷的降解动力学常数k[18-19]。根据不同温度条件下的k 值,以lnk对1/T作线性回归,由公式(3)计算。
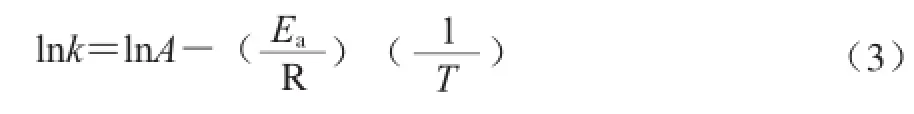
式(3)中:R为气体常数,为8.314 kJ/(mol·K);T为绝对温度/K;直线的斜率为-Ea/R,由直线的斜率即可求出活化能Ea。
采用公式(4)计算反应速率常数。

式(4)中:k为一级反应速率常数,可求出半衰期t1/2。
1.3.5 颜色的测定
利用CIE L a b体系[20-21]测定颜色变化。L为明度,L越大,表示亮度越高,反之越低;+a为红色,-a为绿色;+b为黄色,-b为青色。色差变化用公式(5)计算:
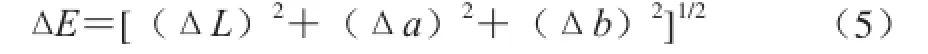
实验过程中用相机记录每次测量前玻璃瓶内果汁颜色,用Color Companion软件分析色值变化,用白色标准纸进行校准,每次取3 次测量值的平均值。
1.4 数据处理
采用Microsoft Excel 2003软件绘制图表,采用SPSS 17.0分析软件进行ANOVA单因素方差分析及差异显著性分析。
2 结果与分析
2.1 温度对黑加仑果汁中花色苷贮藏稳定性的影响
2.1.1 对黑加仑果汁花色苷含量变化的影响
不同可溶性固形物含量黑加仑果汁分别在4、25、40 ℃条件下贮藏60 d对花色苷残留率的影响,结果如图1所示。
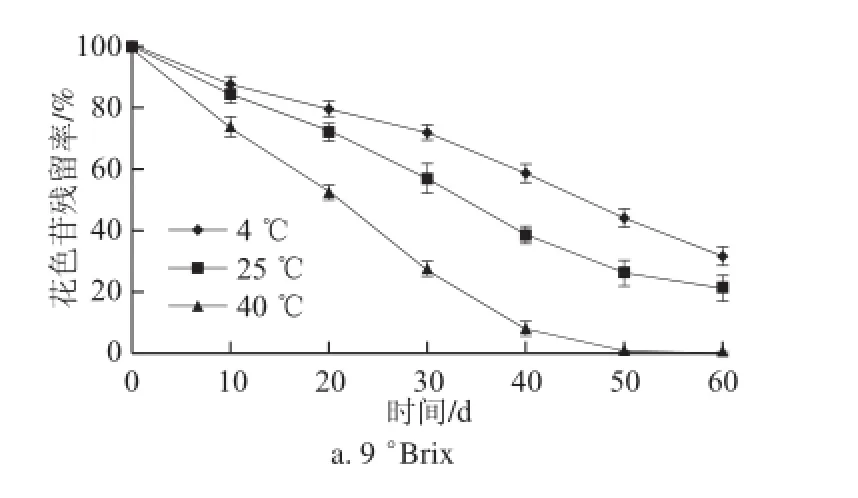
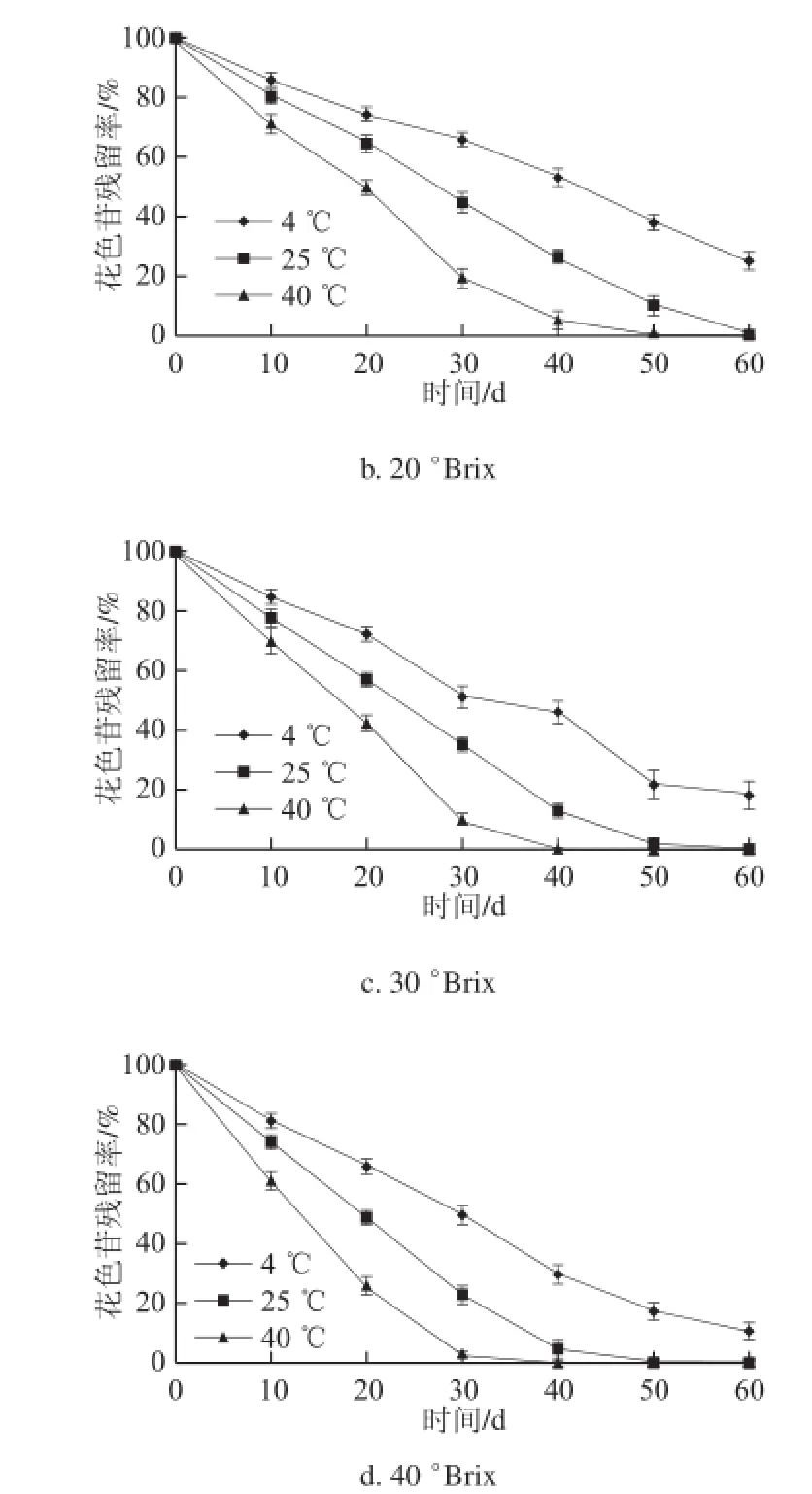
图1 不同贮藏温度条件下黑加仑果汁花色苷残留率随时间的变化Fig.1 Change in residual anthocyanins in blackcurrant juice during storage at different temperatures
从图1可以看出,随着贮藏时间的延长,黑加仑果汁中花色苷含量出现明显的降低,且随着贮藏温度的升高,花色苷残留率减少加快。60 d,4 ℃条件下,可溶性固形物含量9 °Brix花色苷的残留量仅为原来的10.57%(P<0.01),差异达极显著水平;25 ℃条件下在50 d时花色苷残留量已降为0,差异达极显著水平(P<0.01);40 ℃条件下花色苷残留量在40 d时花色苷残留量已为0,差异达极显著水平(P<0.01)。表明随着贮藏温度的升高,花色苷含量的减少速度显著加快,适宜贮藏在低温(4 ℃)条件下。
2.1.2 对黑加仑果汁花色苷降解动力学的影响
根据阿伦尼乌斯(Arrhenius)方程两边同时取对数,并利用花色苷一级反应速率常数的对数lnk与贮藏温度的倒数1/T之间的关系,求出花色苷热降解半衰期t1/2和活化能Ea(kJ/mol),如表1所示。
贮藏过程中花色苷含量逐渐下降,实验发现果汁中花色苷的残留率-ln(ct/ct0)与时间t之间呈现线性关系,相关线性回归系数均大于0.86。说明黑加仑果汁中花色苷的降解反应符合一级反应动力学规律。由表1可知,不同温度条件,黑加仑果汁的花色苷热降解速率常数k、半衰期t1/2及活化能Ea的变化受温度的影响。具体表现为:k值随温度的升高而增大,而半衰期t1/2和活化能Ea值则随之减小,9 °Brix条件下,4 ℃时的半衰期为37 d,40 ℃时的半衰期为11 d,减少了26 d(P<0.01),差异达极显著水平。结果表明高温条件下贮藏黑加仑果汁中花色苷残留率降低最快,半衰期为7~11 d。与辛修锋等[22]对杨梅清汁(pH 3.1,10.5 °Brix)花色苷残留率及降解动力学分析实验结果相似。因此,黑加仑果汁适宜贮藏在低温(4 ℃)条件下。

表1 不同贮藏温度条件下黑加仑花色苷降解动力学参数Table1 Degradation kinetic parameters of blackcurrant anthocyanins at different storage temperatures
2.2 可溶性固形物含量对黑加仑果汁中花色苷贮藏稳定性的影响
2.2.1 对黑加仑果汁花色苷含量变化的影响
将可溶性固形物含量分别为9、20、30、40 °Brix(花色苷初始含量分别为45.120 4、91.149 6、209.650 3、385.281 1 mg/100 g)的黑加仑果汁在4、25、40 ℃条件下贮藏60 d,每10 d测量一次果汁吸光度,并计算花色苷含量和花色苷残留率,根据不同可溶性固形物含量条件下花色苷残留率与时间的关系作图,结果如图2所示。
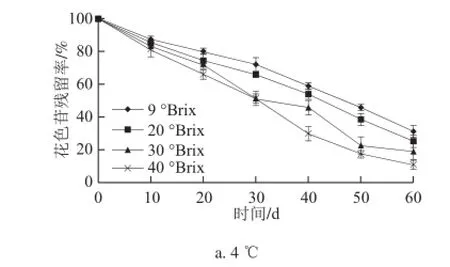
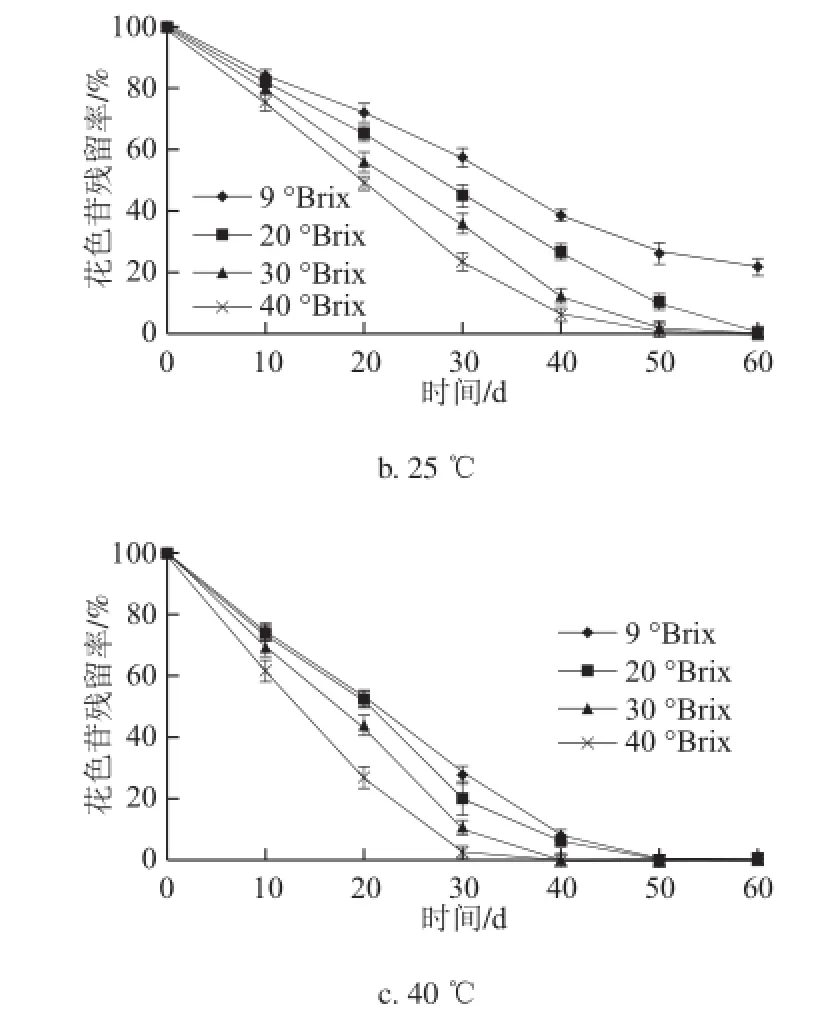
图2 不同含量下黑加仑果汁花色苷残留率变化Fig.2 Change in residual anthocyanins in blackcurrant juice with different initial concentrations during storage
由图2可知,随着贮藏时间的延长,黑加仑果汁中花色苷含量出现显著的降低,且随着果汁含量升 高,花色苷残留率减少加快。贮藏60 d、25 ℃条件下,可溶性固形物含量为9 °Brix的黑加仑果汁中花色苷残留量仅为原来的21.84%(P<0.01);可溶性固形物含量为20 °Brix的黑加仑果汁中花色苷残留量已接近为0(P<0.01);可溶性固形物含量为30 °Brix的果汁花色苷残留量在50 d时花色苷残留量已降为0(P<0.01);可溶性固形物含量为40 °Brix的果汁花色苷残留量在40 d时仅剩2%(P<0.01)。表明随着黑加仑果汁中可溶性固形物含量的升高,果汁中花色苷的残留率减少速度加快。
2.2.2 对黑加仑果汁花色苷降解动力学的影响
贮藏过程中花色苷含量逐渐下降,实验发现果汁中花色苷的残留率-ln(ct/ct0)与时间t之间呈现线性关系,相关线性回归系数均大于0.86。说明贮藏过程中黑加仑果汁中花色苷的降解符合一级反应动力学。根据阿伦尼乌斯(Arrhenius)方程两边同时取对数,并利用花色苷一级反应速率常数的对数lnk与贮藏温度的倒数1/T之间的关系,求出花色苷热降解半衰期t1/2和活化能Ea,如表2所示。
由表2可以看出,在相同贮藏温度条件下,浓缩后的黑加仑果汁中花色苷的降解速率常数k值均大于原果汁,半衰期t1/2和活化能Ea小于原果汁。4 ℃条件下可溶性固形物含量为30 °Brix果汁的半衰期为23 d,同温度条件下,可溶性固形物为9 °Brix果汁的半衰期为37 d,减少了约14 d(P<0.01),差异达极显著水平,说明浓缩后果汁中的花色苷不稳定。本研究的这一结果与Kirca等[23-24]的研究结果一致。但是对果汁进行浓缩处理可以减少果汁的体积,从而减少贮藏和运输过程中的费用,综合考虑,将黑加仑果汁浓缩至30 °Brix贮藏为宜,在4 ℃条件下可贮藏23 d。

表2 不同果汁黑加仑花色苷降解动力学参数Table2 Degradation kinetic parameters of blackcurrant anthocyanins at various initial concentrations
2.3 抗坏血酸对黑加仑果汁中花色苷贮藏稳定性的影响
2.3.1 对黑加仑果汁花色苷含量变化的影响
黑加仑果汁在贮藏之前按照50 mg/L添加抗坏血酸,在4、25、40 ℃条件下贮藏60 d,花色苷残留率与时间关系,结果如图3所示。
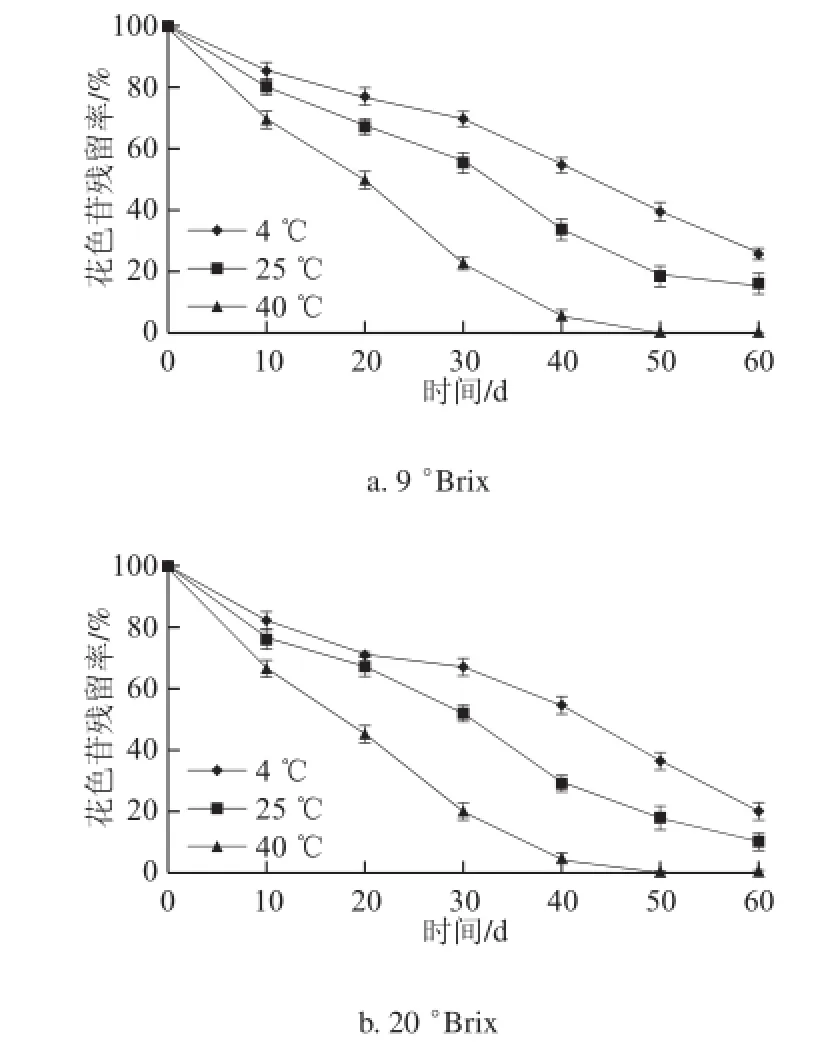

图3 抗坏血酸对不同贮藏温度条件下黑加仑果汁花色苷残留率的影响Fig.3 Effect of vitamin C on anthocyanins in blackcurrant juice at different storage temperatures
从图1与图3比较可以看出,在相同贮藏温度条件下,添加抗坏血酸(图3)比未添加抗坏血酸(图1)的黑加仑果汁中花色苷的残留率低,且随着贮藏温度的升高,花色苷残留率降低比例增大。与曹雪丹等[12]研究的抗坏血酸对蓝莓清汁中花色苷热稳定性的影响结果相似。其中,添加抗坏血酸的可溶性固形物为9 °Brix的样品在25 ℃条件下贮藏60 d,花色苷残留率比未添加抗坏血酸的对照组低4.7%(P<0.01),差异达极显著水平。随着贮藏温度的升高,花色苷残留率降低的比例更大,差异显著性增加。
2.3.2 对黑加仑果汁花色苷降解动力学的影响
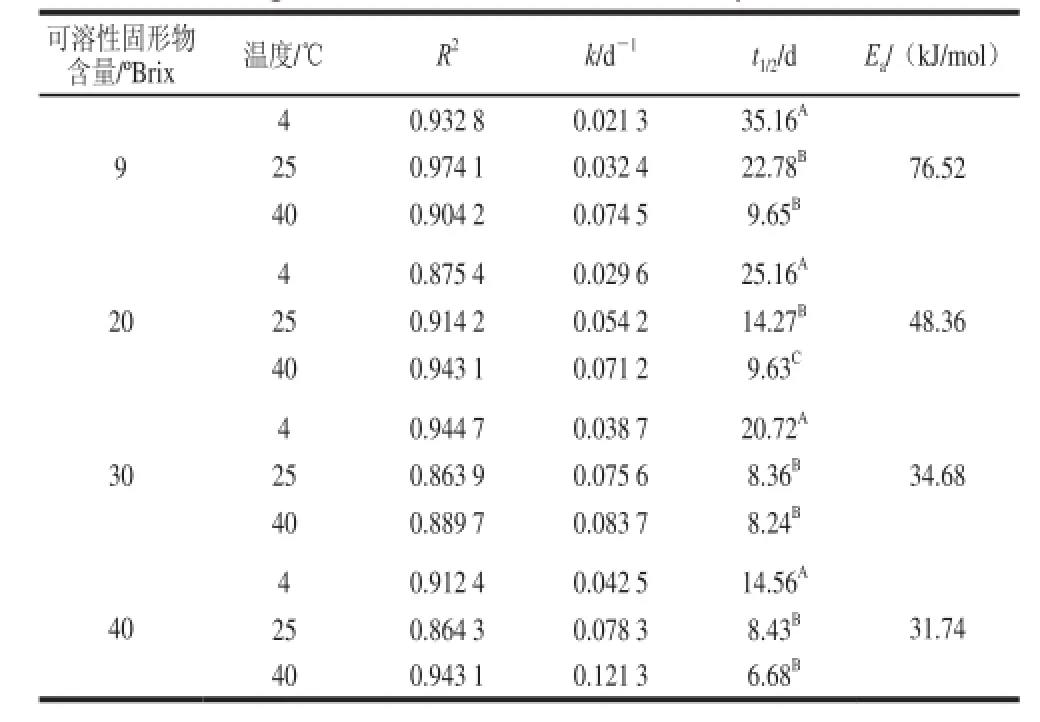
表3 50 mg/L抗坏血酸对黑加仑花色苷热降解动力学参数的影响Table3 Effect of vitamin C on kinetic parameters of thermal degradation of blackcurrant anthocyanins
以花色苷残留率-ln(ct/ct0)对贮藏时间t作图,并拟合相关参数得出降解速率常数k、半衰期t1/2和活化能Ea,结果如表3所示。
由表3可知,与未添加抗坏血酸的对照组(表1)相比,添加组的k值增大,半衰期t1/2和活化能Ea值减小,9 °Brix时半衰期减少约2 d,Ea减小8 kJ/mol(P>0.05);4 ℃条件下,20 °Brix时的半衰期减少约6 d,Ea减小7 kJ/mol(P>0.05);30、40 °Brix时的半衰期减少约3 d。Ea分别减小7 kJ/mol(P>0.05)和3 kJ/mol(P>0.05)。说明抗坏血酸会使黑加仑果汁中花色苷的减少速度略有增大,稳定性降低,这与曹雪丹等[16]研究的抗坏血酸对蓝莓汁花色苷热稳定性的影响结果相似。
2.4 果汁贮藏过程中颜色变化
果汁的色泽是评定果汁品质优良的重要指标之一,为了系统研究黑加仑果汁在贮藏过程中的颜色变化,测定色度(L、a、b值)及色差 E变化是必要的[25]。贮藏过程中温度(4、25、40 ℃)与色度(L、a、b)及 E的关系如表4所示。

表4 花色苷色差值变化(L、a、b)Table4 Color changes of blackcurrant anthocyanins (L ,a and b)
明度(L值)表示溶液的亮度,与溶液中的成色物质有关,明度越高,溶液越亮。从表4可得出,果汁在贮藏过程中色泽变化即色度值(L、a、b)与贮藏时间和温度有良好的相关性,贮藏过程中L值和a值随着花色苷残留率的减少而逐渐降低(P<0.01),差异达极显著水平。温度对色度值变化影响显著(P<0.01),温度越高,L值和a值降低速度越快,4 ℃条件下贮藏60 d时,L值由43.4降至35.1(P<0.01),a值由59.3降至48.7(P<0.01);40℃条件下贮藏60 d时,L值由43.4降至29.1(P<0.01),a值由59.3降至41.8(P<0.01),差异达极显著水平。而b值随着花色苷残留率的减少而逐渐增加,4 ℃条件下贮藏60 d时,b值由29.1增至42.4(P<0.01),40 ℃条件下贮藏60 d时,b值由29.1增至53.4(P<0.01),差异达极显著水平。贮藏过程中E随贮藏时间的延长而变大,说明色差变化显著增大(P<0.01),颜色变化明显。明度(L值)降低,果汁变暗,同时,红色度(a值)减小,黄色度(b值)增加,果汁颜色发生褐变。
黑加仑果汁中的红色度a值和黄色度b值与果汁的可溶性固形物含量之间呈正相关,可溶性固形物含量为30 °Brix的果汁红色度值为87.2,黄色度b值为50.2,可溶性固形物含量为9 °Brix的红色度a值为59.3,黄色度b值29.1,浓度越高,红色度a值和黄色度b值越高。明度L值与可溶性固形物浓度呈负相关,可溶性固形物含量为30 °Brix的果汁亮度L值26.1,含量为9 °Brix的亮度L值为43.4,含量越高亮度越低。
添加抗坏血酸的对照组,色度值也有相同的变化趋势,且L、a、b值下降趋势较未添加抗坏血酸的样品大,表明添加抗坏血酸的果汁颜色变化更为显著(P<0.01),说明添加抗坏血酸的黑加仑浓缩果汁中花色苷减少速度大于未添加抗坏血酸的浓缩果汁,同样可以说明添加抗坏血酸会降低黑加仑果汁中花色苷的稳定性。
3 结 论
1)黑加仑果汁花色苷的贮藏稳定性随温度升高而降低,且变化遵循一级反应动力学。建议在低温(4 ℃)条件下贮藏;2)浓缩后降低了黑加仑果汁中花色苷的稳定性,为了方便贮藏和运输,将黑加仑果汁浓缩至30 °Brix为宜;3)抗坏血酸能够降低黑加仑果汁中花色苷的贮藏稳定性,加速黑加仑果汁中花色苷的减少。建议在贮藏过程中不直接添加抗坏血酸作为抗氧化剂;4)黑加仑果汁中的花色苷含量与色差值L、a、b有很好的相关性。抗坏血酸对花色苷贮藏过程中的颜色褐变具有促进作用。
参考文献:
[1] 刘君, 陈淑英, 唐金. 黑加仑的研究进展及其在新疆的开发利用前景[J]. 中国林副特产, 2013(4): 85-88.
[2] 张琳琳. 黑加仑色素分离、结构初步鉴定及稳定性研究[D]. 哈尔滨: 东北农业大学, 2008.
[3] 李阳, 毕勇毅. 花色苷研究进展[J]. 公共卫生与预防医学, 2009, 20(1): 53-56.
[4] 张妍, 吴秀香. 原花青素研究进展[J]. 中药药理与临床, 2011, 27(6): 112-116.
[5] 贾娜, 孔保华, 刘骞, 等. 加热和光照对黑加仑花色苷清除自由基能力的影响[J]. 食品工业科技, 2012, 33(8): 143-145.
[6] 郭松年, 徐驰, 刘兴华, 等. 温度、pH值和光照对石榴汁花色苷稳定性的影响[J]. 食品与发酵科技, 2009, 45(5): 29-34.
[7] STANCIU G, LUPSOR S, SAVA C, et al. Spectrophotometric study on stability of anthocyanins extracts from black grapes skins[J]. Ovidius University Annals of Chemistry, 2010, 21(1): 101-104.
[8] FOSSEN T, CABRITA L, EYVIND M. Andersen. Colour and stability of pure anthocyanins influenced by pH including the alkaline region[J]. Food Chemistry, 1998, 63(4): 435-440.
[9] XIONG Shaoyuan, LAURENCE M, ALLAN E, et al. Stability and antioxidant activity of blackcurrant anthocyanins in solution and encapsulated in glucangel[J]. Journal of Agricultural and Food Chemistry, 2006, 54(17): 6201-6208.
[10] 郭庆启, 张娜. 树莓果汁中花色苷降解动力学的研究[J]. 中国林副特产, 2011(5): 35-37.
[11] 郭庆启, 张娜, 何娇, 等. 蓝靛果汁花色苷热降解动力学的研究[J].食品与发酵工业, 2011, 37(9): 74-77.
[12] 贾娜, 孔保华, 刘骞, 等. 加热对黑加仑花色苷含量及抗氧化活性的影响[J]. 食品科学, 2012, 33(21): 73-77.
[13] 徐吉祥, 楚炎沛. 色差计在食品品质评价中的应用[J]. 现代面粉工业, 2010(3): 43-45.
[14] 郭松年, 董周永, 孙海燕, 等. 石榴汁花色苷热稳定性及其降解动力学研究[J]. 农业工程学报, 2008, 24(3): 256-259.
[15] 梁淑明, 李汴生, 阮征. 黑加仑果汁加工中的关键工艺及其对果汁品质的影响[J]. 饮料工业, 2008, 11(11): 4-8.
[16] 曹雪丹, 方修贵, 赵凯, 等. 蓝莓汁花色苷热降解动力学及抗坏血酸对其热稳定性的影响[J]. 中国食品学报, 2013, 13(3): 47-53.
[17] MIRSAEEDGHAZI H, EMAM-DJOMEH Z, AHMADKHANIH R. Effect of frozen storage on the anthocyanins and phenolic components of pomegranate juice[J]. Journal of Food Science Technology, 2014, 51(2): 382-386.
[18] 张丽霞, 周剑忠, 顾振新, 等. 黑莓汁花色苷热降解动力学及降解机理[J]. 江苏农业学报, 2011, 27(5): 1111-1116.
[19] BUCHWEITZ M, SPETH M, KAMMERER D R. Impact of pectin type on the storage stability of black currant (Ribes nigrum L.) anthocyanins in pectic model solutions[J]. Food Chemistry, 2013, 139: 1168-1178.
[20] 师萱, 陈娅, 符宜谊, 等. 色差计在食品品质检测中的应用[J]. 食品工业科技, 2009, 30(5): 373-375.
[21] TORSKANGERPOLL K, ANDERSEN O M. Colour stability of anthocyanins in aqueous solutions at various pH values[J]. Food Chemistry, 2005, 89(3): 427-440.
[22] 辛修锋, 余小林, 胡卓炎. 杨梅原汁及浓缩汁中花色苷热降解动力学[J]. 农业工程学报, 2007, 23(9): 251-255.
[23] KIRCA A, OZKAN M, CEMEROGLU B, et al. Effects of temperature, solid content and pH on the stability of black carrot anthocyanins[J]. Food Chemistry, 2007, 101: 212-218.
[24] KIRCA A, CEMEROĞLU B. Degradation kinetics of anthocyanins in blood orange juice and concentrate[J]. Food Chemistry, 2003, 81(4): 583-587.
[25] LI Na, LYNNE T, MARIO F, et al. Color and chemical stability of tea polyphenol (-)-epigallocatechin-3-gallate in solution and solid states[J]. Food Research International, 2013, 53(2): 909-921.
Storage Stability of Anthocyanins in Blackcurrant Juice
ZHAO Yu-hong1,2, JIA Lin-n a1, ZHAO Tie-nan1, GAO Yu-mei1, ZHANG Li-gang3,*
(1. College of Forestry, Northeast Forestry University, Harbin 150040, China; 2. Forest Economy Resource Development and Utilization of Collaborative Innovation Center, Harbin 150040, China; 3. College of Food Science, Northeast Agricultural University, Harbin 150030, China)
In this work, we examined the effects of storage temperature, soluble solid content (SSC) and added antioxidant (ascorbic acid) on the chemical stability, degradation kinetics and color change of anthocyanins in blackcurrant juice. Results showed that blackcurrant anthocyanins were stable at 4 ℃ and an SSC of 9°Brix. With an increase in storage temperature and SSC, the level of residual anthocyanins was decreased. The degradation of anthocyanins during storage followed a firstorder reaction. The higher the reaction rate constant k, the smaller the half-life t1/2, and the lower the activation energy Ea. Addition of 50 mg/L ascorbic acid resulted in a significant increase in the degradation rate constant k of blackcurrant juice anthocyanins and a significant reduction in the half-life t1/2and the thermal degradation activation energy Ea. Therefore, adding ascorbic acid had a positive on the reduction of residual anthocyanins. As the storage period progressed, the content of anthocyanins in blackcurrant juice declined, and significant browning was observed in the juice together with a reduction in brightness and redness and an increase in yellowness. In addition, ascorbic acid could promote the color change of anthocyanins during storage.
blackcurrant juice; anthocyanins; chemical stability; color change; reaction kinetics
TS201.2
A
1002-6630(2014)20-0301-07
10.7506/spkx1002-6630-201420059
2014-02-25
赵玉红(1968—),女,副教授,博士,研究方向为植物活性成分稳定性。E-mail:zhaoyuhong08@163.com
*通信作者:张立钢(1973-),男,副教授,博士,研究方向为生物活性成分开发与利用。E-mail:zhangligang2008@gmail.com

