缓释铜的凹土/海藻酸钠复合微球的制备及性能测试
徐婷婷,李治方,吴 洁,陈 静
(淮阴工学院,江苏 淮阴 223003)
海藻酸钠(sodium alginate,SA)是天然多糖类化合物,具有生物可降解性、毒性低、生物相容性高及生物黏附性好等特点[1-2]。SA能与多价金属阳离子 Ca2+、Al3+等发生化学反应形成三维凝胶网络,该凝胶具有热不可逆性,是传统的药物控释载体、微生物及酶的固定化材料[3-5]。但是,凝胶强度不高削弱了SA载药微球的缓释效果[5-7]。凹土是一种天然一维纳米材料,具有良好的吸附特性[8],作为药物及其辅料在欧美国家已被纳入药典[9]。凹土良好的纳米增强作用可有效提升SA微球的凝胶强度,且其良好的吸附性能与SA的溶胀控释性能具有完美的协同作用,从而显著提升微球的缓释能力。铜(Cu)是生命体必须的微量元素,对血红蛋白的形成起活化作用,促进铁的吸收和利用,在传递电子、弹性蛋白的合成、结缔组织的代谢等方面有重要的意义。缺乏铜会引起贫血、毛发异常、骨骼和动脉异常,以致脑障碍;但是过剩则会引起肝硬化、腹泻、呕吐、运动障碍和直觉神经障碍[10]。通过饲料添加缓释铜制剂以保证 Cu离子代谢的稳定是经济而又有效的促进动物生长的途径。本研究提供的凹土/海藻酸钠复合微球具有良好的载药及缓控释性能,并可进一步用于其它生命体所需的微量元素或药物的缓释控释。
1 实 验
1.1 原材料
凹土(中源矿业提供)。无水氯化钙、氢氧化钠(上海青析化工有限公司);SA(上海化学试剂站分装厂)、磷酸二氢钾(南京化学试剂有限公司)、硝酸(汕头市西陇化工有限公司)、盐酸、硫酸(上海实意化学试剂有限公司),所有试剂均为分析纯。
1.2 Cu离子标准曲线及浓度测定
使用北京普析通用有限责任公司的TAS-990AFG型原子吸收分光光度计测定Cu离子浓度。标准曲线以去离子水为空白样,于324.7 nm波长处测定吸光度[11],回归方程的线性相关系数R2值均在0.999以上。
1.3 复合微球的制备、载药和释放
(1)制备 采用滴制法制备复合微球,40 ℃水浴下搅拌匀化,配制20 g/L SA水溶液。凹土以2 mol/L的硫酸酸化,洗脱至中性后,以水配置成2%浓度浆料,搅拌分散 24 h。将分散好的酸化凹土(AP,acidulated palygorskite)与20 g/L SA水溶液按一定比例混合,于50 ℃水浴下搅拌2 h。将复合物通过恒流泵以7 mL/min的速度滴到2% CaCl2溶液中,持续搅拌交联固化一定时间,收集并用去离子水冲洗。
(2)载药 将制备好的微球浸入1%硫酸铜溶液中吸附4 h后过滤。所得微球以10 mL去离子水洗涤后于50~60℃烘干至恒重。微球吸附Cu的总量和吸附率分别按式(1)和式(2)计算。

式中,W1为添加的Cu的质量;Cf为滤液的浓度;n为稀释倍数;V为缓冲液体积。
(3)释放 称取0.5 g复合微球置于200 mL的pH值为6.8的人工模拟肠磷酸缓冲液中,37 ℃水浴恒温振荡器震荡,转速100 r/min。定时取样。水样过0.45 μm微孔滤膜。Cu的释放率按式(3)计算。
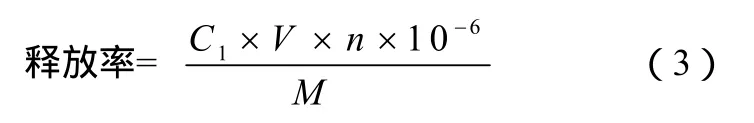
式中,C1为溶液浓度;M为微球吸附Cu的总量。
2 结果和讨论
2.1 凹土对微球载铜和缓释性能的影响
海藻酸盐微球给药系统是近年来研究较多的一类新型口服药物控释载体,已成功应用于多种药物的控制释放,但是其凝胶强度仍有待提高。本研究通过对 SA微球和 SA/AP复合微球进行平行实验,比较两种微球的吸附和累积释放率。
实验结果表明,AP/SA复合微球的吸附率(94.60%)比SA微球(91.82%)高,释放速度显著降低(图1),说明加入凹土的复合微球对硫酸铜的缓释性能有一定的改善。因此,本研究将凹土与SA进行复合。
SA与AP的比例变化会影响微球结构,从而影响微球的载药释药性能。随着 AP/SA比例的增大(10%~40%),Cu2+的吸附率逐渐增大并趋于稳定。AP本身具有良好的吸附性能,其加入对微球的吸附能力体现出一种协同作用。而AP的量增多之后,降低了微球的弹性,从而一定程度上会降低微球的吸附性能。不同凹土含量对Cu2+释放性能的影响见图2,AP/SA的比例为20%时的释放率相对缓慢,且对Cu2+的吸附率也较高(94.60%)。综合考虑吸附与缓释性能,AP/SA的比例为20%为最佳。

图1 凹土对微球累积释放率的影响

图2 AP/SA比例对微球累积释放率的影响
2.2 交联条件对载铜及其缓释的影响
交联条件对形成微球的密实程度有很大影响,因此会显著影响微球的载药与释药性能[12-13]。微球的吸附率随着交联剂CaCl2浓度的增加而先增加后降低(表1)。随着交联时间的增加,微球对 Cu2+的吸附率先增大后趋于稳定(值分别为 94.60%、98.99%、98.98%),但交联时间为0.5 h时缓释控制最为良好(图3)。Cu2+在微球上的载负可能有两种形式:一种是吸附;另一种为微球丰富的毛细孔结构容纳一定的 CuSO4溶液。CaCl2浓度小,交联时间短的时候,三维凝胶网络结构不完善,吸附量和容留量都小,CaCl2浓度增大,交联时间增长,完善的凝胶结构使得微球的吸收能力变强,但是吸附主要是在外表面,且毛细留容量较小。吸附在表面的Cu2+释放路径短,而吸附在内部的Cu2+释放出来要经过较长的路径,从而显示出缓释的效果。因此,虽然随着CaCl2浓度增加和交联时间的延长,微球的吸附性能略有提高,而缓释性能却有所降低。因此,本实验采用CaCl2浓度为2%,交联时间为0.5h。
2.3 微球释放过程中的形态表征
从图4显示的微球在缓冲溶液中的溶胀性能比较中可看出,在药物释放了1 h后,AP/SA复合微球的粒径明显小于SA微球,且微球中心未完全溶胀微球中心仍有蓝色的颗粒状物质,而SA微球的凝胶强度很小而且微球中的铜离子基本完全释放呈白色状。
在pH值为6.8的磷酸盐缓冲液(模拟人工肠液)环境中,微球中的海藻酸根离子与钾离子形成可溶性海藻酸盐,吸水后造成凝胶微球发生不同程度的溶胀,随着时间延长,溶胀的微球开始溶蚀,因此在药物释放过程中,药物扩散与骨架溶蚀同时进行。

表1 CaCl2浓度对微球吸附性的影响

图3 交联时间对微球累积释放率的影响

图4 微球在PBS中释放1 h
2.4 微球的扫描电镜(SEM)图谱
由图5(a)和(d)的对比可见,复合微球的表面比SA微球要褶皱得多,因此药物从微球中释放出来要经过更长的途径,AP/SA复合微球的缓释作用有所提高。图5(b)进一步展示了复合微球外表皱褶的大比表面积,较大的比表面积是复合微球的载药率高的一个重要因素。而图5(c)显示载铜复合微球中有大量的毛细管;微球中毛细孔的毛细作用也可能是微球载铜量提高的重要因素。

图5 微球的电镜照片
3 结 论
滴制法制备载铜AP/SA复合微球的最佳工艺条件是:原料经充分研磨分散,SA浓度2%(质量分数),CaCl2浓度2%(质量分数),AP/SA=1∶5,复合温度50 ℃,交联时间30 min,pH=5。微球烘干前,外表光滑圆润,粒径约为2 mm,烘干后,外表粗糙,粒径约为1 mm。AP/SA复合微球与SA微球相比,吸附率由91.82%提高到94.60%,在2 h内的释放率由66.35%降低到22.78%,得到了一定程度的减缓,这说明在复合微球中,凹土起到了改善其凝胶强度和缓释性能的作用。本复合微球可进一步用于其它生命体所需的微量元素或药物的缓释控释。
[1] August A D,Kong H J,Mooney D J,Alginate hydrogels as biomAPerials[J].Macromolecular Bioscience,2006,6(8):623-633.
[2] 王康,何志敏,海藻酸钠微胶囊的制备及在药物控释中的研究进展[J]. 化学工程,2002,30(1):48-54.
[3] Wu Q H,Wu H,Wang L C,et al. Review on preparation and application of Alginate microspheres as drug carrier[J].China Journal of Traditional Chinese Medicine and Pharmacy,2011,8:1791-1794.
[4] Jin L X. Drug delivery materials in the field of medicine and its application[J].Journal of Clinical RehabilitAPive Tissue Engineering Research,2011,25:4699-4702.
[5] 仲静洁,王东凯,张翠霞,等. 海藻酸钠在药物制剂中的研究进展[J]. 中国新药杂志,2007,16(8): 591-594.
[6] Wee S,Gombotz W R. Protein release from alginate matrices[J].Advanced Drug Delivery Reviews,1998,31:267-285.
[7] Liang H F,Hong M H,Ho R M,et al. Novel method using a temperature-sensitive polymer(methylcellulose) to thermally gel aqueous alginate as a pH-sensitive hydrogel[J].Biomacromolecules,2004,5(5):1917-1925.
[8] Fernaderz M E,Ascencio J A,Mendoza A D. Experimental and theoretical study of palygorskite clays[J].Journal of Material Science,1999,34(6):5243-5255.
[9] Murry Y H. Traditional and new application for kaolin,smectite,and palygorskite[J].Applied Clay Science,2000,17:207-221.
[10] 李松岩. 猪饲料中高剂量的铜锌对环境的影响及其控制[D]. 南京:南京农业大学,2005.
[11] 丁国斌. GB/T7475—1987,水质铜、锌、铅、镉的测定原子吸收分光光度法[S]. 1987.
[12] 吴文果,黄晓楠,王世斌,等. 乳化法制备海藻酸钙/聚组氨酸微胶囊[J]. 化工进展,2009,28(4):673-677.
[13] Haryadi D M,Wang Y W,Lin S,et al. Novel alginate gel microspheres produced by impinging aerosoles for oral delivery of proteins[J].Journal of Microencapsulation,2012,39(3):250-261.

