Ni-Zn复合氧化物用于反应吸附脱除噻吩
魏延雨,李永红,3,孔爱华
(1.天津大学 绿色合成与转化教育部重点实验室,天津300072;2.天津大学 化工学院,天津300072;3.天津大学 精馏技术国家工程研究中心,天津300072)
燃料油中的硫是大气污染的主要来源之一,汽车尾气所造成的污染占城市大气污染的60%以上。随着环保要求的不断提高,减少车用燃料中硫的含量刻不容缓。许多国家都颁布了严格的环境法规,限定车用燃料中的含硫量。美国环保署(EPA)规定到2010年美国的柴油硫质量分数降到15μg/g;欧洲也相继提高了对燃油中硫含量的限制,德国规定到2009年其柴油含硫量控制在10μg/g以内。中华人民共和国环境保护部最新出台的环境法规规定从2011年5月1日起实施第四、第五阶段的标准。第四阶段的标准规定汽油、柴油中硫质量分数小于50μg/g,而第五阶段标准的规定则小于10μg/g。这也意味着我国对油品硫含量的要求正逐步与世界接轨,汽、柴油深度脱硫成为世界范围重要的研究课题。
加氢脱硫(HDS)工艺是目前最主要的脱硫工艺,但其存在一次性投资过大、运行成本高、需要消耗大量氢气等缺点,导致加工成本显著上升[1]。主要的非加氢脱硫技术有传统的酸碱精制及溶剂抽提、烷基化脱硫[2]、吸附脱硫[3-10]、萃取脱硫、氧化脱 硫[11-12]、 膜 分 离 脱 硫[13]、 生 物 脱 硫[14]等。 反应吸附脱硫技术耦合了加氢脱硫与吸附脱硫技术,既克服了加氢脱硫条件苛刻、难于脱除噻吩类硫化物的缺点,又能够显著降低燃油中的硫含量,实现燃料油的深度脱硫,并且具有硫容量大、选择性好、对辛烷值影响小、反应尾气中不含硫、不会造成二次污染等一系列的优点,因此反应吸附脱硫技术具有很好的工业化前景。
目前,反应吸附脱硫的吸附剂主要为金属氧化物类。沉淀法制备的金属氧化物吸附剂具有产品纯度高、沉淀颗粒均匀、粒径小、分散性好等优点,并且工艺简单、操作方便,对原料和设备要求不高[15]。因此,笔者采用均匀共沉淀法制备了镍锌复合金属氧化物吸附剂,并采用BET、XRD方法对吸附剂进行了表征,同时考察了反应条件对吸附剂脱硫性能的影响,初步研究了吸附剂的脱硫机理。
1 实验部分
1.1 原料和试剂
硝酸镍(Ni(NO3)2·6H2O)、硝酸锌(Zn(NO3)2·6H2O)、γ-Al2O3、尿素、正庚烷、环己烷、甲苯、噻吩,均为分析纯,天津市光复科技发展有限公司产品;十二烷基硫酸钠,化学纯,天津市光复科技发展有限公司产品;异戊烯,纯度高于99%,山东恒源祥石化集团公司产品。
1.2 吸附剂的制备
1.2.1 NiO/ZnO、ZnO、NiO吸附剂的制备
采用均匀共沉淀法制备NiO-ZnO、ZnO、NiO吸附剂。称取一定质量的硝酸锌和硝酸镍(或单独称取一定质量的硝酸锌、硝酸镍)与十二烷基硫酸钠、尿素一起溶于适量的去离子水中,298K下搅拌2h生成透亮溶液,然后转移到恒温水浴中在353K恒温10h,由尿素的缓慢水解控制pH值。沉淀完全后,分离、洗涤,393K下干燥12h。干燥后的反应吸附剂前驱体经过压片成型后在773K焙烧5h,然后粉碎过筛,制得所需的20~40目Ni质量分数为15%的吸附剂NiO-ZnO、ZnO、NiO。
1.2.2 NiO/γ-Al2O3吸附剂的制备
采用等体积浸渍法制备不同Ni含量的NiO/γ-Al2O3吸附剂。将筛分好的20~40目的γ-Al2O3等体积浸渍在一定浓度的硝酸镍溶液中,298K下浸渍12h,然后393K干燥12h,并在773K焙烧5h,制备得到Ni质量分数分别为5%、20%的NiO/γ-Al2O3,记为5%NiO/γ-Al2O3、20%NiO/γ-Al2O3。
1.2.3 吸附剂的原位还原
脱硫反应前,在纯H2气氛中,723K、氢气压力0.5MPa、氢气流量100mL/min的条件下,对制备的吸附剂 NiO-ZnO、NiO、5%NiO/γ-Al2O3、20%NiO/γ-Al2O3进行4h原位还原。还原后的吸附剂记作 Ni/ZnO、Ni/NiO、5%Ni/γ-Al2O3、20%Ni/γ-Al2O3。
1.3 催化剂的表征
采用美国Micromeritics公司Tristar-3000全自动比表面及孔隙度分析仪测定在不同吸附压力下的吸附体积,然后利用BET方程计算出样品比表面积,用BJH法计算样品的孔分布。以液氮为吸附介质,吸附温度77K,测试前样品在573K下脱气处理5h。
采用Rigaku D/max 2500v/pc型X射线衍射仪分析反应吸附剂物相结构。Cu靶,λ=0.15406nm,电压40kV,电流80mA,扫描范围10°~70°,扫描速率6°/min。
1.4 模拟油的配制
将噻吩溶于正庚烷中配成质量浓度为100mg/L的模拟油A。将正庚烷、环己烷、异戊烯、甲苯以体积比40∶10∶35∶15配成溶液,然后加入一定量的噻吩配成硫质量浓度为100mg/L的模拟油B。
1.5 反应吸附脱硫工艺流程及吸附剂活性评价
反应吸附脱硫实验在固定床反应器中进行。反应器内径8mm、长30cm。吸附剂粒度20~40目,装填量0.5g。氢气与模拟油的体积比(简称氢/油比,氢气的体积为标准状况下的体积)200,进料液时空速60h-1,反应温度473~773K,反应压力0.2~1.2MPa。采用华东分析仪器厂DL-2B微库仑测硫仪测定反应前后模拟油中的硫质量浓度[16],采用带有FID检测器的气相色谱测定模拟油中其余组分的含量。
1.6 吸附剂硫容的计算
通过记录一定时间段反应器流出油的硫质量浓度可以得到吸附曲线,由式(1)计算吸附剂的硫容。
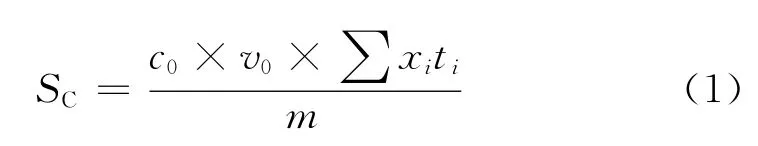
式(1)中,SC为吸附剂的硫容,mg/g;c0为反应器入口模拟油中硫的质量浓度,mg/L;v0为模拟油的流速,L/h;xi为2次取样间隔内的平均脱硫率,%;ti为2次取样的时间间隔,h;m为吸附剂的质量,g。每隔一定时间取样检测反应器流出油中硫的质量浓度。为了同时研究吸附剂的深度脱硫性能以及吸附饱和过程,分别计算了脱硫率为90%和20%的硫容。
通过吸附剂后模拟油中主要成分的损失率由式(2)计算。
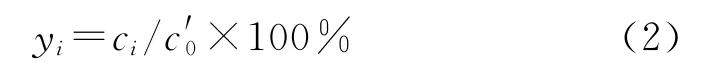
式(2)中,yi为模拟油组分的损失率,%;c′0为模拟油中各组分的初始质量浓度,mg/L;ci为2次取样间隔内产物中各组分的平均质量浓度,mg/L。
吸附剂吸附的硫元素质量及气体中所含硫元素质量分别由式(3)、(4)计算。
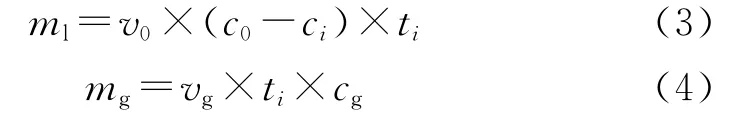
式(3)、(4)中,ml与mg分别为吸附剂吸附的硫元素质量及气体中所含硫元素质量,mg;vg为气体的体积流量,L/h;cg为气体中所含硫元素的质量浓度,mg/L。
2 结果与讨论
2.1 不同处理条件下NiO-ZnO吸附剂的物化性质
2.1.1 比表面积和孔体积
不同处理条件下NiO-ZnO吸附剂的比表面积和孔体积列于表1。由表1可见,制备的新鲜NiO-ZnO吸附剂的比表面积和孔体积都比较大,且比等体积浸渍法制备的吸附剂要大[6]。新鲜NiO-ZnO经氢气预还原后得到的Ni/ZnO吸附剂的比表面积和孔体积均有一定程度的增加,从而增大了与噻吩的接触面积,减少了噻吩在吸附剂中的扩散阻力,这也是Ni/ZnO对噻吩的吸附性能好于NiO-ZnO的一个原因。与新鲜NiO-ZnO相比,再生后的NiO-ZnO的比表面积和孔体积没有明显变化。与新鲜吸附剂相比,吸附饱和后的吸附剂比表面积和孔体积均有显著的降低,说明吸附剂吸附的大量硫化物堵塞了吸附剂的孔道,从而降低了比表面积。
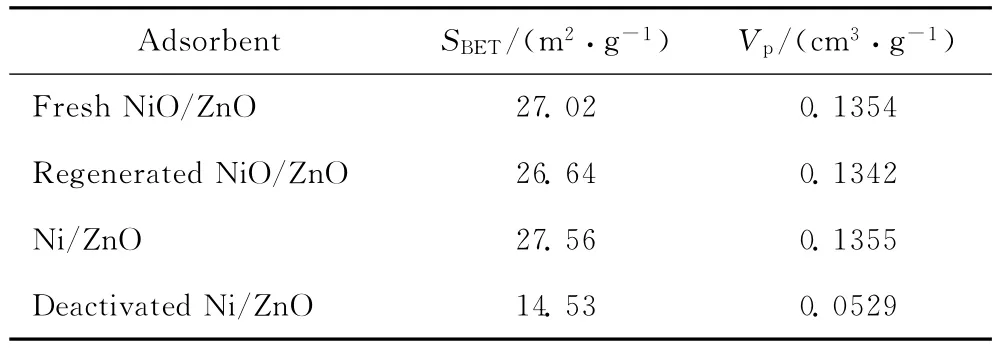
表1 不同处理条件下NiO-ZnO吸附剂的比表面积和孔体积Table 1 Specific surface area and pore volume of NiO-ZnO adsorbent under different treatment conditions
2.1.2 晶相组成(XRD结果)
不同处理条件下NiO-ZnO吸附剂的XRD谱示于图1。从图1看到,新鲜NiO-ZnO和再生后的NiO-ZnO的XRD谱几乎完全一样,说明再生后吸附剂的结构几乎没有变化,吸附剂的再生性能良好;两者均有明显的NiO和ZnO的特征衍射峰,在2θ为30°~40°之间出现较强的ZnO峰,说明ZnO的粒径较大,通过半峰宽估算粒径在16nm左右。Ni/ZnO吸附剂除明显的ZnO、NiO特征衍射峰以外,还出现单质Ni特征衍射峰;其中1个NiO的峰(2θ=37.12°)消失,说明723K还原4h能够将小粒径的NiO完全还原;没有发现Ni-Zn合金的特征衍射峰。Huang等[17]认为,Ni-Zn的存在不利于吸附脱硫,这也是笔者制备的NiO-ZnO吸附剂预还原后吸附性能升高的原因。从图1还可见,吸附饱和的Ni/ZnO吸附剂的NiO、ZnO特征衍射峰的强度逐渐降低,出现了明显的NiS、NiSx、ZnS峰,以及很小的Ni3C峰,说明吸附剂的失活主要是因为硫原子在金属上的吸附以及积炭作用。高温下ZnS、NiS、NiSx、Ni3C在氧气中很容易变成氧化物,这也是该吸附剂容易再生的一个原因。
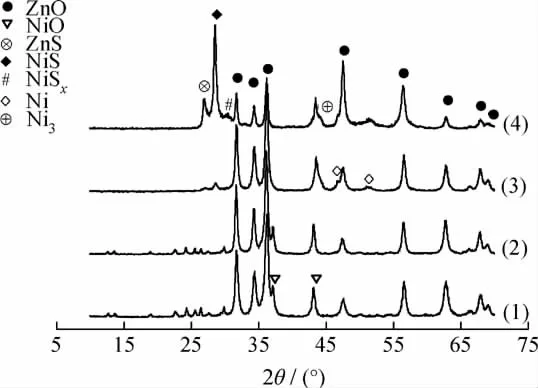
图1 不同处理条件下NiO-ZnO吸附剂的XRD谱Fig.1 XRD patterns of NiO-ZnO adsorbent under different treatment conditions
2.2 预还原对NiO-ZnO吸附脱硫性能的影响
在673K、1.0MPa下 NiO-ZnO和 Ni/ZnO吸附剂对模拟油A中噻吩的吸附穿透曲线示于图2。由图2可见,2种吸附剂对模拟油A均表现出很好的脱硫效果。以Ni/ZnO为吸附剂时,在初始20h内反应器出口油样中检测不到硫,模拟油A中的噻吩全部吸附在Ni/ZnO上;在36h内模拟油的脱硫率均大于90%,可以长时间实现深度脱硫,此时吸附剂的硫容为212mg/g;此后脱硫率逐渐下降,在79h时脱硫率低于20%,吸附剂的硫容达到360mg/g。以NiO/ZnO为吸附剂时,在初始3h内,随着时间的延长,模拟油A的脱硫率逐渐上升;随后脱硫率的变化与Ni/ZnO的相似,在2~31h范围脱硫率均在90%以上,吸附剂的硫容为171mg/g;77h以后脱硫率低于20%,吸附剂的硫容为359mg/g。在此反应条件下,NiO能够逐渐被H2还原为单质Ni,反应后的吸附剂中明显含有NiS、ZnS(见图1)。这说明在吸附噻吩的过程中,噻吩中的硫原子会与金属形成共价键,而共价键的共用电子对偏向硫原子,也就是由金属原子提供电子;Ni2+缺失电子造成其电子密度比Ni原子的小,减弱了S—Ni键,从而不利于噻吩的吸附脱除。同时,预还原后的吸附剂的比表面积和孔体积都有所增加(见表1),从而增加了吸附剂与噻吩的接触面积,减少扩散阻力,利于噻吩的脱除。因此预还原有利于提高改善吸附剂的吸附脱硫性能。
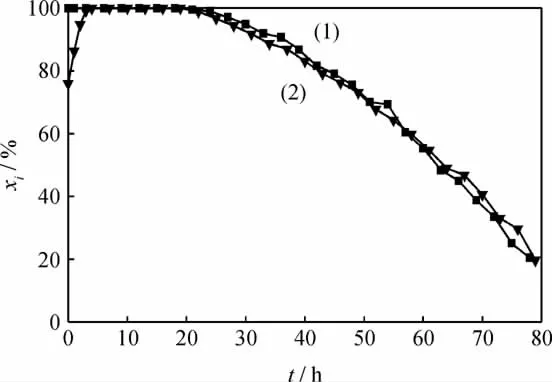
图2 Ni/ZnO和NiO-ZnO吸附剂对模拟油A中噻吩的吸附穿透曲线Fig.2 Adsorption breakthrough curves of Ni/ZnO and NiO-ZnO for thiophene in model oil A
2.3 反应吸附脱硫工艺条件对Ni/ZnO吸附脱硫性能的影响
图3为采用Ni/ZnO吸附剂的反应吸附脱硫工艺中模拟油A的脱硫率随反应温度和压力的变化曲线。从图3(a)看到,在反应温度较低时,脱硫率随温度的升高而快速增大,623K时逐渐趋于稳定,但当温度高于723K时脱硫率又有所下降,因此反应的适宜温度在623~723K,最佳反应温度为673K。
吸附剂与硫化物之间的吸附作用有物理吸附、π络合吸附和化学吸附3种。物理吸附和π络合吸附的作用力均随着温度的升高而降低[18],由此可见,Ni/ZnO对噻吩的吸附主要以化学吸附为主。一般认为,Ni/ZnO对噻吩的吸附过程分为两步。首先是噻吩在Ni原子上的氢解过程,然后是 H2S在ZnO上的吸附过程[19]。温度升高有利于吸附在吸附剂活性位上的噻吩的活化,加快噻吩的氢解过程,从而提高脱硫率。当温度高于723K时,吸附剂晶粒变大,比表面积变小,孔容变小[20],孔结构遭到一定程度的破坏,致使活性位减少,脱硫率下降。这与徐文清等[21]报道的温度越高越有利于Ni/ZnO对FCC汽油吸附脱硫的结论不一致,因为他们所考察的温度范围过窄,只考察到673K,并且其焙烧温度高达823K,在反应温度下对吸附剂的比表面积和孔结构不会造成影响。
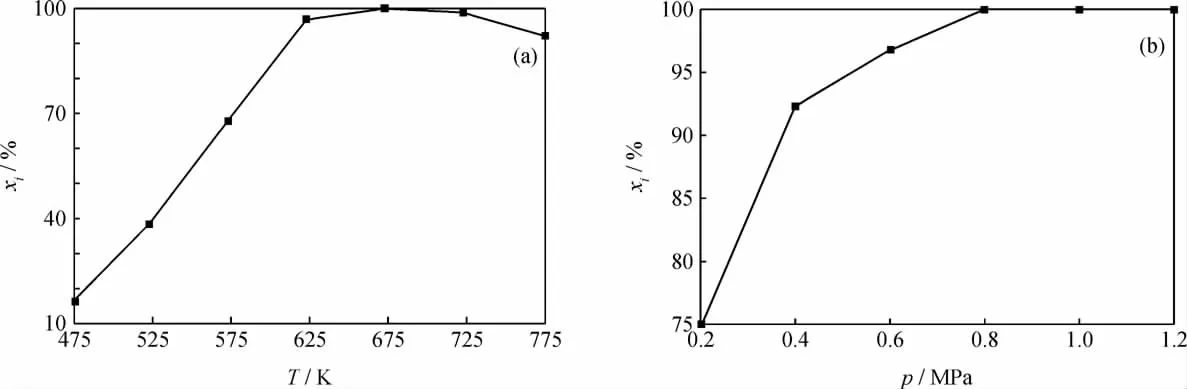
图3 采用Ni/ZnO吸附剂的反应吸附脱硫工艺中模拟油A的脱硫率随反应温度和压力的变化Fig.3 Desulfurization rate of model oil A vs temperature and pressure of reactive absorption with Ni/ZnO adsorbent
从图3(b)看到,反应压力较低时,脱硫率随压力的升高而增加;当压力达到0.8MPa后,脱硫率达到100%;压力继续升高时,脱硫率基本不再变化。考虑到压力越大对生产设备的要求越高,制造成本也越高,因此选择1.0MPa作为最适宜的反应压力。
图4为不同反应条件下Ni/ZnO对模拟油A中噻吩的吸附穿透曲线。从图4看到,573K时,吸附初始阶段的脱硫率就出现明显的下降;随着时间的延长,脱硫率下降的幅度逐渐减小,并趋于平稳。这主要是因为573K下吸附剂的活性低,只有少量的噻吩能够被活化,不具有深度脱硫的能力。但在低脱硫率下,吸附剂依然表现出很高的硫容,硫容为103mg/g。图4中曲线(3)和(4)的变化规律基本相同,说明在1.0MPa反应压力下,在反应温度为673和773K时都能长时间实现模拟油的超深度脱硫。但二者也存在区别。673K时20h内反应器流出油中检测不到硫,36h内脱硫率都在90%以上,硫容达到212mg/g;773K时的初始脱硫率只有95%,并且只在16h内的脱硫率才大于90%,硫容也只有83mg/g,其深度脱硫能力显著降低。因为在773K时吸附剂比表面积、孔结构、活性组分粒径变化的不利影响已经大于反应活性提高的有利影响,不利于深度脱硫。以20%脱硫率作为穿透点,673和773K下的硫容分别为360和348mg/g。由此可见,高温对吸附剂的饱和硫容的影响并不大,温度对吸附剂脱硫性能的影响主要由噻吩在吸附剂活性位上的活化过程引起。从图4还可看到,在0.5MPa下,Ni/ZnO吸附剂已表现出较高的脱硫活性,且脱硫率随时间的变化趋势与1.0MPa时的基本一致,但深度脱硫能力有了明显的降低,只在初始8h内脱硫率超过90%,硫容仅为44 mg/g,而脱硫率在20%时的硫容为180mg/g。压力越大越有利于气体的吸附,在低压下氢气在吸附剂表面的吸附达不到饱和,吸附剂表面的氢浓度低,显著影响了噻吩的氢解反应速率,造成脱硫率的降低。
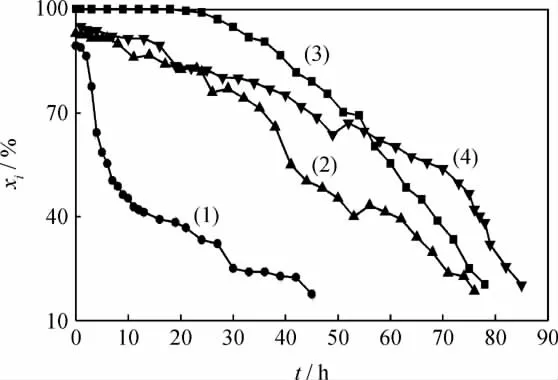
图4 不同反应条件下Ni/ZnO对模拟油A中噻吩的吸附穿透曲线Fig.4 Adsorption breakthrough curves of Ni/ZnO for thiophene in model oil A at different reaction conditions
2.4 模拟油组分对Ni/ZnO吸附脱硫活性的影响
真实汽油中除了链状烷烃以外,还含有环烷烃、烯烃、芳香烃等一系列物质,特别是烯烃和芳香烃,它们与噻吩具有相似的电子结构,对噻吩的脱除具有很大影响。如何提高噻吩相对于烯烃、芳香烃[22]的选择性成为目前吸附脱硫的难点与重点。573K、1.0MPa下,Ni/ZnO吸附剂对模拟油A、B中噻吩的吸附穿透曲线示于图5。从图5看到,模拟油中添加环己烷、异戊烯、甲苯后,吸附剂对模拟油中噻吩的吸附性能降低,脱硫率为20%的硫容从原来的360mg/g降到292mg/g。对含有环己烷、异戊烯、甲苯的模拟油B而言,在反应吸附脱硫的初始6h内,脱硫率达到100%;初始28h内,脱硫率高于90%,硫容为173mg/g。为了确定模拟油中各个组分对吸附剂脱硫性能的影响,考察了脱硫后各个组分的损失率随时间的变化,结果也示于图5。从图5看到,在整个反应吸附脱硫过程中,环己烷和甲苯几乎没有损失,说明它们没有参与反应吸附。由于甲苯的分子结构、电子结构与噻吩有一定的相似性,特别是二者都能与金属原子形成π络合吸附,因而能与噻吩发生竞争吸附,但高温对π络合吸附不利,减弱了甲苯对噻吩吸附的影响,也证明了噻吩在Ni/ZnO上的吸附是化学吸附而不是π络合吸附。异戊烯的损失率随时间的延长逐渐降低,并趋于一个稳定值。由此推测,对脱除油品中噻吩硫影响最大的是烯烃类化合物的存在。Ni/ZnO脱除噻吩时,噻吩首先被吸附在单质Ni上,由于单质Ni具有加氢活性,噻吩中的硫与H2相互作用生成NiS,并继续转变成 H2S,被ZnO吸附而脱除[9]。由于烯烃存在双键,加氢活性高,在反应脱硫过程中也会被吸附在吸附剂上发生加氢反应,占用了吸附剂的部分活性位,从而影响了对噻吩的脱除能力。
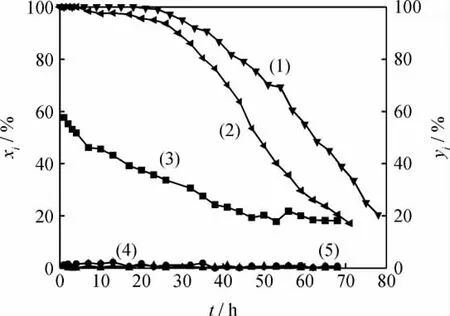
图5 Ni/ZnO对2种模拟油中噻吩的吸附穿透曲线以及模拟油B中各组分的损失率(yi)随时间(t)的变化Fig.5 Adsorption breakthrough curves of Ni/ZnO for thiophene of two model oils and the loss rate(yi)of every component in model oil B vs t
2.5 Ni/ZnO吸附剂的再生性能
吸附剂不仅要有好的吸附性能,并且要有好的再生性能,能够循环利用。吸附饱和后的Ni/ZnO吸附剂在空气中于773K下焙烧5h,然后在氢气氛围中723K还原4h,再考察其反应吸附脱硫性能,结果示于图6。从图6看到,再生后的Ni/ZnO与新鲜Ni/ZnO的吸附脱硫性能几乎没有区别,硫容仅由360mg/g降到358mg/g。因此 Ni/ZnO吸附剂能够再生,可以重复利用。
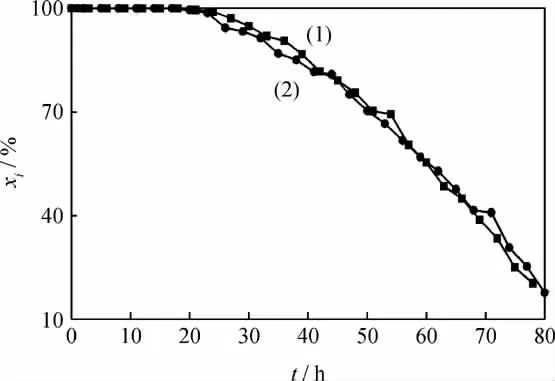
图6 再生后与新鲜的Ni/ZnO对模拟油A中噻吩的吸附穿透曲线Fig.6 Adsorption breakthrough curves of regenerated and fresh Ni/ZnO for thiophene in model oil A
2.6 吸附剂吸附脱硫原理
为了确定吸附剂中各个组分的作用并初步研究吸附剂的脱硫原理,笔者考察了每一测定时刻的30s内 ZnO、Ni/NiO、5%Ni/γ-Al2O3、20%Ni/γ-Al2O34种吸附剂吸附的硫元素质量和反应器出口气相中硫元素质量随时间的变化,结果示于图7。从图7看到,ZnO在初始很短时间内即失去脱硫能力,并且在尾气中没有检测到H2S的存在,由此可见ZnO对噻吩的吸附能力很弱,不具有深度脱硫的效 果;Ni/NiO、5%Ni/γ-Al2O3、20%Ni/γ-Al2O33种吸附剂具有相似的脱硫趋势,随着吸附时间的延长,吸附剂吸附的硫元素质量逐渐下降,气体中的硫元素质量逐渐增加,并且二者都逐渐趋于稳定。由此可见,3种吸附剂中起主要作用的是还原态的Ni原子,噻吩在Ni原子表面能够发生氢解反应生成H2S,而Ni原子可以与H2S继续反应生成NiSx(见图1(4))。这一过程会造成吸附剂表面还原态Ni原子的减少,从而影响噻吩的氢解过程,又会导致生成的H2S减少,Ni原子的硫化过程减弱。噻吩的氢解与Ni原子的硫化相互影响相互制约,初始阶段因为有大量Ni原子存在,噻吩的氢解与Ni原子的硫化速率都很快,因此吸附剂吸附的硫元素质量多,气体中的含硫量低;经过一段时间后两者会趋于平衡,吸附剂吸附的硫元素质量也趋于稳定。Ni/ZnO吸附剂在对模拟油A的吸附脱硫过程中,在初始的20h内脱硫率始终保持100%(见图2),而ZnO、 Ni/NiO、5%Ni/γ-Al2O3、20%Ni/γ-Al2O34种吸附剂在反应开始后吸附的硫元素质量持续减少,600min后仅能吸附微量的硫元素,由此可以看出Ni与ZnO在脱硫过程中具有协同作用。ZnO能够快速捕捉生成的 H2S[23],抑制NiSx的生成,从而使吸附剂一直保持高的脱硫活性。通过以上分析可以推断,吸附剂脱硫过程包括两步,即噻吩先在Ni原子上进行氢解生成H2S,然后生成的H2S快速与ZnO结合生成ZnS。
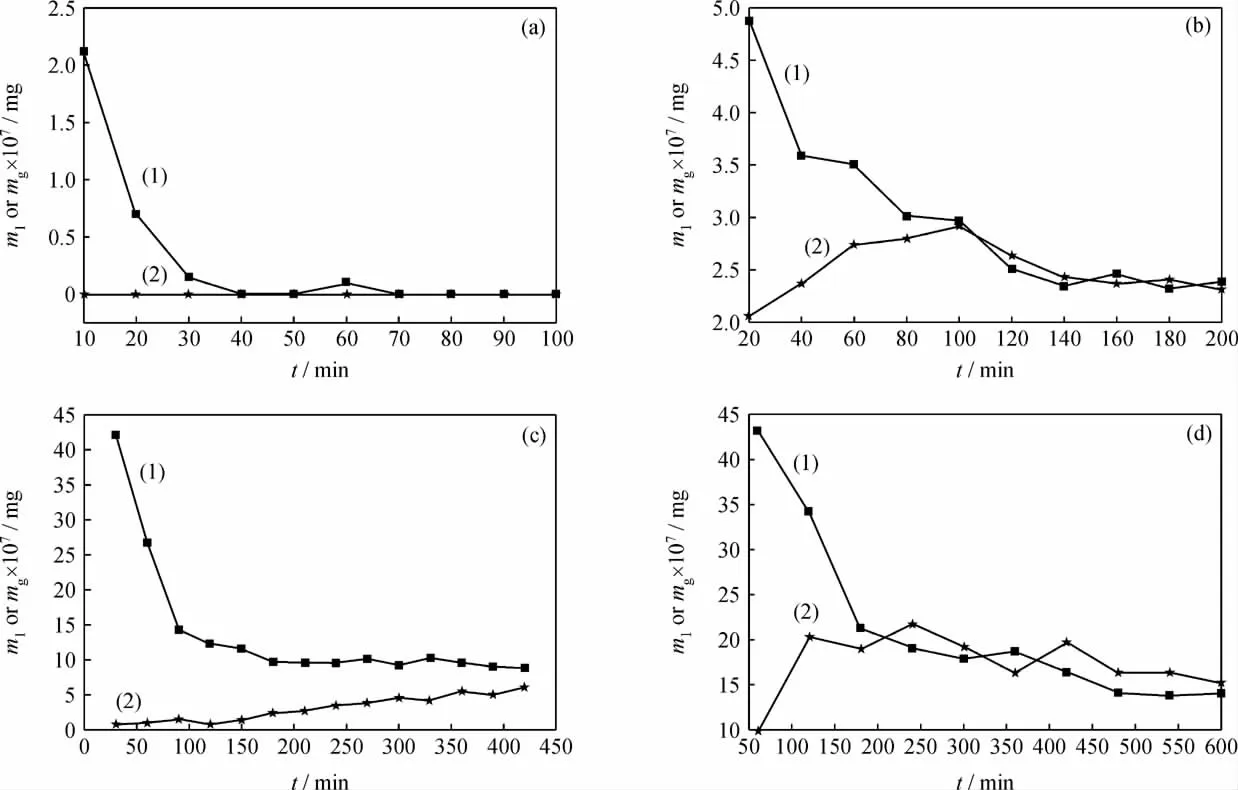
图7 4种吸附剂吸附的和出口气体中的硫元素质量随吸附时间(t)的变化Fig.7 Sulfur masses of adsorbed on four adsorbents and outlet gas vs t
3 结 论
(1)均匀共沉淀法制备的NiO-ZnO复合氧化物吸附剂具有较大的比表面积和孔体积,且粒径小,在16nm以内。预还原有利于改善吸附剂的脱硫性能,最佳反应吸附脱硫的温度和压力分别为673K、1.0MPa。
(2)模拟油中的各种组分对吸附剂脱硫性能的影响各不相同,环烷烃、芳烃的存在对吸附剂脱硫性能没有影响,烯烃的存在会占用一部分吸附剂的活性位,与噻吩发生竞争吸附,但影响不是很大。最优条件下,与不含烯烃的模拟油A相比,对含有烯烃的模拟油B进行吸附脱硫的脱硫率为90%时,吸附剂的硫容仅从212mg/g降为175mg/g。
(3)在脱除油品中噻吩的过程中,Ni/ZnO中的Ni与ZnO之间存在协同作用;脱硫过程分两步,即噻吩先在Ni原子上进行氢解生成H2S,然后生成的H2S快速与ZnO结合生成ZnS。Ni/ZnO吸附剂失活的主要原因是NiSx、ZnS和积炭的生成。这些物质在高温下很容易与空气中的氧发生作用而除去,因此只需要简单方法就可以使失活的Ni/ZnO吸附剂再生,且再生后的吸附剂的脱硫性能基本不变,可以重复使用,具有潜在的工业应用价值。
[1]安高军,周同娜,柴永明,等.轻质油品非加氢脱硫技术[J].化学进展,2007,19(9):1331-1344.(AN Gaojun,ZHOU Tongna,CHAI Yongming,et a1.Nonhydro-desulfurization technologies of light oil[J].Progress in Chemistry,2007,19(9):1331-1344.)
[2]许娟,刘宗社,夏俊玲.催化裂化汽油烷基化脱硫技术研究及进展[J].石油与天然气化工,2011,40(1):54-62.(XU Juan,LIU Zongshe,XIA Junling.Research and progress on alkylation of FCC gasoline desulfurization technology[J].Chemical Engineering of Oil & Gas,2011,40(1):54-62.)
[3]尹海燕,李春虎,王林学,等.NiO/γ-A1203吸附剂表面的噻吩反应吸附性能研究[J].中国海洋大学学报,2010,40(6):131-136.(YIN Haiyan,LI Chunhu,WANG Linxue,et al.Reactive adsorption of thiophene on NiO/γ-Al2O3adsorbent[J].Periodical of Ocean University of China,2010,40(6):131-136.)
[4]范景新,王刚,张文慧,等.Ni基吸附剂上催化裂化汽油反应吸附深度脱硫性能研究[J].现代化工,2009,29(1):207-209.(FAN Jingxin, WANG Gang,ZHANG Wenhui,et al.Deep desulfurization of FCC gasoline by reactive adsorption over nickel-based adsorbent[J].Modern Chemical Industry,2009,29(1):207-209.)
[5]张宴铭,胡廷平.ZnO/TiO2/γ-A1203吸附剂制备及其催化重汽油脱硫性能的评价[J].武汉工业学院学报,2010,29 (2):35-39.(ZHANG Yanming, HU Tingping.Preparation of adsorbent ZnO/TiO2/γ-A12O3for heavy FCC gasoline desulfurization[J].Journal of Wuhan Polytechnic University,2010,29(2):35-39.)
[6]杨静,石秋杰,李包友.ZnO基复合载体负载Ni催化剂催化噻吩加氢脱硫[J].南昌大学学报(理科版),2008,33(1):42-45 (YANG Jing,SHI Qiujie,LI Baoyou.Properties of Ni supported on ZnO-based mixed oxides for hydrodesulfurization of thiophene[J].Journal of Nanchang University(Natural Science),2008,33(1):42-45.)
[7]南军,于海斌,薛群山,等.低温固相法制备纳米氧化锌及其在脱硫中的应用[J].工业催化,2010,18(8):46-50.(NAN Jun,YU Haibin,XUE Qunshan,et al.Synthesis and desulfurization behaviors of nanosized ZnO sorbent prepared by low-temperature solid-state reaction[J].Industrial Catalysis,2010,18(8):46-50.)
[8]HUANG Lichun,WANG Guofu,QIN Zhangfeng,et al.A sulfur K-edge XANES study on the transfer of sulfur species in the reactive adsorption desulfurization of diesel oil over Ni/ZnO[J].Catalysis Communications,2010,11(7):592-596.
[9]FAN Jingxin,WANG Gang,SUN Yu,et al.Research on reactive adsorption desulfurization over Ni/ZnO-SiO2-Al2O3adsorbent in a fixed-fluidized bed reactor[J].Ind Eng Chem Res,2010,49(18):8450-8460.
[10]ZHANG Jingcheng,LIU Yunqi,TIAN Shuang,et al.Reactive adsorption of thiophene on Ni/ZnO adsorbent:Effect of ZnO textural structure on the desulfurization activity[J].Journal of Natural Gas Chemistry,2010,19(3):327-332.
[11]RAMIREZ-VERDUZCO L F,MURRIETA-GUEVARA F,GARCIA-GUTIERREZ J L,et al.Desulfurization of middle distillates by oxidation and extraction process[J].Petroleum Science and Technology,2004,22(1-2):129-139.
[12]HE Y,LUO W,WANG Y,et al.Removing sulfur or nitrogen containing compound in gasoline and diesel fuel using oxidation and extraction method in ion liquid at room temperature:CN,TW200619370-A[P].2006-06-16.
[13]ZHAO Changwei,LI Jiding,CHEN Jian,et al.Separation of sulfur/gasoline mixture with polydimethylsiloxane/polyetherimide composite membranes by pervaporation[J].Chinese Journal of Chemical Engineering,2009,17(4):707-710.
[14]MEHRAN S, AMARJEET B, ARGYRIOS M.Biodesulfurization of refractory organic sulfur compounds in fossil fuels[J].Biotechnology Advances,2007,25(6):570-596.
[15]闫波,李琳琳,邵纯红,等.常温纳米ZnO脱硫剂制备方法的研究及进展[J].黑龙江大学自然科学学报,2006,23(2):163-167.(YAN Bo,LI Linlin,SHAO Chunhong,et al.Studies and progress in preparation methods of nanometer ZnO desulfurizer used at ambient temperature [J]. Journal of Natural Science of Heilongjiang Universit,2006,23(2):163-167.)
[16]韩春玉.微库仑法在汽油吸附脱硫中的应用[J].现代化工,2010,39(1):5-10(HAN Chunyu.Application of the micro-coulometry in adsorptive desulfurization of gasoline[J].Contemporary Chemical Industry,2010,39(1):5-10.)
[17]HUANG Lichun,QIN Zhangfeng,WANG Guofu,et al.A detailed study on the negative effect of residual sodium on the performance of Ni/ZnO adsorbent for diesel fuel desulfurization[J].Ind Eng Chem Res,2010,49(10):4670-4675.
[18]AGUINAGA A,MONTES M,ASUA J M.Effect of the preparation on the initial toxicity of supported nickel catalysts deactivated by thiophene[J].Journal of Chemical Technology and Biotechnology,1991,52(3):369-381.
[19]ANDREY R,IGOR B,JEAN-PIERRE B.Reactive adsorption of thiophene on Ni/ZnO:Role of hydrogen pretreatment and nature of the rate determining step[J].Applied Catalysis B:Environmental,2008,84(3):766-772.
[20]刘晓钰,郭平均,周功兵,等.焙烧温度对Cu/ZnO水煤气变换催化剂开停循环性能的影响[J].化学学报,2010,68 (24):2523-2528.(LIU Xiaoyu, GUO Pingjun,ZHOU Gongbing,et al.Cu/ZnO water-gas shift catalysts calcined at different temperatures for shutdown/start-up operation [J]. Acta Chimica Sinica,2010,68(24):2523-2528.)
[21]徐文清,熊纯清,周广林,等.Ni/ZnO吸附剂脱除催化裂化汽油中的硫[J].石油学报(石油加工),2008,24(6):739-743.(XU Wenqing,XIONG Chunqing,ZHOU Guanglin,et al.Removal of sulfur from FCC gasoline by using Ni/ZnO as adsorbent[J].Acta Petrolei Sinica(Petroleum Processing Section),2008,24(6):739-743.)
[22]宋华,孙兴龙,王园园,等.AgY吸附剂的吸附脱硫性能及竞争吸附研究[J].化学反应工程与工艺,2011,27(3):230-234.(SONG Hua,SUN Xinglong,WANG Yuanyuan,et al.Performance of adsorptive desulfurization and competitive adsorption over AgY zeolites[J].Chemical Reaction Engineering and Technology,2011,27(3):230-234.)
[23]BEZVERKHYY I,SAFONOVA O V,AFANASIEV P,et al.Reaction between thiophene and Ni nanoparticles supported on SiO2or ZnO:In situ synchrotron X-ray diffraction study[J].J Phys Chem C,2009,113(39):17064-17069.

