氢化可的松对酮康唑经大鼠皮肤透过性的影响
苏碧雅,李国锋,熊璐琪,赵博欣
(南方医科大学南方医院药学部,广东广州 510515)
糖皮质激素类药物能有效防治皮肤炎症[1],但是糖皮质激素的滥用问题已经引起广泛关注,长期使用会引起皮肤组织学的变化,皮肤变薄是长期用药产生的副反应之一[2],皮肤细胞培养实验中,在培养基中加入糖皮质激素14 d后,可引起表皮层细胞减少,同时观察到皮肤萎缩,皮肤表皮层变薄,角质细胞增殖受到抑制,真皮层胶原蛋白合成量减少[3]。目前受到广泛关注的是糖皮质激素长期使用后引起皮肤改变及其机制,尚未见糖皮质激素经皮给药后引起的组织学改变对其他药物经皮透过影响方面的研究,未见关于糖皮质激素类药物和其他经皮给药制剂联合使用时相互作用的研究。本文选择了氢化可的松这种代表性的糖皮质激素进行了这方面的研究。
1978年口服酮康唑片剂应用于临床,1981年2%酮康唑乳膏上市[4]。酮康唑具有广泛的药理学作用,有多种适应证,但酮康唑具有明显的肝脏毒性[5],口服给药后肝脏毒性明显,所以局部体表真菌感染一般会选择外用酮康唑。因此,本文在评价正常皮肤和使用氢化可的松皮肤两周后大鼠皮肤透过性差异实验中,选择了酮康唑这种常用的抗真菌药物作为评价药物。
1 仪器与试剂
1.1 仪器 日本岛津LC-20A高效液相色谱仪,SPD-20AT检测器;TK-20A型药物透皮扩散试验仪(上海锴凯科技贸易有限公司);Thermo Scientific Sorvall Legend Mach 1.6/R台式离心机(上海托莫斯科学仪器有限公司);PB110S电子天平(德国Sartorins公司);HWS-26型电热恒温水浴锅(上海一恒科技有限公司);松下电动剃毛刀等。
1.2 试剂 酮康唑对照品(中检所,批号100294-200602),酮康唑原料药(纯度≥99%,广州越迪化工有限公司分装),氢化可的松对照品(Sigma公司),氢化可的松原料药 (纯度≥99.3%,深圳市益飞商贸有限公司)。高效液相试剂甲醇为色谱纯,水为双蒸去离子水,乳膏基质辅料等其他试剂均为分析纯。
1.3 动物 正常SPF级♂ Wistar大鼠,体质量(250±10)g,由南方医科大学实验动物中心提供,合格证号为SCXK(粤)2006-0015。实验期间给予普通饲料和清洁饮水。
2 方法
2.1 氢化可的松乳膏剂的配制(1%含药量) 处方:氢化可的松原料药10 g,硬脂酸100 g,单硬脂酸甘油酯50 g,液体石蜡140 ml,白凡士林50 g,甘油50 g,十二烷基硫酸钠(SDS)1 g,三乙醇胺3.5 g,蒸馏水616 ml。配制步骤:将上述药物水相和油相分别加热至80℃(水相温度略高于油相),将水相缓缓加入油相中,按同一方向随加随搅拌,继续搅拌冷却至60℃左右时,将此混合液逐步加入到氢化可的松的甘油糊状物中,仍按同一方向随加随搅拌,冷凝后停止搅拌,即得,共制成1 000 g。
2.2 动物实验 12只Wistar♂大鼠,体质量(250±10)g,随机分为2组,每组6只,分别为对照组(Control group)和氢化可的松组(HC group)。大鼠固定后,用剃须刀将腹部毛剃除干净,两组分别涂空白乳膏或氢化可的松乳膏(剂量为2 g·d-1),给药面积约6 cm2(2 cm×3 cm),涂药后大鼠仰躺固定以防大鼠舔食乳膏,2 h后用脱脂棉蘸生理盐水除去腹部残留乳膏,清洁腹部皮肤,放回鼠笼,每天给药1次,连续给药2周。
2.3 酮康唑经氢化可的松组和空白乳膏组大鼠皮肤体外透皮实验
2.3.1 酮康唑乳膏的制备(2%含药量) 处方:酮康唑原料药20 g,硬脂酸100 g,单硬脂酸甘油酯50 g,液体石蜡 140 ml,白凡士林 50 g,甘油 50 g,十二烷基硫酸钠(SDS)1 g,三乙醇胺3.5 g,蒸馏水616 ml。配制步骤:将上述药物水相和油相分别加热至80℃(水相温度略高于油相),将水相缓缓加入油相中,按同一方向随加随搅拌,继续搅拌冷却至60℃左右时,将此混合液逐步加入到酮康唑的甘油糊状物中,仍按同一方向随加随搅拌,冷凝时停止搅拌,即得,共制成1 000 g。
2.3.2 体外Franz实验 取给药2周后的大鼠,用10%水合氯醛腹腔注射麻醉(剂量30 mg·kg-1),用脱脂棉沾生理盐水擦干净皮肤,取下鼠皮,放血处死动物。小心的用沾有生理盐水的脱脂棉除去皮下脂肪待用。取已处理好的大鼠腹部皮肤固定在扩散池中,透皮扩散有效内径为1.8 cm,接收室体积为6.5 ml,接收液为10%乙醇PBS(pH 7.4)。整个实验过程(37.0±0.2)℃水浴,300 r·min-1搅拌。分别称取酮康唑乳膏或空白乳膏(空白乳膏透过液用于方法学专属性考察和酮康唑标准曲线的配制)2 g加于供应室中,供应室上用保鲜膜封口,防止水分蒸发。分别于 0.5、1、2、4、6、8、12 和 24 h 取样 0.5 ml,同时补充相同体积相同温度的新鲜接收液。样品离心10 min(15 000 r·min-1),取上清液注入HPLC测定酮康唑的浓度。
2.4 酮康唑HPLC检测方法的建立
2.4.1 色谱条件 选用 ECOSIL C18色谱柱(5 μm,250×4.6 mmI.D.),流动相为甲醇 -0.02 mol·L-1磷酸二氢钾溶液(70∶30)(水相用0.01 mol·L-1的NaOH溶液调节pH到6.8),流速:1.0 ml·min-1,紫外检测波长235 nm,柱温35℃。
2.4.2 酮康唑对照品储备液配制 精密称定酮康唑标准品20 mg,置100 ml容量瓶中,加甲醇溶解并定容至刻度,即得质量浓度为200 mg·L-1的酮康唑甲醇储备液。
2.4.3 标准曲线绘制 将酮康唑对照品储备液逐一稀释(稀释溶剂为氢化可的松组皮肤给空白乳膏后的Franz透过液),得质量浓度分别为12.5、6.25、3.13、1.56、0.78、0.39、0.20、0.10、0.05 mg·L-1的标准品溶液,注入HPLC测定峰面积,得到标准曲线。
2.4.4 精密度试验 取12.5、3.13、0.10 mg·L-13个不同浓度的酮康唑标准品,每日重复测定3次,记录峰面积,连续3 d,计算日内精密度和日间精密度。
2.4.5 加样回收率实验 精密称取酮康唑细粉适量,按低、中、高3个标准加入到已知浓度的酮康唑标准品溶液中,超声5 min溶解后定容,过滤。测样品中酮康唑浓度,计算加样回收率,加样量见Tab 1。
2.5 酮康唑稳定性实验 酮康唑具有酰胺基和醚基结构,容易氧化变质[6],因此本实验做了稳定性研究。
2.5.1 氢化可的松用药后的皮肤对酮康唑稳定性的影响 取使用氢化可的松给药2周后的大鼠腹部皮肤3份,每份约6 cm2,分别加生理盐水多次研磨制成组织悬液,15 000 r·min-1离心15 min后取上清液,以该上清液为溶剂,配制12.5、3.13、0.10 mg·L-13个不同浓度的酮康唑溶液,每个浓度用不同皮肤悬液配3份,共9份,配制后0.5、12、24 h分别做HPLC检测,计算配制浓度和实测浓度的差异性。
2.5.2 酮康唑标准品稳定性研究 取12.5、3.13、0.10 mg·L-13个不同浓度的酮康唑标准品溶液分别于配制后第 0、2、4、6、8、12 和 24 h 测定酮康唑峰面积,计算RSD。
2.6 自制乳膏剂药物含量的测定
2.6.1 氢化可的松乳膏供试液的制备 精密称取氢化可的松乳膏2 g(相当于氢化可的松20 mg),置烧杯中,加甲醇约30 ml,在水浴上加热使溶解,再置冰水中冷却,滤过,滤液置100 ml容量瓶中,如此提取3次,滤液并入量瓶中,用甲醇稀释至刻度,摇匀,离心后注入液相色谱仪检测[7]。按上述方法配制3份样品,计算含量平均值和RSD。
2.6.2 酮康唑乳膏供试液的制备 酮康唑乳膏提取方法参照“2.6.1”,按上述方法配制3份样品,计算平均值和RSD。
2.7 统计学处理 实验结果采用SPSS 13.0软件进行统计。计量资料结果用±s表示。正常组与HC组大鼠皮肤渗透速率比较采用独立样本t检验(Independent-Sample T Test,2-tailed)。
3 结果
3.1 HPLC方法学考察
3.1.1 专属性 分别取空白乳膏皮肤透过液、酮康唑对照品溶液和8 h酮康唑乳膏皮肤透过液做HPLC检测,可见酮康唑保留时间约为9.5 min,分离良好(Fig 1)。

Fig 1 HPLC chromatograms of ketoconazole
3.1.2 线性范围 测定质量浓度分别为12.5、6.25、3.13、1.56、0.78、0.39、0.20、0.10、0.05 mg·L-1酮康唑溶液的峰面积,所得标准曲线回归方程为Y=3e-5X-0.3102(r2=0.9999),线性范围为0.05~12.5 mg·L-1,线性良好。
3.1.3 精密度 取12.5、3.13、0.10 mg·L-13个不同浓度的酮康唑标准品溶液,每日重复测定3次,记录峰面积,连续3 d,计算得日内精密度和日间精密度的RSD均<3.5%。
3.1.4 加样回收率实验 精密称取酮康唑细粉适量,按低、中、高3个标准加入到已知浓度的酮康唑溶液中,超声5 min溶解后用定容至刻度,过滤,做HPLC检测,结果见Tab 1。

Tab 1 The average recovery of ketoconazole(n=9)
3.2 酮康唑稳定性实验结果
3.2.1 氢化可的松用药后的皮肤对酮康唑稳定性的影响 计算得,9份样品(实测浓度/配制浓度)×100%的范围在95% ~105%之间,RSD<4.684%,这说明给药后皮肤中残留的氢化可的松和乳膏剂基质对酮康唑HPLC检测的干扰不影响检测。
3.2.2 酮康唑标准品稳定性研究 取12.5、3.13、0.10 mg·L-13个不同浓度的酮康唑标准品溶液分别于配制后第 0、2、4、6、8、12 和 24 h 测定酮康唑峰面积,计算所得RSD均<1.56%,表明供试品溶液在室温下稳定性良好。
3.3 自制氢化可的松乳膏和酮康唑乳膏质量检查结果
3.3.1 主药含量测定 自制氢化可的松乳膏剂中氢化可的松的平均含药量为0.92%,RSD为0.7%,自制酮康唑平均含药量为2.01%,RSD为3.2%。均符合药典规定的90%~110%标示量区间。
3.3.2 乳膏剂稳定性评价 称取1 g乳膏加2 ml水5 000 r·min-1离心10 min后无分层现象。乳膏置于4℃保存1个月后没有出现酸败和异味。
3.4 Franz实验结果 测得的样品药物浓度按下列公式计算单位面积的累计透过量(permeated A-mount quantity,Q)

方程式中V:接受池的体积;Cn:第n个取样点测得药物的浓度;A:有效扩散面积(本实验中为2.5434 cm2);Ci:第i(i≤n-1)个取样点测得的药物浓度。对各个时间点累计药物透过量进行线性回归,得回归方程,其斜率即为药物渗透速率(penetrating rate,PR,μg·h-1·cm-2)(Tab 2,Fig 2)。空白乳膏组的渗透速率约为氢化可的松组的两倍,两组渗透速率差异有显著性(P<0.01)。
Tab 2 The PR of ketoconazole through different group rats’skin(±s,n=6)
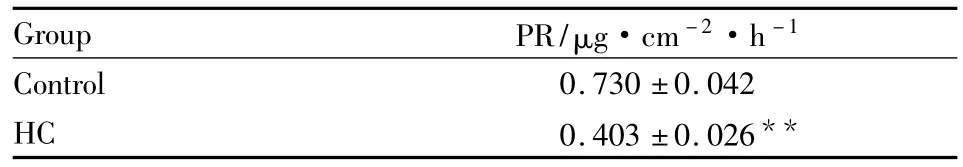
Tab 2 The PR of ketoconazole through different group rats’skin(±s,n=6)
**P<0.01 vs control group
Group PR/μg·cm-2·h -1 Control 0.730±0.042 HC 0.403±0.026**
4 讨论
在给药实验中,需要设置空白乳膏对照组,因此借鉴了文献中的处方,选用了自制HC乳膏剂,而非市售制剂,便于制作空白乳膏设立对照组进行比较。在体外透过实验中,需要建立皮肤透过液中酮康唑的HPLC检测方法,做专属性考察,故依据有关资料,自拟了配方,也选用了酮康唑自制乳膏,便于做空白对照。经质量考察发现自制乳膏质量合格,完全满足实验需要。
糖皮质激素类药物的副作用是经皮给药制剂研究中很受关注的一部分,很多研究者也从各方面证实了糖皮质激素类药物的各种不良反应及其产生机制,而较少关注糖皮质激素类药物引起的皮肤改变对合用药物(或皮质激素给药后使用药物)经皮透过的影响。
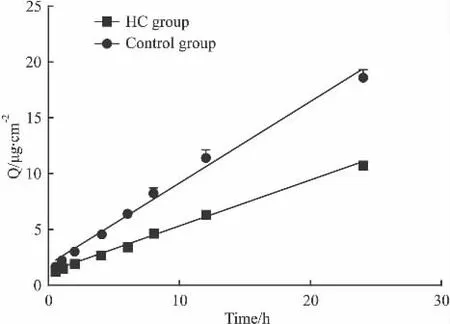
Fig 2 The ketoconazole permeated amount(Q)-time curve chart
本文初步证实糖皮质激素氢化可的松引起的皮肤改变会导致酮康唑经皮透过量减少、渗透速率降低。查阅文献表明为国内外首次报道。一般认为,长期使用糖皮质激素后,其引起的皮肤变薄、脂肪萎缩可能造成透过量的增加,但我们发现了与预测相反的结果,有必要进一步进行体内实验(如腹部给药后取血检测药动学参数,以及在体微透析实验等)来验证这种结果,以及通过细胞培养实验来分析可能的机制等,有关工作我们正在进行中。
选用常用的抗真菌药酮康唑乳膏作为实验制剂,得到了有差异的结论,这说明糖皮质激素类药物经皮给药一段时间引起的皮肤组织学改变确实能影响其他药物的经皮渗透和吸收过程。但本实验只采用了酮康唑作为实验药物进行了考察,糖皮质激素类药物经皮给药后引起的皮肤组织学改变对其他经皮给药制剂透过性的影响有待选定更多实验制剂后做进一步考察,以证实这种影响是否具有普遍性。
连续使用氢化可的松乳膏2周后引起的皮肤改变会导致酮康唑经皮透过量的减少,渗透速率降低。患者在长期使用氢化可的松乳膏后再使用酮康唑经皮给药制剂时可能需考虑调整剂量,以保证药物疗效。
[1]李 鑫,杨 蕊,臧 强,等.糖皮质激素的药理作用机制研究进展[J].国际药学研究杂志,2009,36(1):27-30.
[1]Li X,Yang R,Zang Q.Pharmacological actions of glucocorticoids:progress in mechanisms[J].Int J Pharm Res,2009,36(1):27-30.
[2]李林峰.肾上腺糖皮质激素类药物在皮肤科的应用[M].北京:北京大学医学出版社,2004:71.
[2]Li L F.The Application of glucocorticoid drugs in dermatology[M].Beijing:Peking University Medical Press,2004:71.
[3]Zöller N N,Kippenberger S,Thaci D,et al.Evaluation of beneficial and adverse effects of glucocorticoids on a newly developed fullthickness skin model[J].Toxicol In Vitro,2008,22(3):747-59.
[4]王爱平,李若瑜.2%酮康唑乳膏在皮肤科疾病中的应用[J].中国真菌学杂志,2010,5(3):179-83.
[4]Wang A P,Li R Y.The application of 2%ketoconazole cream in dermatology[J].Chin J Mycol,2010,5(3):179-83.
[5]逄晓云,刘晓琰,沈金芳.酮康唑致严重肝损1例[J].中国医院药学杂志,2009,29(18):1579.
[5]Pang X Y,Liu X Y,Shen J F.A case of serious liver injury caused by Ketoconazole[J].Chin J Hospital Pharm,2009,29(18):1579.
[6]邢东志,邢 晗,宝 玲.复方酮康唑软膏的处方设计试验[J].中国现代药物应用,2010,4(16):165.
[6]Xing D Z,Xing H,Bao L.The formulation design of compound ketoconazole ointment[J].Chin J Mod Drug Applic,2010,4(16):165.
[7]郑一美,骆光亘.不同乳化剂对酮康唑乳膏含量测定影响的研究[J].中国现代应用药学杂志,2008,25(7):653-4.
[7]Zheng Y M,Luo G G.Study on determination of ketoconazole with different emulsifier in its cream[J].Chin J Mod Appl Pharm,2008,25(7):653-4.

