UPLC法测定酮康唑制剂中酮康唑的含量
庞 滂杨晓莉牛建功
(1 西安杨森制药有限公司,陕西 西安 710043;2 陕西省食品药品检验所,陕西 西安 710065)
UPLC法测定酮康唑制剂中酮康唑的含量
庞 滂1杨晓莉2牛建功1
(1 西安杨森制药有限公司,陕西 西安 710043;2 陕西省食品药品检验所,陕西 西安 710065)
目的建立酮康唑系列不同制剂产品含量测定的UPLC方法。方法采用Waters ACQUITY UPLC BEH C18色谱柱(2.1×100 mm,1.7 µm),0.34%硫酸四丁基氢铵溶液-乙腈为流动相,梯度洗脱,流速为0.3 mL/min,检测波长为230 nm,柱温40 ℃。结果酮康唑对照品溶液线性范围为:0.1~150 µg/mL,r=0.9999(n=9);片剂:回收率为98.33%~99.80%,RSD为0.43%(n=6);乳膏剂:回收率为99.45%~102.24%,RSD为1.21%(n=6);2%洗剂:回收率为98.61%~101.24%,RSD为1.08%(n=6)。结论UPLC法简便、灵敏、准确、重复性好,可用于酮康唑系列不同制剂产品的质量控制。
酮康唑;超高效液相色谱法;含量
酮康唑系列产品主要包括酮康唑片剂、酮康唑乳膏和酮康唑洗剂,均为抗真菌类药物,其主要成分都为酮康唑[1-3]。采用超高效液相色谱法(UPLC)同时测定不同制剂的酮康唑产品中酮康唑的含量,结果满意,该法可用于控制制剂的质量。
1 仪器与试药
Waters ACQUITY型UPLC,酮康唑对照品(中国药品生物制品检定所,批号为100294-200602,校正因子:0.999);硫酸四丁基氢铵(TBAHS,分析纯);乙腈(色谱纯);酮康唑片剂(西安杨森制药有限公司,批号为110902514);酮康唑乳膏(西安杨森制药有限公司,批号为111208542);酮康唑洗剂(西安杨森制药有限公司,批号为111116945)。
2 方法与结果
2.1 色谱条件。色谱柱:Waters ACQUITY UPLC BEH C18色谱柱(2.1× 100 mm,1.7 µm);流动相:0.34%硫酸四丁基氢铵溶液-乙腈为流动相,梯度洗脱(梯度表见表1);柱温:40 ℃;流速:0.3 mL/min;检测波长:230 nm;进样量:5 µL。
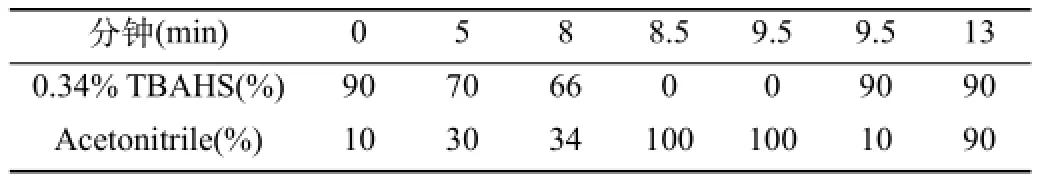
表1 梯度表
2.2 溶液制备:取酮康唑对照品适量,精密称定,加甲醇制成100 µg/mL的溶液作为对照品溶液。分别取酮康唑片剂、乳膏剂和洗剂适量,按规格用甲醇制成100 µg/mL的溶液作为酮康唑制剂的供试品溶液。按照处方及工艺制备不含酮康唑的空白样品适量,照上述方法制备成空白辅料溶液。
2.3 方法学考察
2.3.1 专属性试验:阴性对照品溶液测定结果表明,在与酮康唑保留时间相应位置上无吸收,表明其他成分对本品的酮康唑含量测定无干扰,方法专属性良好(图1)。
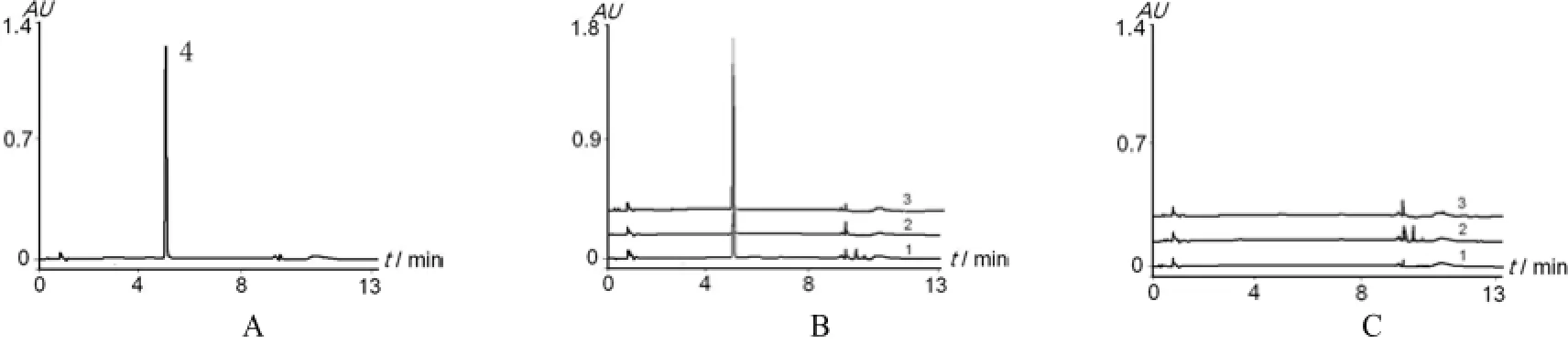
图1 超高效液相色谱图[1. 片剂(Tablet);2. 乳膏剂(Cream);3. 2%洗剂(2% Lotion);4. 酮康唑(Ketoconazole);A.对照品(Reference substance);B. 供试品(sample);C. 空白辅料(Blank)]
2.3.2 线性关系考察:用甲醇准确配制1 mL中含酮康唑1.25 mg的储备液,然后用甲醇逐步稀释至150、125、100、50、25、10、5、1、0.1 µg/mL系列溶液,进样量5 µL。按照上述色谱条件测定峰面积,以峰面积对溶液质量浓度进行线性回归,得回归方程Y=3×107X+6540.1,r=0.9999(n=9)。结果表明,酮康唑质量浓度在0.1~150 µg/mL与峰面积线性关系良好。
2.3.3 重复性试验:分别取片剂、乳膏、洗剂的供试品溶液各6份,依法测定。测得RSD分别为:片剂0.20%(n=6);乳膏剂:0.29%(n=6);2%洗剂:0.69%(n=6),表明方法重复性良好。
2.3.4 稳定性试验:分别取同一份片剂、乳膏、洗剂的供试品溶液,分别在制备后0、2、4、6、8 h时进样测定。测得RSD分别为:片剂0.43%;乳膏剂:0.17%;2%洗剂:0.66%,表明供试品溶液在8 h内基本稳定。
2.3.5 中间精密度试验:分别取片剂、乳膏、洗剂供试品溶液各6份,分别由A、B、C 3人分别在不同的时间用同一台设备,依法测定。测得RSD分别为:片剂0.47%;乳膏剂:0.68%;2%洗剂:0.73%,表明中间精密度良好。
2.3.6 回收率试验:分别取片剂、乳膏、洗剂空白样品各6份,分别精密加入线性储备液6、4、2 mL,加甲醇稀释至刻度,依法测定。测得回收率分别为:片剂为98.33%~99.80%,RSD为0.43%(n=6);乳膏剂为99.45%~102.24%,RSD为1.21%(n=6);洗剂为98.61%~101.24%,RSD为1.08%(n=6)。
2.3.7 含量测定:取“2.2溶液制备”下对照品溶液和供试品溶液,按上述色谱条件进样5 µL,按外标法计算其标示含量,测得结果为:片剂97.8%,RSD为0.2%(n=6);乳膏剂100.4%,RSD为0.3%(n=6);和2%洗剂103.4%,RSD为0.7%(n=6)。
3 讨 论
3.1 流动相的选择:对流动相的种类和比例进行了系列试验,结果表明选用0.34%硫酸四丁基氢铵溶液和乙腈的梯度比例洗脱最佳。
3.2 检测波长和柱温的选择:经试验表明,酮康唑在230 nm处峰形最好,且在柱温40 ℃时分离度和峰形最佳。
3.3 辅料的影响:专属性试验结果表明,空白辅料对酮康唑制剂的含量测定无影响。
实验表明,采用UPLC方法对酮康唑不同制剂进行含量测定,快速、简便、灵敏、重现性好,利于更好地控制产品质量。
[1]国家药典委员会.中国药典(二部)[M].2010版.北京:中国科技医药出版社,2010:679.
[2]李华侃.茜素红荷移分光光度法测定酮康唑含量[J].理化检验(化学分册),2013,49(4):479-480.
[3]张艳红,孙丽建,李强,等.高效液相色谱法测定缓释微球中酮康唑的含量[J].黑龙江大学工程学报,2012,3(3):42-44.
R917
B
1671-8194(2015)03-0058-02

