阿德福韦酯对拉米夫定耐药慢性乙型肝炎的疗效观察
曹 荣 胡旭东 程海林 柏 涛 黄少平 夏 冰 甘洪颖
武汉市医疗救治中心肝病科(湖北武汉,430023)
拉米夫定 (LAM)是最早用于治疗慢性乙型肝炎 (CHB)的核苷类似物,能有效抑制乙型肝炎病毒 (HBV)的复制而广泛应用于临床,但其所带来的YMDD耐药变异问题也日益突出。我们采取单用或联用阿德福韦酯治疗拉米夫定YMDD耐药的CHB患者,取得了一定的效果,现报道如下。
1 资料与方法
1.1 一般资料 我院2008年5月-2010年5月门诊和住院收治的拉米夫定YMDD变异耐药的CHB患者80例,男49例,女31例,年龄19~61(39.5±9.8)岁。临床诊断符合2000年 (西安)全国病毒性肝炎和肝病学术会议修订的病毒性肝炎防治方案的标准[1],且符合下列入选条件:治疗前连续服用LAM至少1年,HBV DNA≥105copies/ml,血清丙氨酸氨基转移酶 (ALT)超过正常值上限 (ULN)但≤10×ULN,经检测发现YMDD变异 (采用特异性引物体外扩增技术检测,试剂盒由杭州博康公司提供),排除其他肝病、肝硬化或肝癌者。将80例患者随机分为治疗组40例和对照组40例,两组患者在性别、年龄、症状及治疗前实验室检查结果方面差异无显著性意义 (P>0.05)。见表1。
1.2 治疗方法 治疗组40例患者继续给予拉米夫定 (葛兰素史克公司)100 mg/次口服,1次/d,同时给予阿德福韦酯(贺维力,葛兰素史克公司)10mg/次口服,1次/d,治疗72周;对照组40例患者单用阿德福韦酯10mg/次口服,1次/d,治疗72周。
1.3 实验室检查 采集两组患者治疗前、治疗12周、24周、48周、72周时的血液标本,分别检测HBV DNA定量(罗氏公司Lightcycle PCR仪及其试剂,HBV DNA<1.0×103拷贝/ml为检测下限)、ALT(采用贝克曼全自动生化分析仪检测)及HBeAg/HBeAb(采用Abbott酶联免疫吸附法)。并观察血常规、尿常规、肾功能及药物不良反应。

表1 两组患者的基线值比较
1.4 统计学方法 率的比较采用卡方检验,计量资料的比较采用t检验。
2 结果
2.1 两组患者治疗不同时段血清HBV DNA阴转率的比较两组在12、24、48周HBV DNA转阴率均呈逐步提高 (P>0.05),而在72周时治疗组明显高于对照组且差异有统计学意义 (P<0.05)。提示单用阿德福韦酯或与拉米夫定联用,均对病毒复制有较好抑制作用,但随着时间延长两药联用效果更好。治疗后两组HBV DNA转阴情况 (HBV DNA<1.0×103拷贝/ml)见表2。

表2 两组患者治疗不同时段HBV DNA阴转情况比较
2.2 两组患者治疗不同时段血清ALT复常率的比较 两组ALT复常率在12、24、48周比较差异无统计学意义 (P>0.05)。72周时两组比较差异有统计学意义 (P<0.05),见表3。
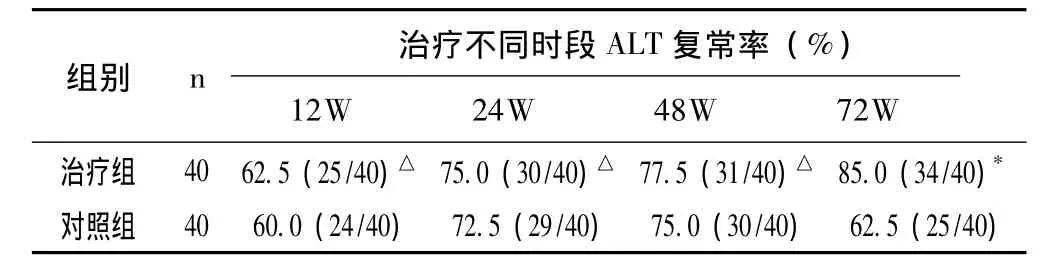
表3 两组患者ALT复常情况比较 (%)
2.3 两组患者治疗不同时段HBeAg阴转率及HBeAg/HBeAb血清学转换率比较 两组治疗12、24、48、72周时HBeAg阴转率及HBeAg/HBeAb血清学转换率无统计学差异。见表4。
2.4 阿德福韦酯耐药情况分析 对照组中5例患者于72周出现病毒学突破 (均伴有ALT升高,HBV DNA定量出现反跳现象),经检测2例为rtA181V突变,1例为rtA181T突变,2例为rtN236T突变;阿德福韦酯耐药发生率为12.5%(5/40),5例患者在阿德福韦酯治疗期间HBV DNA水平均未降至检测限以下。治疗组中无患者出现病毒学突破。两组间的阿德福韦酯耐药发生率差异有显著性意义 (P<0.05)。
2.5 不良反应 治疗期间两组患者耐受性良好,无患者因血清肌酐升高或其他肾功能损害而停药,均未发生严重不良事件。
3 讨论
拉米夫定是第一个被批准用于抗HBV的核苷类似物,但长期使用易导致YMDD变异而耐药,从而导致乙型肝炎的复发。阿德福韦酯与拉米夫定同为核苷类似物,但二者的作用机制不同,由于阿德福韦酯作用于DNA多聚酶的不同靶点,其抗病毒作用位点不同于拉米夫定[2]。目前已证实阿德福韦酯与拉米夫定不具有交叉耐药性,并对HBV野生株和YMDD变异株均有抑制作用[3],而成为拉米夫定耐药后首选药物。
阿德福韦酯对YMDD变异的病毒有较强的抑制作用[4],但对野毒株作用较弱[5];LAM对YMDD变异株无效,但LAM耐药后对野生病毒株仍敏感[6]。本研究结果提示,单用阿德福韦酯或与拉米夫定联用,均对抑制病毒复制及生化学改善有较好作用,但随时间延长,在72周时两药联用HBV DNA转阴率及ALT复常率明显高于对照组 (P<0.05),其原因可能是在停用拉米夫定单用阿德福韦酯过程中,HBV野生株大量复制,耐药株会逐渐被野毒株所取代,而单用阿德福韦酯对野生株作用相对较弱,不能有效抑制病毒的复制所致。另外,可能随疗程延长,出现新的针对阿德福韦酯耐药株导致再次出现病毒学突破。对照组中有5例患者于72周出现病毒学突破 (均伴有ALT升高,HBV DNA定量出现反跳现象),经检测两例为rtA181V突变,1例为rtA181T突变,两例为rtN236T突变,阿德福韦酯耐药发生率为12.5%(5/40)。而治疗组中无患者出现病毒学突破0%(0/40),两组间比较差异有显著性意义 (P<0.05)。Yeon等对67例拉米夫定耐药患者研究发现,阿德福韦酯单药治疗易出现对阿德福韦酯耐药,阿德福韦酯的耐药变异率在第1年为6.4%,第2年为25.4%[7]。另有研究发现,拉米夫定耐药患者加用阿德福韦酯,可提高疗效,降低对阿德福韦酯耐药发生率[8]。多项临床研究决定了目前新的观点认为二者联合长期使用可以明显降低耐药出现[9,10]。
综上所述,单用阿德福韦酯或与拉米夫定联用,均对抑制YMDD变异耐药的CHB患者HBV复制及生化学改善有较好的作用,但随着时间延长,拉米夫定与阿德福韦酯长期联合应用不仅可提高拉米夫定耐药患者病毒学及生化学疗效,且可减少病毒突破及生化反弹,减少耐药发生,安全性良好,效果优于阿德福韦酯单药治疗。

表4 两组患者治疗后HBeAg阴转率及HBeAg/HBeAb血清学转换率比较
[1]中华医学会传染病与寄生虫病学分会、肝病学分会.病毒性肝炎的诊断标准[J].中西医结合肝病杂志,2001,11(1):56-60.
[2]王宇明,陈耀凯,张大志,等.阿德福韦酯治疗拉米夫定耐药慢性乙型肝炎的临床研究[J].中华肝脏病杂志,2006,14(1):803-805.
[3]BRUNELLEM N,JACQUARD A C,PICBOUD C,et al.Suscep tibility to antivirals of a human HBV strain with mutations conferring resistance to both lamivudine and adefovir [J].Hepatology,2005,41(7):1391-1398.
[4]BAKER DE.Adefovir dipivoxil:focus onits use in the treatment of chronic hepatitisB [J].Rev Gastroenterol Disord,2005,5(2):89-100.
[5]CHEN CJ,YANG HI,SU J,et al.Risk of hepatocellular carcinomaacross a biological gradient of Serum hepatitis B virus DNA level[J].JAMA,2006,295(1):65-73.
[6]马明,刘新钰,张汗荣,等.YMDD变异后继续使用及停用拉米夫定的临床转归分析 [J].中华传染病杂志,2005,23(2):132-134.
[7]YEON JE,YOO W,HONG SP,et al.Resistance to adeforir dipivoxil in lamivudine resistant chronic hepatitisB patients treated with adeforir dipivoxil[J].Cut,2006,55(10):1488-1495.
[8]MA RCELLIN P,ASSLAH T,BOYER N.Treatment ofchronic hepatitis B [J].J Viral Hepat,2005,12(4):333-345.
[9]MOON J H ,CHO M ,YOON K T,et al.The efficacy of adefovir dipivoxil monot herapy and the incidence of genotypic resistance to ade2fovir dipivoxil in patients with lamivudine-resistant chronic hepatitis B infection [J].Korean J Hepatol.2008,14(7):503-512.
[10]LAMPERTICO P,VIGANòM ,MANENTI E,et al.Low resistance to adefovir combined with lamivudine:a 3-year study of 145 lamivudine-resistant hepatitis B patients[J].Gastroenterology,2007,133(10):1445-1451.

