高效液相色谱法测定氨基酸口服液中L-色氨酸的不确定度评定*
保志娟,周瑾艳,杨亦
(广东省计量科学研究院,广东 510405)
高效液相色谱法测定氨基酸口服液中L-色氨酸的不确定度评定*
保志娟,周瑾艳,杨亦
(广东省计量科学研究院,广东 510405)
采用高效液相色谱法测定氨基酸口服液中L-色氨酸的含量,对测量结果的不确定度进行评定。结果表明,标准曲线校准和测量重复性是测量过程中不确定度的主要来源,其中标准曲线校准对合成不确定度的影响最大。当氨基酸口服液中L-色氨酸的测定结果为8.8 μg/mL时,其扩展不确定度为1.1 μg/mL。
L-色氨酸;高效液相色谱法;氨基酸口服液;测量不确定度
色氨酸通常以游离或结合态广泛存在于生物体中,是人类和动物必需的8种氨基酸之一。人体不能制造它,而必须从膳食中摄取[1,2]。色氨酸对生物的生长和氮平衡非常重要,色氨酸缺乏或代谢错误会引起一系列疾病;另一方面,色氨酸也可作为疾病的治疗药物。随着人们对健康的重视,各种氨基酸保健食品越来越被大众熟悉和接受。
准确测定保健食品中的色氨酸含量,对评价保健品质量、指导用户选购意义重大。笔者利用液相色谱二极管阵列法定量测定了氨基酸口服液中L-色氨酸的含量,并根据 《化学分析中不确定度的评估指南》[3]和《测量不确定度评定与表示》[4],对测量的不确定度进行了评定。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:Alliance 2675型,配2998型二极管阵列检测器,美国Waters 公司;
L-色氨酸纯度标准物质:GBW(E) 100260,纯度为(99.7±0.7)%,广东省计量科学研究院;
L-色氨酸纯度标准储备液:100 μg/mL,精密称取约5.00 mg L-色氨酸标准品,用水溶解并准确定容至50 mL,于4℃冰箱中保存;
甲醇:色谱纯;
水:超纯水,电阻率为18.2 MΩ·cm;
氨基酸口服液:10 mL/支,市售。
1.2 仪器工作条件
色谱柱:Waters C18柱(250 mm×4.6 mm,5 μm);柱温:35℃;进样量:10 μL;检测波长:280 nm;流动相:甲醇(A)–水(B);梯度洗脱程序:流动相A初始值体积分数为30%(保持2 min),2~10 min内A体积分数由30%变化为70%,10~14 min,A体积分数由70%变化至40%,14~15 min,B由体积分数40%变化至30%;流速:1.0 mL/min。环境温度:(20±5)℃;相对湿度:不大于70%。
1.3 实验步骤
取市售氨基酸口服液1支,摇匀,准确移取1.0 mL,置于10 mL容量瓶中定容,用0.45μm滤膜过滤,上机测试,用外标曲线法定量。
2 测量不确定度来源
高效液相色谱法测定氨基酸口服液中L-色氨酸含量的不确定度主要来源:L-色氨酸纯度标准储备液的配制、标准曲线校准、样品处理、色谱峰面积测量及重复性测量。
3 数学模型
氨基酸口服液中L-色氨酸的浓度可表示为:

式中:csp——样品溶液中L-色氨酸的质量浓度,µg/mL;
Ax——样品溶液中L-色氨酸的色谱峰面积,μV·s;
c0——标准工作液中L-色氨酸的质量体积浓
度,µg/mL;
Vsp——氨基酸口服液的定容体积,mL;
A0——标准工作液中L-色氨酸的色谱峰面积,μV·s;
4 测量不确定度评估[3,4]
4.1 标准曲线校准引入的不确定度
分别取50,100,300,500 μL及1.0,2.0 mL的L-色氨酸标准溶液,用水定容,摇匀,配制成不同浓度的标准工作液,按1.2仪器工作条件进行分析。
对以上6种浓度的L-色氨酸系列标准溶液分别测定6次,得到相应的峰面积,并计算峰面积平均值,测定结果列于表1。
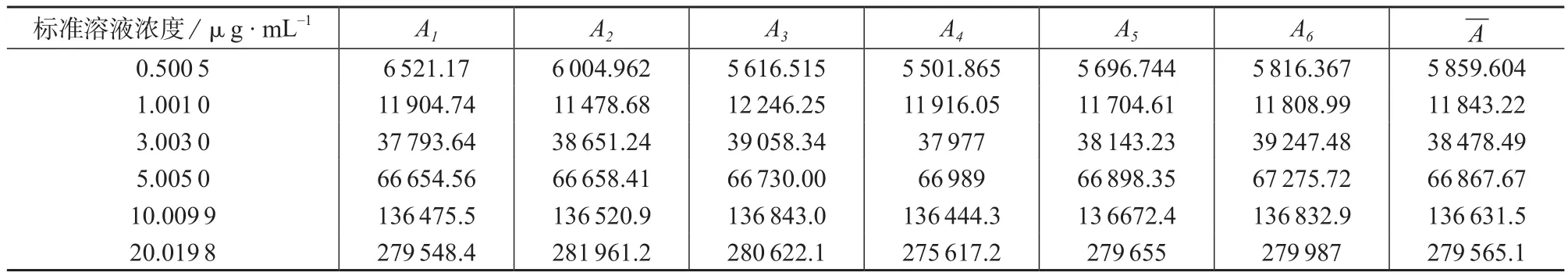
表1 系列标准溶液的色谱峰面积
用最小二乘法拟合标准溶液浓度–峰面积校准曲线,得线性回归方程A=14 055.9c –2 751.99 ,相关系数r =0.999 94。在标准工作溶液中,L-色氨酸的浓度为c0时测量所产生的不确定度u(c0)为:
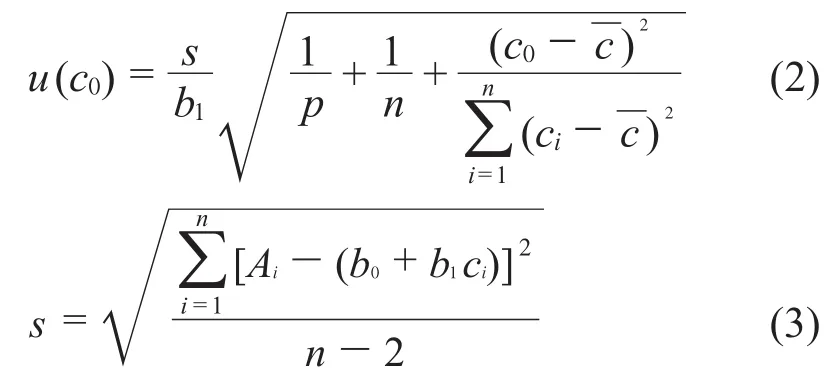
式中:s——标准溶液峰面积残差的标准偏差;
b1——校准曲线的斜率;
p——被测样品的测量次数,p=6;
n——6种标准溶液总测试次数,n =36;
c0——L-色氨酸样品溶液对应于标准工作曲线的浓度,c0=0.880 109 µg/mL;
Ai——标准溶液色谱峰面积;
ci——标准溶液的浓度,µg/mL。
将表1中的数据代入式(2)、式(3)计算求得u(c0)=0.051 98 µg/mL。
标准溶液中L-色氨酸的质量体积浓度c0的不确定度仅与峰面积不确定度有关,而与标准溶液不确定度无关,也不与从同一溶液中逐次稀释产生必然的相关性[3],故标准贮备液稀释成标准溶液所产生的不确定度可以忽略,urel(c0)=u(c0)/c0=0.059 06。
4.2 L-色氨酸标准储备液浓度引入的不确定度
(1)L-色氨酸标准物质纯度引入的不确定度
L-色氨酸标准物质证书标示的纯度P为(99.7±0.7)%,取容量因子k=2,则L-色氨酸标准物质纯度引入的标准不确定度u(P)=0.007/k =3.5×10–3,urel(P)=u(P)/P=3.51×10–3。
(2)标准物质称量引入的不确定度
检定证书给出了天平的最大允许误差为±0.01 mg。标准不确定度分量应重复计算两次,一次是空盘,另一次为毛重,因为每一次称量均为独立的观测结果。实验实际称取标准物质5.02 mg,由此得到标准物质称量引入的标准不确定度u(m)=0.008 2 mg,则urel(m)=0.008 2/5.02=1.633×10–3。
(3)标准储备溶液定容体积引入的不确定度
标准储备液定容使用50 mL单标线A级容量瓶,定容体积引入的不确定度u(V)由以下两项合成得到:
①容量瓶的体积引入的不确定度u1(V)。检定证书给定容量允差为±0.05 mL,按照矩形分布计算,不确定度分量= 0.028 87(mL)。
②实验温度波动引入的容量瓶体积不确定度u2(V)。实验室的温度波动范围为±5℃,水的热膨胀系数为2.1×10–4/℃,按矩形分布计算,=0.030 3(mL)。
合并以上两项,得标准储备溶液定容体积引入的不确定度:

L-色氨酸标准储备液浓度引入的相对标准不确定度urel(S)可由urel(P),urel(m),urel(V) 3项合成而得:
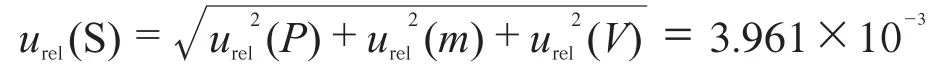
4.3 样品处理引入的不确定度
移液管和容量瓶定容不确定度来源:排出或定容体积的重复性、体积校准时的不确定度以及由实验室温度与取样器皿校准时温度不一致而带来的不确定度,其中排出或定容体积的重复性归入整个测试程序统一考虑。
体积校准不确定度:取样采用1 mL的A级移液管,定容时采用10 mL的A级容量瓶。按照检定规程JJG 196–2006要求,1 mL移液管的最大允许误差为0.008 mL,10 mL容量瓶的最大允许误差为0.02 mL,近似为矩形分布。则移液管的标准不确定度为(mL),容量瓶的标准不确定度为=0.011 5 mL。
温度引入的不确定度:实验室的实际温度波动范围为±5℃,1 mL移液管标准不确定度为(mL),10 mL容量瓶标准不确定度为=6.06×10–3(mL),则氨基酸口服液取样体积的合成标准不确定度
样品定容体积引入的的不确定度u(V2)为:
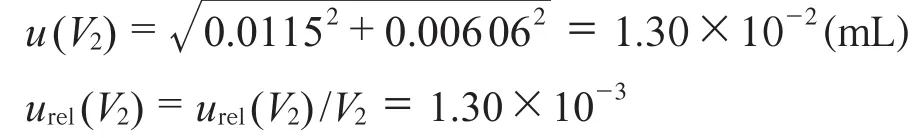
4.4 色谱峰面积引入的不确定度
根据仪器说明书和积分仪的一般性能指标分析,目前用于液相色谱仪色谱峰面积积分处理的最大误差为0.2%~1%,取1%,按均匀分布考虑,则色谱峰面积的标准不确定度为:

其相对标准不确定度为:
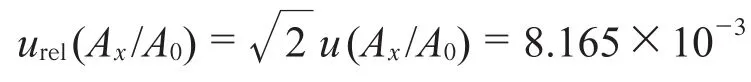
4.5 重复性引入的标准不确定度
对氨基酸口服液样品进行6次重复测量,测量覆盖本方法的全过程,同时反映称量、体积等分量的重复性。测得样品含量分别为8.17,9.06,8.83,9.07, 8.80,8.87 µg/mL,平均值=8.80 µg/mL,标准偏差s =0.329 µg/mL。
因此,重复性引入的相对不确定度为:

4.6 合成标准不确定度
相对标准不确定度由式(4)合成:

把相关数据代入(4)式,求得urel(w)=0.061 9,标准不确定度u (w)=urel(w)×w =0.55 μg/mL。
4.7 计算扩展不确定度
取置信水平P =95%,包含因子k =2,计算扩展不确定度U =k×u (w)=1.1 μg/mL。
5 结果表示
氨基酸口服液中L-色氨酸测量结果可以表达为:w =(8.8 ±1.1)μg/mL。
6 结论
分析结果表明,标准曲线校准及样品测定的重复性是液相色谱法测定氨基酸口服液中L-色氨酸含量的主要不确定度来源,其中标准曲线校准对总不确定度的影响最大。原因是由于测试样品的浓度接近检测限,样品测试的重复性变差,通过选择合适的、可行的试验方案,譬如富集样品中L-色氨酸等可以有效减小不确定度,保证测量结果的准确、可靠。
[1] Mackay G M, Forrest C M, Stoy N, et al.Tryptophan metabolism and oxida tive stress in patients with chronic brain injury[J].Eur J Neurol,2006(13): 30–42.
[2] Agazzi A, Ponti F D, Giorgio R D, et al.Review of the implications of dietary tryptophan intake in patient with irritable bowel syndrome and psychiatric disorders[J].Dig Liver Dis,2003,35(8): 590–595.
[3] CNAS–GL06:2006 化学分析中不确定度的评估指南[S].
[4] JJF 1059–1999 测量不确定度评定与表示[S].
Uncertainty Evaluation of Determinnation of L-Tryptophan in Amino-Acid Oral Liquid by HPLC
Bao Zhijuan, Zhou Jinyan, Yang Yi
(Guangdong Institute of Metrology, Guangdong 510405, China)
L-trypotphan (TRP) in amino-acid oral liquid was detected by HPLC,and the measurement uncertainty was evaluated. The results indicated that the calibration of the standard curve and repeatability mainly affected the measurement uncertainty of L-TRP in amino-acid oral liquid. The calibration of the standard curve was the largest contribution to the whole measurement uncertainty. As the content of L-TRP was 8.8 μg/mL,the expanded uncertainty was 1.1 μg/mL.
L-tryptophan; HPLC; amino-acid oral liquid; measurement uncertainty
O657.7
A
1008–6145(2012)02–0014–03
10.3969/j.issn.1008–6145.2012.02.004
* 广东省质监局科技计划项目(2010CB01)
联系人:保志娟;E-mail: baozhij@yahoo.com.cn
2011–10–20

