桂皮酸–8-羟基喹啉稀土配合物的合成、表征及与牛血清白蛋白的作用*
李小芳,冯小强 杨声
(天水师范学院生命科学与化学学院,甘肃天水 741001)(定西师范高等专科学校,甘肃定西 743000)
桂皮酸–8-羟基喹啉稀土配合物的合成、表征及与牛血清白蛋白的作用*
李小芳,冯小强 杨声
(天水师范学院生命科学与化学学院,甘肃天水 741001)(定西师范高等专科学校,甘肃定西 743000)
合成了以桂皮酸、8-羟基喹啉为配体,以镱、铕为中心离子的稀土配合物,采用元素分析、摩尔电导、红外光谱、紫外光谱和荧光光谱法进行表征,并采用紫外光谱和荧光光谱研究了配合物与牛血清白蛋白(BSA)的相互作用。结果表明,随着配合物浓度的增加,BSA紫外光谱表现出明显的增色效应,配合物可有规律地猝灭BSA的荧光。
桂皮酸;8-羟基喹啉;稀土配合物;牛血清白蛋白
药物进入人体需通过血浆的存储和运输,到达受体部位而产生药理作用。血清白蛋白是血浆中含量最丰富的蛋白质,研究药物与血清白蛋白的相互作用,对了解药物的作用机制具有重要的意义。因此,从不同角度研究以白蛋白为代表的蛋白质与具有生物活性小分子间的相互作用,已成为一个非常活跃的研究课题[1]。
稀土元素具有很好的抗炎、杀菌、抗癌、抗凝血、镇痛作用[2],有关稀土配合物抑菌活性的研究已有许多报道[3–6]。桂皮酸在医药工业中用来制造“心可安”、局部麻醉剂、杀菌剂、止血药等,在农药工业中作为生长促进剂和长效杀菌剂。另外,含氮杂环化合物8-羟基喹啉也是一类具有杀菌、抗炎功能的物质,常被用作杀菌剂。笔者首次合成了以桂皮酸、8-羟基喹啉为配体,以镱、铕为中心离子的稀土配合物,以期获得具有长效杀菌作用的配合物,并研究了合成的两种三元配合物与牛血清白蛋白(BSA)的相互作用。有关桂皮酸–8-羟基喹啉稀土配合物与BSA相互作用的研究未见报道。该研究为今后进一步扩大稀土的应用及从事稀土生物无机化学、药物化学、生物热化学等领域的研究提供了一些具有应用价值的信息,对开拓稀土药物化学的新领域具有一定的意义。
1 实验部分
1.1 主要仪器与试剂
RE2O3(RE: Eu,Yb):甘肃稀土公司;
BSA溶液:1.0×10–5mol/L,北京奥博星生物技术责任有限公司;
电导率仪:DDS-307型,上海雷磁仪器厂;
傅立叶红外光谱仪:Spectrum One型,美国Perkin Elmere公司;
元素分析仪:Vario EL Ⅲ型,德国Elementar公司;
紫外可见光谱仪:UV–2450型,日本岛津公司;
荧光光谱仪:RF–5301PC型,日本岛津公司;
精密pH计:PHS–3D型,上海精密科学仪器有限公司。
1.2 三元配合物的合成及表征[7]
将含有1 mmol 的稀土氧化物放入小烧杯,滴加HNO3溶液(1+1),于水浴中加热溶解,继续加热蒸干。向含有5 mmol桂皮酸的95%乙醇溶液中加入4 mmol/L的NaOH溶液,调节至pH 6.0~6.5后,加入0.3 g 8-羟基喹啉,磁力搅拌下,将上述混合液中滴入含有5 mmol RE (NO3)3·6H2O的95%乙醇溶液中,即产生沉淀,室温继续搅拌24 h,陈化沉淀12 h,过滤,用95%乙醇洗涤数次,再用丙酮洗涤3次,真空干燥。采用KBr压片法测定三元配合物的红外光谱。将三元配合物及配体配成浓度为0.1 mg/mL的DMSO溶液,在190~500 nm范围内测定紫外光谱和荧光光谱。
1.3 配合物与BSA的作用
在10 mL比色管中依次加入2.0 mL Na2HPO4– NaH2PO4(pH 7.4)缓冲液、2.0 mL BSA溶液及一定量的三元配合物工作液,以二次蒸馏水定容后作用12 h,在240~320 nm扫描紫外光谱;设定激发和发射狭缝宽度均为3 nm,λex=280 nm,在290~450 nm测定其荧光光谱。
2 结果与讨论
2.1 配合物的组成及溶解性
稀土离子的含量用EDTA络合法测定,根据配合物的元素分析结果,可确定配合物的组成为REL2·L'(RE: Eu,Yb;L:桂皮酸;L':8-羟基喹啉)。配合物不溶于乙醚、环己烷、乙酸乙酯和氯仿等极性较小的有机溶剂,可溶于THF、DMF和DMSO中,难溶于水。在25℃,以1.0 mg/mL DMSO溶液为溶剂,测得Eu –桂皮酸–8-羟基喹啉和Yb –桂皮酸–8-羟基喹啉配合物的摩尔电导分别为13.94,12.05 μS/cm,表明配合物在DMSO中均属非电解质。
2.2 配合物的表征
2.2.1 红外光谱
各配合物的红外光谱基本相似,但明显有别于游离配体,具体数据见表1。
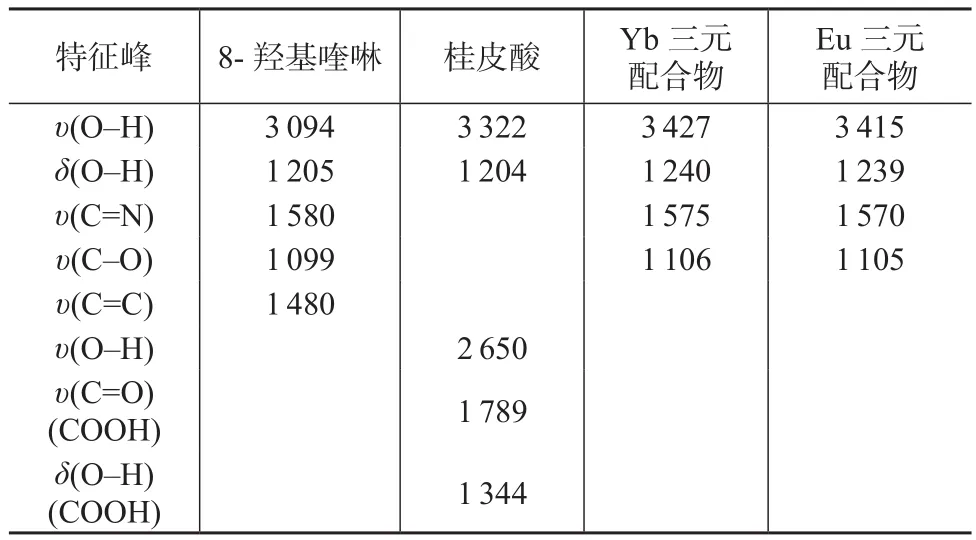
表1 三元配合物及其配体的主要红外光谱数据 cm–1
8-羟基喹啉有5个特征吸收峰:O-H(3 094 cm–1),O-H(1 205 cm–1),C=N(1 580 cm–1),C-O (1 099 cm–1),C=C(1 480 cm–1),形成配合物后O-H红移到3 415~3 427 cm–1,O-H红移到1 240 cm–1附近,表明羟基氧原子和稀土离子成键;同时C=N吸收峰有位移,表明8-羟基喹啉中氮原子也参与了配位;另外,C-O位移到1 105 cm–1附近,C=N位移到1 570~1 575 cm–1,说明氧原子和氮原子也参与了配位,而桂皮酸中羧基参与配位。
2.2.2 紫外及荧光光谱
各配合物在DMSO中的紫外和荧光光谱数据见表2。
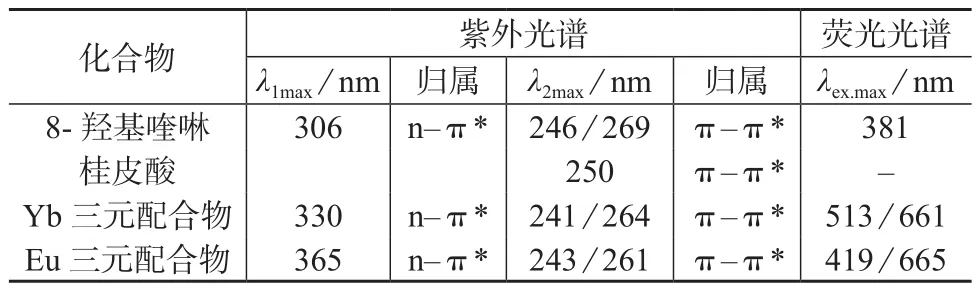
表2 三元配合物及配体的紫外和荧光光谱数据
由紫外光谱数据可知,λ1是B吸收带,表明化合物中含有芳核,λ2是K吸收带,表明化合物中存在共轭体系。K吸收带和B吸收带都具有8-羟基喹啉的特征,可见其紫外吸收主要由配体决定,体现出配体的性质。8-羟基喹啉的吸收远强于桂皮酸,所以后者常被掩盖。吸收带的红移或蓝移都表明了稀土离子和配体有成键作用。在DMSO中,配合物的荧光光谱主要表现为配体的荧光,而稀土离子的特征荧光相对比较弱,这是因为DMSO本身可以作为配体对中心离子配位,配体与稀土之间的能量转移因溶剂作用而发生变化,使稀土离子不能有效地发射出特征荧光[4]。
2.3 配合物与BSA相互作用的紫外光谱
Eu –桂皮酸–8-羟基喹啉、Yb –桂皮酸–8-羟基喹啉对BSA的紫外光谱的影响分别见图1、图2。由图1、图2可知,BSA在280 nm处有一强吸收峰,是其肽链上的色氨酸和酪氨酸的苯杂环π–π*跃迁引起的,且吸收强度随配合物浓度的增加而增强,说明稀土三元配合物诱导BSA分子发生类似降低pH值所出现的蛋白质肽链伸展现象[8],使包围在BSA分子内部的色氨酸和酪氨酸残基的芳杂环疏水基团裸露出来,使吸收强度增强。紫外光谱表明稀土三元配合物与BSA混合后发生了相互作用;另外,在254~257 nm附近有一吸收峰,且吸收强度随着稀土三元配合物浓度的增大而增强,可归属三元配合物的吸收峰。
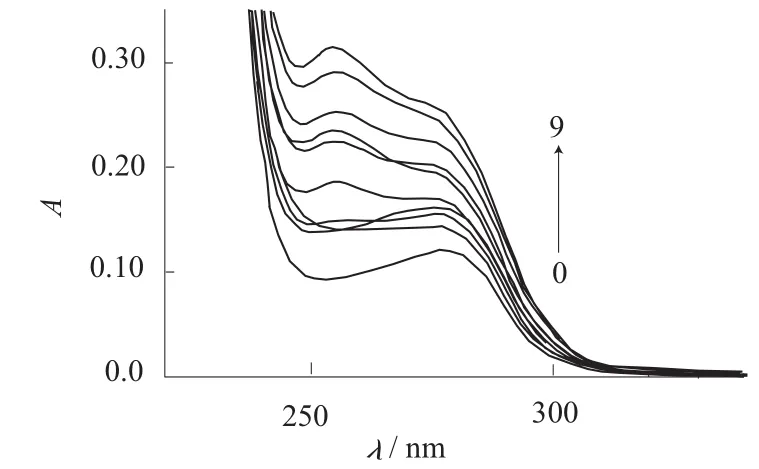
图1 Eu – 桂皮酸–8-羟基喹啉对BSA紫外吸收光谱的影响
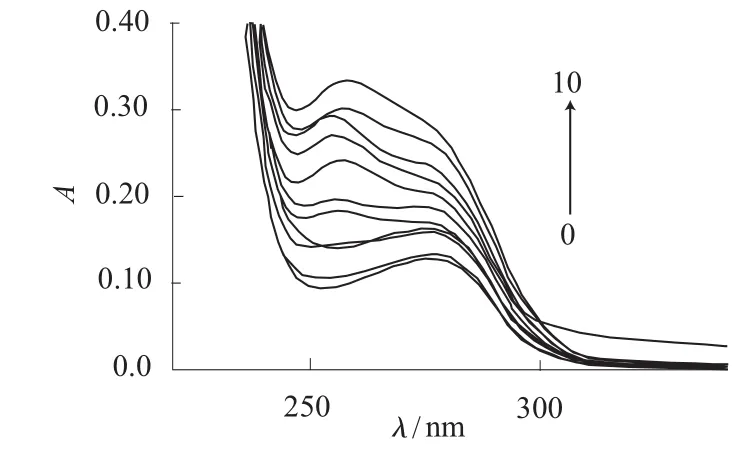
图2 Yb –桂皮酸–8-羟基喹啉对BSA紫外吸收光谱的影响
2.4 配合物与BSA相互作用的荧光光谱
蛋白质分子中因含有色氨酸、酪氨酸和苯丙氨酸等氨基酸残基而产生内源性荧光。由于这些氨基酸具有不同的结构,荧光强度比为100∶9∶0.5,故在大多数情况下,可认为蛋白质的荧光主要来自色氨酸残基的贡献,而且含色氨酸残基的蛋白质的天然荧光及其变化直接反映了蛋白质中色氨酸残基本身及其周围环境的变化。蛋白质的荧光猝灭可用于研究药物与蛋白质的结合信息。BSA在激发波长λex=280 nm时,最大发射波长λem=348 nm。在同一条件下,向BSA溶液中分别滴加Eu –桂皮酸–8-羟基喹啉、Yb –桂皮酸–喹啉配合物溶液前后的荧光光谱见图3、图4。
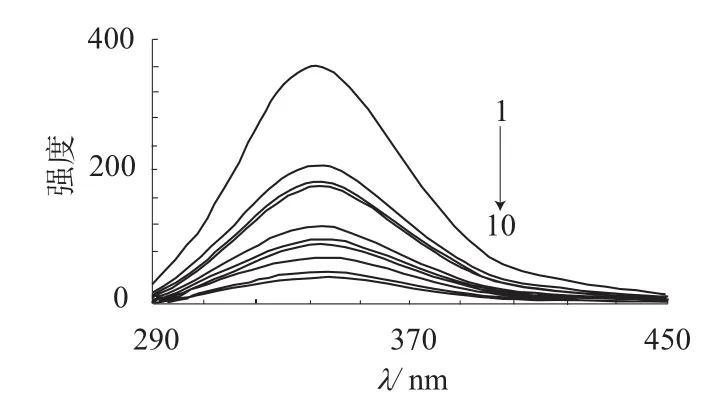
图3 桂皮酸–喹啉–Eu对BSA荧光强度的影响
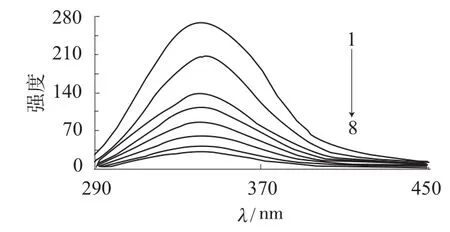
图4 桂皮酸–喹啉–Yb对BSA荧光强度的影响
由图3、图4可知,随着配合物浓度的增加,BSA荧光强度有规律地降低,但发射峰的位置和形状基本不变,说明两种配合物对BSA的荧光具有猝灭作用。
3 结语
Eu/Yb –桂皮酸–喹啉能诱导BSA分子发生蛋白质肽链伸展现象,使包围在BSA分子内部的色氨酸和酪氨酸残基的芳杂环疏水基团裸露出来,从而使吸收强度增强;Eu/Yb –桂皮酸–8-羟基喹啉与BSA能发生相互作用,对BSA的荧光具有猝灭作用。
[1] 黄波,邹国林,杨天鸣.阿霉素与牛血清白蛋白结合作用的研究[J].化学学报,2002,60(10): 1 867–1 871.
[2] 霍春芳,张冬艳,刘进荣,等.稀土对芽孢菌的抑菌作用机理研究[J].化学学报,2002,60 (6): 1 065–1 072.
[3] 张丽红,张冬艳,卢庆华,等.小檗碱与稀土硝酸盐二元配合物的合成、表征及抑菌作用[J].中国稀土学报,2010,28 (6):751–755.
[4] 梁福沛,唐献兰,胡瑞祥,等.稀土–烟酸–8-羟基喹啉三元配合物合成、表征及其抑菌活性[J].稀有金属,2000,24(4): 265–269.
[5] 朱早龙,刘景旺,达文燕,等.稀土姜黄素大环配合物的合成、表征及其荧光性质和抑菌活性研究[J].化学通报,2009(1): 59–65.
[6] Prem kumar T,Govindarajan S. Antimicrobial study on trivalent lighter rare-earth complexes of 2-pyrazinecarboxylate with hydrazinium cation [J].World Journal of Microbiology and Biotechnology,2006,22 (10): 1 105–1 110.
[7] 李小芳,冯小强,杨声,等.镧–磺基水杨酸–8-羟基喹啉三元配合物合成、表征及其抑菌活性[J].合成纤维,2010,39(7):30–33.
[8] 玄光善,吴效楠,李玉平.荧光光谱法研究乙酰水杨酸和牛血清蛋白的相互作用[J].光谱实验室,2005,22 (7): 861–864.
Synthesis Characterization and Interaction of Rare Earth Complexes of Cinnamic Acid with 8-hydroxyquinoline and Bovine Serum Albumin
Li Xiaofang, Feng Xiaoqiang
(School of Life Sciences and Chemistry, Tianshui Normal University, Tianshui 741001, China)
Yang Sheng
(Ding Xi Teachers’College, Dingxi 743000, China)
Two kinds of ternary complexes of rare earth,with cinnamic acid and 8-hydroxyquinoline were synthesized,and investigated by using elemental analysis,molar conductance,FT–IR,UV and fl uorescence spectroscopy methods. The interactions of ternary complexes with BSA were studied by UV and fluorescence spectroscopy. Results showed that the absorption intensity of BSA increased with the increasing of complex concentration,and the fl uorescence intensity of BSA was quenched regularly by the ternary complexes.
cinnamic acid; 8-hydroxyquinoline; rare earth complex; bovine serum albumin (BSA)
O627181
A
1008–6145(2012)02–0029–03
10.3969/j.issn.1008–6145.2012.02.008
*天水师范学院物理无机化学重点学科基金项目(ZD0840);天水师范学院中青年教师科研资助项目(TSA1003)
联系人:李小芳;E-mail: lix_f06@lzu.edu.cn
2012–02–08

