国产注射用比伐卢定对冠状动脉介入治疗患者凝血功能的影响
马岚 姚义安 李继敏 刘学波
目前,临床上在冠心病患者行冠状动脉介入治疗(PCI)时,指南推荐常规给予普通肝素(UFH)抗凝治疗。普通肝素主要通过与抗凝血酶结合加速自然激活而间接抑制凝血酶活性,静脉给药后起效迅速。由于其临床作用有限[1-2],为进一步降低缺血事件发生,常与阿司匹林、血小板ADP受体抑制剂、血小板糖蛋白GPⅡb/Ⅲa抑制剂以不同方式联合应用[3],但同时也带来了血小板减少、出血率增加、输血增加等风险,并导致死亡率增加[4]。
比伐卢定(bivalirudin)是以水蛭素结构为基础的由20个氨基酸组成的单链多肽,可与凝血酶活性位点和底物识别位点可逆性结合的凝血酶直接抑制剂。药理研究显示,静脉给比伐卢定后,平均消除半衰期为24 min,抗凝活性随剂量增加而延长,抗凝活性在0.25~2.00 h达峰。美国食品药品管理局于2000年批准比伐卢定作为一种新型抗凝药物上市,CACHET、REPLACE-2、ACUITY 等临床试验表明,比伐卢定与普通肝素相比,能够明显减少缺血事件及出血事件的发生率[5-7],降低血小板减少症的发生率[8],降低医疗费用[9]。目前,已有国产比伐卢定上市,其有效性和安全性如何,目前相关资料较少,本研究的主要目的是通过临床试验评价国产注射用比伐卢定作为抗凝剂对PCI治疗患者凝血功能的作用。
1 对象和方法
1.1 研究对象
2010 年4 月至2011年2月期间在同济大学附属东方医院DSA室行择期PCI术的患者50例,所有患者年龄在18~70岁之间,诊断为稳定型心绞痛或不稳定型心绞痛,均经桡动脉入路行冠状动脉造影术及支架置入术,排除急性心肌梗死、严重冠脉病变、24 h内曾溶栓治疗、PCI术前12 h内静脉注射过普通肝素或低分子肝素(做冠脉造影时使用的肝素忽略不计)、有出血倾向、严重高血压未控制、肝肾功能异常、试验相关药物过敏史、血小板和凝血时间异常者。根据造影结果,对病变适于行PCI术并符合入选和排除标准者,予签署知情同意书后,按入组顺序进行随机分组(采用南京医科大学临床研究随机分组系统电脑软件),分别进入肝素组(对照组,25例)和比伐卢定组(25例)。
1.2 研究用药
普通肝素钠(江苏豪森药业股份有限公司,批号:1002116);国产注射用比伐卢定(江苏豪森药业股份有限公司,批号:2009L06720);
1.3 方法
试验方案规定,两组患者术前至少给予3 d氯吡格雷口服,75 mg/d,如术前服药未满3 d,术前给予氯吡格雷负荷量300 mg。对照组在PCI术前静脉推注肝素125 U/kg(参考ISAR REACT 3A试验),静脉注射5 min后检测活化凝血时间(activated clotting time,ACT)[ACT测定仪(美国美敦力公司,型号:ACT200)]。若ACT值小于225 s(参考 REPLACE-2研究),需追加肝素3000 U。比伐卢定组PCI术前静脉注射比伐卢定0.75 mg/kg作为负荷剂量,然后立即静脉滴注1.75 mg·kg-1·h-1至手术结束,静脉注射5 min后检测ACT值,若ACT值小于225 s,需追加剂量,据患者的体质量,按剂量0.3 mg/kg计算所需药量。在PCI术前和药物使用后5 min、手术结束即刻(即停药即刻)、停药后30 min、2 h分别测定ACT。分别在用药前、用药结束后6、24和72 h通过全自动凝血功能测定仪检测活化部分凝血酶时间(APTT)、凝血酶时间(PT)、凝血酶原时间(TT)、纤维蛋白原(FIB)指标。并观察术后3 d患者的心血管事件(有无胸痛发作,心肌梗死发生),心肌酶(TnT变化)及出血事件(皮下瘀斑、穿刺部位血肿等定义为小出血事件,需要紧急输血、定义为大出血事件,消化道出血和泌尿系出血分别用粪隐血和尿隐血来评价)。
1.4 统计学方法
2 结果
2.1 一般情况
两组患者年龄、性别、TT、APTT、PT、FIB、肝肾功能,差异均无统计学意义(均为P>0.05),见表1。高血压和糖尿病患者术前均已用药物控制在正常范围。两组患者用药5 min的ACT均大于225 s,无一例追加剂量。
2.2 ACT变化
比伐卢定组用药后5 min、术后即刻ACT值明显大于对照组(P<0.05);PCI术前和停药后30 min,两组患者ACT差异无统计学意义;停药后2 h ACT值显著小于对照组(P<0.05)(见表2)。
2.3 凝血功能变化
监测两者术后凝血4项,比较均无统计学意义(均为P>0.05)(表3)。
2.4 比伐卢定对凝血功能及血小板的影响
比伐卢定对凝血4项的敏感性的顺序是TT>APTT>PT>FIB(表4),对血小板无明显影响。
2.5 两组病例3 d临床事件及出血事件
两组之间心血管临床事件的发生,出血事件的发生及术后TNT变化均无明显差别,在小出血事件和泌尿系出血方面,比伐卢定组较对照组稍低。见表5。
3 讨论
冠心病已成为我国城乡居民致残、致死的主要原因之一,每年大约70万人死于冠心病,约占全部死亡的四分之一[10],冠状动脉介入治疗及围手术期的抗血小板药物、抗凝药物的应用显著降低了ACS的缺血事件并发症,降低了致死率和致残率[11]。
普通肝素静脉给药方便,起效快,故目前PCI术中常规应用普通肝素抗凝。但由于普通肝素存在自身的缺点,其抗凝的效果并不全面,有增加术中血栓的风险,虽然增加剂量可以带来更好的抗凝效果,但同时也增加了出血的风险[12]。联合应用GPⅡb/Ⅲa受体拮抗剂可减少术中及术后急性血栓等缺血事件的发生[13],但同样可带来出血事件的增加及血小板减少的风险[12-13]。
表2 两组患者ACT值变化情况(±s,s)
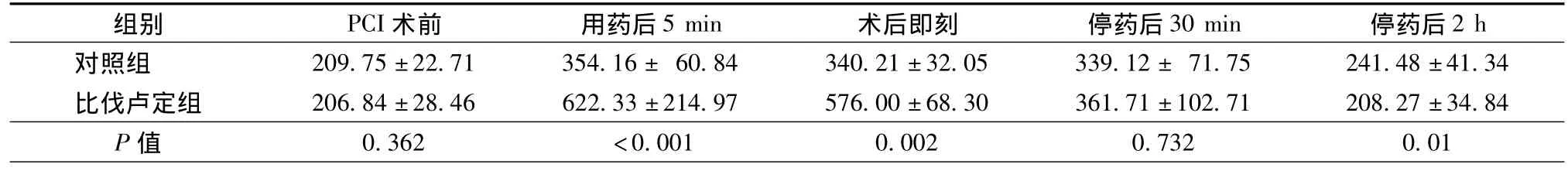
表2 两组患者ACT值变化情况(±s,s)
2 h对照组 209.75±22.71 354.16± 60.84 340.21±32.05 3组别 PCI术前 用药后5 min 术后即刻 停药后30 min 停药后39.12± 71.75 241.48±41.34比伐卢定组 206.84±28.46 622.33±214.97 576.00±68.30 361.71±102.71 208.27±34.84 P值0.362 <0.001 0.002 0.732 0.01
表3 两组患者术后凝血四项比较(±s)
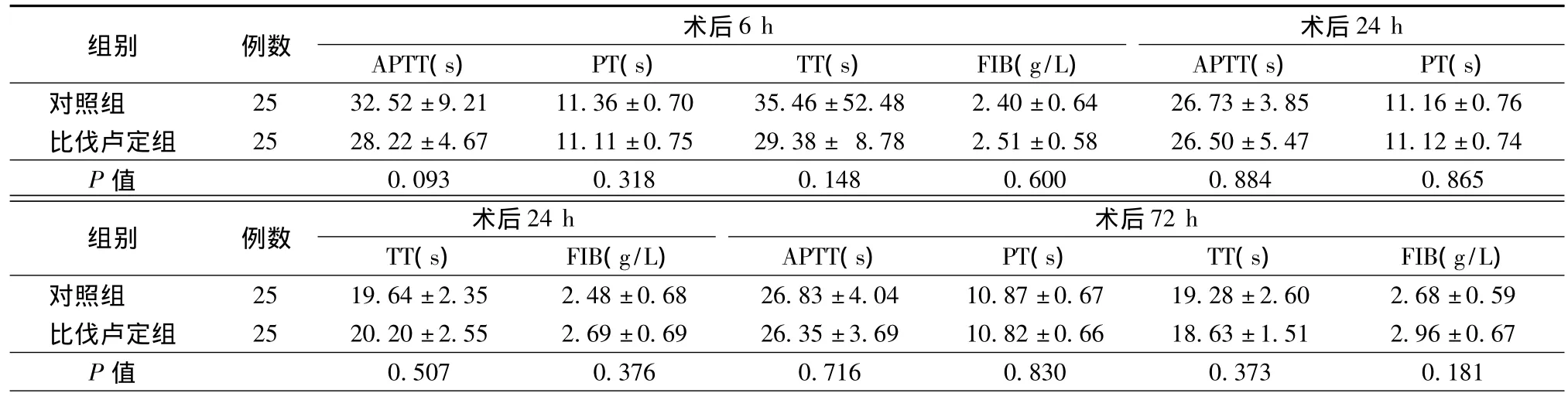
表3 两组患者术后凝血四项比较(±s)
组别 例数 术后6 h APTT(s) PT(s) TT(s) FIB(g/L)24 h APTT(s) PT(s)术后对照组 25 32.52±9.21 11.36±0.70 35.46±52.48 2.40±0.64 26.73±3.85 11.16±0.76比伐卢定组 25 28.22±4.67 11.11±0.75 29.38± 8.78 2.51±0.58 26.50±5.47 11.12±0.74 P值0.093 0.318 0.148 0.600 0.884 0.865组别 例数 术后24 h TT(s) FIB(g/L)术后72 h APTT(s) PT(s) TT(s) FIB(g/L)对照组 25 19.64±2.35 2.48±0.68 26.83±4.04 10.87±0.67 19.28±2.60 2.68±0.59比伐卢定组 25 20.20±2.55 2.69±0.69 26.35±3.69 10.82±0.66 18.63±1.51 2.96±0.67 P值0.507 0.376 0.716 0.830 0.373 0.181
表4 比伐卢定术前术后凝血四项、血小板的比较(±s)
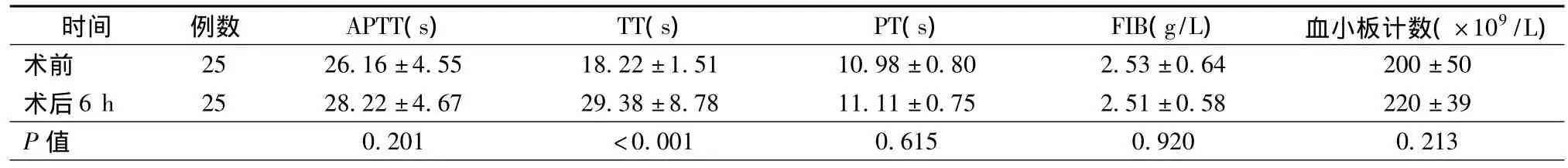
表4 比伐卢定术前术后凝血四项、血小板的比较(±s)
时间 例数 APTT(s) TT(s) PT(s) FIB(g/L) 血小板计数(×109/L)术前 25 26.16±4.55 18.22±1.51 10.98±0.80 2.53±0.64 200±50术后6 h 25 28.22±4.67 29.38±8.78 11.11±0.75 2.51±0.58 220±39 P值0.201 <0.001 0.615 0.920 0.213
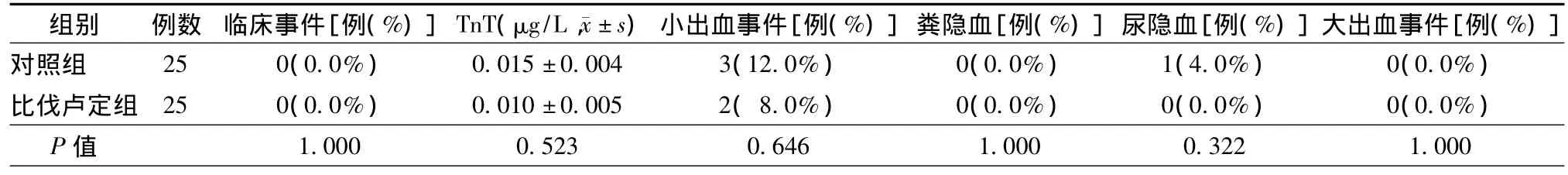
表5 两组术后3 d临床事件及出血事件比较
比伐卢定可直接抑制凝血酶原,作用不需要其他辅助因子的参与,而且也不会影响其他凝血因子,与肝素活化血小板不同,它可抑制血小板的活化,进而降低缺血事件的发生。在我们的研究之前,国外已有多项报道指出,比伐卢定可作为PCI术中肝素的替代药物,它与肝素相比,有效性相似,但安全性更高,发生缺血事件少而且出血的风险低[5-7,14]。由于出血并发症少,2005年ESC在PCI指南推荐比伐卢定可作为UFH或LMWH(低分子肝素)的替代药物用于稳定冠心病患者的PCI。2005年ACC/AHA在PCI指南推荐比伐卢定在合并HIT(肝素诱导的血小板减少)的患者中替代UFH或LMWH。
本研究将50例经冠状动脉造影确诊冠心病并行PCI术患者,随机均分成比伐卢定组和对照组,分别使用国产比伐卢定和肝素钠。两组基线资料差异均无统计学意义,手术时间范围未超过比伐卢定药物达峰时间,提示比伐卢定组和对照组两组有良好的对比性。PCI过程中,用药后5 min患者比伐卢定组ACT显著长于对照组,术后即刻ACT比伐卢定组较对照组延长,这显示出国产比伐卢定相对于肝素钠具有起效快,效果好的优点。而停药后2 h比伐卢定组ACT显著短于对照组,提示比伐卢定的半衰期较肝素短,代谢更快的优点。其线性剂量依赖性抗凝活性的特点,使得静脉给药后,快速起效并迅速逆转至失效。术后3 d心血管事件两组之间差异无统计学意义,提示国产比伐卢定在PCI术中抗凝有效性同肝素相当。本临床试验结果与国外大规模临床实验结论基本一致,证明了国产注射用比伐卢定具有起效快、抗凝作用强,半衰期短,安全性高等优点,可替代肝素安全、有效地用于PCI术中。而术后对照组出血事件数略高于比伐卢定组,但两组之间差异无统计学意义,没有得出比伐卢定安全性优势,分析原因可能与样本量小、患者危险分层较低、观察时间短等因素有关,需要更多临床病例研究来进一步证实。
[1]Xiao Z,Theroux P.Platelet activation with unfractionated heparin at therapeuticconcentrations and comparisonswith alowmolecular-weight heparin and with a direct thrombin inhibitor.Circulation,1998,97:251-256.
[2]Sobel M,Fish WR,Toma N,et al.Heparin modulates integrin function in human platelets.J Vasc Surg,2001,33:587-594.
[3]The PURSUIT Trail Investigators.Platelet Glycoprotein Ⅱb/Ⅲa in UnstableAngina:ReceptorSuppression Using Integrilin Therapy.Inhibition of platelet glycoprotein Ⅱ b/Ⅲ awith eptifibatide in patients with acute coronary syndromes.N Engl J Med,1998,339:436-443.
[4]Centurión OA.Bivalirudin in contemporary percutaneous coronary intervention for non-ST-segment elevation acute coronary syndromes:What is the current role of platelet glycoproteinⅡb/Ⅲa receptor inhibitor agents?Crit Pathw Cardiol,2011,10:87-92.
[5]Lincoff AM,Kleiman NS,Kottke-Marchant K,et al.Bivalirudin with planned or provisional abciximab versus low-dose heparin and abciximab during percutaneous coronary revascularization:results of the Comparison of Abciximab Complications with Hirulog for Ischemic Events Trial(CACHET).Am Heart J,2002,143:847-853.
[6]Lincoff AM,Bittl JA,Harrington RA,et al.REPLACE-2 Investigators.Bivalirudin and provisional glycoprotein Ⅱb/Ⅲa blockade compared with heparin and planned glycoproteinⅡb/Ⅲa blockade during percutaneous coronary intervention:REPLACE-2 randomized trial.JAMA,2003,289:853-863.
[7]Aoki J,Lansky AJ,Mehran R,et al.Early stent thrombosis in patients with acute coronary syndromes treated with drug-eluting and bare metal stents:the Acute Catheterization and Urgent Intervention Triage Strategy trial.Circulation,2009,119:687-698.
[8]Kiser TH,Burch JC,Klem PM,et al.Safety,efficacy,and dosing requirements of bivalirudin in patients with heparininduced thrombocytopenia.Pharmacotherapy,2008,28:1115-1124.
[9]Schwenkglenks M,Toward TJ,Plent S,et al.Cost-effectiveness of bivalirudin versus heparin plus glycoprotein Ⅱb/Ⅲa inhibitor in the treatment of acute ST-segment elevation myocardial infarction.Heart,2012 Feb 7.[Epub ahead of print]
[10]He J,Gu D,Wu X,et al.Major causes of death among men and women in China.N Engl J Med,2005,353:1124-1134.
[11]Rogers WJ,Frederick PD,Stoehr E,et al.Trends in presenting characteristics and hospital mortality,among patients with ST elevation and non-ST elevation myocardial infarction,in the National Registry of Myocardial Infarction from 1990 to 2006.Am Heart J,2008,156:1026-1034.
[12]Chew DP,Bhatt DL,Lincoff AM,et al.Defining the optimal activated clotting time during percutaneous coronary intervention.Circulation,2001,103:961-966.
[13]Lincoff AM,Califf RM,Topol EJ.Platelet glycoprotein Ⅱb/Ⅲa blockade in coronary artery disease.J Am Coll Cardiol,2000,35:1103-1115.
[14]Kumar D,DangasG, Mehran R, etal. Comparison of Bivalirudin versus Bivalirudin plus glycoprotein Ⅱb/Ⅲa inhibitor versus heparin plus glycoprotein Ⅱb/Ⅲa inhibitor in patients with acute coronary syndromes having percutaneous intervention for narrowed saphenous vein aorto-coronary grafts(the ACUITY trial investigators).Am J Cardiol,2010,106:941-945.

