阿托伐他汀或瑞舒伐他汀与氯吡格雷合用在非ST段抬高型急性冠状动脉综合征患者支架置入术后的近期疗效比较
叶慧明 彭建军 任利辉 雷力成 杨诺 王佐岩 杨水祥
他汀类药物与氯吡格雷合用常规用于经皮冠状动脉介入治疗术(percutaneous coronary intervention,PCI)的患者,近年学者提出阿托伐他汀与氯吡格雷合用可显著降低氯吡格雷的抗血小板作用[1],可能与二者均经细胞色素P450(CYP)3A4代谢有关。瑞舒伐他汀作为主要经过CYP2C9代谢的他汀类药物[2],不仅降脂作用可与阿托伐他汀媲美,同时在与氯吡格雷合用时可能不影响氯吡格雷的抗血小板作用,但是否心脏事件发生率更低而优于阿托伐他汀,目前暂无定论。国内对该问题的文献相对较少,本研究拟比较阿托伐他汀和瑞舒伐他汀分别与氯吡格雷合用对接受PCI术的非ST段抬高型急性冠状动脉综合征(non-ST segment elevation acute coronary syndrome,NSTE-ACS)患者的血小板聚集功能及近期疗效的影响。
1 对象和方法
1.1 研究对象
入选2010年6月至2011年6月在我院行冠状动脉造影及介入治疗(PCI)的NSTE-ACS的患者154例,使用随机数字法分为阿托伐他汀组(74例)和瑞舒伐他汀组(80例),男性107例,年龄38~84岁,平均(58±10)岁。入选标准为NSTE-ACS(包括不稳定心绞痛、非ST段抬高心肌梗死)并成功行冠状动脉支架置入术的患者。主要排除标准为出血倾向,活动性消化性溃疡,1年内患脑血管意外,有抗血小板和抗凝药物治疗禁忌证者。
1.2 研究方法
入院后给予氯吡格雷(赛诺菲安万特制药有限公司,批号:IA688)75 mg/d和阿司匹林(德国拜耳医药保健有限公司,批号:BG06799)100 mg/d使用5 d以上或氯吡格雷300 mg和阿司匹林300 mg顿服12 h后,按标准行冠状动脉造影及支架置入术,术后阿司匹林片100 mg/d,氯吡格雷75 mg/d维持治疗至少1年。入院后同时给予瑞舒伐他汀(阿斯利康制药有限公司,批号:JD856)10 mg/d或阿托伐他汀(辉瑞制药有限公司,批号:123511K)20 mg/d。有肌酸肌痛主诉及肌酶、转氨酶升高史者排除在外。根据临床情况酌情使用硝酸酯类、血管紧张素转换酶抑制剂和(或)血管紧张素抑制剂及血小板糖蛋白Ⅱb/Ⅲa拮抗剂(GPI)(术后维持24~36 h)等药物。
1.3 氯吡格雷抗血小板作用检测
采用二磷酸腺苷(ADP)诱导的血小板聚集力比浊法测定来评价氯吡格雷的抗血小板作用。采取静脉血5 ml置于含0.129 mol/L柠檬酸钠的真空采血管中,30 min内将全血在20℃温度下以1500 r/min离心2.5 min。将富血小板血浆于37℃下孵育3 min后,加入10 μmol/L的ADP,记录其血小板聚集率(LG-PABER血小板记录仪,北京世帝科学仪器公司)。分别记录入院时、手术当日、PCI术后3、7 d、术后1及6个月的血小板聚集率,30 min内送检。
1.4 结果判断和随访
研究终点及定义:主要终点为6个月的主要不良心血管事件(major adversecardiacevents,MACE)。MACE定义为心原性死亡、非致死性心肌梗死、靶血管血运重建。次要终点为支架内血栓形成和出血事件。随访患者术后随访6个月,随访方式包括门诊复查、再住院和(或)电话随访。记录随访期间发生的心原性死亡、非致死性心肌梗死、靶血管重建术、支架内血栓形成及出血事件。
1.5 统计学方法
2 结果
2.1 两组基本情况比较
两组质子泵抑制剂(PPI)的使用率均达18%左右,且GPI的使用率亦达33%左右(但所有患者均未使用超过36 h),所有基础临床情况及用药情况差异无统计学意义(均为P>0.05)。见表1。
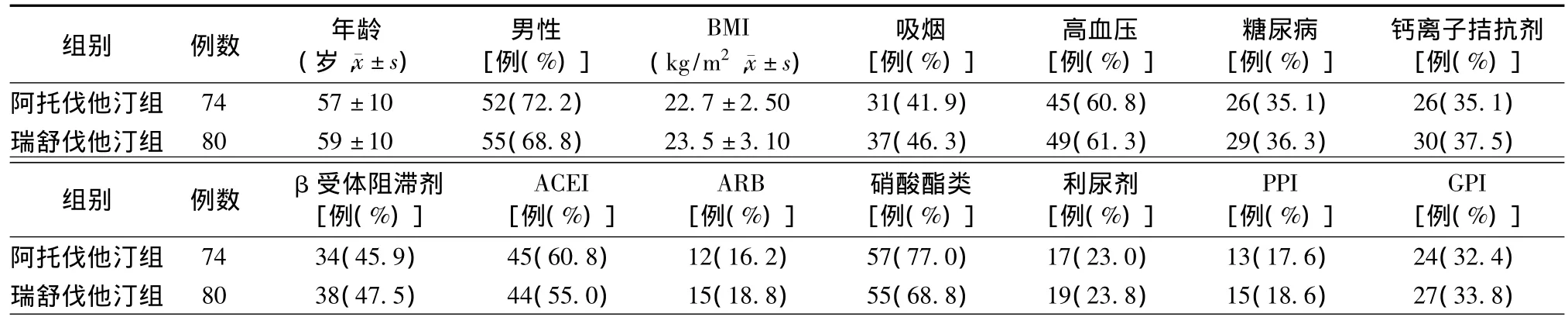
表1 患者临床基线情况及用药情况
表2 血小板聚集功能变化情况(%,±s)

表2 血小板聚集功能变化情况(%,±s)
注:与基线值比较,aP<0.05,两组同期比较均为P>0.05
个月阿托伐他汀组 74 57.2±10.3 32.5±11.2a组别 例数 基线 术前当日 术后3 d 术后7 d 术后1个月 术后6 30.7±12.5 31.5±9.3 30.3± 9.9 32.1±8.9瑞舒伐他汀组 80 59.1±9.8 30.4±10.1a 29.5±11.8 30.1±9.6 29.5±10.4 29.9±9.3

表3 患者6个月时MACE情况[例(%)]
2.2 两组血小板聚集功能比较
两组患者氯吡格雷75 mg/d服用5 d以上或术前12 h以上顿服氯吡格雷300 mg以上,于手术当天均能达很好的血小板聚集抑制率(在基线的基础上,术后3 d的血小板聚集功能平均下降43% ~49%左右,与基线比较P<0.01),术后3、7 d、1及6个月均能维持一个较稳定的低水平血小板聚集率(约30%左右),两组同期比较差异无统计学意义。见表2。
2.3 两组预后比较
随访6个月,两组住院期间、术后1及6个月的MACE发生率差异无统计学意义。心原性死亡两组各1例;非死亡性心肌梗死,阿托伐他汀组2例,瑞舒伐他汀组1例;靶血管重建率阿托伐他汀组6例,瑞舒伐他汀组7例;肯定支架内血栓形成阿托伐他汀组1例(术后2个月经冠状动脉造影证实),很可能支架内血栓形成瑞舒伐他汀1例(术后3个月出现,未行冠状动脉造影,仅根据心电图及临床表现推测);出血事件在瑞舒伐他汀组住院期间发生1例,但不需输血治疗。见表3。
3 讨论
硫酸氯吡格雷作为一种噻吩吡啶类药物非活性前体85%在体内经肠道水解吸收后,在肝脏仍需2步生物转化才成为活性产物,其代谢为活性产物的过程中的两种最重要的酶是CYP3A4和CYP2C19,活性产物与血小板膜表面ADP激活的P2Y12受体不可逆的结合而发挥抗血小板激活和聚集的作用[3]。而亲脂性他汀类降脂药(洛伐他汀、辛伐他汀和阿托伐他汀)的清除主要是CYP3A4依赖的、而亲水性他汀类降脂药(氟伐他汀、普伐他汀和瑞舒伐他汀)的清除是非CYP3A4依赖的。早期Lau等[1]报道正服用亲脂性的阿托伐他汀患者,即使在负荷量氯吡格雷(300 mg)后仍没达到预期的血小板抑制。随后Lau等[4]的一个前瞻性随机临床试验,认为300 mg氯吡格雷负荷量的抗血小板作用仍会受到阿托伐他汀的影响,而600 mg的氯吡格雷的抗血小板作用则没有受到影响,提示其中有竞争性抑制的机制存在。但另有一些研究显示,阿托伐他汀和氯吡格雷共同服用没有影响到氯吡格雷的抗血小板作用,特别是在600 mg氯吡格雷负荷剂量时[5-6],而且发现数周后复查血小板聚集功能也不存在受影响情况[6-7]。上述差异的原因有可能是CYP3A4在个体的表达差异可达40倍,CYP3A4作用的底物代谢个体差异也可达10倍。然而在真实世界中是否会增加主要不良心脏事件呢?PCI术患者的临床试验有些研究发现可能增加心脏事件风险[8],有些研究认为不会增加心脏事件风险[9],但这些研究都集中在普伐他汀、氟伐他汀与阿托伐他汀、辛伐他汀的比较。对于瑞舒伐他汀与阿托伐他汀的比较研究相对较少。本研究显示,无论CYP3A4代谢依赖的阿托伐他汀组(20 mg/d)还是非CYP3A4依赖的瑞舒伐他汀组(10 mg/d)在与氯吡格雷合用时,两组10 μmol/L ADP诱导的血小板聚集功能差异在基线、PCI术当日、术后3、7 d、1及6个月均无统计学意义,提示在本研究的剂量下两组的氯吡格雷的抗血小板活性没有受到他汀类降脂药种类的影响,同时住院期间出血事件及之后的支架内血栓形成发生率的差异无统计学意义,6个月的MACE发生率两组差异亦无统计学意义。本研究使用的阿托伐他汀及瑞舒伐他汀的剂量是临床中常用剂量,目前临床试验证实大剂量的阿托伐他汀或瑞舒伐他汀可以逆转斑块,至于更大的剂量是否对氯吡格雷的抗血小板作用有影响,目前仍有争议,但非CYP3A4代谢依赖的他汀似乎更有优势。最近一篇随机临床试验报道,阿托伐他汀20 mg或瑞舒伐他汀10 mg亦能使轻度冠状动脉粥样硬化斑块逆转[10],可能使这种担心会减少些。只要经过P4503A4代谢的药物理论上都可能影响氯吡格雷的代谢,本研究中的GPI应用比例达30%左右,但两组的应用比例的差异无统计学意义,且均只在围手术期应用36 h,GPI(本研究用的均是替罗非班)半衰期短,不会影响到PCI术后3 d PAR的检测;PPI应用比例达18%左右,是目前明确可影响氯吡格雷代谢的药物之一,但是两组的比例差异亦无统计学意义,对两组间的PAR及结果的差异影响小,但对于高危人群目前仍建议避免与奥美拉唑类PPI合用。
本研究初步证明了常规剂量的阿托伐他汀(20 mg/d)及瑞舒伐他汀(10 mg/d)与氯吡格雷合用在NSTE-ACS支架置入术患者中对10 μmol/L ADP诱导的血小板聚集率的影响差异无统计学意义,且6个月的MACE发生率差异亦无统计学意义。但因对氯吡格雷的反应存在个体差异、药物相互作用的差异,本研究样本例数偏少,不除外样本选择偏差可能,尚需大样本量的随机、多中心临床试验的研究证实。
[1]Lau WC,Waskell LA,Watkins PB,et al.Atorvastatin reduces the ability of clopidogrel to inhibit platelet aggregation:a new drug-druginteraction.Circulation,2003,107:32-37.
[2]Martin PD,Warwick MJ,Dane AL et al.Metabolism,excretion,and pharmacokinetics of rosuvastatin in healthy adult male volunteers.Clin Ther,2003,25:2822-2825.
[3]Kazui M,Nishiya Y,Ishizuka T,et al.Identification of the human cytochrome P450 enzymes involved in the two oxidative steps in the bioactivation of clopidogrel to its pharmacologically active metabolite.Drug Metab Dispos,2010,38:92-99.
[4]Lau WC,Neer CJ,Tait AR,et al.Higher doses of clopidogrel overcome the atorvastatin-clopidogreldrug-drug interaction.Circulation,2005,112:II-295.
[5]Piorkowski M,Weikert U, Schwimmbeck PL, et al.ADP induced platelet degranulation in healthy individuals is reduced by clopidogrel after pretreatmentwith atorvastatin.Thromb Haemost,2004,92:614-620.
[6]Serebruany VL,Midei MG,Malinin AI,et al.Absence of interaction between atorvastatin or other statins and clopidogrel.Resultsfrom the Interaction Study.Arch Intern Med,2004,164:2051-2057.
[7]Mitsios JV,Papathanasiou AI,Elisaf M,et al.The inhibitory potency of clopidogrel on ADP-induced platelet activation is not attenuated when it is co-administered with atorvastatin(20 mg/day)for 5 weeks in patients with acute coronary syndromes.Platelets,2005,16:287-292.
[8]Gulec S,Ozdol C,Rahimov U,et al.Myonecrosis after elective percutaneous coronary intervention:effect of clopidogrel-statin interaction.J Invasive Cardiol,2005,17:589-593.
[9]Trenk D,Hochholzer W,Frundi D,et al.Impact of cytochrome P450 3A4-metabolized statins on the antiplatelet effect of a 600-mg loading dose clopidogrel and on clinical outcome in patients undergoing elective coronary stent placement.Thromb Haemost,2008,99:174-181.
[10]Lee CW,Kang SJ,Ahn JM,et al.Comparison of Effects of Atorvastatin(20 mg)Versus Rosuvastatin(10 mg)Therapy on Mild Coronary Atherosclerotic Plaques(from the ARTMAP Trial).Am J Cardiol.2012 Mar 20.[Epub ahead of print]

