脑康通泰分散片的制备及溶出度测定*
王 维 ,李洪起 ,邹俊忠 ,任晓文
(1.天津中医药大学,天津 300193;2.释药技术与药代动力学国家重点实验室,天津 300193;3.天津药物研究院,天津 300193;4.天津药物研究院药业有限责任公司,天津 300193)
脑康通泰分散片由银杏叶、丹参、川芎等药材组成,具有活血化瘀、通经活络等功效,主要用于脑中风后遗症,具有较好的疗效。制成分散片后在水中能迅速崩解均匀分散,与普通片剂相比具有崩解迅速、吸收快、生物利用度高等特点,也可加水分散后冲服用或含于口中吞服、吮服,分散片兼有片剂和液体制剂的优点,尤其适合于老、幼及吞含药物有困难的患者[1],制备脑康通泰分散片具有临床用药顺应性和市场开发前景,笔者对脑康通泰分散片的处方工艺进行研究并对其溶出度测定方法进行研究。
1 仪器与试药
1.1 仪器 ZRS-8G智能溶出试验仪 (天津天大天发科技有限公司),UV-2550紫外-可见分光光度计(日本岛津),单冲压片机(北京国药龙立科技有限公司),ZB-1C智能崩解仪(天津大学精密仪器厂)。
1.2 试药 磷酸氢钙,连云港德邦化工有限公司;微晶纤维素,德国JRS公司;交联聚维酮,德国JRS公司;二氧化硅,湖州展望化学药业有限公司;硬脂酸镁,营口奥达制药有限公司。自制脑康通泰分散片(批号 20100701、20100702、20100703);自制脑康通泰片(批号 20100710、20100711、20100712)、自制脑康通泰胶囊(批号 20100805、20100806、20100807)。
2 方法与结果
2.1 处方前研究 脑康通泰浸膏为淡褐色粉末,几乎不溶于水和乙醇,略有吸潮。根据药理实验结果和拟定的临床人用剂量确定制剂规格(标示量)为每片含脑康通泰浸膏200 mg。按照中国药典对分散片的要求,笔者对处方筛选的原则以休止角、硬度、崩解时限、颗粒流动性等为指标考察处方。
2.2 处方筛选与制备工艺
2.2.1 处方筛选 根据分散片的常用处方并结合脑康通泰的特点及质量考核标准进行筛选[2-3],处方筛选设计见表1。综合考察分析,最终采用处方6。
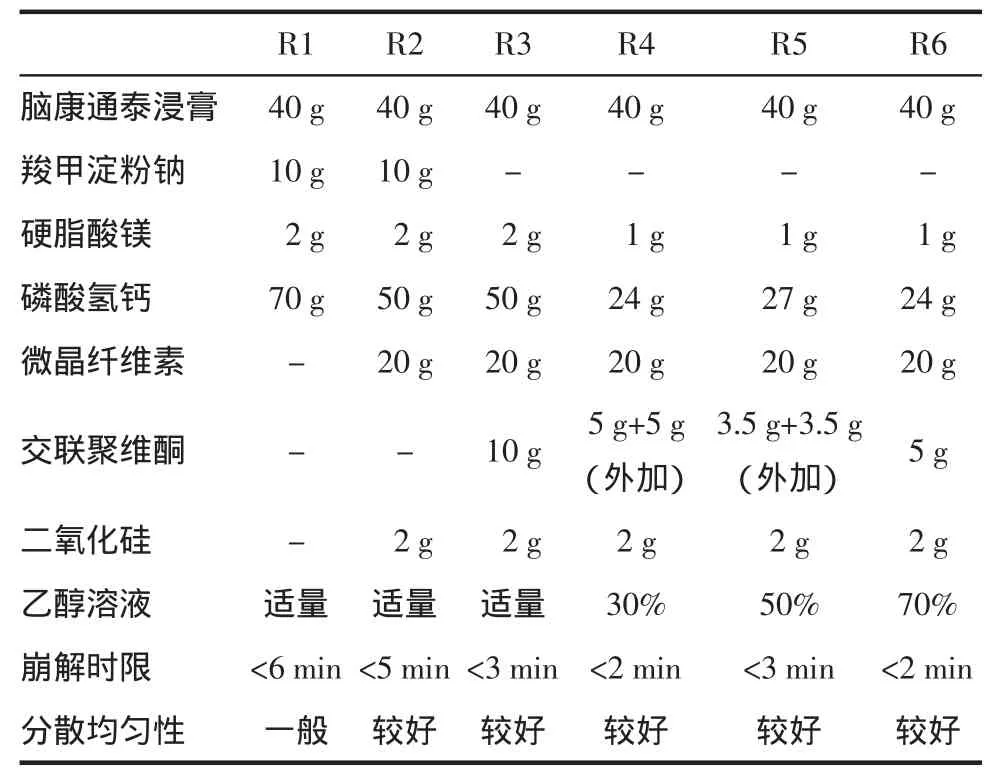
表1 处方设计Tab.1 Formulation design
以R1为基础处方,对崩解剂进行筛选得出交联聚维酮为崩解剂优于羧甲基淀粉钠,加入二氧化硅后片子的崩解速度大大提高,同时能够使主料达到充分的分散作用。由于加入的辅料量比较大,片子外观也不美观,且片面有花斑,外观不美观。为了改变片面外观、降低用量,对处方中的辅料进行调整,综合物料流动性及崩解情况认为,处方6各个指标都达到分散片的要求。
2.2.2 制备工艺 将浸膏粉过80目筛,辅料过100目筛。先称取处方量辅料混合均匀,加入脑康通泰浸膏粉充分混匀,用70%乙醇制软材,24目筛制粒,55℃烘干2 h。将上述颗粒加入硬脂酸镁、二氧化硅充分混匀,24目筛整粒,按标示量压片。
2.3 优化处方的性质考察[4]片剂外观:片表面色泽均匀、完整光洁、硬度适中。
崩解时限:取本品6片,置于崩解仪吊篮的玻璃管中,浸入1000 mL烧杯中,启动仪器,各片均应在药典规定时间内全部崩解。
分散均匀性:取本品2片,置于100 mL水中,充分搅拌分散均匀,3 min内颗粒能全部通过2号筛,符合中国药典规定。
2.4 溶出度检查[5]
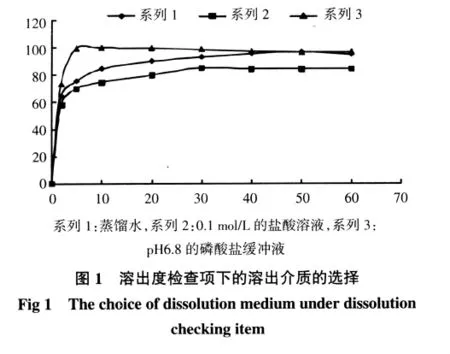
2.4.1 溶出介质选择 选择了蒸馏水,0.1 mol/L的盐酸溶液,pH6.8的磷酸盐缓冲液进行比较实验,结果见图1。从图1可见在蒸馏水,0.1 mol/L的盐酸溶液,pH6.8的磷酸盐缓冲液之间,在0~3 min内,3条曲线走势相同,3 min以后系列3迅速提升易导致突释;系列2上升速度最慢;系列1提升速度居中。比较而言,系列1提升速度居中且走势平滑。最终采用900 mL蒸馏水为溶出介质,既经济又方便。
2.4.2 波长选择 取本品10片,精密称定,研细,精密称取适量(约相当于平均片质量),加蒸馏水900mL,水浴50℃加热30 min,放冷,量取续滤液5 mL,加蒸馏水稀释至10 mL,摇匀。于紫外-可见分光光度计上在190~500 nm波长处扫描,结果最大吸收波长为270 nm。
取空白混合辅料500 mg,按上述方法操作,结果在270 nm处无吸收峰,阴性无干扰,故选用270 nm为测定波长。
2.4.3 百分之百释放量的吸收度测定 取本品10片,精密称定,研细,精密称取适量(约相当于平均片质量),至900 mL三角量瓶中,加蒸馏水900 mL,水浴50℃加热30 min,放冷,滤过,量取续滤液5 mL,加蒸馏水稀释至10 mL,摇匀。于270 nm波长处测定吸收度。
2.4.4 标准曲线制备 取本品10片,精密称定,研细,精密称取适量(约相当于平均片质量),至900 mL三角量瓶中,加蒸馏水900mL,水浴50℃加热30min,放冷,滤过,将此时滤液指定为相当于溶出度的100%,再分别吸取 1、2、4、5、6、8mL 分别置于 10 mL量瓶中,加蒸馏水稀释至刻度,摇匀,以蒸馏水为空白,分别于270 nm处测定吸收度。以相对标示量(%)为横坐标,吸收度为纵坐标作图,得标准曲线。吸收度在0.137~1.280之间呈良好的线性关系。标准曲线的回归方程为Y^=0.012 7X+0.ue=1,相关系数r=0.9999。
2.4.5 溶液稳定性实验 取20100701批样品,依法操作,于室温下分别取溶液两份,在 0、15、30、45、60、90、120 min于270 nm处测定吸收度,吸光度无明显变化。求得相对标准偏差(RSD)为0.21%,表明该溶液在2 h内稳定。
2.4.6 重复性实验 取20100701批样品,照《中国药典》溶出度测定法,以900 mL水为溶出介质,选择转速为 100 r/min,依法操作,经 2、5、10、20、30、40、50和60 min时,取溶液8 mL,滤过,精密量取续滤液5 mL,加蒸馏水稀释至10 mL,摇匀。分别于270 nm波长处测定吸收度,计算每片的溶出度,按上述方法重复操作6次,结果显示全溶出曲线均一性良好,RSD%均小于2%。
2.5 溶出度测定 由于中药制剂化学成分的复杂性以及中国中药制剂发展的特殊性,对中药制剂中体外溶出度实验的研究方法还不太成熟,国家药品中还没有收载含中药溶出度检查的项目。在研究过程中参照《中国药典》溶出度测定法进行测定。根据脑康通泰分散片的特点,并查阅了大量文献,确定以900 mL水为溶出介质,转速为100 r/min,并且于270 nm波长处测定吸收度。此方法测定溶出度准确、可靠,能准确地反映该药物的体内体外的相关性。
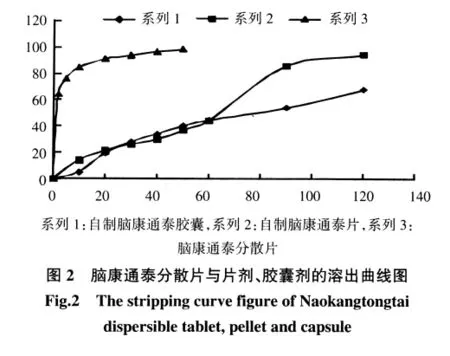
2.6 自制分散片与自制普通制剂溶出度对比 分别取自制脑康通泰片与自制脑康通泰胶囊,依照《中国药典》溶出度测定法,以900 mL水为溶出介质,选择转速为 100 r/min,依法操作,经 10、20、30、40、50、60、90 和 120 min 时,取溶液 8 mL,滤过,精密量取续滤液5 mL,加蒸馏水稀释至10 mL,摇匀。分别于270 nm波长处测定吸收度,计算溶出度,绘制溶出度-时间曲线图与脑康通泰分散片的溶出曲线图进行比较,结果表明分散片30 min溶出度达到75%以上,而同比片剂和胶囊剂只有30%,其溶出度明显优于脑康通泰片与脑康通泰胶囊。结果见图2。
3 讨论
1)由于本品以中药浸膏为原料,其黏度大、吸湿性强,故崩解时限的关键是选择适合的崩解剂,本品处方以交联聚维酮与二氧化硅为混合崩解剂,有效地增加了分散片的崩解性。
2)本实验采用湿法制粒压片法制备分散片,在制软材步骤中黏合剂的选择及用量起到重要作用,经过实验筛选,30%的乙醇所制的软材时有结块,50%的乙醇略好,为了混合均匀,所以选择70%的乙醇作黏合剂最好。
3)以确定的溶出度的测定方法,比较脑康通泰分散片与普通片,胶囊的溶出度,结果显示分散片30 min溶出度达到75%以上,而同比普通片剂和胶囊剂只有30%,其溶出度明显优于脑康通泰片与脑康通泰胶囊。
[1]冯耀荣,袁 强.中药口服给药新剂型研究进展[J].中华中医药学刊,2009,27(4):793-795.
[2]吴培源,段 韵,朱祖驰.中药分散片的处方设计与优选试验[J].中国医药导报,2008,5(2):44-46.
[3]杨心刚,段国豪,赵仪学.花红分散片的制备工艺及质量控制[J].时珍国医国药,2008,19(5):1208-1209.
[4]国家药典委员会.中国药典二部[S].北京:中国医药科技出版社,2010:附录5.
[5]向 阳,黄志军,熊富良,等.银杏叶分散片的溶出度研究[J].药物分析杂志,2010,30(8):1428-1431.

