吉西他滨联合顺铂治疗晚期三阴性乳腺癌的临床观察
吴梅红,王 梅,王雅杰
(第二军医大学附属长海医院肿瘤科,上海200433)
三阴性乳腺癌(triple-negative breast cancer,TNBC)是指雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)及人类表皮生长因子受体2(human epidermal growth factor receptor-2,HER-2)均表达为阴性的乳腺癌,大多数分子分型为basal-like型[1]。此类型乳腺癌对蒽环类和紫杉类药物为主的化疗方案敏感,但有较高的复发和远处转移率,预后最差。对于晚期转移的TNBC患者,因已在辅助治疗中使用过蒽环、紫杉及环磷酰胺类药物,姑息化疗尤其是一线治疗失败后的二线方案选择受限。吉西他滨联合顺铂是转移性乳腺癌治疗的有效策略之一,研究证实TNBC可能对DNA损伤的顺铂更为敏感[2]。近期国外的多项Ⅱ期临床试验提出,相对于非 TNBC,吉西他滨联合顺铂对TNBC的疗效更优[3]。本研究回顾性分析了2007年1月至2010年12月间37例使用吉西他滨联合顺铂方案化疗的复发或转移的晚期乳腺癌患者,现将结果报道如下。
1 资料与方法
1.1 一般资料 37例女性乳腺癌患者,发病年龄37~56岁,中位年龄 47岁。均行乳腺改良根治术或扩大根治术后,原发肿瘤经病理学证实为乳腺癌且行免疫组化检测。ER、PR(-)的判断标准是免疫组织化学法(immunohistochemistry,IHC)(-),HER-2(-)的判断标准是 IHC(-)、IHC(+)或IHC(++)但经显色原位杂交法/荧光原位杂交法进一步检测为阴性。至少有1个可测量的客观病灶。既往已在新辅助、辅助或姑息化疗中应用过蒽环类和紫杉类药物。现有经CT、磁共振成像、全身骨扫描或穿刺取活检等检查确诊的转移病灶,至少有1个病灶可测量。
1.2 分组及化疗方案 37例患者,根据 ER、PR、HER-2表达情况分为2组,ER、PR、HER-2均为阴性为TNBC组;另一组为非TNBC。化疗方案为吉西他滨联合顺铂,具体用药为:吉西他滨1000 mg/m2静脉滴注第1、8天;顺铂75 mg/m2静脉滴注,总量分3 d给予,每21天重复。每周期评价不良反应,化疗3个周期后评价疗效。化疗时常规予以止吐等辅助用药,出现Ⅲ度以下不良反应按常规处理,出现Ⅲ度以上不良反应化疗药物减量。如肿瘤病灶进展则更换化疗方案。
1.3 疗效和不良反应评价 疗效评价按实体瘤疗效评价标准,分为完全缓解(complete remission,CR),部分缓解(partial remission,PR),稳定(stable disease,SD)及进展(progressive disease,PD)。CR、PR和SD患者应在4周后再次重新测量肿瘤病灶,仍达CR、PR和SD标准者方可最后评定为CR、PR和SD。有效率为获得CR或PR的患者数占总患者数的百分比,疾病获益率(disease benefit rate,DBR)为获得CR、PR及SD的患者数占总患者数的百分比。患者出现PD立即更换化疗方案。无进展生存期(progression free survival,PFS)为化疗开始到肿瘤出现继发进展生长的时间。毒性反应参照WHO(1998年)抗癌药物急性或亚急性不良反应的评价标准分成0~Ⅳ度。
1.4 统计学方法 采用SPSS 16.0软件进行统计分析。发生率以个数和百分比表示。正态分布数据以均数±标准差(±s),均数比较采用t检验,率的比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床特征 TNBC组8例,中位年龄46岁;非TNBC组29例,中位年龄48岁。两组临床特征见表1。
2.2 有效率、控制率及PFS 所有患者总有效率为37.8%,其中TNBC组总有效率为37.5%,非 TNBC组总有效率为37.9%。两组比较,差异无统计学意义(χ2=0.000495,P >0.05)。所有患者总获益率为67.6%,其中 TNBC组为87.5%,非 TNBC组为62.1%,两组比较,差异无统计学意义(χ2=1.85,P>0.05)。但 TNBC组中,PFS长于非 TNBC组(表2)。
2.3 疗效影响因素观察 对各组进行影响因素分析后,考虑疗效的可能影响因子有转移部位、现转移灶、靶向治疗及GP方案应用时期,但因病例数有限,分析误差较大。值得提出的是非TNBC组中ER-HER2+亚组1例患者,多发淋巴结转移,二线应用本方案化疗,联合Herceptin疗效达CR,PFS为13.0个月。
2.3.1 患者转移灶情况 TNBC组中转移灶数目<2个4例,2例PR,2例 SD,均临床获益,平均PFS(6.6±3.1)个月。对比转移灶数目>2个4例,1例PR,2例 SD,平均 PFS(3.7 ±2.0)个月,两组比较差异有统计学意义(t=3.59,P <0.01)。
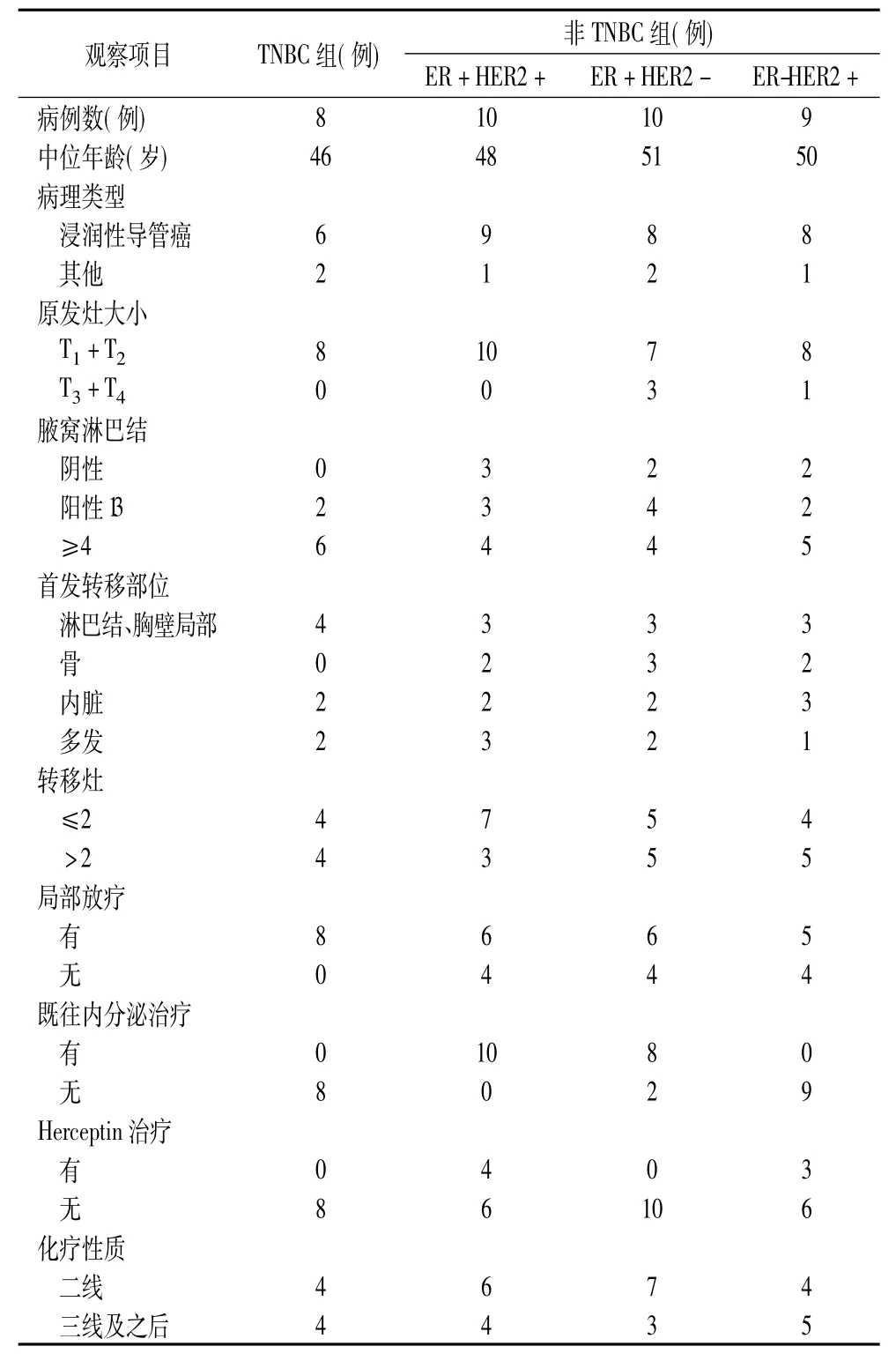
表1 两组患者临床特征
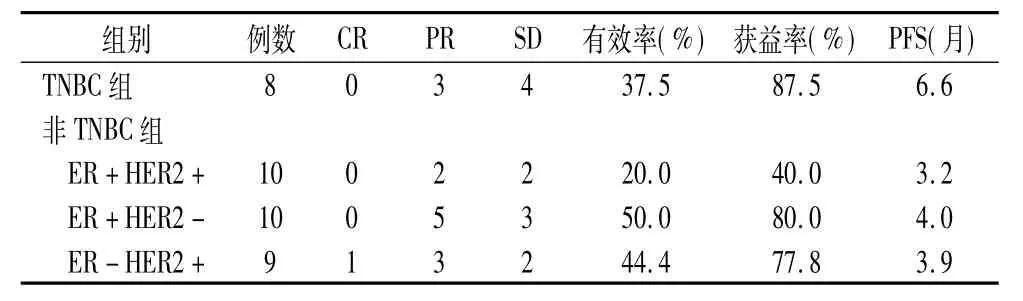
表2 两组有效率、获益率及PFS
2.3.2 化疗性质 TNBC中二线化疗4例,2例PR,2例SD,均临床获益,平均PFS 7.46个月。三线及之后化疗4例,1例PR,2例SD,平均PFS 5.5个月。
2.3.3 化疗疗效 与非TNBC组的各亚组相比,TNBC组疗效明显优于非TNBC组ER+HER2+组,有效率分别为37.5%和20.0%,两组比较差异极显著(χ2=8.10,P <0.01);临床获益率分别为 87.5%和40.0%,两组比较差异显著(χ2=4.23,P <0.05);PFS分别为6.6个月和3.2个月(表2)。
2.4 不良反应 主要观察到的不良反应为骨髓抑制及消化道反应。实验中观察到非TNBC性组1例因Ⅳ度骨髓抑制而换用其他方案治疗。两组不良反应中骨髓抑制以白细胞减少及血小板降低为主,TNBC组及非 TNBC组3~4度白细胞减少分别为1例、6例,3~4度血小板减少分别为2例、3例,两组各项比较差异无统计学意义(χ2=1.39,P >0.05)。偶见肝脏功能损伤及皮疹。所有不良反应在停药后或对症处理后可恢复正常。
3 讨论
TNBC的发病风险及复发转移的模式均异于其他亚型的乳腺癌。对于复发或转移性乳腺癌患者的一线化疗方案,NCCN指南已提出首选蒽环类联合紫杉类,而对于一线失败的患者,指南尚无明确推荐。
吉西他滨联合顺铂方案在临床已广泛应用于非小细胞肺癌、晚期胆系肿瘤、膀胱癌等恶性肿瘤。该方案用于非小细胞肺癌中疗效与紫杉类药物联合顺铂方案相比无统计学差异[4],在膀胱癌中与含蒽环类的甲氨蝶呤、长春新碱、阿霉素和顺铂(M-VAC)方案相比疗效相同,而安全和耐受性更好[5]。临床上,该联合方案用于乳腺癌的多个Ⅱ期临床试验结果也已报道,吉西他滨联合顺铂方案是晚期转移的乳腺癌,经蒽环类及紫杉类药物治疗失败后的又一选择。徐兵河等[6]在多个国内临床试验中报道,蒽环类耐药的乳腺癌中该方案治疗的总有效率为44%~52%,主要的毒性反应为中性粒细胞和血小板减少[7]。因此,吉西他滨联合顺铂治疗晚期乳腺癌有效且毒性可耐受。在一项国外的多因素分析[8]中,TNBC亚组中3年无疾病进展及总生存均低于非TNBC亚组(分别为63%对76%,HR=1.86,P < 0.01;74% 对 89%,HR=2.53,P <0.01)。在先前几乎无化疗的患者中,ER/PR(-)亚组缓解率为43%(9/21),而ER/PR(+)亚组缓解率为8%(2/25)(HER2结果不详)[3]。而另一项回顾性研究中[9],TNBC与非TNBC的中位无进展生存期分别为5.3个月和1.7个月(P=0.058)。吉西他滨联合顺铂方案对晚期乳腺癌患者疗效确切,且可能对TNBC患者疗效优于非TNBC患者。
乳腺癌的治疗手段较多,本研究中患者多在既往治疗中已采用多种治疗手段,因此,主要观察指标PFS受多个个体因素影响。本研究中行吉西他滨联合顺铂方案治疗晚期乳腺癌患者,总有效率为37.8%,其中TNBC组总有效率为37.5%,非 TNBC组总有效率为37.9%。两组相比PFS有明显差异(6.6个月对3.7个月),TNBC组较非TNBC组延长明显,与目前国内外报道相仿[10]。转移灶情况、化疗性质可能是化疗效果的主要影响因素。在本研究中发现转移灶数目少,二线治疗的TNBC患者疗效优于转移灶数目多、三线及之后治疗的患者。
与非TNBC组的各亚组相比,TNBC组疗效明显优于非TNBC组ER+HER2+组。尽管ER+HER2+组有内分泌治疗及Herceptin治疗的优势,但在本研究中,对吉西他滨联合顺铂方案的疗效却差于TNBC,其原因可能与TNBC的病理特点及吉西他滨与顺铂的作用机制有关。多数TNBC患者伴随着BRCA1基因的突变。正常BRCA1基因可通过激活S期和G2/M期DNA损伤检测点及后续DNA修复机制导致肿瘤细胞对损伤DNA靶向的化疗药物耐药。同时,它也可以激活细胞有丝分裂的纺锤体检测点而激活凋亡途径使肿瘤细胞对作用于纺锤体的药物敏感[11,12]。因而,理论上BRCA1基因功能缺失会使肿瘤细胞对损伤DNA靶向的化疗药物如顺铂敏感。顺铂可通过与DNA结合形成链内、链间交叉键,从而破坏DNA。而吉西他滨主要作用于G/S期,在细胞内经脱氧胞嘧啶激酶作用,活化成具有活性的代谢产物双氟二磷酸脱氧胞苷和双氟三磷酸脱氧胞苷,且其本身还可以抑制脱氧胞嘧啶脱氨酶,减少细胞内代谢物的降解而具有自我增效的作用。双氟二磷酸脱氧胞苷和双氟三磷酸脱氧胞苷可以抑制DNA合成,干扰DNA的自我修复,且可阻止RNA的合成,最终导致细胞凋亡。吉西他滨800~1200 mg/m2在乳腺癌的治疗中单药的一线治疗的有效率为25%~37%,二线治疗中为18%~28%[13],已于2004年被批准为转移性乳腺癌的一线用药。在体外实验中也已经证实吉西他滨和顺铂联合用药具有协同作用,吉西他滨可以克服由于细胞上调DNA修复基因导致的顺铂耐药[14]。
多西他赛联合表阿霉素往往是临床最常选择的一线治疗方案,而临床多选的二线治疗方案多为紫杉类为主的联合方案或蒽环类为主的联合方案。本研究中吉西他滨联合顺铂治疗TNBC与目前美国国家综合癌症网络指南推荐的治疗复发转移性乳腺癌的标准方案吉西他滨联合紫杉醇相比[15],疗效相当,有效率分别为37.5%和41.4%,PFS为6.6个月和6.14个月。可能影响本方案疗效的影响因素有转移灶情况及应用时期等。但因本研究病例数较少,尚待进一步扩大样本量行临床观察以证实。
综上所述,吉西他滨联合顺铂化疗方案对于晚期一线复发的TNBC疗效较非TNBC更为敏感,值得临床推广,针对TNBC患者特别是一般情况较好,内脏转移病灶数目不多及二线化疗者尤为推荐。
[1]Kreike B,Van KM,Horlings H,et al.Gene expression profiling and histopathological characterization of triple-negative/basal-like breast carcinomas[J].Breast Cancer Res,2007,9(5):R65.
[2]Uhm JE,Park YH,Yi SY,et al.Treatment outcomes and clinicopathologic characteristics of triple-negative breast cancer patients who received platinum-containing chemotherapy[J].J Cancer,2009,124(6):1457-1462.
[3]Chew HK,Doroshow JH,Frankel P,et al.Phase Ⅱ studies of gemcitabine and cisplatin in heavily and minimally pretreated metastatic breast cancer[J].J Clin Oncol,2009,27(13):2163-2169.
[4]Schiller JH,Harrington D,Belani CP,et al.Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer[J].N Engl J Med,2002,346(2):92-98.
[5]Von der MH,Sengelov L,Roberts JT,et al.Long-term survival results of a randomized trial comparing gemcitabine plus cisplatin,with methotrexate,vinblastine,doxorubicin,plus cisplatin in patients with bladder cancer[J].J Clin Oncol,2005,23(21):4602-4608.
[6]徐兵河,李凯,刘端琪,等.吉西他滨联合顺铂治疗50例蒽环类耐药性晚期乳腺癌[J].中国癌症杂志,2003,13(6):579-581.
[7]路丹,李永萍.吉西他滨及其联合方案治疗晚期乳腺癌的研究进展[J].医学综述,2009,15(21):3291-3293.
[8]Liedtke C,Mazouni C,Hess K,et al.Response to neoadjuvant therapy and long-term survival in patients with triple-negative breast cancer[J].J Clin Oncol,2008,26(15):43.
[9]Koshy N,Quispe D,Shi R,et al.Cisplatin-gemcitabine therapy in metastatic breast cancer:improved outcome in triple negative breast cancer patients compared to non-triple negative patients[J].Breast,2010,19(3):246-248.
[10]Somali I,Alacacioglu A,Tarhan MO,et al.Cisplatin plus gemcitabine chemotherapy in taxane/anthracycline-resistant metastatic breast cancer[J].Chemotherapy,2009,55(3):155-160.
[11]Farmer H,McCabe N,Lord CJ,et al.Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy[J].Nature 2005,434(7035):917-921.
[12]陈露.国产吉西他滨联合顺铂治疗48例晚期乳腺癌临床观察[J].中国医药导报,2011,32(17):70-71.
[13]Seidman AD.Gemcitabine as single-agent therapy in the management of advanced breast cancer[J].Oncology,2001,15(2):11-14.
[14]Achanta G,Pelicano H,Feng L,et al.Interaction of p53 and DNAPK in response to nucleoside analogues:Potential role as a sensor complex for DNA damage[J].Cancer Res,2001,61(24):8723-8729.
[15]Albain KS,Nag SM,Calderillo-Ruiz G,et al.Gemcitabine plus Paclitaxel versus Paclitaxel monotherapy in patients with metastatic breast cancer and prior anthracycline treatment[J].J Clin Oncol,2008,26(24):3950-3957.

