N,N-二苄基-L-谷氨酸及其金属配合物的合成、表征及生物活性
金龙飞,王彦荣,吴勇飞,吴腊梅
(中南民族大学 化学与材料科学学院,武汉 430074)
生物能量体系中主要组分有ATP、ADP和相关的酶系,其ATP为生物体系细胞能量成分,是能量的贮存和转运载体.在生物体中,ATP与ADP的转换,通过ATP合酶的参与,能够正常自如的进行.由Efraim Racker等从牛心线粒体中提取的F0F1-ATPase,可利用跨膜的电化学质子梯度驱动ADP磷酸化生成ATP.在F0F1-ATPase中,催化中心为F1头部(F1-ATPase),是生物体能量转换的核心酶[1-3].研究和模拟F0F1-ATPase和F1-ATPase,设计高效专一的三磷酸腺苷分解酶模型化合物,将生物能量体系改造或移植到宏观应用体系,具有重要的理论意义与实际意义.
基于谷氨酸与三磷酸腺苷分解酶和辅酶的特征结构残基基团的相似性,因而研究谷氨酸衍生物及其配合物,将有可能寻找到影响三磷酸腺苷分解活性的化合物或配合物.在研究L-谷氨酸-5-甲酯及其配合物中,笔者已经得到初步的证实[4].本文拟进一步以L-谷氨酸为原料合成N,N-二苄基-L-谷氨酸(H2bbga)(见图1)及其金属配合物,并考察修饰后的谷氨酸衍生物及其金属配合物对三磷酸腺苷分解的生物活性.本文所研究的工作,拟将为深入研究具有三磷酸腺苷分解酶和辅酶活性的模拟化合物打下较好的基础.
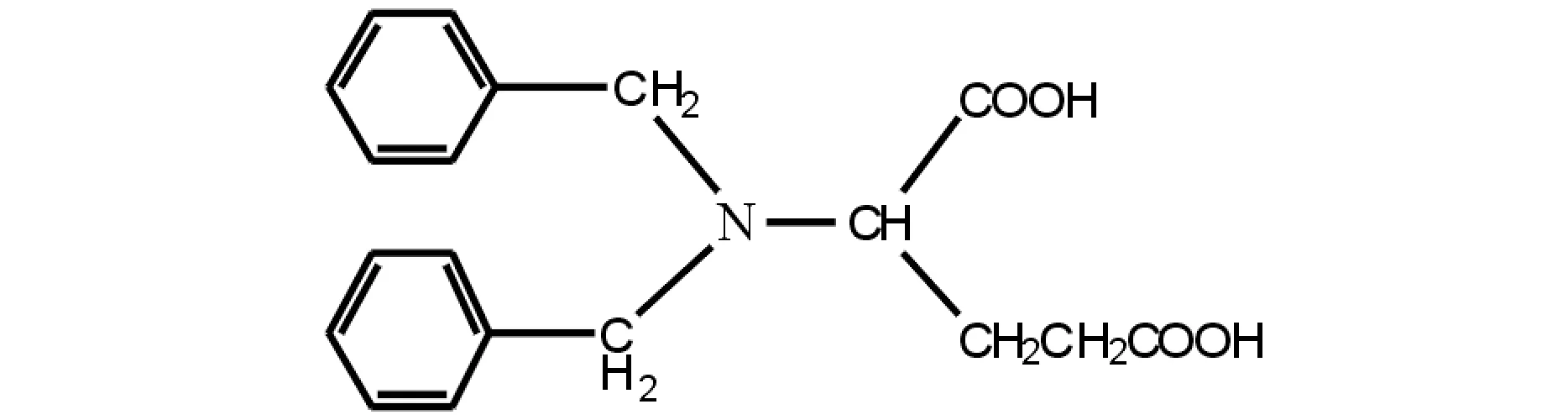
图1 N,N-二苄基-L-谷氨酸
1 实验部分
1.1 仪器和试剂
Perkin Elmer 2400 CHN 型元素分析仪;FT-IR NEXUS智能型高分辨傅立叶红外光谱仪:KBr压片;VARIAN Mercury PLUS-300核磁共振仪:溶剂为DMSO-d6;UV-265可见紫外分光光度计:25 ℃测量,波段范围190~700 nm;pH-25型酸度计;X-4数字熔点仪.
氯化苄、无水甲醇、无水乙醇、无水乙醚、MgCl2·6H2O、Ca(OH)2、MnCl2·4H2O、NiCl2·6H2O、CoCl2·6H2O、CuCl2·2H2O、ZnCl2、NaOH、Na2CO3·10H2O、N,N-二甲基甲酰胺(DMF)、盐酸、硫酸、LiOH、钼酸铵、硫酸亚铁,均为分析纯;L-谷氨酸、三磷酸腺苷二钠,为生物试剂.
1.2 实验方法
1.2.1 H2bbga的合成
H2bbga的合成参照文献[5]进行.取L-谷氨酸2.94 g (0.02 mol)和NaOH 1.60 g (0.04 mol),室温下将二者于50 %乙醇溶液中混合均匀.搅拌下加入氯化苄4.60 mL (0.04 mol).加热回流,并分批加入5.72 g (0.02 mol)Na2CO3·10H2O.反应4 ~ 5 h后,减压蒸馏除去溶剂,加入4.0 mol·L-1HCl至不再产生沉淀为止(pH = 2.0 ~ 3.0).过滤,并用热水和乙醚洗涤.所得产物用水进行重结晶.室温下真空干燥至恒重.纯品为白色粉末状固体.产率: 79.9 %.m.p.= 214 ~ 215 ℃.元素分析,测定值:C 69.79,H 6.28,N 4.37 %;计算值(C19H21NO4):C 69.71,H 6.17,N 4.28 %.1H NMR(DMSO-d6),δ:12.24 (s,2H),7.20 ~ 7.38 (m,10H),3.55 ~ 3.85 (m,4H),3.10 ~ 3.20(t,1H,J=7.50Hz),2.15 ~ 2.40 (m,2H),1.85 ~ 1.95 (m,2H).FT-IR (KBr压片,cm-1):3030 vs br,1616 vs,1404 s,1028 s ,1581 s,1495 m,776 m,696 m.UV-vis:在230 nm (以DMF作溶剂)处有吸收峰.
1.2.2 N,N-二苄基-L-谷氨酸镁配合物([Mg(bbga)(H2O)]·2H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75 %乙醇中,加热至50 ℃,搅拌,并缓慢滴加3 mL溶有0.12 g (0.60 mmol)MgCl2·6H2O的50 % 乙醇溶液,用0.10 mol·L-1的NaOH溶液调节pH = 6.0 ~ 6.5至不再出现沉淀为止.继续搅拌反应3 ~ 4 h.反应完毕后,减压蒸馏,加入10 ~ 15 mL无水乙醚.待溶液中出现大量白色沉淀物后,过滤,用蒸馏水洗涤,干燥.产率: 65.2 %,m.p > 300 ℃.元素分析,测定值:C 56.32,H 6.01,N 3.22 %;计算值(C19H25MgNO7):C 56.53,H 6.24,N 3.47 %.FT-IR (KBr压片,cm-1):3482 s,3032 vs br,1611 vs,1408 s,1583 s,1032 s ,748 m,706 m,556 m,465 m.
1.2.3 N,N-二苄基-L-谷氨酸钙配合物([Ca(bbga)(H2O)]·2H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75 %乙醇中,加热至50 ℃,搅拌,并缓慢滴加5 mL溶有0.04 g (0.05 mmol)Ca(OH)2的50 %乙醇溶液,调节pH = 6.0 ~ 7.0至不再出现沉淀.继续反应3 ~ 4 h.反应完毕后,减压蒸馏,然后加入10 ~ 15 mL无水乙醚,待溶液中出现大量白色沉淀物后,过滤,用蒸馏水洗涤,干燥.产率: 75.3 %,m.p.> 300 ℃.元素分析,测定值:C 54.11,H 5.82,N 3.30 %;计算值(C19H25CaNO7):C 54.40,H 6.01,N 3.34 %.FT-IR (KBr压片,cm-1):3480 s,3026 vs br,1611 vs,1406 s,1582 s,1030 s ,749 m,700 m,539 m,438 m.
1.2.4 N,N-二苄基-L-谷氨酸锰配合物([Mn(bbga)(H2O)]·2H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75 % 乙醇中,加热至50 ℃,搅拌,并缓慢滴加3 mL溶有0.11 g (0.55 mmol)MnCl2·4H2O的无水乙醇溶液,用0.10 mol·L-1的NaOH溶液调节pH = 5.5 ~ 6.0,溶液变为浅黄色.继续反应3 ~ 4 h.反应完毕后,减压蒸馏,然后加入10 ~ 15 mL无水乙醚.待溶液中出现灰色沉淀物,过滤,用蒸馏水洗涤,干燥.产率: 82.2 %.m.p.> 300 ℃.元素分析,测定值:C 52.42,H 5.67,N 3.14 %;计算值(C19H25MnNO7):C 52.54,H 5.80,N 3.22 %.FT-IR (KBr压片,cm-1):3382 vs br,3025 vs br,1618 vs,1405 s,1582 s,1029 s ,744 m,710 m,553 m,436 m.
1.2.5 N,N-二苄基-L-谷氨酸钴配合物([Co(bbga)(H2O)]·H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75% 乙醇中,加热至50 ℃,搅拌,并缓慢滴加3 mL溶有0.13 g (0.55 mmol)CoCl2·2H2O的无水乙醇溶液,用0.10 mol·L-1的NaOH溶液调节pH = 5.0 ~ 5.5,溶液由浅红色变为深红色.继续反应3 ~ 4 h.反应完毕后,减压蒸馏,然后加入10 ~ 15 mL无水乙醚,溶液中出现浅红色沉淀物.过滤,用蒸馏水洗涤,干燥.产率: 76.1 %,m.p.> 300 ℃.元素分析,测定值:C 54.11,H 5.38,N 3.09 %;计算值(C19H23CoNO6):C 54.29,H 5.52,N 3.33 %.FT-IR (KBr压片,cm-1):3400 vs br,3027 vs br,1614 vs,1407 s,1582 s,1031 s ,751 m,703 m,556 m,446 m.
1.2.6 N,N-二苄基-L-谷氨酸镍配合物([Ni(bbga)(H2O)]·H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75% 乙醇中,加热至50 ℃,搅拌,并缓慢滴加3 mL溶有0.13 g (0.55 mmol)NiCl2·6H2O的无水乙醇溶液.用0.10 mol·L-1的NaOH溶液调节pH = 5.0 ~ 6.0,溶液颜色加深.继续反应3 ~ 4 h.反应完毕后,减压蒸馏,然后加入10 ~ 15 mL无水乙醚,溶液中出现浅绿色沉淀物.过滤,用蒸馏水洗涤,干燥.产率: 78.9 %,m.p.> 300 ℃.元素分析,测定值:C 54.14,H 5.36,N 3.15 %;计算值(C19H23-NNiO6):C 54.32,H 5.52,N 3.33 %.FT-IR (KBr压片,cm-1):3402 vs br,3024 vs br,1613 vs,1413 s,1588 s,1029 s ,745 m,705 m,539 m,442 m.
1.2.7 N,N-二苄基-L-谷氨酸铜配合物([Cu(bbga)(H2O)]·H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75 %乙醇中,在35 ℃下搅拌使其完全溶解.然后缓慢滴加5 mL溶有0.10 g (0.60 mmol)CuCl2·2H2O的无水乙醇溶液.溶液中出现绿色沉淀.继续反应3 ~ 4 h.反应完毕后,冷却至室温,过滤,蒸馏水洗涤,干燥.产率: 75.6 %,m.p.> 300℃.元素分析,测定值:C 53.58,H 5.40,N 3.21 %;计算值(C19H23CuNO6):C 53.70,H 5.46,N 3.30 %.FT-IR (KBr压片,cm-1):3390 vs br,3029 vs br,1610 vs,1407 s,1580 s,1029 s ,749 m,700 m,526 m,463 m.
1.2.8 N,N-二苄基-L-谷氨酸锌配合物([Zn(bbga)(H2O)]·2H2O)的合成
将0.33 g (1.00 mmol)H2bbga溶于20 mL 75 % 乙醇中,加热至50 ℃,搅拌,并缓慢滴加3 mL溶有0.8 g (0.55 mmol)ZnCl2的无水乙醇溶液.用0.10 mol·L-1的NaOH溶液调节pH=6.0 ~ 5.5.继续反应3 ~ 4 h.反应完毕后,减压蒸馏,再加入10 ~ 15 mL无水乙醚,溶液中出现白色沉淀物.过滤,用蒸馏水洗涤,干燥.产率: 78.2 %,m.p.> 300 ℃.元素分析,测定值:C 51.23,H 5.52,N 3.02 %;计算值(C19H25NO7Zn):C 51.31,H 5.67,N 3.15 %.FT-IR (KBr压片,cm-1):3398 vs br,3026 vs br,1613 vs,1408 s,1582 s,1033 s ,746 m,703 m,529 m,455 m.
1.2.9 化合物对三磷酸腺苷二钠分解的催化活性测试
反应终止后,其反应液中无机磷含量可衡量三磷酸腺苷二钠催化分解反应的效果(活性).基于无机磷可与硫酸钼酸铵反应生成有色化合物,因此无机磷含量可采用比色法测定.
具体化合物对三磷酸腺苷二钠分解活性的测定,可通过测定混合体系的OD值后,比较无机磷标准曲线得相应的无机磷含量,即可判断出活性影响[4].
2 结果与讨论
2.1 合成和结构光谱分析
2.1.1 配体N,N-二苄基-L-谷氨酸(H2bbga)的组成及结构
H2bbga不溶于水、乙醚,可溶于甲醇、乙醇,在甲醇中的溶解度较乙醇大,并易溶于DMF、DMSO等极性较大的有机溶剂.元素分析的测量结果与理论计算结果相符,证明了合成产物与拟合成化合物元素组成的一致性.
1H NMR谱图中,12.24处的单峰可归属为 2 个-COOH的质子,7.20 ~ 7.38处的多重峰可归属为2个Ar-的质子,3.55 ~ 3.85处的多重峰可归属为2个Ar-CH2-的质子,3.10 ~ 3.20处的三重峰可归属为N-CH-的质子,2.15 ~ 2.40处的多重峰可归属为亚甲基-CH2-COOH的质子,1.85 ~ 1.95处的多重峰可归属为亚甲基-CH2-CH2-COOH的质子.
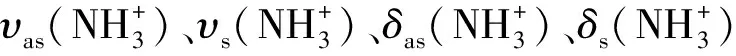
UV-vis光谱中,在 230 nm (以DMF作溶剂)处存有一个吸收峰,可认为因苯环上的C=C双键的π-π*跃迁而产生的.
2.1.2 H2bbga配合物的组成及红外光谱
采用等摩尔系列法对H2bbga与MnCl2·4H2O、NiCl2·6H2O、CoCl2·6H2O、和CuCl2·2H2O形成的配合物的组成比进行了测定.结果表明,这些配合物的组成比均为1∶1.另外对配合物进行了银氨溶液定性分析,检验的结果证实所有配合物均未含有氯离子.根据同类配体形成的配合物结构, H2bbga与MnCl2·4H2O、NiCl2·6H2O、CoCl2·6H2O、和CuCl2·2H2O形成的配合物的组成应为 [M(bbga)(H2O)]·nH2O[6,7].基于相似的反应条件和表征数据,金属离子钙、镁和锌的配合物组成也应为[M(bbga)(H2O)]·nH2O.结合元素分析数据,笔者推测配合物的可能组成结构分别为[Mg(bbga)(H2O)]·2H2O、[Ca(bbga)(H2O)]·2H2O、[Mn(bbga)(H2O)]·2H2O、[Co(bbga)(H2O)]·H2O、[Ni(bbga)(H2O)]·H2O、[Cu(bbga)(H2O)]·H2O和 [Zn(bbga)(H2O)]·2H2O.
在金属配合物的红外光谱中,3029 cm-1附近吸收峰为苯环上的C-H伸缩振动峰,1580 cm-1、1495 cm-1为苯环上的C=C的骨架振动峰,749、700 cm-1附近吸收峰为苯环面外弯曲振动峰.这些谱峰的出现,说明了生成物中有苯环存在.位于1618~1610 cm-1的谱峰应该归属于υas(COO-)吸收峰,1413~1407 cm-1是υs(COO-)吸收峰,与配体H2bbga的υas(COO-)、υs(COO-)谱峰相比,两者均未有较大的移动,这说明配合物中羧基仍是以单齿配位的模式与M(Ⅱ)成键的.位于1033~1029 cm-1的谱峰归属于υ(C-N)吸收峰,其与配体中的υ(C-N)伸缩振动大约相差5~1 cm-1.υ(C-N)吸收峰的位移说明了氨基团的氮原子参加了配位.此外,在556~526 cm-1和465~436 cm-1处吸收峰,可分别被指认为υ(N-M)和υ(O-M)伸缩振动[6,7].
所有配合物的图谱中,在3390 cm-1附近均出现一个很宽的吸收峰,这表明配合物中包含了结晶水,这与元素分析的结果一致.
2.2 化合物对三磷酸腺苷二钠分解的催化活性的测试
通过比色法测定的实验数据,从无机磷标准曲线中查出的目标配体及配合物体系OD对应的无机磷含量见表1.

表1 化合物体系的磷含量
由表1可知,室温下,对ATP分解反应,可认为配体H2bbga无催化活性.而配合物中,Ca(Ⅱ),Mg(Ⅱ)和 Mn(Ⅱ)配合物对ATP分解反应均具有一定的活性,其活性顺序为[Mg(bbga)(H2O)]·2H2O = [Mn(bbga)(H2O)]·2H2O > [Ca(bbga)(H2O)]·2H2O;Co(Ⅱ)、Ni(Ⅱ)、Cu(Ⅱ)和Zn(Ⅱ)的配合物则可认为无活性.
3 结语
以L-谷氨酸为主要原料,通过一系列的反应合成了配体N,N-二苄基-L-谷氨酸,并进一步合成了Mg(Ⅱ)、Ca(Ⅱ)、Mn(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)、Cu(Ⅱ)和Zn(Ⅱ)的配合物.应用比色法测定了目标配体N,N-二苄基-L-谷氨酸及其配合物体系对应的无机磷含量.结果表明,配体N,N-二苄基-L-谷氨酸对三磷酸腺苷二钠的分解反应无催化活性;而配合物[Mg(bbga)(H2O)]·2H2O、[Mn(bbga)(H2O)]·2H2O 和[Ca(bbga)(H2O)]·2H2O对三磷酸腺苷二钠的分解反应则具有一定的活性.
[1] Boyer P D.The ATP synthase-a splendid molecular machine[J].Annu Rev Biochem,1997,66:717-749.
[2] Robert F S.Chemistry prize taps the energy of life [J].Science,1997,278: 579-580.
[3] Skou J C.The energy coupled exchange of Na+for K+across the cell membrane: The Na+,K+-pump [J].FEBS Lett,1990,268(2): 314-316.
[4] 金龙飞,沈月松,吴勇飞,等.L-谷氨酸-5-甲酯金属化合物的合成、表征和生物活性的研究[J].中南民族大学学报:自然科学版,2011,30(1): 17-20,24.
[5] Yamazaki Y.Substituted amino acids [J].Yakugaku Zasshi,1966,86(11): 1105-1108.
[6] Antolini L,Marcotrigiano G,Menabue L,et al.Coordina-tion behavior ofL-glutamic acid:spectroscopic and structural properties of (L-glutamato)(imidazole)copper(II),(L-glutamato)(2,2'-bipyridine)copper(II),and aqua(L-glutamato)(1,10-phenanthroline)copper(II)trihydrate complexes [J].Inorg Chem,1985,24: 3621-3626.
[7] 杨宇翔,郇伟伟,纪国媛,等.缬氨酸锑和缬氨酸铋配合物的制备与结构分析[J].同济大学学报:自然科学版,2011,39(3): 451-455.

