维持性血液透析患者肝素抗凝方式的改进
申志祥,邢昌赢,刘 燕
(1.南京医科大学第一附属医院(江苏省人民医院)肾内科,江苏 南京 210029;2.江苏省省级机关医院,江苏 南京 210024)
随着透析技术逐渐改善,透析患者远期生存率逐渐提高,肝素已成为最为普遍应用的抗凝剂之一,但是与低分子肝素相比,其副作用也日益凸显[1],故如何减少肝素用量成为大家关注的话题。为此我们从改进肝素给药方式入手,寻找减少肝素用量的可靠方法,现报道如下。
1 资料和方法
1.1 一般资料
江苏省省级机关医院血液净化中心维持性血液透析患者 55例,其中男 30例,女 25例,年龄 32~79岁,均在血液透析中使用普通肝素进行抗凝,维持性血液透析时间 2~27年,使用一次性 PMMA膜透析器,面积为1.3 m2,碳酸氢盐透析液,每周透析3次,血流量 250~300mL/min,透析液流量 500mL/min,血液透析开始前予生理盐水500mL(含普通肝素20mg,125 u/mg,江苏常州千红生化制药股份有限公司,批号 091022)冲洗透析器和透析管路,均排除使用对出凝血有影响的药物,如华法令、水蛭素、双嘧达莫等。
1.2 肝素给药方式
55例患者均采用自身前后对照,记录两种不同的给药部位所用首剂肝素量及肝素总量。(1)静脉组:按常规肝素使用方法于血液透析开始前按 0.2~0.8mg/kg从静脉注入,启动透析泵、肝素泵,持续将维持量肝素按 4~24mg/h注入动脉壶。55例患者肝素用量均已个体化。(2)动脉组:改进后的肝素使用方法在开始血液透析引血进动脉管路后,立刻将首量肝素注入动脉管路,启动肝素泵,持续将维持量肝素注入动脉壶。两组均于血液透析结束前1 h停肝素泵。动脉组根据透析器凝血等级、凝血参数等调整肝素用量。动脉组肝素调整方法:首次使用新的给药方法时首剂量肝素及维持量肝素均维持原先常规给药方法的剂量不变,连续观察 3次凝血等级及凝血参数,从而增加或减少原剂量的20%,直至凝血等级稳定在0或Ⅰ级,凝血参数维持在目标值范围内,并记录首剂肝素量及肝素总量。
1.3 观察指标
(1)抗凝效果:透析器使用时间以及透析器和管路凝血情况分为4级[2]。0级:无凝血或有数条纤维凝血;Ⅰ级:部分凝血或成束纤维凝血;Ⅱ级:严重凝血或半数以上纤维凝血;Ⅲ级:透析器静脉压明显增高需更换透析器或管路凝血。(2)透析前、透析开始 5,120 min及透析后各时间点的部分凝血活酶时间(APTT)。(3)透析器血室容积测定:血室容积采用北京伦拿创业医疗设备有限公司生产自动复用机测得。(4)两组患者最终首剂肝素量及肝素总量。(5)透析前后肌酐、尿素氮变化。
1.4 统计方法
2 结 果
2.1 抗凝效果
静脉组0级 14例次 (25%),Ⅰ级 41例次(75%);动脉组0级 31例次(56%),Ⅰ级 24例次(44%),与静脉组相比动脉组患者透析器凝血等级明显下降(χ2=10.87,P<0.01)。
2.2 凝血指标变化
治疗前后,患者 APTT比较差异均无统计学意义(P>0.05)。见表1。
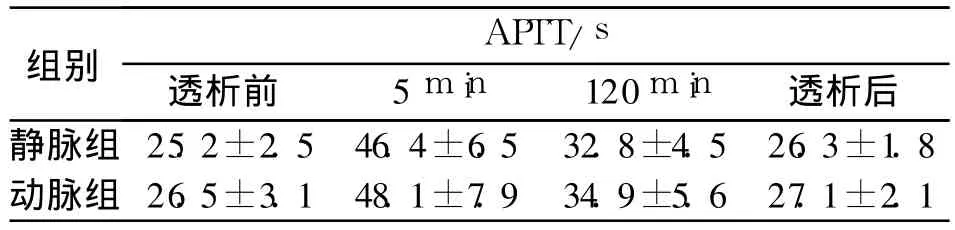
表1 静脉组和动脉组透析前后凝血指标
2.3 血室容积变化
静脉组透析器血室容积为(79.78±5.22)mL,动脉组透析器血室容积为(80.89±2.52)mL;两组血室容积无明显差异(P>0.05)。
2.4 静脉组和动脉组肝素用量
与静脉组相比,动脉组血液透析中首次肝素及肝素总量均明显减少(P<0.05),见表2。

表2 静脉组与动脉组肝素用量
2.5 透析前后肌酐、尿素氮变化
动脉组与静脉组比较无统计学意义(P>0.05),见表3。

表3 静脉组和动脉组透析前后血清尿素氮及肌酐
3 讨 论
维持性血液透析时,血液通过管道引出体外,经过透析器弥散交换物质,又通过管道回到体内,如果不用抗凝剂,这一过程可引起机体凝血和血栓形成的变化[3],应用抗凝剂是为了防止血液在透析管路及透析器中凝固,保证体外循环的通畅,使血液透析顺利进行。
普通肝素因抗凝作用强大,且价格低廉,是目前国内外血液净化治疗中广泛使用的抗凝剂。相对于普通肝素而言,低分子量肝素有确切的抗凝作用、出血危险性小、生物利用度高等优点[1],但其价格较高。普通肝素是一族天然的酸性蛋白多糖,相对分子质量(Mr)3 000~56 000。其分子中硫酸根带强大负电荷,可与抗凝血酶Ⅲ(ATⅢ)呈 1∶1结合,并使 ATⅢ构型改变,而灭活凝血酶、因子Ⅹa、Ⅸa、Ⅺa、Ⅻa以及激肽释放酶活性的70%。同时普通肝素还激活肝素辅因子,发挥抗凝作用[4-5]。但是普通肝素的副作用不容忽视,可有出血、过敏反应、血小板减少;长期使用可出现骨质疏松、高脂血症及脱发等[4,6],因此最小剂量的应用肝素显得尤为重要。
血液透析过程中,影响凝血的因素众多,如透析膜、血流量和透析液流量的不同,透析器是否复用,透析前透析器和透析管路的冲洗情况等。本研究中观察对象透析处方均已个体化,均使用膜面积为1.3 m2的一次性 PMMA膜透析,血流量在250~300mL/min之间,统一对透析前管路及透析器进行预处理。对血液透析时肝素抗凝监测常用APTT、活化凝血时间(ACT)、凝血时间(CT)。但 ACT的重复性比 APTT差,尤其在低血浆肝素浓度时。而CT操作耗时长,标准化与重复性均较差[4]。本研究选择APTT作为肝素抗凝的检测指标。在透析过程中监测不同时间点 APTT,根据目标值和透析器及透析管路凝血等级调整肝素用量,最终使透析器及透析管路凝血等级在0或Ⅰ级,比较两组肝素总量及追加用量 。结果显示两组APTT无统计学差异,动脉端给药组比静脉端给药组肝素用量减少,具有显著性差异。同时两组透析器凝血等级及血室容积改变无统计学差异。以上数据说明在达到相同的抗凝效果下,动脉组肝素用量比静脉组肝素用量明显减少,为理想的肝素给药方式。同时为避免肝素用量减少影响透析效果,我们监测两组透析前后肾功能改变情况,结果显示两组在肌酐及尿素氮的清除效率上达到相同的效果,结果证实动脉端给药不影响透析效果。在透析治疗结束后,无一例患者穿刺处压迫时间较前延长,说明这种给药方式没有增加出血风险。
动脉端给药是如何达到减少肝素用量这一结果的呢?已知凝血反应为瀑布效应,一旦启动将产生逐级放大效应,因此在血液进入透析管路和滤器时充分阻断凝血反应最为重要,因此我们选择在把血液引出体外的动脉端肝素给药,在血液进入透析管路和滤器前充分阻断凝血反应,即能达到最大的抗凝效果[7];同时当从动脉管路给首剂肝素时,高浓度的肝素血液首先接触透析管路及透析器,带强负电荷肝素迅速吸附到管路及透析膜表面,从而大大减少血液中蛋白质分子在管路及透析膜的吸附,减少血小板的活化。因此选择动脉端肝素给药能有效触发瀑布效应,达到理想的抗凝效果。由于普通肝素为Mr5000~20000的黏多糖蛋白,很少为滤器清除,因此选择普通肝素推荐在透析器前给药,以达到体外抗凝作用强于患者体内抗凝作用的效果。
长期以来,肝素静脉端给药作为常规方式在临床上得到广泛应用,而我们通过上述试验证实选择动脉端给药在减少肝素用量上具有明显优势,值得在临床推广。
[1]吴素梅,何劲松.低分子肝素在血液透析抗凝中的应用[J].中国生化药物杂志,2003,24(5):254-255.
[2]贺鹤群,朱建华,邵亚娣.局部肝素抗凝在高危出血倾向患者连续性血液净化中的作用[J].现代实用医学,2009,21(2):109-111.
[3]Schetz M.Anticoagulation in continuousrenal replacement therapy[M].//Ronco C,Bellomo R,Greca L.Blood Purification in Intensive Care.Basel:Conerib Nephrol,Karger,2001:132,283-303.
[4]王振义,李家增,阮长耿,等.血栓与止血基础理论与临床[M].3版,上海:上海科学技术出版社,2004:683,790-792.
[5]Ireland H A,Boisclair M D,Lane D A,etal.Hemodialysis and heparin.Alternative methods of measuring heparin and of detecting activation of coagulation[J].Clin Nephrol,1991,35(1):26.
[6]Monchi M,Berhmans D,Ledoux D,etal.Cirate vs.heparin for anticoagulation in continuousveno-venoushem of iltration:aprospective randomized study[J].Intensive Care Med,2004,30(2):260-265.
[7]孙雪峰.如何选择血液透析的抗凝治疗方案[J].中国血液净化,2008,7(6):335-337.

