国际药品专利制度的棘轮效应与中国因应

摘 要:国际上药品专利保护水平持续提升,棘轮效应相伴而生。TRIPS“最低标准”阻止保护水平降低,构成药品专利制度棘轮的止回棘爪;在主体—行为二元视角下,跨国药企与属国及各自驱动策略相互作用形成棘轮的前进动力,引发TRIPS-Plus规则向全球扩散的驱动效果。基于共生理论进行分析,棘轮效应与跨国药企的共生力成正比关系,其实质是属国为提升其共生力而营造有利外部环境的结果。通过审视域外相关立法模式,最后指出,中国应积极运用横向体制转换策略,完善信息交流与利益表达机制;利用“建设性模糊”转换适用国际新制度,采取限缩路径防范专利权扩张风险。
关键词:药品专利制度;棘轮效应;共生理论;共生力
DOI:10.6049/kjjbydc.2023120234
中图分类号:D923.42
文献标识码:A
文章编号:1001-7348(2025)02-0142-10
1 国际药品专利制度的棘轮效应及其现实困境
专利具有稀缺性、垄断性和创新性,是企业不可多得的优质竞争资源。在药品知识产权领域,药品专利攸关制药企业核心经济利益[1]。然而,以西方国家和医药产业为中心的国际药品专利制度并未考虑南北国家间知识鸿沟。为追逐超额垄断利润,代表制药业利益集团的跨国药企及其属国,持续在全球范围内推动药品专利的强化保护,棘轮效应随之产生。受其影响,中国先后引入药品专利纠纷早期解决、药品试验数据独占保护、药品专利保护期延长等国际新制度,但由于尚处在制度构建初期,相关法律法规不健全,极易引发私权扩张风险。另一方面,中国是仿制药大国,而且仿制药行业整体处于仿制水平较低、Ramp;D投入不高、研发技术基础薄弱的阶段[2-3]。
学界关于药品专利制度的探究形成了丰硕成果。学者们或在理论层面审视药品专利权与公共健康权的冲突和协调问题[4],或从制度实践论证现有国际规范对药品专利保护的推动作用及其合法性[5]。随着社会的发展和认知的深入,学界在新问题的回应上稍显不足:一是尽管认为西方跨国药企是知识产权国际保护的幕后推手[6],并承认棘轮效应在该领域的显现[7],但就关涉制药业核心利益的药品专利制度是否同样存在棘轮效应,并未予以明确回答;二是针对知识产权国际保护棘轮效应的描述多为概括性论述,缺少体系化思考,忽略了与棘轮效应基本要素的有机结合。
知识产权是一门最具科技含量、最多知识要素的综合性学科[8],除作为法学的传统研究对象外,管理学也尤其关注。因此,基于法学与管理学交叉视角,多领域、全方位考察知识产权显得非常必要。在此背景下,面对国际药品专利的强化趋势与本土药企转型受阻、民众平价药获取困境之间的矛盾,有必要采用新的研究维度,将棘轮效应运用于药品专利制度的趋势分析,并借助管理学共生理论探寻其实质成因,进而依据中国社会的现实语境提出可行的法治对策。
1.1 棘轮效应与国际药品专利制度
1.1.1 棘轮效应的内涵
棘轮效应源于一种由棘轮、止回棘爪、驱动棘爪组合而成的间歇性单向运动齿式机构——棘轮机构。此种机构只能单向前进,无法后退运动,由这一现象所提炼出的事物发展规律称为棘轮效应[9]。由于棘轮效应实现单向运动,运动方向正确与否就非常重要,如果方向错误,那么由于棘轮的单向推动,只会在错误的道路上越走越远,从而出现一方受益、他方受损的状况。当然,判定运动方向根本上还是要看事物本身的性质及其发展规律。
广义的棘轮效应用于解释各个领域的一切不可逆性。其在社会科学领域的运用最早源自经济学,主要指人的消费习惯形成之后难以改变。在管理学中,有学者将棘轮效应定义为:相关主体在目标设定时,以历史业绩为主要指标,致使目标易升难降[10]。Weitzman[11]认为,目标制定过于依赖历史业绩将导致负面激励效应,经理人可能隐藏部分努力以避免未来设定更高目标。总之,无论是经济学的消费习惯研究,还是管理学的目标设定分析,均表明棘轮效应具有不可逆转的特性,且极易引发负面效果。
棘轮效应内含4个基本要素:棘轮、止回棘爪、驱动棘爪和驱动效果,其中止回和驱动棘爪以棘轮为轴心运行,前者阻止棘轮后退,后者推动棘轮前进,两者相互作用产生单向运动的驱动效果,这一运作机制与国际药品专利制度发展趋势的内在逻辑不谋而合。
1.1.2 国际药品专利制度发展趋势
药品专利是棘轮效应的主体要素——棘轮,且是各方主体利益博弈的焦点,南北国家围绕是否强化其保护展开了激烈争论。因此,明晰棘轮效应在药品专利制度中的作用机制,首先需厘清其发展脉络与立法概况。回溯历史进程,国际药品专利制度经历了两大发展阶段。
(1)形成与完善阶段:《与贸易有关的知识产权协定》(以下简称TRIPS)至《多哈宣言》时期。在TRIPS之前,药品一直游离在专利保护的客体范畴之外,药品研发成果可随意被低成本仿制。此外,新药研发投入高、风险大,加上为符合药品审评机构安全规定所付出的合规代价,导致总体成本居高不下,跨国药企的商业利益难以得到有效保护。故在“乌拉圭回合”谈判中,西方国家不满于世界知识产权组织(WIPO)的弱执行力[12],力争将药品专利保护纳入世界贸易体制管辖,试图建立更加开放、精确的谈判平台以反馈利益诉求。1995年,谈判各方根据马拉喀什协定建立世界贸易组织(WTO),TRIPS应运而生。TRIPS打破了WIPO框架下知识产权公约的运作模式[13],以药品专利保护的“最低标准”及相关程序性规定对各成员的国内立法产生了较大约束力,标志着国际药品专利制度的正式形成。
TRIPS框架下的药品专利制度突出了药品专利的私权属性以及对利润的过分追求,却无视发展中国家在医疗卫生领域的现实考量,因而为日后的药品获得运动埋下了伏笔。2001年WTO通过《多哈宣言》,确立了公共健康优于私权保护原则和以强制许可为代表的权利限制制度在国际社会的适用。宣言在一定程度上缓解了发展中国家公共医疗负担,也完善了国际药品专利制度。
(2)强化阶段:后TRIPS时期。后TRIPS的前缀是“后”,意指一种难以名状的超越之势。在内容上,“后”既保留了与人们熟悉事物的联系,又加以否定[14]。这表明当今社会存在与TRIPS相联系的事物,它超越并否定了TRIPS的既有规则,促使进入后TRIPS时代。
TRIPS使药品专利的高保护标准在世界范围内得以确立,但是跨国药企及其属国并未止步于此,依旧不遗余力地在一系列自由贸易协定(Free Trade Agreement, FTA)中推行高于TRIPS的保护标准,即TRIPS-Plus规则。TRIPS-Plus规则是指可以产生TRIPS-Plus效果的各类条约[15],其内容涵盖药品专利纠纷早期解决、药品试验数据独占保护和药品专利保护期限延长等国际新制度,目的在于提高对药品专利的保护水平并限制TRIPS的灵活性安排。从TRIPS-Plus规则伊始,国际药品专利制度进入后TRIPS时代的强化阶段。
1.2 国际药品专利制度棘轮效应的现实困境
知识产权属于工具性制度,除具有占有、计划和自卫功能外,还可作为一种调节机制,以此分配利益和转移负担[16]。而通过某种法律制度,具有平等主体资格和契约自由的个人对财产的利用要么是为自身谋取利益,要么是转嫁负担至他人[17]。在知识财产范围内,药品专利制度也发挥着同样的调节作用,并成为跨国药企及其属国在全球范围内撷取利润、转嫁负担的制度工具,其凭借棘轮效应带来的贸易竞争优势促进自身福利增长,同时,造成发展中国家利益损失[18]。
1.2.1 立法弹性空间受限
在TRIPS框架内,发展中国家享有“量体裁衣”式确立规则的自由和主权。同时,协议中相当数量的“建设性模糊”(Constructive ambiguity)条款为成员国内部的制度设计提供了可操作的弹性空间[19]。然而,棘轮效应的出现,导致这一空间被急剧压缩。
(1)TRIPS-Plus规则造成“建设性模糊”条款数量锐减。正是由于TRIPS成员国数量庞大,经济社会发展国别差异明显,诸多“建设性模糊”条款和强制许可制度才得以纳入该协议。但进入后TRIPS时代,TRIPS-Plus规则限制了TRIPS的灵活性安排,含有“建设性模糊”的条款数量大幅减少。例如由美国主导的《跨太平洋伙伴关系协议》(TPP),其目标是致力于达成无例外的综合性FTA,不仅削弱了TRIPS的弹性空间,还缺少例外条款加以制约。可见,发展中国家依靠“建设性模糊”条款进行本土立法的自主空间遭到限缩。
(2)国际贸易与投资规范限制了发展中国家的弹性立法空间。国际贸易与投资规范中涉及征用征收和国民待遇的条款是西方社会胁迫发展中国家强化药品专利保护的又一制度利器[20]。基于上述规则,除为维护公共利益,并以非歧视手段且程序正当或给予合理补偿外,有关国家不得采取任何方式对私人财产征收征用、适用权利限制制度或采取国有化措施,但药品专利强制许可却被排除在上述范围之外。因此,以上条款同样成为阻碍发展中国家弹性立法的制度壁垒。
1.2.2 产业竞争阻滞,药品获取困难
一方面,尽管国际社会试图努力改善全球公共卫生环境,但发展中国家的国内医疗形势仍不容乐观。另一方面,南北国家制药企业分处全球医药产业价值链的两端。这演化为一种双重矛盾,即具有私权属性的药品专利权与具有公益属性的健康权、发达国家医药产业与发展中国家本土产业之间的矛盾,而棘轮效应下国际新制度的普及致使这些矛盾愈发激烈。
(1)国际新制度导致发展中国家制药企业仿制成本提高,竞争优势丧失。在药品试验数据独占保护方式下,未经权利人许可,其它企业不得使用其试验数据通过药品审评机构的注册审批。众所周知,药品的低成本仿制和价格优惠是仿制药企参与市场竞争的主要方式。但在独占期内,由于未经同意不得使用权利人的药品试验数据,因而仿制药企无法通过仿制药的生物等效性和安全性审查而获批上市。这意味着发展中国家制药企业在仿制过程中将承受高昂成本而被迫抬升药价,抵消了价格方面的竞争优势,从而面临恶劣的产业环境,民众的药品获取困境也随之加深。
(2)国际新制度催生出药品生命周期管理策略,给医药产业发展和药品获取带来威胁。药品生命周期管理是跨国药企为达到市场垄断目的,变相提升专利期限的反竞争策略[21]。如通过申请次级专利构建“专利丛林”的方式实现专利常青,从而延长专利寿命以维持药品专利的高回报率,但此举会不当延误仿制药入市时间。仿制药是专利保护期届满,其它企业均可仿制的药品,此类药品成本投入低,价格优惠,可大幅降低公共医疗支出。但药品生命周期管理策略的实施无疑会促使风险厌恶型的仿制药企为避免潜在的侵权纠纷而延迟仿制药上市。与此同时,仿制药延迟上市会引发专利药长期垄断的后果,致使相关市场缺乏竞争活力,公共卫生环境也随之恶化。
2 国际药品专利制度棘轮效应的运行机制
分析国际药品专利制度棘轮效应的运行机制,需在前述发展趋势的基础上,剖析其深层次原理,衡量多方主体利益,进而基于棘轮效应的基本要素及运作机制探寻其实质所在。
2.1 止回棘爪——TRIPS“最低标准”
止回棘爪可以阻止棘轮机械向后倒退。在药品专利领域,TRIPS的“最低标准”在协调药品专利保护一体化方面作用显著,其明确药品可作为专利客体与其它类型专利一起受到同等保护,起到止回棘爪的作用。
(1)协议第一条规定了成员国的最低保护义务,允许各成员以此为基准,且不与本协议相违背的前提下,设置更加广泛的保护范围。最低保护义务集中反映了TRIPS在药品专利国际保护体系中的地位和作用,同时也是该协议成员国最主要的国际法义务。从法的渊源考察,这一义务首先是成员国基于TRIPS文本的条约法义务[22]。国家是拟制意义上的国际法主体,通常由一定的政府行使国家主权或条约规定的其它权利并履行相应义务。在国家不履行义务或存在履行瑕疵时须承担相应的国际法责任,并以WTO争端解决机制下的强制力为保障,确保各成员在国内立法时“最低标准”的有效实施。
(2)协议下的“最低标准”是药品专利保护的地板而非天花板[23],各成员国只能在“最低标准”的基础上为药品专利提供国内保护,由此在国际社会树立了新标杆。那些有意加入WTO以享受贸易优惠的发展中国家纷纷将其奉为圭臬,力争与国际接轨,却忽视了高标准保护可能引发的不利后果。而已经实施“最低标准”的成员又或主动或被动地通过自主立法、双边条约、区域协定等进一步提高药品专利的保护和执法标准。如智利在接受TRIPS协定的“最低标准”安排后,又与美国缔结FTA并成为《全面进步跨太平洋伙伴关系协定》的成员,由此进一步提高了其国内的药品专利保护水平[24]。
总之,许多发展中国家为促进自身经济社会发展,积极融入全球化浪潮,在西方国家“胡萝卜加大棒”的政策引导下陆续接受了TRIPS的制度安排,同时以WTO争端解决的强制力为保障,使得药品专利制度的棘轮无法后退。
2.2 驱动棘爪——跨国药企与属国的驱动策略
驱动棘爪发挥着推动棘轮向前运动的功能。有学者提出,知识产权与贸易的结合构成知识产权保护棘轮的驱动棘爪,同时强调跨国公司的重要作用。但由于该观点本身存在局限而无法完全适用于药品专利领域:①知识产权动力学认为,知识产权国际立法是在知识产权行为主体——国家和私人集团的推动下,根据相互作用的宏观背景和规律展开的[25],所以,仅对跨国公司予以肯定,而忽视了国家在其中扮演的重要角色,实有重此抑彼之嫌;②将知识产权保护棘轮的根本驱动力简单归结为知识财产与贸易的挂钩,缺少现实层面的实证考察。在主体—行为二元视角下,跨国药企和属国及各自驱动策略的相互作用才是药品专利制度棘轮的真正推力。
2.2.1 微观层面:跨国药企驱动策略
跨国药企以实用主义为导向,侧重自身利益诉求,是微观层面的驱动主体。通过实施组建医药产业同盟、派驻利益代表的驱动策略,跨国药企的利益关切在相关政策中得到充分考虑与体现。
(1)组建医药产业同盟。为实现商业利益最优,跨国药企将医药行业中原本存在竞争关系的企业联合起来,建立同盟关系。美国药品研究与制造企业协会(PhRMA)即是这一同盟策略的产物。成立于1958年的PhRMA,其成员囊括辉瑞、拜耳、阿斯利康、第一三公株式会社、强生、礼来等诸多大型跨国药企。该组织不断向美国阐述专利保护对于激励新药研发的关键作用,号召政府优化专利政策为药品创新和医学进步营造正向制度环境。另外,除单一的医药产业同盟外,还存在一些跨行业同盟组织。如成立于1986年的美国知识产权委员会(简称IPC),吸纳了包括医药、软件、化学、电子以及计算机等行业的跨国巨头,并以推进知识产权的国际保护为宗旨[26]。IPC曾联合欧洲和日本的同僚起草了一份基于发达国家的知识产权法律草案并提交给当时的关税与贸易总协定秘书处,这就是后来TRIPS协定的雏形。基于在全球贸易领域的共同利益,以PhRMA和IPC为代表的产业同盟不断吸纳成员、投资政治、整合信息与积累经验,再利用极富侵略性和有组织的游说活动对属国贸易与专利保护政策的制定施加影响,并获得一定权力。如美国1979年修订的“301条款”就允许“私人集团采取公开的手段推动现有贸易协定的实施”[27]。
(2)派驻利益代表进驻属国机构。在政策设计的具体过程中,属国政府虽拥有独立的信息来源与收集渠道,但制药企业作为市场竞争的参与者,更能切实感受到域外立法对贸易活动的影响。因此,为精准表达利益诉求,畅通信息交流渠道,跨国药企依靠自身专业优势,派驻具有医药政策研究背景的代表进入属国贸易政策制定机构。以辉瑞公司为例,其首席执行官和国际部门负责人都曾先后担任美国贸易谈判咨询委员会知识产权特别小组的成员。而更为典型的是以医药产业同盟派驻代表的方式进行干预[28],如PhRMA的主席兼首席执行官Stephen J Ubl,其是全球公认的卫生领域知识产权倡导者和政策专家,曾助推美国食品药品管理局(FDA)的药品审批流程改革[29]。从20世纪90年代开始,利益代表逐渐从属国总统手中获得与贸易相关的一些权力,如1988年美国《综合贸易竞争法》规定,利益代表可判断他国贸易活动是否损害属国利益、决定是否采取贸易报复等,由此导致其对相关政策制定的影响持续增强[30]。
2.2.2 宏观层面:属国驱动策略
属国从整体战略出发,以国家利益安排为考量,是宏观层面的驱动主体。作为国际法意义上的立法主体,属国可直接推动相关立法,而主要策略是体制转换。体制转换是指国际主体基于权力约束,通过条约谈判、立法动议或标准设置等手段推动相关议题的谈判、协商从在先平台转向另一平台,以改变现状[31]。后TRIPS时代,药品专利领域的体制转换是由TRIPS转向FTA。FTA作为新的议题谈判平台,具有以下优势:
(1)FTA起点低、速度快、连续性强。以上优势使得FTA无论在谈判进度还是缔结概率上都较TRIPS略高一筹。而且由于属国在全球的经济地位举足轻重,会诱使相当一部分国家在缔结FTA时作出不小的让步以换取短期经济效益。比如约旦为获得美国投资,在2001年与其签署FTA,接受了保护水平更高的TRIPS-Plus规则,但结果并未促进约旦本土制药业的进步,而且,其国内药品价格平均上涨20%[32]。
(2)对非FTA成员国形成暗示或压力。FTA的缔结会在很大程度上作为一种既定事实对其它非FTA成员国形成压力或暗示,使其认为协定中的相关条款存在合理之处,因而接受甚至积极推广FTA。例如墨西哥在加入北美自由贸易协定(NAFTA)前,其国内药品专利保护水平并不高,但加入后在相关谈判中积极推动其它国家接受美国倡议的保护标准。
(3)促使TRIPS的“建设性模糊”条款趋于精确化。TRIPS协定为尽可能吸纳更多国家以实现涵盖范围的广泛性,会对某些问题模糊处理以形成共识。但当议题谈判平台转移至FTA后,属国往往会采取扩大保护范围、延长保护时限等方式,推动“建设性模糊”条款精确化,以此实现强化药品专利保护之目的。
上述措施与跨国药企的驱动策略相互作用、相互影响,推动国际药品专利水平持续强化,构成药品专利制度棘轮的驱动棘爪。
2.3 驱动效果——TRIPS-Plus规则向全球扩散
驱动效果是止回棘爪和驱动棘爪作用于棘轮的结果外显。后TRIPS时代大量FTA的缔结,表明药品专利制度棘轮的驱动效果逐渐显露,即TRIPS-Plus规则向全球扩散,而美国在其中发挥了关键作用。截至2023年,美国已与约20个国家签署并生效共计14项 FTA。其中,除加拿大、韩国、以色列和澳大利亚外,其余均为发展中国家,包括巴林、智利、哥伦比亚、中美洲五国(哥斯达黎加、尼加拉瓜、萨尔瓦多、危地马拉、洪都拉斯)、约旦、墨西哥、摩洛哥、多米尼加、阿曼、巴拿马、秘鲁、新加坡[33]。TRIPS-Plus规则在上述国家的扩散过程呈现出以下特点:
(1)从空间分布考察,大致可分为4类扩散形式:①以双边谈判缔结FTA,敦促谈判国严格落实相关条款,如美国与新加坡、约旦、韩国、新加坡等10个国家,这是TRIPS-Plus规则扩散的主要形式;②直接透过区域性谈判,将TRIPS-Plus规则一次性扩散至多个国家,如中美洲自由贸易协定(DR-CAFTA)和NAFTA,前者涉及中美洲5个国家,后者涉及加拿大、墨西哥,直接透过区域性谈判是效率最高的一种扩散形式;③将尚未加入的国家纳入现有FTA,如美国通过与多米尼加进行谈判,将其纳入DR-CAFTA;④有关国家在谈判过程中退出,但最终仍缔结了FTA,如美国与哥伦比亚、秘鲁等(梁志文,2014)。统计结果如图1所示。
(2)从时间序列考察,大致可划为4个扩散阶段:第1阶段以NAFTA为主,该协定中涉及药品试验数据保护的内容与TRIPS第39.3条类似,并为药品试验数据设置了不少于5年的独占保护时限;第2阶段是TRIPS缔结后达成的FTA,共同特点是美国将缺少弹性空间的保护规范向其贸易伙伴特别是发展中国家推广;第3阶段以美国“新贸易政策”两党共识为标志,体现在美国与秘鲁、哥伦比亚和巴拿马的FTA中,这一共识要求美国在涉及知识产权、劳工标准和环境问题的FTA谈判中采取更平衡的政策;第4阶段以2008年金融危机为起点,西方国家的地缘政治和经济实力发生重要变化,美国以复苏20世纪80年代的竞争力和创新力为目标,加速扩散TRIPS-Plus规则的步伐(梁志文,2014)。
综上所述,棘轮效应在国际药品专利制度中的运作机制得以明确,而该领域何以出现这一效应有待后续考察。对于此,管理学的共生理论提供了一种可资借鉴的研究范式,有利于理解棘轮效应的实质成因。
3 共生理论视域下国际药品专利制度棘轮 "效应的实质成因
共生是指共生单元以实现净利益最优为目标,在一定的共生环境中按照某种共生模式形成的共生体或共生系统[34]。共生理论认为,人类生存是一种共生的生存,而权威共生作为共生形式之一,通常以各自比较优势为基础进行分工合作,共同面对生存之竞争,是一种相互需求、相互依存的生存结构,更是人类基本共生结构的本质形式。
跨国药企与属国在经济目的、贸易分工、立法参与等方面有着各自比较优势,又相互依存,彼此需要,存在构成权威共生关系的极大可能。因此,需对其作进一步识别,这也是明确棘轮效应实质成因的现实前提。
3.1 基于质参量兼容原理的共生关系识别
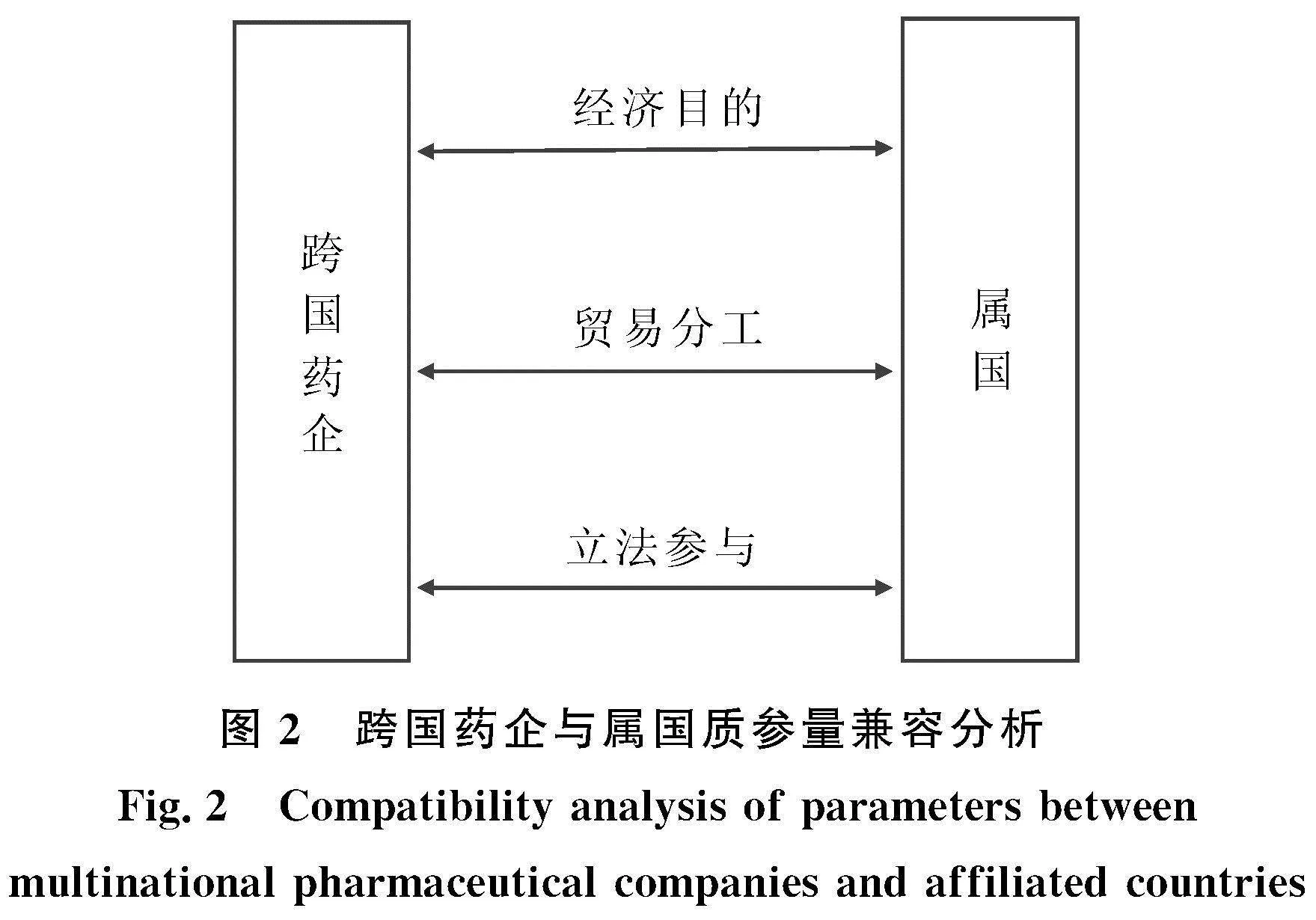
质参量兼容原理是共生关系的判定依据,属于共生理论的子原理。质参量反映的是决定行为主体内在性质及其变化的一系列因素。各主体间是否构成共生关系,取决于是否具备某种内在联系,这种内在联系体现为质参量的相互表达,即质参量的兼容[35]。对照质参量兼容原理,有利于判断跨国药企与属国间共生关系。第一,在经济目的上,属国以税收等方式获取经济收益从而增强经济实力,跨国药企通过开展贸易活动获得经济利益。尽管各自运行逻辑不同,但都将目标指向了经济利益,两者追求经济利益的契合性为共生关系的形成奠定了基础。第二,在贸易分工上,跨国药企是直接参与医药贸易竞争的市场主体,具有市场垄断优势,但其作为私权主体,难与国家主权相抗衡。属国可依靠自身强大的经济、军事实力,为跨国药企的贸易活动保驾护航,但无法在自由市场中直接介入贸易活动,参与利益分配。第三,在立法参与上,跨国药企非国际法主体,无法直接参与国际药品专利制度的相关立法,但其拥有专业化的医药专利管理和服务部门,可为属国相关政策的制定提供智力支持。属国作为国际法主体,可直接参与相关立法的谈判与制定,但缺少专业化的信息收集与整合渠道,更无法站在市场主体的立场上切实感知域外制度对本国产业的影响[36]。
通过上述分析,跨国药企与属国可以在经济目的、贸易分工和立法参与3个质参量上相互表达和兼容,因而构成权威共生关系(见图2)。
3.2 基于共生力与共生度的实质成因分析
从共生行为维度分析,共生模式分为寄生、偏利共生、非对称性互惠共生和对称性互惠共生4种。共生系统的进化总是从低阶向高阶发展,而共生系统的建立往往从偏利共生开始,向对称性互惠的共生模式演化[37]。企业竞争行为的本质是为获得支配资源的权威,最终目的是达到更高层次的共生,因此,决定企业竞争力高低的主要因素是企业的共生力。企业共生力是指一个行为主体与其它行为主体之间的共生能力,并与企业的共生度成正比关系。企业共生度是企业作为一个有机整体与他人、人类社会的共生程度和范围。一般来说,在其它条件不变的前提下,企业共生力会随着共生度的提升而得到增强[38]。
在跨国药企与属国的权威共生关系中,一方面,跨国药企为属国带来经济利益,并帮助解决就业、医疗等有关的社会问题;另一方面,通过组建医药产业同盟、派驻利益代表,与属国搭建高效畅通的信息交流与利益表达机制,进而在实现共生关系良性互动的基础上使两者之间的共生度得到大幅提升。这意味着跨国药企共生力的增强成为必然,因为共生度的提升会促使属国为跨国药企在国际医药市场竞争中创造有利的外部政策环境,即一种棘轮效应显著的药品专利强保护环境。
在这个意义上,跨国药企共生力的提升与棘轮效应的强弱同样成正比关系。因为企业的运作需要一个良好的外部环境,包括政策环境、法律环境、社会环境等,这些环境的创建都需要政府发挥作用,而与政府共生度的提高对于创建良好外部环境有着重要作用。医药产业是专利密集型产业,深受专利政策、法规的影响。对跨国药企而言,国际药品专利制度的保护强度越高,即棘轮效应越明显,外部政策法规环境对其共生力的提升就越有利。从现实层面考证,属国通过实施体制转换策略,将药品专利议题谈判平台由TRIPS转移到FTA,保护规范也随之从TRIPS“最低标准”发展到TRIPS-Plus规则,国际药品专利制度的棘轮效应便在这种保护水平持续提升的过程中不断凸显,而这一发展趋势对跨国药企共生力的增强起到积极助推作用。
基于以上分析,棘轮效应在国际药品专利制度领域的显现是一种必然,它顺应跨国药企在医药市场竞争中追求共生力提升的需要,并为其在全球贸易竞争中追逐超额垄断利润创造了有利制度条件 。
经过共生理论的检视,国际药品专利制度棘轮效应的实质成因得以明晰。而如何应对这一趋势,仍需考察域外相关立法,以借鉴有益经验缓解棘轮效应带来的现实困境。
4 域外药品专利制度立法模式与经验启示
医药产业与专利政策关系密切,各国会依据技术发展的不同阶段制定不同专利政策。在技术积累阶段,国家往往会构建宽松的保护环境,对药品专利实施弱保护。进入创新阶段后,就会实施严格的保护政策,对药品专利实施强保护[39]。
由于处在技术发展的不同阶段,南北国家在面对棘轮效应时采用了不同的药品专利保护范式。南方国家处于积累阶段,以宽松立法模式为导向。北方国家处于创新阶段,相关立法以强化保护为主。本文选取两种模式典型国家的相关立法进行分析。
4.1 美欧强化保护模式
美国和欧盟制药业以创新药企为主,是采用强化保护模式的典型。两者通过创新药品专利规则,实现严格保护的立法目标。
(1)扩大专利侵权声明类型。仿制药简化申请(Abbreviated New Drug Application,ANDA)是美国药品专利纠纷早期解决机制的核心内容。根据ANDA程序,申请人可利用此前已获批的专利药安全性和有效性数据向FDA递交与被仿制专利药具有生物等效性的证明文件,同时须在法案预设的4项专利声明中选择一项:①未进行专利登记;②登记专利已到期;③登记专利到期后,再将仿制药品上市销售;④登记专利应当被宣告无效,或其生产、使用、销售等行为不构成专利侵权。另外,美国《专利法》第271条(e)(2)款规定:若提交ANDA申请是以获得在专利到期前从事受专利保护药品的商业生产、使用、销售或使用药品专利方法的批准为目的,则申请行为视为专利侵权。这表明在ANDA程序下4类专利声明均可成为司法机关立案或管辖要件(杨婧等,2021),权利人可就任一声明类型发起专利侵权诉讼。
(2)设置“8+2+1”规则,叠加适用PTA和PTE。为促进新药研发和仿制药适时上市,在药品试验数据方面,欧盟创设了“8+2+1”规则,为药品试验数据提供了全球最长的独占保护时限。根据规则,药品试验数据的最低保护时限为8年,另再赋予权利人2年的市场专有权。对于具有重要临床效益的专利药,创新药企可再获得1年的市场专有权。在专利期延长方面,美国设置了专利保护期调整(Patent Term Adjustment,PTA)和专利保护期延长(Patent Term Extension, PTE)两种不同类型的延长规则。前者为专利授权审批过分延误的补偿,后者是药品注册审批阶段导致的管制性延长。根据PTE的计算公式,其补偿范围覆盖了从药品试验到上市所有可能会延误专利审批的阶段(李亚林等,2020)。同时,PTE起算点是在原专利到期日的基础上给予保护期的延长,而原专利到期日包括根据PTA调整后的专利到期日。因此,专利期延长的具体时间可在调整后专利到期日的基础上叠加计算,即PTA和PTE可叠加适用。
强化保护模式对中国的启示在于,盲目提高药品专利保护标准无益于中国医药产业发展与公共卫生环境改善。就美欧来说,创新药企占据其制药业主体,决定了保护政策难以向仿制药企倾斜。相比之下,在中国,制药业以仿制药企为主,跨国药企为创新药企主体。盲目采纳美欧经验,势必阻碍中国医药产业发展,同时会加剧跨国药企对本土药企的打压,因此,限缩路径下的制度设计更有益于中国医药产业的长远未来。
4.2 印度宽松立法模式
印度制药业以仿制药企为主,是采用宽松立法模式的典范,其始终遵循在履行国际义务的前提下,积极维护本国利益的价值取向。1970年,印度专利法将药品排除在受保护客体范围外,直至2004年为履行TRIPS协定下的国际义务才对专利法予以修订,为医药相关产品提供专利保护。总体而言,印度的制度实践呈现出宽松的立法特征。
(1)严格限制药品专利客体范围。印度为药品提供专利保护后,舆论担忧此举会促使药价急升,导致民众药品可及性下降。因此,2005年4月,印度政府指定专家组以下列原则作为政策导向要素,为其专利政策提供建议:①促进本土医药产业创新能力提升;②考虑当前药品研发水平;③兼顾平衡基于国际法义务所承担的私权保护与社会公众的健康权益。综合以上要素,专家组认为,已知物质的新构造、新用途以及新特性的简单发现(该简单发现无法与其起到的现有治疗功能区别开来),印度专利法不会为其提供法律保护[40]。上述观点在“诺华公司诉印欧联盟案”中得到了贯彻。2007年,印度诺华公司就印度专利管理机关驳回其抗癌药“格列卫”的专利申请提起诉讼。案件审理过程中,印度法院明确表示涉案药物“格列卫”的新剂型并没有提升疗效,不具备“发明”的条件,并以此判定诺华败诉[41]。此外,受这一条件限制,印度的现有专利授予标准可有效规避跨国药企实施产品跳转、专利常青等属于药品生命周期管理策略的限制竞争行为。
(2)利用TRIPS的“建设性模糊”。药品试验数据的独占保护会变相延长专利保护期限。对此,印度借助“建设性模糊”下的弹性政策空间,对TRIPS进行转化适用,进而解决这一问题。其表现在以下3点:①若相关机构对须提交未公开试验数据作为药品注册审批的这一必要条件未置可否,则与TRIPS规定的受保护要件抵触,印度专利法也无保护之必要;②TRIPS虽要求对含“新”化学实体的药品试验数据提供保护,但对“新”的含义界定存在模糊之处,因此可通过严格的含义限定,调和与印度立法政策的矛盾;③就协议内容来看,TRIPS并未强制要求对此类试验数据予以独占保护,故印度也毋须修改药品专利授予审查程序(刘华等,2009)。
宽松立法模式对中国的启示在于,制度构建应以国情为基础,善于运用国际条约的“建设性模糊”条款。印度制药业以仿制药企为主,因此其制度实践充分体现了维护本国利益、规避产业短板的灵活思路。中国医药产业境况与印度类似,但在制度构建过程中忽视了对“建设性模糊”的有效运用。因此,可借鉴印度经验,充分利用国际协议的“建设性模糊”进行制度内化,构建适宜本土产业发展的宽松保护环境。
5 国际药品专利制度棘轮效应的中国因应
5.1 运用横向体制转换策略,完善信息交流与利益表 ""达机制
属国体制转换是一种“自上而下”的纵向转换策略,且棘轮效应的不可逆性意味着现有药品专利保护水平难以倒退。面对棘轮效应困境,我国可从以下两方面加以完善。
(1)在国际层面,积极运用横向体制转换策略。我国作为发展中国家,民众医疗负担较重,制药产业发展缓慢,尚不足以单独应对棘轮效应带来的压力。而且,跨国药企及其属国可能利用既有规范构建一个逐层递进且日趋精确化的保护网络,进一步提升保护强度。对此,我国可采用横向体制转换策略,基于多个国际组织参与药品专利的规则制定进而寻求积极成果。首先,联合其它发展中国家积极维护当前以TRIPS为核心的药品专利保护多边框架体系,这是防止药品专利国际保护环境继续恶化的前提之一。例如,印度、巴西一直是对抗强化药品专利保护“侵袭”的排头兵,并始终坚持自身立场,力促药品专利规则的公正与合理。相比之下,中国在相关议题的谈判上多为被动。因此,可加强与其它国家尤其是印度、巴西等发展中国家的联合与合作,协调立场,寻求在医药产业、公共医疗方面的共同利益,有效维护以TRIPS为核心的药品专利保护标准。其次,探索新兴区域性国际组织或国际合作机制,践行横向转换策略,以此种方式参与到药品专利议题的谈判与协商中是当今可能的实践路径之一。面对未来,我国可考虑以“一带一路”、自由贸易区、WTO为平台,形成“点线面”的多层格局,协同推进相关议题的谈判。其中,“一带一路”是我国积极探索引导药品专利规则谈判的重要契机。从既有实践看,尽管中国与“一带一路”共建伙伴尚未形成有约束力的知识产权条约。但是,中国与共建伙伴间已经就诸多知识产权议题达成倡议和谅解备忘录,这些具有软法性质的文件有助于中国与共建伙伴就药品专利议题展开进一步合作。
(2)在国内层面,完善信息交流与利益表达机制。决定企业竞争力的关键是企业与政府的共生度。跨国药企通过组建医药产业同盟、派驻利益代表,与属国建立完善的信息交流与利益表达机制,进而大幅提升与属国间的共生度。在我国,行业协会为企业提供行业信息等服务,具有类似医药产业同盟的作用。现行对外贸易法规定,包括制药企业在内的对外贸易经营者可依法成立或参加有关协会、商会,并依据章程为成员提供包括药品专利政策在内的法律服务。但我国相关建设较为落后,且缺少政策参与的具体程序与途径。因此,若要进一步释放医药行业协会活力,充分发挥其积极作用,就要完善政策参与途径,构建高效的信息交流与沟通机制。具体包括以下3点:一是建立开放的政府体系和信息公开机制,尤其是协会与政府间的日常沟通以及协商、公告、评论、听证等多元性参与机制。二是落实政府重大政策征询机制。作为医药行业组织的重要力量,医药行业协会具有自身优势和信息资源。政府在出台重大决策和相关政策之前听取医药行业协会的意见,应成为一种基本制度和规范,这对于促进政府决策和药品专利政策的科学化具有举足轻重的作用。三是畅通医药行业协会参政议政途径。医药行业协会拥有各大制药企业的高级人才,对行业和社会发展具有独特见解和直观认识。积极吸纳这类人员的力量,通过人大、政协等合法的参政议政途径,能够让政府吸收到关于行业治理的建议和意见,有利于提升药品专利政策制定的科学性。
5.2 充分运用“建设性模糊”,防范专利权扩张风险
公共健康利益的维护需对私人权利作出合理限制,企业共生力的提高也有赖于在强化共生度的基础上为其创造有利的外部环境。从本质上看,无论是美欧的强化保护还是印度的宽松立法,两者在制度实践上都精准选择了适宜本土国情的立法模式。相较而言,中国缺少对本土医药产业与公共卫生环境的精准评估,使得相关立法难以准确反映本国利益。鉴于以仿制药企为主的产业状况以及民众药品可及性提升的需要,中国应选择适宜本土语境的适度宽松立法模式。
(1)充分运用“建设性模糊”,转换适用国际新制度。中国的药品专利立法整体上处于被动接受的状态,相比而言,印度在很大程度上坚持自主立法的方式,面对西方国家的压力时,印度善于灵活运用“建设性模糊”条款带来的弹性立法空间,而中国一定程度上忽视了这一重要措施。以药品实验数据独占保护制度为例,我国《药品试验数据保护实施办法(暂行)(征求意见稿)》(以下简称《征求意见稿》)在对试验数据独占权的保护条件、期限与方式等方面进行规定的同时,严格遵守了TRIPS第39.3条设置的相关要求。但因对“建设性模糊”的弹性空间利用不足,引发了关于试验数据保护边界的争议。在此基础上,即使跨国药企存在恶意抬高药价、限制药品供给等市场滥用行为,也难以有效规制。为此,可从权利机制的内部设计和外部规范入手,明确其保护界限。首先,在内部设计上,明确专利强制许可在药品试验数据独占保护制度中的适用,以形成对试验数据独占权的限制。特别在公共危机出现时,为确保药品持续性供给,除对药品实施强制许可外,有必要积极推进药品安全有效性数据的强制许可。目前来看,《征求意见稿》并未涉及与强制许可有关的规定,故可在后续完善时增设并细化强制许可条款,使其具有可操作性。其次,在外部规范上,建立起与药品数据垄断相对应的反垄断监管体系。药品试验数据独占权与药品专利权有着类似的市场垄断效果,因为这些数据对于药品市场化具有关键作用,试验数据的独占保护势必会带来对药品的市场独占,从而形成一种对专利和数据的双重垄断。因此,对于由跨国药企滥用药品试验数据独占权所引发的、超越权力内部限制规则范畴的、具有严重反竞争效果的市场垄断行为,有必要建立相应的反垄断监管体系予以外部管控。
(2)以限缩路径为导向,防范专利权扩张风险。创新药企占据美欧制药业主体的产业状况决定了制度构建的利益天平不会过度向仿制药企倾斜,因此,其药品专利立法也多以权利扩张为导向。以药品专利纠纷早期解决机制为例,美国将4类专利声明均作为司法机关立案或管辖要件的实质就是权利的扩张。由于中国相关制度以美国制度为蓝本,且制度建设尚未完善,因而存在一定的权利扩张倾向。《药品专利纠纷早期解决机制实施办法(试行)》(以下简称《办法》),在仿制药申请人提出4类专利声明后,专利权人或利害关系人对声明有异议的,可在法定期限内就申请上市仿制药是否侵犯其相关专利权向人民法院提起诉讼。由此可见,4类专利声明都可成为人民法院立案或管辖要件,这实际扩大了专利侵权诉讼的声明范围,跨国药企可利用这一规则任意就所有声明类型向仿制药企提起诉讼,将其拖入诉讼泥潭,加重药企诉讼负担[42]。因此,《办法》应剔除不易引发专利纠纷的声明类型,限制只有在仿制药申请人向药品监督管理部门提出专利权无效或未侵犯专利权声明时,药品专利权人才能向人民法院提起侵权诉讼,避免专利权人大范围发起诉讼,对仿制药上市产生不利影响。
6 结语
药品行业专利规则对社会发展影响深远,故其制度构建需兼顾多方利益进行整体考量。近年来,中国持续推进医药领域监管体制改革,在此背景下,讨论棘轮效应的现实困境与中国因应具有理论与现实意义。此外,将共生理论作为分析工具,在新的系统化视角下深入探究国际药品专利领域的棘轮效应。结合域外立法模式分析,中国应基于本土社会现实语境,从国内、国际两个层面,构建适宜仿制药企业发展的药品专利保护环境,提高民众的药品可及性。
参考文献:
[1] 刘鑫. 药品数据专有权国际立法溯源与中国制度安排[J].科技进步与对策,2024,41(6):139-148.
[2] 牛剑钊,林兰,马锐,等. 中国仿制药研究及监管现状[J]. 中国新药杂志,2014,23(1):6-10.
[3] 黄一帆.辉瑞 Paxlovid 医保谈判出局,新冠药物未来该如何定价[EB/OL]. (2023-01-09) [2023-11-26]http://www.peopledailyhealth.com/index.php.
[4] HELFER L R. Mediating interactions in an expanding international intellectual property regime[J]. Case Western Reserve Journal of International Law,2004,36(1):123-136.
[5] ABBOTT,FREDERICK M. The WTO medicines decision: world pharmaceutical trade and the protection of public health[J]. American Journal of International Law,2006,99(2):317-358.
[6] 梁志文. 美国自由贸易协定中药品TRIPS-Plus保护[J]. 比较法研究,2014,28(1):125-140.
[7] PETER DRABOS. Securing the future of" intellectual property: intellectual property owners and their nodally coordinated enforcement pyramid[J]. Case Western Reserve Journal of International Law,2004,36(1):53-78.
[8] 吴汉东. 知识产权中国化应用研究[M]. 北京:中国人民大学出版社,2014:2.
[9] 朱淑娣. 中美知识产权行政法律保护制度比较: 捷康公司主动参加美国337行政程序案[M]. 北京:知识产权出版社,2012:61-68.
[10] 刘梦宁,刘运国. 经济政策不确定性、目标设定与棘轮效应[J]. 会计研究,2022,43(7):89-106.
[11] WEITZMAN M L. The \"Ratchet Principle\" and performance incentives[J]. Bell Journal of Economics,1980,11(1):302-308.
[12] 何华. 知识产权全球治理体系的功能危机与变革创新:基于知识产权国际规则体系的考察[J].政法论坛,2020,38 (3):66-79.
[13] 何隽. 创新驱动的知识产权政策[M]. 北京:知识产权出版社,2018:28-33.
[14] 乌尔里希·贝克. 风险社会:新的现代性之路[M]. 南京:译林出版社,2018.
[15] 韩成芳. 药品专利制度的现实困境及反思[J]. 科技进步与对策,2021,38(15):118-124.
[16] 彼得·德霍斯. 知识财产法哲学[M]. 周林,译.北京:商务印书馆,2017.
[17] PASHUKANIS E B. Law and Marxism: a general theory[M]. United Kingdom:Pluto Press,1978.
[18] A SAMUEL ODDI. The international patent system and third world development: reality or myth [J]. Duke Law Journal,1987,36(5):831-878.
[19] SON KB,LOPERT R,GLEESON D,et al. Moderating the impact of patent linkage on access to medicines: lessons from variations in South Korea,Australia,Canada,and the United States[J]. Global and Health,2018,14(1):1-11.
[20] 张艳梅.“一带一路”背景下FTA药品专利规则的中国选择[J]. 社会科学战线,2018,41(8):217-227.
[21] 李蓓,易继明. 药品专利常青化策略及应对之探讨[J]. 科技与法律,2019,29(1):1-10.
[22] 张乃根. 论TRIPS协议义务[J]. 浙江社会科学,2002,18(5):68-75.
[23] 吴汉东. 知识产权国际保护制度的变革与发展[J]. 法学研究,2005,31(3):126-140.
[24] REIN J. International governance through trade agreements: patent protection for essential medicines[J].Northwestern Journal of International Law amp; Business,2001,21(2):379-408.
[25] 吴汉东,郭寿康. 知识产权制度国际化问题研究[M]. 北京:北京大学出版社,2010.
[26] SELL S K. Industry strategies for intellectual property and trade: the quest for trips, and post-trips strategies[J]. Cardozo Journal of International and Comparative Law,2002,10(1):79-108.
[27] FISHER B S,STEINHARDT R G I. Section 301 of the trade act of 1974: protection for U.S. exporters of goods, services, and capital[J].Law amp; Poly Intl Bus,1982,14(3):569-690.
[28] GADBAW R M. Intellectual property and international trade: merger or marriage of convenience[J].Vand. J. Transnatl L,1990,22(2):223-242.
[29] PHRMA. Stephen J UbL: president and chief executive officer [EB/OL]. (2020-04-06)[2023-07-24]https://www.phrma.org/resource-center/Topics/Leaders/Stephen-J-Ubl.
[30] PATRICK T,LENNON. Economic issues under the omnibus trade and competitiveness act of 1988: an overview[J]. University of Miami Inter-American Law Review,1989,21(2):387-408.
[31] 张猛. 知识产权国际保护的体制转换及其推进策略——多边体制、双边体制、复边体制[J]. 知识产权,2012,26(10):80-89.
[32] MALPANI,ROHIT. All costs,no benefits: how the US-Jordan free trade agreement affects access to medicines[J].Journal of Generic Medicines,2009,6(3):206-217.
[33] THE UNITED STATES TRADE REPRESSENTIVE. Free trade agreement[EB/OL]. (2020-04-06)[2024-1-7]http://ustr.gov/trade-agreements/free-trade-agreements.
[34] 刘志辉. 共生理论视域下政府与社会组织关系研究[M]. 天津:天津人民出版社,2017.
[35] 袁纯清. 共生理论及其对小型经济的应用研究(上)[J]. 改革,1998,14(2):100-104.
[36] SELL S K. Private power, public law: the globalization of intellectual property rights[M]. United Kingdom:Cambridge University Press,2003.
[37] 李良贤. 基于共生理论的中小企业竞合成长研究[M].北京:经济管理出版社,2011.
[38] 吴飞驰. 企业的共生理论:我看见了看不见的手[M]. 北京:人民出版社,2002.
[39] 王珍愚,郑榕,崔映宇,等. 美日印医药专利政策比较及对我国的启示[J]. 云南财经大学学报,2019,35(9):19-27.
[40] 游文亭. 发展中国家药品专利权与公民健康权的博弈与平衡——以巴西和印度为例[J]. 电子知识产权,2018,22(7):38-47.
[41] SUPREME COURT OF INDIA. Novartis AG v. Union of India[EB/OL].(2013-04-01) [2024-01-09]http: //www.Supremecourtofindia.nic.in/outtoday/patent.pdf.
[42] 冯振龙,周莹. 仿制药专利挑战行为拟制侵权的合理性证成及制度建构[J]. 中国科技论坛,2023,39(4):142-150,157.
The Ratchet Effect of the International Pharmaceutical Patent System and China's Response
Abstract:Today's international pharmaceutical patent system is centered on Western countries and their industries and does not take into account the knowledge gap between countries in the South and the North. In pursuit of excessive monopoly profits,international pharmaceutical companies representing private interests and their affiliated countries continue to push for enhanced protection of pharmaceutical patents on a global scale,and the ratchet effect comes along with it. At present, academic discussions on the ratchet effect in the field of international pharmaceutical patents are still insufficient, for it is not clarified if the ratchet effect exists in the patent system of pharmaceuticals, and there is a lack of systematic thinking about the ratchet effect on the international protection of intellectual property rights. The development of patent rules in the pharmaceutical industry has a profound impact on the development of society, and therefore the construction of its system needs to take into account the interests of multiple parties. In recent years, China has continued to promote the reform of the regulatory system in the pharmaceutical field. Therefore, it is of theoretical and practical significance in this context to discuss the dilemmas of the ratchet effect and China's response to it.
This paper applies the ratchet effect to the trend analysis of the pharmaceutical patent system, explores its substantive causes with the help of the symbiosis theory of management, and then puts forward feasible countermeasures to the rule of law based on the reality of the Chinese society. Combining the development history of the international pharmaceutical patent system with the basic elements of the ratchet effect, this study explores the internal logical relationship between the two. It firstly explains the specific connotation and operation mode of the ratchet effect and emphasizes the importance of the direction of movement from the perspective of unidirectional movement.The development trend of the international pharmaceutical patent system has been systematically discussed, as well as the dilemmas the developing countries are confronting with due to the ratchet effect, such as limited legislative flexibility, stagnation of industrial competition, and difficulties in accessing medicines.
Then the study makes an operational interpretation and analysis of the causes. It combines the basic elements of the ratchet effect with the international pharmaceutical patent system, thus clarifying the specific operation mechanism of the former in this field. Specifically, the TRIPS \"minimum standard\" resists regression in the level of protection and constitutes the stopping paw of the ratchet of the pharmaceutical patent system; under the subject-behavior dichotomy, the interaction between multinational pharmaceutical enterprises and their affiliated countries and their respective driving strategies create the driving force of the ratchet and trigger the spread of the TRIPS-Plus rules to the global market. Furthermore, the study draws on the management theory of symbiosis to explore the substantive causes of the ratchet effect, i.e., the result of the creation of a favorable external environment by the affiliated countries in order to enhance the symbiotic power of the pharmaceutical industry's private groups.
Finally, it summarizes and analyzes overseas experience and China's response. After clarifying the operation mechanism and substantive causes of the ratchet effect of the international pharmaceutical patent system, this part zooms in on a concrete response to the ratchet effect. Firstly, two different modes of pharmaceutical patent protection in response to the ratchet effect are examined under the perspective of comparative law: the enhanced protection mode represented by the United States and the European Union, and the lax legislation mode represented by India. In view of the development of China's pharmaceutical industry and the reality of the public healthcare environment, the latter model is more meaningful. Secondly, in terms of specific measures, the paper presents suggestions, including applying the strategy of horizontal institutional transformation, improving the mechanism of information exchange and expression of interests, and making full use of \"constructive ambiguity\" to prevent the risk of patent expansion. Taking into account the foreign legislative model, China should, based on the realities of the domestic society, build a pharmaceutical patent protection environment suitable for the development of generic enterprises at both the domestic and international levels, so as to improve the accessibility of medicines to the public.
Key Words:Pharmaceutical Patent System;Ratchet Effect;Symbiotic Theory;Symbiotic Force

