益肾固精暖脐贴制备工艺的研究
包晴 高元航 廖卓 王璐 黄莉 唐林 黄超文 杨磊

〔摘要〕 目的 研究益肾固精暖脐贴的提取工艺及其成型工艺。方法 以蛇床子素、羟基-α-山椒素、金丝桃苷以及浸膏得率为考察指标,以提取时间、提取溶媒倍数、乙醇浓度为考察因素,运用Box-Behnken设计-响应面法优选出最佳提取工艺;以凝胶贴膏的初黏力、持黏力、剥离强度、感官评价为指标,采用D-最优混料设计优选益肾固精暖脐贴的最佳成型工艺。结果 益肾固精暖脐贴的最佳提取工艺为回流提取120 min,提取溶媒倍数为12,乙醇浓度为57%,同法提取2次;最佳成型工艺的质量比为NP700占6.00%、PVP-k90占0.60%、甘羟铝占0.15%、填充剂5.76%、EDTA-2Na占0.10%、甘油占21.76%、柠檬酸占0.20%、水和药液总量占65.43%。结论 该实验优选的益肾固精暖脐贴的提取工艺及其凝胶贴膏的制备工艺稳定可行,可为该产品的进一步开发利用提供参考。
〔关键词〕 益肾固精暖脐贴;高效液相色谱法;Box-Behnken-设计响应面法;D-最优混料设计;凝胶贴膏
〔中图分类号〕R283.6 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2024.06.012
Preparation process of Yishen Gujing Nuanqi Patch
BAO Qing1, GAO Yuanhang1, LIAO Zhuo1, WANG Lu2, HUANG Li2,
TANG Lin2, HUANG Chaowen3, YANG Lei2*
1. The First Clinical School of Chinese Medicine, Hunan University of Chinese Medicine, Changsha, Hunan 410007, China; 2. The First Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410007, China; 3. The Hospital of Hunan Academy of Chinese Medicine, Changsha, Hunan 410006, China
〔Abstract〕 Objective To study the extraction process and molding process of Yishen Gujing Nuanqi Patch (YSGJNQP). Methods Using osthole, hydroxy-α-sanshool, hyperoside, and extract yield as evaluation indicators, and extraction time, extraction solvent ratio, and ethanol concentration as factors, the Box-Behnken response surface method was used to optimize the optimal extraction process. Taking the initial adhesion, holding adhesion, peeling strength, and sensory evaluation of the gel patch as indicators, the D-optimal mixture design was used to optimize the optimal molding process for YSGJNQP. Results The optimal extraction process for YSGJNQP was reflux extraction for 120 minutes, with an extraction solvent ratio of 12 and an ethanol concentration of 57%, repeated twice using the same method. The optimal molding process had a mass ratio of 6.00% NP700, 0.60% PVP-k90, 0.15% glycoxyaluminium, 5.76% filler, 0.10% EDTA-2Na, 21.76% glycerin, 0.20% citric acid, and 65.43% total amount of water and medicinal solution. Conclusion The optimized extraction process and gel patch preparation process for YSGJNQP in the study are stable and feasible, providing a reference for further development and utilization of this product.
〔Keywords〕 Yishen Gujing Nuanqi Patch; high performance liquid chromatography; Box-Behnken response surface method; D-optimal mixture design; gel paste
固精益肾暖脐膏出自《摄生秘剖》卷四,主要由花椒、蛇床子、韭菜子、肉桂、母丁香、麝香、附子、硫黄组成,用于治疗男子精寒,阳事痿弱,举而不坚,坚而不久,白浊遗精等症[1]。该方中所含化学成分主要有黄酮类、香豆素类、酰胺类、挥发油类等,原制剂中部分药物是采用油炸的方式对药物进行有效成分的提取,但此方式有着高温破坏药物成分,产生空气污染的弊端[2],且经过高温的提取,有效成分留存较少,为进一步优化方案,本实验以醇提取来代替油炸提取,根据成分及其药效综合考察,决定将处方分为两部分,花椒、蛇床子、韭菜子、附子这四味药以醇提的方式提取,肉桂、母丁香、硫黄、麝香制备成粉末做填充剂参与药物的成型。蛇床子中最具代表性的香豆素类成分蛇床子素具有温补肾阳的作用[3-5];花椒在处方中占比最高,含有能够发挥温中止痛的作用的山椒素[6-7];花椒和蛇床子中都含有能够改善肾阳虚证,提高免疫力的金丝桃苷[8],因此本实验选用这三个成分以及浸膏得率为指标来优选提取工艺。
原制剂为黑膏药,传统制备方式是将药物油炸之后再下丹形成膏状物,黑膏药中的铅经过长久接触后会在体内积累,发生中毒反应[9],对身体健康造成危害。随着贴膏制剂的发展,凝胶贴膏开始步入市场。凝胶贴膏是指原料药物与适宜的亲水性基质混匀后涂布于背衬材料上制成的贴膏剂,作为一种新型透皮给药载体,与传统黑膏药相比,凝胶贴膏具有使用方便、刺激性小、载药量大、保湿性好、透皮吸收率高、用药依从性好等显著优点[10-12]。
Box-Behnken设计-响应面法是采用多元二次回归方程来拟合实验数据,寻求最优工艺参数,常用于制剂工艺研究[13]。因试验因素选取较多,为了避免多因素之间的相互影响,采用了D-最优混料设计来优化处方配比,D-最优混料设计固定各基质总量不变,预测结果准确性高,更适合凝胶贴膏的处方优化[14]。
本实验采用Box-Behnken设计-响应面法与D-最优混料设计法优选出益肾固精暖脐贴最佳的提取工艺和成型工艺,以期为益肾固精暖脐贴的进一步开发利用提供参考。
1 仪器与材料
1.1 仪器
Agilent1260型HPLC色谱仪(G7117C型DAD检测器,G7130A型柱温箱,G7129A型自动进样器,G7111A型四元泵)、Agilent C18色谱柱(5 μm,4.6 mm×250 mm)(美国安捷伦科技有限公司);SK5200H型超声波清洗器(上海科导超声仪器有限公司);AUX-220型十万分之一分析天平(日本SHIMADZU公司);JB-160型电动搅拌器(上海析牛莱伯仪器有限公司);HG-810型胶带初黏性试验机(东菀市华国精密仪器有限公司);XK-203型触摸屏款拉力机(东菀市欣科仪器仪表有限公司);CBY-2DY型持粘性测试仪(济南百戈实验仪器有限公司);AUX-220型万分之一分析天平(日本SHIMADZ公司);101-3S型电热恒温干燥箱(绍兴市沪越仪器设备有限公司)。
1.2 试剂与药材
对照品金丝桃苷(成都曼斯特生物科技有限公司,批号:MUST-14052113,质量分数≥98%);羟基-ɑ-山椒素(成都埃法生物科技有限公司,批号:AFCD2611,质量分数≥98%);蛇床子素(中国食品药品检定研究院,批号:110822-202111,质量分数≥98%);磷酸(H3PO4,国药集团化学试剂有限公司,批号:20211027);乙腈为色谱纯(德国Merck公司);其余试剂均为分析纯;聚乙烯吡咯烷酮(PVP-k90)(山东优索化工科技有限公司,批号:119197009100);聚丙烯酸钠(NP700)(日本昭和电工株式会社,批号:291470A);甘羟铝(日本协和化学工业株式会社,批号:SG-0663);高岭土(河南铂润铸造材料有限公司);柠檬酸(批号:20221109)、EDTA-2Na(批号:20230109)、甘油(批号:20221208)、无水乙醇(批号:20221102)均购自国药集团化学试剂有限公司;水为纯化水。
肉桂、母丁香、麝香、硫黄、花椒、蛇床子、黑顺片、韭菜子均购于湖南南国药都饮片公司,经湖南中医药大学第一附属医院杨磊主任药师鉴定为正品。
2 提取工艺方法与结果
2.1 含量测定
2.1.1 色谱条件 Agilent C18色谱柱(5 μm, 4.6 mm×250 mm),柱温30 ℃;流动相:乙腈(A)-水(含0.1%磷酸,B),梯度洗脱程序:0~20 min,10%~20%A;20~25 min,20%~30%A;25~45 min,30%~50%A;45~50 min,50%~60%A;50~60 min,60%A;流速1 mL/min;检测波长0~42 min为256 nm,42~53 min为270 nm,53 min之后为322 nm;进样量5 μL。
2.1.2 溶液的制备 对照品溶液:精密称取各对照品适量,加甲醇制成每1 mL含金丝桃苷0.074 mg、羟基-?琢-山椒素0.326 mg、蛇床子素0.216 mg的混合溶液,摇匀,即得。
供试品溶液:按照处方比例称取花椒、蛇床子、韭菜子、黑顺片共60 g,置于圆底烧瓶中,加入10倍量50%乙醇,提取1 h,过滤提取液并浓缩至50 mL,精密量取提取液1 mL置于25 mL容量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
阴性样品溶液:分别取缺蛇床子、缺花椒、缺蛇床子和花椒的阴性样品,按照供试品方法制备,即得。
2.1.3 专属性考察 取空白溶剂甲醇以及“2.1.2”项下制备对照品溶液、供试品溶液、阴性样品溶液依次进样5 μL,如图1所示,结果表明对照品与供试品溶液3种成分色谱峰保留时间一致且分离度良好,空白对照及饮片中其他组分对测定无干扰,表明方法专属性良好。
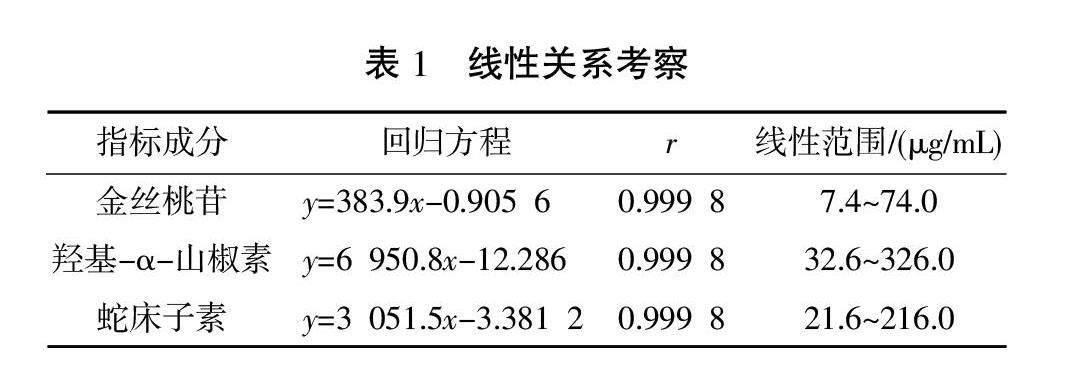
2.1.4 线性关系考察 精密吸取“2.1.2”项下制备的对照品溶液0.1、0.2、0.4、0.6、0.8、1 mL置于1 mL量瓶中,用甲醇稀释至刻度,即得到系列质量浓度的对照品溶液。按照“2.1.1”项下色谱条件进行进样分析。以各成分进样质量浓度为横坐标(x)、峰面积为纵坐标(y),用最小二乘法进行线性回归分析,得回归方程及线性范围。3种成分的回归方程、r值及线性范围见表1。
2.1.5 精密度试验 取“2.1.2”项下方法制备的混合对照品溶液,按照“2.1.1”项下色谱条件连续进样6次,计算3种成分峰面积的RSD值,结果显示金丝桃苷、羟基-?琢-山椒素、蛇床子素峰面积的RSD分别为1.08%、0.67%、0.70%,表明仪器精密度良好。
2.1.6 稳定性试验 取同一供试品溶液,按照“2.1.1”项下色谱条件,分别于0、2、4、8、12、24 h进行进样测定,计算3种成分峰面积的RSD值,结果显示金丝桃苷、羟基-?琢-山椒素、蛇床子素峰面积的RSD分别为0.95%、0.94%、0.93%。表明供试品溶液在24 h内的稳定性良好。
2.1.7 重复性试验 取同一批次的药材,依照“2.1.2”项下方法平行制备6份供试品溶液,按照“2.1.1”项下色谱条件进行进样测定,计算含量并记录峰面积。结果显示金丝桃苷、羟基-ɑ-山椒素、蛇床子素的平均含量为0.74、2.50、0.89 mg/mL,其RSD值分别为0.75%、0.70%、0.72%,表明该方法重复性良好。
2.1.8 加样回收率试验 取已知含量的提取液6份,每份取样量0.5 mL,按照质量浓度1∶1的比例加入对照品,依据“2.1.2”项下供试品溶液进行制备,再依据“2.1.1”项下色谱条件进行测定并计算回收率。结果显示金丝桃苷、羟基-?琢-山椒素、蛇床子素的平均加样回收率分别为101.99%、102.63%、94.79%,其RSD值分别为2.73%、1.78%、2.66%,表明所建立的方法可行。
2.2 浸膏得率测定
精密量取提取液10 mL,置于已经恒重好的蒸发皿中,水浴蒸干,将蒸发皿放入105 ℃烘箱中干燥3 h,取出,置于干燥器中冷却30 min,称定重量。浸膏得率=(干膏质量×总体积)/(取样量×总生药量)×100%。
2.3 熵权法评价
首先测定不同提取方法所得供试品溶液中金丝桃苷、羟基-?琢-山椒素、蛇床子素和浸膏得率,建立初始化决策矩阵Xij。对数据进行归一化处理后建立概率矩阵Pij;其次,计算各指标信息熵Eij及权重系数Wj,得出金丝桃苷、羟基-?琢-山椒素、蛇床子素和浸膏得率权重系数分别为0.24、0.26、0.27、0.23,再根据Wj通过线性加权计算综合评分Y。
2.4 单因素考察提取工艺
取处方药材花椒、蛇床子、韭菜子、黑顺片共60 g,考虑实际生产中不会进行药物粉碎,所以为避免粉碎对提取结果造成偏差,因此在实验过程中也不进行粉碎,以不同浸泡时间(0、30、60、90、120 min)、不同提取时间(30、60、90、120、150 min),不同乙醇浓度(10%、30%、50%、70%、90%)、不同提取溶媒倍数(6、8、10、12、14倍)以及不同提取次数(1、2、3次)为考察条件进行提取试验。按照“2.1.2”项下的操作制备供试品溶液,进行金丝桃苷、羟基-?琢-山椒素、蛇床子素以及浸膏得率的含量测定。根据熵权法计算结果,结果见图2。
2.5 Box-Behnken设计-响应面法优选提取工艺条件
通过单因素实验的考察结果来看,由于评分随浸泡时间的增加而降低,因而浸泡时间不作为考察因素;本实验选取对提取工艺有直接影响的因素,分别为提取时间(A)、提取溶媒倍数(B)、乙醇浓度(C),各因素选取低、中、高3个水平,固定提取次数为2次进行提取,以金丝桃苷、羟基-?琢-山椒素、蛇床子素以及浸膏得率的综合评分为评价指标。试验设计表及结果见表2。
2.5.1 模型拟合及方差分析 采用Design Expert
13.0.1软件,对数据进行拟合,结果表明二次多项回归方程模型较优(P<0.000 1,失拟项P=0.187 3)。最终得到二次多项回归方程为:Y=0.755 2+0.003 1A+0.138 5B+0.326 6C+0.019 3AB-0.096 7AC-0.042 4BC-0.053 1A2+0.028 5B2-0.240 0C2,R2=0.993 9,表明此设计模型拟合度较优,可用此模型对本实验提取工艺进行分析和预测。
2.5.2 条件优化、预测与验证 采用Design Expert
13.0.1软件,绘制提取时间、提取溶媒倍数、乙醇浓度之间的3D响应面图,具体结果见图3,根据模型进行预测得出本实验最佳提取方案为提取时间120 min,提取溶媒倍数为12,乙醇浓度为57%,评分预测值为0.928。按照此条件进行3次验证实验,最终结果见表3。由此可知,优化后的工艺稳定性较好、重复性较高,因此该建立的数学模型能够良好的预测结果。
3 成型工艺方法与结果
3.1 样品制备
药液制备:称取母丁香、肉桂、硫黄、麝香打粉备用,其余药材加12倍量的60%乙醇回流2 h,滤过,提取两次,合并滤液,将液体蒸至无醇味,浓缩至相对密度为1.15~1.20(60 ℃),即得。
益肾固精凝胶贴膏制备:取PVP-k90,加20倍水溶胀,待溶胀完全之后,加入柠檬酸和药液混匀作为A相备用;将母丁香、肉桂、硫黄、麝香粉碎与高岭土混合作为填充剂备用;取适量的甘油、NP700、EDTA-2Na以及甘羟铝混匀作为B相备用。先将A相和填充剂混匀,在搅拌过程中加入B相,待膏体成型之后,置于背衬材料上,过涂布机涂布成型,放置至膏体成型,裁剪,即得。
3.2 指标评价
参照《中华人民共和国药典》2020年版[15]以及文献[16-17],以初黏力(20分)、持黏力(20分)、剥离强度(20分)以及感官评价(透布程度、均匀性、涂展性、皮肤追随性、反复揭贴性)(5×8分)为评价指标,总分为100分。
3.2.1 初黏力 取3片供试品,在18~25 ℃、相对湿度40%~70%条件下放置2 h以上,将供试品固定于30°倾斜板中央,膏面向上,去除防黏层,使钢球自斜面顶端自由滚下,并记录膏体能黏住的最大球号钢球。
评分标准:按公式X/Xmax×20 评分,X为试验中的实际测定值,Xmax为试验中最高测定值。
3.2.2 持黏力 将贴膏裁剪成3×10 cm,于18~25 ℃、相对湿度40%~70%条件下放置2 h以上,去除防黏层,将供试品贴于试验板上,用滚压轴在供试品上来回滚动三次,使贴膏完全贴合试验板,再将贴膏放置20 min之后进行测定,于试验板下端挂一500 g砝码,记录贴膏从试验板上脱落的时间。
评分标准:按公式Y/Ymax×20评分,Y为试验中的实际测定值,Ymax为试验中最高测定值。
3.2.3 剥离强度 将贴膏裁剪成2.5×10 cm,于18~25 ℃、相对湿度40%~70%条件下放置2 h以上。去除防黏层,将供试品贴于试验板上,用滚压轴在供试品上来回滚动3次,使贴膏完全贴合试验板,再将贴膏放置20 min再进行测定,在凝胶贴膏的一端做180°的折返,并将该端夹在试验机的拉力测定仪夹具上,以100 mm/min的速度将凝胶贴膏从试验板上拉离,测定其剥离强度。
评分标准:按公式Z/Zmax×20评分,Z为试验中的实际测定值,Zmax为试验中最高测定值。
3.2.4 感官评价 以透布程度、均匀性、皮肤追随性、涂展性以及反复揭贴性多指标综合评分为感官评分[14]。评分标准见表4。
3.3 单因素实验及结果
经过前期实验,确定使用PVP-k90作为增黏剂,固定其他成分的用量,分别对PVP-k90(0.3%、0.4%、0.5%、0.6%、0.7%)、柠檬酸(0.15%、0.20%、0.25%、0.30%、0.35%)、甘油(15%、20%、25%、30%、35%)、NP700(4.0%、4.5%、5.0%、5.5%、6.0%)、甘羟铝(0.10%、0.15%、0.20%、0.25%、0.30%)、EDTA-2Na(0.1%、0.2%、0.3%、0.4%、0.5%)以及填充剂(3%、4%、5%、6%、7%)的用量进行考察和载药量的筛选(6.4、12.8、19.2、25.6、32.0 g/100 cm2),以初黏力、持黏力、剥离强度及感官评分来评价凝胶贴膏的性状。结果见图4。
3.4 D-最优混料设计优选益肾固精暖脐贴成型工艺
在单因素的基础上,得到各个基质的用量范围,固定载药量为12.8 g/100 cm2,对其余基质进行考察,分别为PVP-k90(A)0.4%~0.6%,柠檬酸(B)0.20%~0.30%,甘油(C)15%~25%,NP700(D)5%~6%,甘羟铝(E)0.15%~0.25%,EDTA-2Na(F)0.1%~0.3%,填充剂(G)5%~7%。
评分标准:计算综合评分,评分公式为综合评分=初黏力评分(X)+持黏力评分(Y)+剥离强度评分(Z)+感官评分(S),采用Design-Expert13.0.1软件进行D-最优混料设计,结果见表5。
3.4.1 模型拟合 采用Design-Expert13.0.1软件对表5数据进行拟合,R2=0.955 9。通过分析可得,模型具有显著性(P=0.002 1<0.05);失拟项P=0.771 9>0.05,由此可知该模型拟合度良好,可用于预测。
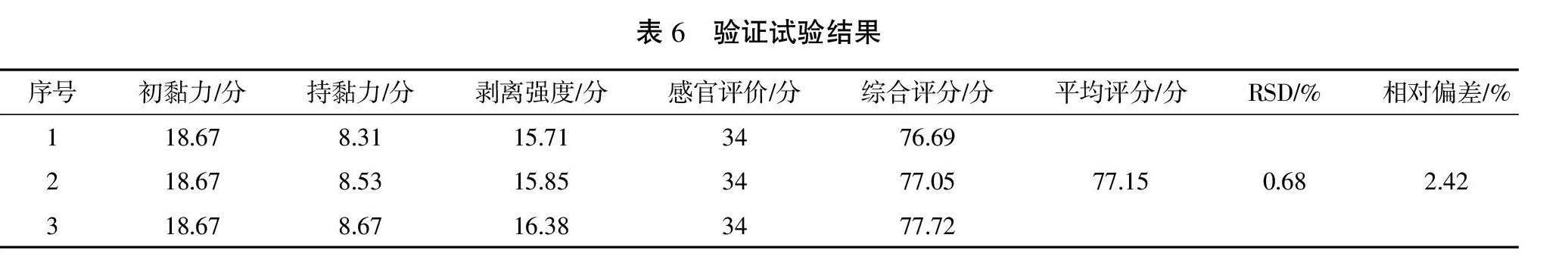
3.4.2 验证试验 以综合评分最高值为优化目标,按照模型预测的结果显示,最优工艺的质量占比分别为NP700 6.00%、PVP-k 900.60%、甘羟铝0.15%、填充剂5.76%、EDTA-2Na 0.10%、甘油21.76%、柠檬酸0.20%、水和药液总量65.43%,综合评分预测值为79.06。按照最优组合进行3次验证实验,结果见表6,最优处方的综合评分与预测值接近,提示该工艺稳定可行,D-最优混料设计法预测性良好,结果可靠。
4 讨论
凝胶贴膏作为一种新型贴膏,目前在对其质量进行评价方面并没有一个特别完善的标准,《中华人民共和国药典》中暂未收录凝胶贴膏的制备方法,但收录了贴膏的指标评价方法,通过查阅文献,发现大部分学者是通过结合《中华人民共和国药典》标准测定贴膏的初黏力、持黏力、剥离强度以及感官评价来对贴膏的物理性能进行评价,但也有学者提出初黏力和持黏力乃是非量化指标,实验中影响因素较多,导致结果的重现性较差,因此选取胶强度等为指标进行评价[18]。实验过程中发现,如果凝胶贴膏能够稳定的被制备成型,在贴膏能够稳固成型的基质比例内,那么初黏力、持黏力、剥离强度以及感官评价可以有效的评价贴膏成型质量,因此,选取这几个指标在固定范围内进行成型实验研究。不仅如此,影响贴膏成型的还有其基质材料的因素,本实验前期通过考察不同种类的基质并且使用了不同厂家的甘羟铝,NP700、聚乙烯醇等进行实验,发现不同厂家的贴膏基质质量参差不齐,对贴膏的成型具有一定影响,所以材料的选取也是制备好凝胶贴膏的一重要因素。
通过本实验方法选取出的贴膏制备工艺,成品外观平整、色泽均匀、黏附性好,可为益肾固精凝胶贴膏的进一步开发提供参考。
参考文献
[1] 洪 基. 摄生总要[M]. 张 蒿, 朱为坤, 校注. 北京: 中国中医药出版社, 2023: 83-84.
[2] 张 璐, 李兆玉, 蔡文腾, 等. 星点设计-效应面法优化黄玉膏成型工艺研究[J]. 中国现代应用药学, 2022, 39(4): 467-474.
[3] 赵 炎. 基于IL-11/ERK1/2信号通路探讨蛇床子素改善肾纤维化的机制研究[D]. 武汉: 华中科技大学, 2022.
[4] SONG G S, ZHOU L, SHENG N, et al. Simultaneous quantification of 16 bioactive constituents in Common cnidium fruit by liquid chromatography-electrospray ionization-mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2015, 107: 304-310.
[5] LU Q, FENG Q S, YU J X, et al. Metabolomics and serum pharmacochemistry revealed the preventive mechanism of Gushudan in kidney-Yang-deficiency-syndrome rats[J]. Biomedical Chromatography: BMC, 2023, 37(3): e5569.
[6] 贺梦媛, 张 兵, 徐 桐, 等. 花椒化学成分、药理作用研究进展及质量标志物预测分析[J]. 山东中医杂志, 2022, 41(12): 1351-1358.
[7] 张萌萌, 王 丹, 魏大能, 等. 基于血清药物化学的花椒温中止痛的质量标志物研究[J]. 中草药, 2022, 53(9): 2731-2739.
[8] 赵雪晗, 仝 建. 多囊卵巢综合征中西医结合治疗与护理研究[J]. 现代医药卫生, 2020, 36(5): 753-755.
[9] 胡 楠, 曹 欢, 笔雪艳. 基于前处理方法改进的海马万应膏质量标准提升研究[J]. 黑龙江医药, 2023, 36(1): 1-4.
[10] 张 宇, 包旭宏, 王 峰, 等. 中药凝胶贴膏的历史渊源与制备工艺研究进展[J]. 中华中医药杂志, 2023, 38(6): 2769-2774.
[11] 李 宁, 蒋境兴, 武英茹, 等. 中药凝胶贴膏剂制剂处方及成型工艺研究进展[J]. 辽宁中医药大学学报, 2022, 24(8): 134-138.
[12] 范俊锋, 周 艳, 吴雪茹, 等. 通络止痛贴膏的薄层鉴别及初步稳定性考察[J]. 中国中医药现代远程教育, 2023, 21(3): 146-148.
[13] 宋 燕, 冉 姗, 孙方方, 等. Box-Behnken设计-响应面法优化木鳖子霜炮制工艺[J]. 中草药, 2019, 50(2): 382-387.
[14] 梅佳华, 王 涛, 查丽春, 等. D-最优混料设计制备复方蜘蛛香凝胶贴膏及初步药效学考察[J]. 中草药, 2022, 53(11): 3329-3337.
[15] 国家药典委员会. 中华人民共和国药典: 2020年版[M]. 北京: 中国医药科技出版社, 2020: 143-144.
[16] 周 艳, 严春霞, 范俊锋, 等. 筋骨疗伤贴膏基质处方的优化研究[J]. 按摩与康复医学, 2022, 13(24): 50-52.
[17] 林世源, 黄慧琳, 陈 卉, 等. 白花丹巴布剂的基质处方优选及其体外透皮吸收研究[J]. 中国现代应用药学, 2020, 37(16): 1963-1967.
[18] 李 栋, 唐永和, 王海洋, 等. D-最优混料设计优化实脾消水凝胶贴膏的处方[J]. 中国药师, 2021, 24(12): 2249-2252, 2292.

