来那度胺治疗淋巴瘤中国专家共识(2024 年版)
中国抗癌协会淋巴瘤专业委员会
淋巴瘤是一组起源于淋巴造血系统的恶性肿瘤,病理类型复杂,异质性强,发病率正呈现不断上升的趋势。近年来,在细胞毒药物治疗的基础上,小分子靶向药物、双特异性抗体、抗体偶联药物、细胞治疗等方法不断发展,淋巴瘤患者的预后生存持续改善。来那度胺在惰性B 细胞淋巴瘤治疗中的作用较早被证实,目前由于用药可及性提高,临床应用也越来越多。为了更好地指导临床医生合理、有效、安全地应用来那度胺治疗淋巴瘤,中国抗癌协会淋巴瘤专业委员会组织专家制订了本共识。
1 来那度胺抗肿瘤机制
来那度胺是一种免疫调节剂,详细的作用机制尚未明确。有研究显示其能够抑制TNF-α、IL-1、IL-6及IL-12 的分泌,促进IL-10 分泌,诱导肿瘤细胞凋亡,激活肿瘤微环境中T 细胞和NK 细胞活性,发挥免疫调节的抗肿瘤作用[1]。E3 泛素连接酶cereblon(CRBN)被初步认为是来那度胺发挥免疫调节抗肿瘤活性的直接分子靶标。研究发现弥漫性大B 细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL)的活化B 细胞(activated B-cell,ABC)亚型对来那度胺更敏感,ABC亚型淋巴瘤细胞有B 细胞受体(B-cell receptor,BCR)介导的NF-κB 信号通路过度激活以及干扰素调节因子4(interferon regulatory factor 4,IRF4)高表达的特点,来那度胺可以通过调节CRBN 抑制IRF4 的表达,从而使BCR 依赖的NF-κB 信号通路下调,抑制肿瘤细胞的生长[2-3]。此外,研究还发现来那度胺通过调节CRBN 诱导T 细胞抑制因子ikaros 和aiolos 的降解,刺激T 细胞活化[4]。来那度胺联合治疗也显示较好的协同增效机制,如抗CD20 单抗体联合来那度胺可增强抗体依赖细胞介导的细胞毒作用[5]。
2 来那度胺在淋巴瘤常见亚型中的应用共识
来那度胺在淋巴瘤常见亚型中的应用共识汇总,见表1。
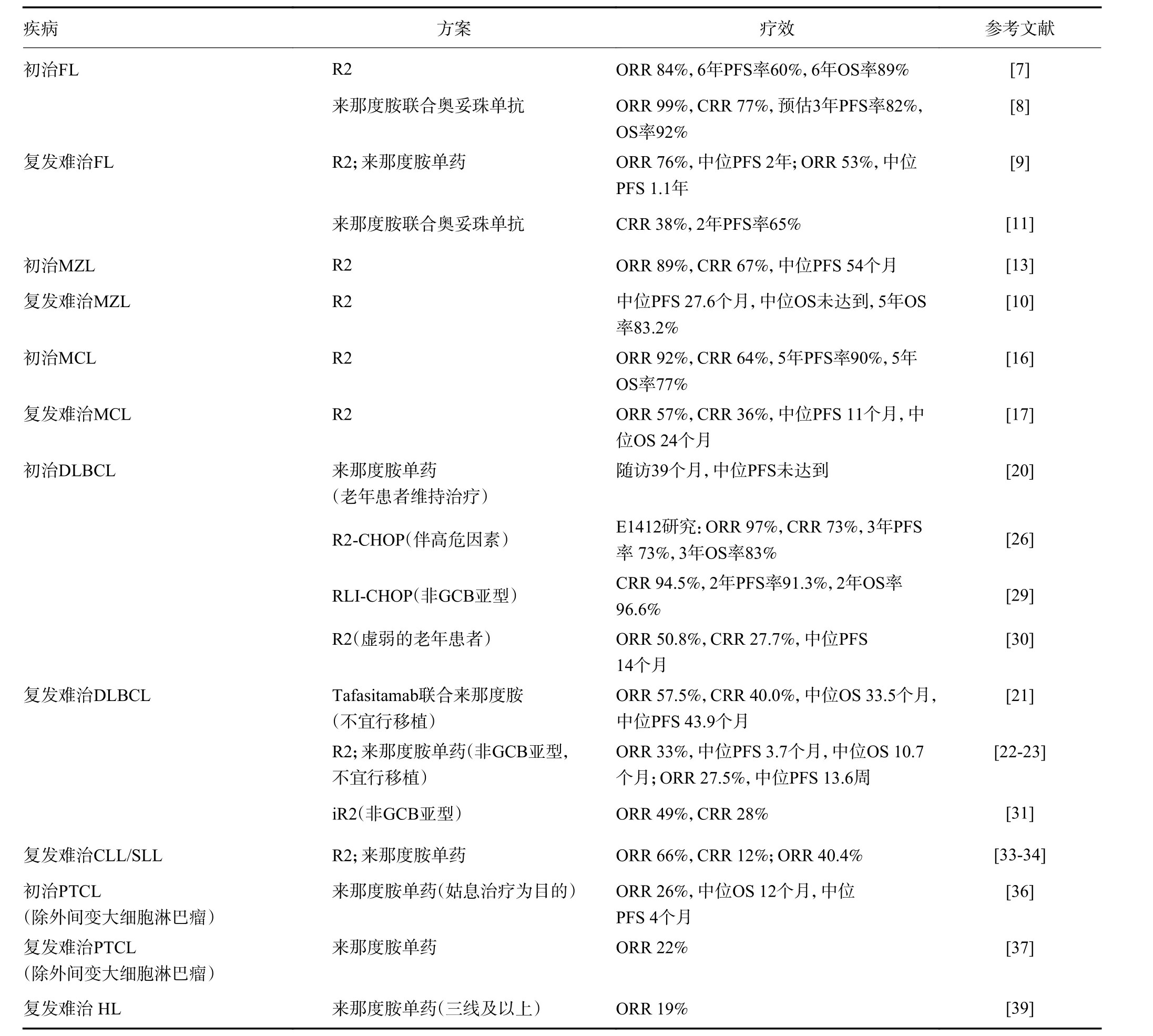
表1 来那度胺在淋巴瘤常见亚型中的应用共识
2.1 滤泡性淋巴瘤
滤泡性淋巴瘤(follicular lymphoma,FL)是来源于滤泡生发中心的惰性B 细胞淋巴瘤。中国FL 的发病率占非霍奇金淋巴瘤的8%~23%,临床表现以淋巴结肿大伴或不伴骨髓受累和脾肿大为特征[6]。对于有系统治疗指征的初治FL 患者,抗CD20 单抗联合化疗是最常用的治疗方法。RELEVANCE 研究结果显示,来那度胺联合利妥昔单抗(R2)治疗进展期高肿瘤负荷的初治FL 患者,疗效与利妥昔单抗联合化疗方案相似,客观缓解率(objective response rate,ORR)分别为84% 和89%,中位随访72 个月,两组中位无进展生存期(progression-free survival,PFS)和总生存期(overall survival,OS)均未达到,6 年PFS 率分别为60%和59%,6 年OS 率均为89%,且无新增安全性事件,是一种可选择的无化疗替代方案[7]。LYSA 研究结果显示,对于初治的高肿瘤负荷FL 患者,来那度胺联合奥妥珠单抗也具有良好的临床疗效,ORR 为99%,完全缓解率(complete response rate,CRR)为77%,中位随访3.7 年,预估3 年PFS 率82%,OS 率92%,≥3 级中性粒细胞减少症发生率47%,其他不良反应发生率低[8]。基于复发/难治(relapsed/refractory,R/R)FL 患者的研究结果显示,R2 方案对比来那度胺单药疗效更佳,且不良反应相似,ORR 分别为76%和53%(P=0.029),中位随访2.5 年,来那度胺单药组中位PFS 为1.1 年,R2 组为2 年[9]。AUGMENT研究显示,R/R FL 患者相较于利妥昔单抗联合安慰剂方案治疗,R2 方案可显著改善PFS,两组中位PFS 分别为39.4 个月和14.1 个月(P<0.001)[10]。来那度胺联合奥妥珠单抗治疗R/R FL 患者的CRR 为38%,2 年PFS 率为65%[11]。因此,共识推荐来那度胺联合抗CD20 单抗可以作为初治和R/R FL 患者的治疗选择,尤其适用于不可耐受化疗的患者。若患者不适合抗CD20 单抗治疗,来那度胺单药也可作为推荐治疗方案。

表2 来那度胺治疗方案的推荐用法
2.2 边缘区淋巴瘤
边缘区淋巴瘤(marginal zone lymphoma,MZL)是一组起源于滤泡边缘区的惰性B 细胞淋巴瘤,约占非霍奇金淋巴瘤的7%,临床表现多样,根据受累部位不同,主要分为黏膜相关淋巴组织结外边缘区淋巴瘤、脾脏边缘区淋巴瘤和结内边缘区淋巴瘤[12]。针对病因的抗幽门螺旋杆菌、丙型肝炎病毒等治疗非常重要。对于有系统治疗指征的初治MZL 患者,抗CD20 单抗联合化疗是最常用的治疗方法。由于发病率较低,来那度胺治疗MZL 患者数据多来源于与FL 患者共同纳入的临床研究。R2 治疗初治MZL 患者的ORR为89%,CRR 为67%,中位PFS 为54 个月[13]。AUGMENT 研究中,R2 和利妥昔单抗联合安慰剂方案治疗R/R MZL 患者,中位随访65.9 个月,中位PFS 分别为27.6 个月和14.3 个月,中位OS 均未达到,5 年OS 率分别为83.2%和77.3%,R2 疗效优于利妥昔单抗单药治疗[10]。来那度胺联合奥妥珠单抗治疗MZL缺乏临床试验的数据,但有研究提示含奥妥珠单抗方案可用于治疗利妥昔单抗耐药的R/R MZL 患者[14]。因此,共识推荐来那度胺联合抗CD20 单抗可以作为初治和R/R MZL 患者的治疗方案,尤其是对于预估不可耐受化疗的老年虚弱R/R MZL 患者。若患者不适合抗CD20 单抗治疗,来那度胺单药也可作为推荐治疗方案。
2.3 套细胞淋巴瘤
套细胞淋巴瘤(mantle cell lymphoma,MCL)是一种起源于滤泡套区的B 细胞淋巴瘤,占非霍奇金淋巴瘤的6%~8%,临床表现主要有淋巴结肿大、脾肿大,且容易结外侵犯,包括骨髓和消化道。MCL 兼具侵袭性淋巴瘤的侵袭性和惰性淋巴瘤的不可治愈性特点,某些疾病表现为白血病型[15]。抗CD20 单抗联合化疗是最常用的治疗方法,以布鲁顿氏酪氨酸激酶(BTK)抑制剂为代表的靶向药物治疗显著提高MCL 患者的疗效。对于不可耐受免疫化疗和BTK 抑制剂治疗的初治MCL 患者,R2 方案持续治疗的研究显示,ORR 为92%,CRR 为64%,中位随访64 个月,3 年和5 年PFS率和OS 率分别为80%、90%和64%、77%[16]。R2 方案治疗R/R MCL 患者的ORR 为57%,CRR 为36%,中位缓解持续时间、PFS 和OS 分别为19 个月、11个月和24 个月[17]。因此,共识推荐来那度胺联合抗CD20 单抗可以作为初治和R/R MCL 患者不可耐受免疫化疗和BTK 抑制剂治疗或上述治疗耐药后的治疗方案,来那度胺可以持续应用至疾病进展或不良反应不可耐受。若患者不适合抗CD20 单抗治疗,来那度胺单药也可作为推荐方案。
2.4 DLBCL
DLBCL 是一种来源于成熟B 细胞的侵袭性淋巴瘤,是最常见的淋巴瘤类型,占非霍奇金淋巴瘤的25%~50%,临床表现、分子遗传学异常、治疗反应和预后均具有高度异质性,主要表现为淋巴结肿大和(或)淋巴结外受累[18]。利妥昔单抗联合CHOP(R-CHOP)方案仍然是初治DLBCL 患者的标准治疗,但是对于伴高国际预后指数(international prognostic index,IPI)评分、非生发中心(non-germinal center B-cell,non-GCB)或ABC 亚型等预后不良因素的患者,R-CHOP方案的疗效仍有待提高。有研究证实维泊妥珠单抗(抗CD79B 单抗偶联剂)联合R-CHP 方案较RCHOP 方案显著提高了IPI 评分≥2 分的DLBCL 患者的疗效[19]。来那度胺在DLBCL 中的应用尚存争议。REMARC 研究证实来那度胺在60~80 岁之间老年初治患者维持治疗中的疗效,经6~8 个周期R-CHOP治疗获得CR 或PR 的DLBCL 患者,来那度胺维持治疗组比较安慰剂组具有明显的PFS 获益(HR=0.708;P=0.0135)[20]。L-MIND 研究[21]评估了tafasitamab 联合来那度胺治疗R/R DLBCL 患者的疗效,在经过≥35 个月的随访后,ORR 为57.5%,CRR 为40.0%,中位OS 为33.5 个月,中位缓解持续时间为43.9 个月。来那度胺单药治疗R/R DLBCL 的ORR约为20%,无论前期是否行自体造血干细胞移植,来那度胺可以作为挽救治疗方法之一,且在non-GCB亚型中获益更显著[22]。R2 方案用于R/R DLBCL 的ORR 约为33%,中位PFS 及OS 分别为3.7 个月和10.7 个月[23]。来那度胺联合或不联合利妥昔单抗方案在R/R 原发中枢神经系统淋巴瘤(primary central nervous system lymphoma,PCNSL)中也具有一定活性,R2 方案治疗的最佳ORR 为67%[24]。R2 联合甲氨蝶呤、替莫唑胺方案治疗初治PCNSL 患者,CRR 79%,2 年PFS、OS 分别达62%和67%[25]。
具有某些不良预后特征的DLBCL 患者可能从来那度胺联合治疗方案中获益,但仍需要进一步证实。E1412 研究入组Ⅱ期伴大肿块、进展期、IPI 评分≥2 分、ECOG 评分≤2 分的初治DLBCL 患者,无论细胞起源分型,来那度胺联合R-CHOP(R2-CHOP)比较R-CHOP 方案,中位随访3 年,R2-CHOP 减少34%的进展和死亡风险,3 年PFS 分别为73%和61%(P=0.03),3 年OS 率分别为83%和75%(P=0.05)[26]。ROBUST 研究入组初治ABC 亚型DLBCL 患者,比较R2-CHOP 和R-CHOP 方案的疗效,所有意向人群中未达到主要研究终点PFS 获益,但在Ⅲ/Ⅳ期和IPI≥3 分患者中观察到R2-CHOP 延长PFS 的积极趋势[27]。分子机制研究发现non-GCB DLBCL 患者伴PIM1、SPEN、MYD88 等基因突变和NF-kB、JAK-STAT 等炎症信号通路激活对R2-CHOP 方案具有更大的获益[28]。利妥昔单抗、来那度胺、伊布替尼(RLI)联合CHOP 方案治疗初治non-GCB DLBCL 患者,结果显示CRR 为94.5%,中位随访31 个月,2 年PFS 和OS率分别为91.3%和96.6%[29]。R2 方案治疗老年虚弱的初治DLBCL 患者,ORR 为50.8%,CRR 为27.7%,中位随访24 个月,中位PFS 为14 个月[30]。伊布替尼联合来那度胺联合利妥昔单抗(iR2)治疗R/R non-GCB DLBCL 患者,ORR 为49%,CRR 为28%[31]。
因此,共识推荐来那度胺单药可以作为老年初治DLBCL 诱导治疗后获得客观缓解患者的维持治疗,来那度胺联合R-CHOP 方案可以作为伴特殊不良预后特征DLBCL 患者的治疗选择。来那度胺联合或不联合抗CD20 单抗可用于不可耐受化疗的R/R non-GCB DLBCL 患者,以及不可耐受高强度化疗或化疗耐药的PCNSL 患者。此外,tafasitamab 联合来那度胺可用于不宜行移植的R/R DLBCL 患者。
2.5 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤
慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(chronic lymphocytic leukemia/small lymphocytic lymphoma,CLL/SLL)是一种常见的惰性 B 细胞克隆性增殖性疾病,临床表现主要为外周血淋巴细胞增多、肝脾及淋巴结肿大和骨髓受累[32]。具有系统治疗指征患者的首选治疗方案是抗 CD20 单抗联合化疗和(或)BTK 抑制剂。有研究显示,来那度胺联合利妥昔单抗治疗R/R CLL/SLL 患者的 ORR 为 66%,CRR 为 12%,中位治疗失败时间 17.4 个月,36 个月的生存率 71%[33]。来那度胺治疗 R/R CLL 患者结合细胞遗传学和基因突变特征的疗效分析显示,有 del(17p)的患者 ORR低于无 del(17p)的患者(21.7%:47.1%,P=0.049),来那度胺对于具有不良遗传特征(包括 TP53 突变或 IGHV 未突变)的 R/R CLL 仍然有效[34]。因此,共识推荐来那度胺联合或不联合 CD20 单抗方案可以用于 R/R CLL/SLL 患者的治疗,尤其适用于不可耐受免疫化疗和 BTK 抑制剂治疗或上述治疗耐药的患者。
2.6 外周T 细胞淋巴瘤
外周T 细胞淋巴瘤(peripheral T-cell lymphoma,PTCL)是一组来源于成熟T 细胞的淋巴瘤,占所有非霍奇金淋巴瘤的5%~15%,临床表现以淋巴结肿大为主,也常出现结外受累,多具有高度侵袭性,疾病进展迅速,总体预后较差[35],CHOP 方案为基础的联合化疗仍是初治PTCL 患者的首选治疗方案。维布妥昔单抗(抗CD30 抗体偶联药)显著提高CD30 阳性PTCL 患者的疗效,尤其是间变大细胞淋巴瘤。来那度胺在PTCL 患者中具有一定活性。来那度胺单药治疗PTCL 的ORR 为26%,中位OS 为12 个月,中位PFS 为4 个月[36]。有研究显示来那度胺在血管免疫母细胞T 细胞淋巴瘤中反应较佳,ORR 为31%[37]。因此,共识推荐来那度胺单药可以作为以姑息治疗为目的PTCL 患者的治疗选择,初始治疗时需要关注燃瘤反应。
2.7 霍奇金淋巴瘤
霍奇金淋巴瘤(Hodgkin lymphoma,HL)是来源于生发中心B 细胞的侵袭性淋巴瘤,约占淋巴瘤的10%,临床表现多以淋巴结肿大为首发症状,晚期可累及肝脾、骨髓、消化道等[38]。多药联合化疗和放射治疗的综合治疗仍是HL 的首选治疗。维布妥昔单抗(抗CD30 抗体偶联药)和免疫检查点抑制剂(抗PD-1/PD-L1 单抗)进一步提高了HL 患者的疗效。来那度胺在HL 患者中具有一定活性,来那度胺单药治疗R/R HL 的ORR 为19%[39]。因此,共识推荐来那度胺单药可以作为以姑息治疗为目的HL 患者三线以上的治疗选择。
3 来那度胺应用方法及注意事项
3.1 用药方法
来那度胺推荐每日在基本相同的时间点服用,不应打开、破坏和咀嚼胶囊,最好用水完整送服,可与食物同服,也可空腹服用。若错过服药时间<12 h,可补服该次用药。若错过服药时间>12 h,不再补服该次用药,推荐在第2 天的正常服药时间点服用,不要因漏服同时服用2 日的剂量。
来那度胺在不同方案中用法用量不同,具体剂量还需要根据白细胞计数、肾脏功能、年龄等因素综合判断。来那度胺治疗推荐方案的用法用量总结,见表2。
3.2 不良反应剂量调整和特殊人群用药
3.2.1 不良反应剂量调整 来那度胺治疗相关的不良反应中血液学不良反应(中性粒细胞减少和血小板减少)最常见,其次为静脉血栓栓塞症(当与地塞米松联合使用时),其他常见不良反应包括皮疹、疲劳、腹泻、便秘、恶心、肌肉痉挛等。来那度胺治疗相关的不良反应多发生在早期而较少出现累积不良反应[40]。建议出现3 级或4 级来那度胺相关不良反应时,对剂量进行调整,见表3。

表3 来那度胺剂量调整推荐
血液学不良反应的处理和剂量调整:1)血小板计数首次降至<50×109/L,暂停来那度胺治疗,至少7 天检查1 次全血细胞计数,待血小板计数恢复至≥50×109/L,按低一级剂量水平重新治疗,若后续再次下降至<50×109/L,暂停来那度胺治疗,至少7 天检查1 次全血细胞计数,待血小板恢复至≥50×109/L,按更低一级剂量水平(剂量水平-2、剂量水平-3)重新治疗,不得低于剂量水平-3;2)中性粒细胞计数首次降至<1.0×109/L 至少7 天或降至<1.0×109/L 伴发热(体温≥38.5℃)或降至<0.5×109/L,暂停来那度胺治疗,至少7 天检查1 次全血细胞计数,待中性粒细胞恢复至≥1.0×109/L,按低一级剂量水平(剂量水平-1)重新治疗,若后续再次下降至<1.0×109/L 至少7 天或降至<1.0×109/L 伴发热(体温≥38.5℃)或降至<0.5×109/L,暂停来那度胺治疗,至少7 天检查1 次全血细胞计数,待中性粒细胞恢复至≥1.0×109/L,按更低一级剂量水平(剂量水平-2、剂量水平-3)重新治疗,不得低于剂量水平-3。
非血液学不良反应的处理和剂量调整:对于被判断为与来那度胺治疗有关的3 级或4 级不良反应,应停止治疗,当不良反应消退至2 级,可以考虑按低一级剂量水平重新开始治疗,或终止治疗。
3.2.2 特殊人群用药 来那度胺主要通过肾脏排泄,严重肾功能不全的患者可能无法耐受治疗。因此,肾功能不全的患者在选择来那度胺治疗时,应根据肌酐清除率(creatinine clearance rate,CLcr)谨慎调整起始剂量,并在治疗期间对肾功能进行持续监测,见表4。

表4 肾功能不全患者起始剂量推荐
3.3 注意事项
3.3.1 皮疹 既往使用沙利度胺时曾发生过4 级皮疹的患者应避免使用。发生1 级皮疹时,可局部外用糖皮质激素或口服抗组胺药物治疗直至痊愈。2 级及以上的皮疹,暂停来那度胺给药,待不良反应降为1 级,可考虑重新开始用药。若出现血管性水肿、4 级皮疹、剥脱性或大疱性皮疹,或怀疑出现Stevens-Johnson 综合征、中毒性表皮坏死松解症或药物反应伴嗜酸粒细胞增多和全身性症状,则必须立即停止来那度胺用药,不良反应降为1 级后也不建议重新开始用药[41]。
3.3.2 肿瘤溶解综合征 接受来那度胺治疗的患者应考虑预防肿瘤溶解综合征(tumor lysis syndrome,TLS)的发生。TLS 临床表现为恶心、呕吐、呼吸短促、心律不齐、少尿、意识障碍、关节不适等,实验室检查表现为高钾、高尿酸、高磷、低钙、高乳酸脱氢酶。TLS 预防治疗包括水化、碱化和别嘌醇或非布司他治疗预防尿酸升高,定期检测离子、肾功能等生化指标。
3.3.3 燃瘤反应 接受来那度胺治疗尤其是伴高肿瘤负荷的患者,推荐给予糖皮质激素预防燃瘤反应(tumor flare reaction,TFR),如强的松20 mg 口服5~7 天,在随后的5~7 天中逐渐减量停药。尤其是PTCL 和CLL/SLL 患者,建议从低剂量开始应用,逐渐增加来那度胺的剂量。TFR 的临床表现为用药后发生疼痛性淋巴结肿大、淋巴结肿大伴局部炎症、骨痛,也可以发生脾脏肿大、低热和(或)皮疹,治疗方法建议糖皮质激素治疗,如强的松25~50 mg 口服5~10 天;抗组胺药治疗皮疹或瘙痒,如氯雷他定10 mg口服,每日1 次。
3.3.4 血栓 接受来那度胺治疗的患者推荐预防血栓事件发生,建议在血小板>50×109/L 情况下给予肠溶阿司匹林口服100 mg,每日1 次;已经行其他药物抗凝治疗的患者,无需再给予阿司匹林。
4 结语
本共识基于前瞻性临床研究及真实世界的数据,对临床如何规范合理应用来那度胺治疗淋巴瘤患者提出共识推荐,供临床医生参考。随着淋巴瘤新药研发成功应用于临床,需要不断探索来那度胺为基础的新的联合方案,总结不良反应监测及防治措施的经验,从而逐步提高来那度胺在淋巴瘤中的应用价值。
共识编写专家委员会
专家组组长:
张清媛 哈尔滨医科大学附属肿瘤医院
石远凯 中国医学科学院肿瘤医院
冯继锋 江苏省肿瘤医院
专家组成员(按姓氏拼音顺序排列):
白鸥 吉林大学白求恩第一医院
曹军宁 复旦大学附属肿瘤医院
高玉环 河北医科大学第四医院
顾康生 安徽医科大学第一附属医院
胡建达 福建医科大学附属协和医院
黄慧强 中山大学肿瘤防治中心
景红梅 北京大学第三医院
李小秋 复旦大学附属肿瘤医院
李文瑜 广东省人民医院
李晓玲 辽宁省肿瘤医院
李玉富 郑州大学附属肿瘤医院/河南省肿瘤医院
李志铭 中山大学肿瘤防治中心
刘鹏 中国医学科学院肿瘤医院
秦燕 中国医学科学院肿瘤医院
双跃荣 江西省肿瘤医院
宋永平 郑州大学第一附属医院
苏丽萍 山西省肿瘤医院
孙秀华 大连医科大学附属第二医院
王华庆 南开大学天津人民医院
王欣 山东省立医院
王昭 首都医科大学附属北京友谊医院
吴剑秋 江苏省肿瘤医院
吴辉菁 湖北省肿瘤医院
伍钢 华中科技大学同济医学院附属协和医院
邢晓静 辽宁省肿瘤医院
徐兵 厦门大学附属第一医院
姚志华 郑州大学附属肿瘤医院/河南省肿瘤医院
周辉 湖南省肿瘤医院
周生余 中国医学科学院肿瘤医院
邹德慧 中国医学科学院血液病医院
邹立群 四川大学华西医院
赵文辉 哈尔滨医科大学附属肿瘤医院
张明智 郑州大学第一附属医院
执笔人:
刘艳艳 郑州大学附属肿瘤医院/河南省肿瘤医院
张会来 天津医科大学肿瘤医院
李兰芳 天津医科大学肿瘤医院
赵曙 哈尔滨医科大学附属肿瘤医院
本文无影响其科学性与可信度的经济利益冲突。

