高通量血液透析联合血液透析滤过对终末期肾病患者尿毒症毒素与炎症因子水平的影响
田津生,张怡静
天津市中医药研究院附属医院 (天津 300120)
终末期肾病即慢性肾脏病进入终末期阶段,患者预后差,随着病情不断进展,肾功能持续降低,患者体内尿毒症毒素大量聚集并引发水肿、恶心、皮肤瘙痒及呕吐等症状,导致病情加重,增加治疗难度[1]。高通量血液透析是临床治疗终末期肾病的重要措施,其通透性良好,可有效清除大分子毒素,但对蛋白结合类毒素产生的清除效果有限,还需联合其他类型血液透析技术展开治疗[2]。血液透析滤过所用滤过膜具有高通透性,可有效滤出血液中的毒素,再输入同等量的置换液,达到治疗目的[3]。基于此,本研究旨在探讨高通量血液透析联合血液透析滤过在终末期肾病患者中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2020 年1 月至2022 年12 月我院收治的70例终末期肾病患者,根据随机数字表法进行分组,每组35 例。试验组男22 例,女13 例;年龄41~74 岁,平均(55.80±4.72)岁;原发疾病:糖尿病肾病6 例,肾小球肾炎14 例,高血压肾病11 例,其他4 例;病程1~7 年,平均(3.08±0.40)年。对照组男20 例,女15 例;年龄42~72 岁,平均(55.63±4.90)岁;原发疾病:糖尿病肾病5 例,肾小球肾炎17 例,高血压肾病10 例,其他3 例;病程1~7 年,平均(3.02±0.41)年。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。所有入选患者均了解本研究内容。
纳入标准:符合《肾脏病学》[4]中终末期肾病的相关诊断标准;肾小球滤过率(esti mated glomerular filtration rate,eGFR)<15 ml(min·1.73 m2);年龄18~75 岁;入组前30 d 未开展会对本研究产生影响的相关治疗;预计生存期>6 个月;患者自愿参与研究且已签署知情同意书。排除标准:并发活动性出血;存在感染性疾病;患有恶性肿瘤;合并严重肝功能异常;存在精神障碍。
1.2 方法
对照组采用费森尤斯4008S 透析机与费森尤斯FX60 聚砜膜透析器进行高通量血液透析治疗,参数设置为:面积1.4 m2,超滤系数46 ml/(h·mmHg),血流量200~350 ml/min,透析液流速设置500 ml/min,温度36~37 ℃。4 h/次,3 次/周。
试验组采取高通量血液透析联合血液透析滤过治疗。高通量血液透析每2 周5 次,操作方法同对照组。血液透析滤过通过费森尤斯FX600 血滤器进行,参数设置为:血流速度270 ml/min,透析液流速500 ml/min,采取后置换形式,置换量20 L,4h/次,每2 周1 次。。
两组均治疗6 个月。
1.3 观察指标
(1)临床疗效:以《临床疾病诊断依据治愈好转标准》[5]为依据拟定标准,评价两组疗效。治疗后,患者的高脂血症、高磷血症及高尿酸血症等均显著缓解,且血肌酐(serum creatinine,SCr)水平降低幅度超过25%,即显效;治疗后,患者的高脂血症、高磷血症及高尿酸血症等均缓解,且10%≤SCr 水平降低≤25%,即有效;治疗后,患者的高脂血症、高磷血症及高尿酸血症等均无变化,甚至加重,且SCr水平降低不足10%,即无效。治疗总有效率=(显效例数+有效例数)/总例数×100%。(2)尿毒症毒素:治疗前后,收集患者早晨空腹肘静脉血3 ml,离心(3 000r/min,10 min)后检测两组血β2微球蛋白(β2-microglobulin,β2-MG)、甲状旁腺激素(parathyroid hormone,PTH)、半胱氨酸蛋白酶抑制剂C(cystatin C)水平。(3)炎症因子水平:治疗前后,收集患者早晨空腹肘静脉血3 ml,离心(3 000r/min,10 min)后后检测两组超敏-C 反应蛋白(high-sensitivity C-reactive protein,hs-CRP)水平。(4)肾功能水平:治疗前后,收集患者早晨空腹肘静脉血3ml,离心(3 000r/min,5 min)后测定两组肾功能水平,包括eGFR、SCr 与尿素氮(blood urea nitrogen,BUN)。
1.4 统计学处理
采用SPSS 20.0 统计软件对数据进行处理。计量资料以±s 表示,采用t检验。计数资料以率表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
试验组治疗总有效率高于对照组,差异具有统计学意义(P<0.05),见表1。
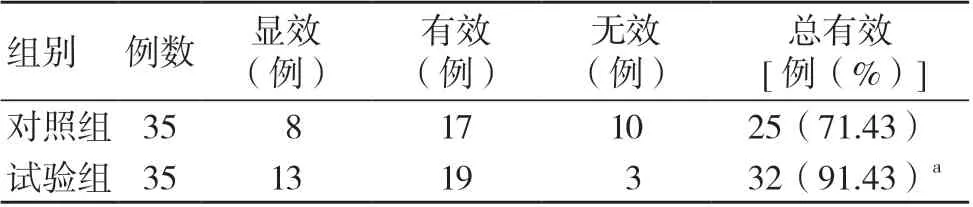
表1 两组临床疗效比较
2.2 两组尿毒症毒素水平比较
治疗前后,两组β2-MG、PTH、Cystatin C 水平低于治疗前,且试验组低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组尿毒症毒素水平比较(±s)

表2 两组尿毒症毒素水平比较(±s)
注:与同组治疗前对比,aP<0.05;β2-MG 为血β2 微球蛋白,PTH 为甲状旁腺激素,Cystatin C 为半胱氨酸蛋白酶抑制剂C
组别例数β2-MG(mg/L)PTH(pg/ml)治疗前治疗后治疗前治疗月后对照组 35 19.44±2.09 10.85±1.38a 686.96±60.15 491.15±44.73a试验组 35 19.52±2.01 9.41±1.22a 687.05±60.03 435.09±40.07a t 0.163 4.6250.006 5.523 P 0.871<0.0010.995<0.001组别例数Cystatin C(mmol/L)治疗前治疗后对照组 355.31±0.652.92±0.51a试验组 355.49±0.602.51±0.46a t 1.2043.532 P 0.2330.001
2.3 两组炎症因子水平比较
治疗后,两组hs-CRP 均低于治疗前,试验组低于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组炎症因子水平对比 (±s)

表3 两组炎症因子水平对比 (±s)
注:与治疗前对比,aP<0.05;hs-CRP 为超敏-C 反应蛋白
组别例数hs-CRP 水平(mg/L)治疗前治疗后对照组3515.41±1.2212.53±2.26a试验组3515.49±1.207.36±1.22a t 0.27711.909 P 0.783<0.001
2.4 两组肾功能水平比较
治疗前,两组各项肾功能指标比较,差异无统计学意义(P>0.05);治疗后,两组eGFR 水平高于治疗前,且试验组高于对照组,SCr 与BUN水平低于治疗前,且试验组低于对照组,差异有统计学意义(P<0.05),见表4。
表4 两组肾功能水平比较(±s)

表4 两组肾功能水平比较(±s)
注:与同组治疗前对比,aP<0.05;eGFR 为肾小球滤过率,SCr 为血肌酐,BUN 为尿素氮
组别例数 eGFR(ml/min·1.73 m2)SCr(μmol/L)治疗前治疗后治疗前治疗后对照组 35 13.53±1.13 17.51±1.66a 808.96±147.51 361.15±66.21a试验组 35 13.59±1.02 19.76±1.59a 809.08±146.88 301.15±59.70a t 0.233 5.7910.003 3.982 P 0.816<0.0010.997<0.001组别例数BUN(mmol/L)治疗前治疗后对照组 3526.47±3.629.19±1.96a试验组 3526.55±3.516.38±1.80a t 0.094 6.247 P 0.925<0.001
3 讨论
近年来,终末期肾病发病率逐年升高,已成为影响人们健康、加重社会经济负担的主要疾病[6]。对于终末期肾病患者,临床多以肾脏替代疗法展开治疗,可有效清除患者体内的代谢毒素,抑制病理性因子大量蓄积对组织器官造成损伤,调节水电解质的平衡[7]。高通量血液透析为一种临床常见的肾脏替代疗法,通透性良好,可使较大分子毒素顺利进入透析液,但单一治疗效果有待提高[8]。因此,研究适宜的联合治疗方案成为临床研究重点。
本研究结果显示,试验组总有效率高于对照组(P<0.05),提示高通量血液透析联合血液透析滤过治疗终末期肾病患者的临床疗效较好。β2-MG、PTH、Cystatin C 属于大中分子毒素的重要标记物,可直接穿过肾小球,并可在机体中大量聚集,致使器官组织发生淀粉样改变,影响患者疗效及预后[9]。本研究结果显示,试验组β2-MG、PTH、Cystatin C水平低于对照组(P<0.05),提示高通量血液透析联合血液透析滤过可提高终末期肾病患者的尿毒症毒素清除效果。高通量血液透析所用滤器的超滤系数大于20 ml/(h·mmHg),具有较强的水力学通透性及扩散性,同时其疏水性、亲水性可维持平衡状态,有效改善血液及膜间的相容性,通过对流原理、弥散原理可有效清除患者血液大中分子毒素,达到净化血液的目的[10]。血液透析滤过技术集血液透析方案及血液滤过方案于一体,合理应用高通透性透析滤过膜,可同时发挥溶质弥散功效与对流作用。其中弥散作用能够充分清除小分子毒素,而对流作用则可有效清除中分子毒素,维持血流动力学稳定。以高通量血液透析联合血液透析滤过进行治疗,2 种方案可优势互补,增强大中分子毒素的清除效果,提高血液净化效果,改善患者预后[11]。hs-CRP 水平属于临床常见的炎症因子指标,正常情况下处于低表达状态,受肾功能受损、免疫功能障碍等因素的影响,hs-CRP 在终末期肾病患者中的表达异常升高,且与患者病情程度呈正相关[12]。本研究结果显示,治疗后,试验组血清hs-CRP 水平均低于对照组,eGFR 水平高于对照组,而SCr 与BUN 水平则低于对照组(P<0.05),表明高通量血液透析联合血液透析滤过可下调终末期肾病患者的炎症因子水平,改善肾功能指标。高通量血液透析治疗时,透析器内高分子聚合膜孔的通透性较强,同时膜的生物相容性偏高,能有效清除炎症因子、葡萄糖与胰岛素等物质,改善血管功能障碍程度与细胞毒性的损伤程度[13]。同时,高通量透析膜具有高通透性与高扩散性等特点,借助高通量血液滤器可合理控制透析容量,发挥溶质转运功能,转运血液内的大分子物质,有效分离、清除毒素,降低血清β2-MG 与PTH 水平,抑制毒素累积,同时生成无致热源、无菌置换液,并补充到患者身体中,抑制炎症反应,降低炎症因子水平。血液透析滤过技术通过模拟肾小球的过滤重吸收功能,可清除患者血液内多余水分与溶质,以置换液弥补肾小管部分功能。且可有效清除中大分子物质,通过充分清除尿毒症毒素,防止炎症因子被激活。高通量合成膜可增加透析液流量与对流量,清除血液内代谢废物、有毒物质,改善患者血流动力学指标与耐受性,安全性高[14]。高通量血液透析联合血液透析滤过通过促进患者透析期间生物相容性及增强血流动力学稳定性,缓解机体炎症反应及生物活性反应,加快血液内尿毒症毒素的清除速度,并可补充物质热源及无菌置换液,防止炎性细胞因子被大量激活,改善肾功能[15];此外,充分滤出血液内毒素体液的同时,将同等剂量的置换液输入患者体内,可增强超滤量,有效清除机体中的多余水分、代谢废物,缓解肾脏压力,改善患者肾功能水平。但本研究仍有不足,如终末期肾病患者的病例存在选择性偏倚、样本量与观察指标较少、观察时间短、未随访远期预后情况,后期仍需开展进一步研究,以验证研究结论的准确性。
综上所述,高通量血液透析联合血液透析滤过治疗终末期肾病患者的效果显著,可增强尿毒症毒素清除效果,降低炎症因子水平,改善肾功能指标。

