生活饮用水中乙二胺四乙酸和次氮基三乙酸含量测定
王雪婷 郑 斌
乙二胺四乙酸(EDTA)是一种重要的络合剂,被广泛应用于生活中的各方面[1-5]。次氮基三乙酸又称氨三乙酸、氮川三乙酸,能与各种金属离子形成络合物。乙二胺四乙酸二钠生产过程中排出的废水中含有少量的EDTA、次氮基三乙酸(NTA)、羟基乙酸及甲酸等有机杂质,会造成水污染[6],其中,EDTA在环境中难以被生物降解,会对黏膜、上呼吸道、眼睛及皮肤产生刺激作用[7];NTA进入人体会有诱发癌症的风险,且NTA及其钠盐对胎儿有致畸性[8]。长期饮用含EDTA、NTA的水可能会对人体健康产生不良影响[9]。
目前,EDTA的检测方法主要有滴定法、气相色谱法、离子色谱法、高效液相色谱法和液相色谱—三重四极杆串联质谱法等[10-12]。滴定法无法对两种物质进行同时测定,很难将EDTA络合物与其他络合物分开,误差大、操作繁琐,而且还需要基准物质进行标定;气相色谱法则需要对NTA进行酯化使其具备挥发性后方可进行测定,处理过程比较复杂,且衍生效率会影响分析的准确度,检出限达不到要求;采用离子色谱法分析NTA简单易行,主要是由于NTA易溶于水,且以离子形式存在于水溶液中,但目前未见离子色谱法同时测定饮用水中EDTA和NTA的相关研究,且离子色谱柱的价格昂贵;而液相色谱—三重四极杆串联质谱法的测定成本较高。液相色谱法是目前检测食品中EDTA含量最多的方法,但有关NTA的检测研究却较少[13-15]。试验拟针对水中EDTA和NTA的检测方法进行研究,以期为生活用水的检测提供依据。
1 材料与方法
1.1 材料与设备
水样:市售矿泉水;
液相色谱仪:U3000型,配DAD检测器,赛默飞世尔科技(中国)有限公司;
电子天平:BSA02S型,赛多利斯科学仪器(北京)有限公司;
离心机:H2050R型,长沙高新技术产业开发区湘仪离心机仪器有限公司;
涡旋振荡器:MS3型,德国艾卡公司;
超声波清洗机:KQ-800DE型,昆山市超声仪器有限公司;
pH计:PB-10型,精度为0.01,赛多利斯科学仪器(北京)有限公司;
色谱柱:Thermo-C18(4.6 mm×250 mm),赛默飞世尔科技(中国)有限公司。
1.2 试剂
配制溶液用水:GB/T 6682规定的二级水;
乙二胺四乙酸(EDTA)、次氮基三乙酸(NTA):上海安谱科技股份有限公司;
甲醇:色谱纯,上海安谱科技股份有限公司;
盐酸、磷酸(H3PO4):优级纯,国药集团化学试剂有限公司;
甲酸:色谱纯,国药集团化学试剂有限公司;
四丁基溴化铵、乙酸钠、三氯化铁:分析纯,国药集团化学试剂有限公司。
1.3 试验方法
1.3.1 溶液配制
(1) 10 mmol/L三氯化铁溶液:称取0.165 5 g三氯化铁溶于90 mL水中,加入1.0 mL盐酸,转移至100 mL容量瓶中,用水定容,混匀,该溶液可保存6个月。
(2) 0.22 mmol/L三氯化铁溶液:吸取220 μL浓度为10 mmol/L的三氯化铁溶液于10 mL容量瓶中,加水定容,摇匀,现配现用。
(3) 磷酸缓冲溶液(pH 2.5):称取6.071 g一水合磷酸二氢钠于100 mL容量瓶中,加水超声溶解,定容,用少量磷酸溶液(50%)调节pH值至2.5。
(4) 流动相B:称取3.04 g一水合磷酸二氢钠和0.65 g四丁基溴化铵于1 000 mL容量瓶中,加900 mL水超声溶解,加入1.0 mL浓度为10 mmol/L的三氯化铁溶液,定容,用少量磷酸调节pH值至2.5。
1.3.2 标准溶液的配制
(1) EDTA和NTA标准储备液:分别称取约10 mg的EDTA和NTA标准品,用水溶解并定容至10 mL棕色容量瓶中,得质量浓度为1 000 mg/L的标准储备溶液,转移至储液瓶中,4 ℃贮藏备用。
(2) EDTA和NTA标准溶液:分别吸取100 μL EDTA和NTA标准储备液于10 mL容量瓶,制备质量浓度为10 mg/L的混合标准中间溶液,将标准中间溶液稀释,配制成质量浓度为0.1,0.2,0.4,0.8,1.0,2.0 mg/L的系列标准工作溶液。
1.3.3 试样处理 取1.0 mL水样于1.5 mL棕色进样小瓶中,加50 μL浓度为0.22 mmol/L三氯化铁溶液和50 μL磷酸缓冲溶液,涡旋混匀,静止放置衍生2 h,过0.22 μm水相滤膜后上液相色谱测定。以空白水样品进行空白试验。
1.3.4 仪器参数及测定条件 色谱条件:色谱柱为Thermo-C18(250 mm×4.6 mm);检测器波长258 nm;柱温30 ℃;流速1.0 mL/min;进样量100 μL;流动相A为甲醇,流动相B为0.2 mmol/L四丁基溴化铵—磷酸缓冲溶液(pH 2.5);梯度洗脱程序:0~2.00 min,90% B;2.00~5.00 min,60% B;5.00~7.00 min,20% B;7.00~10.10 min,90% B;10.10~12.00 min,90% B。
1.3.5 方法学考察 分别取质量浓度为0.1,0.2,0.4,0.8,1.0,2.0 mg/L的系列标准工作溶液1.0 mL,加入50 μL浓度为0.22 mmol/L的氯化铁溶液和50 μL磷酸缓冲溶液,涡旋混匀,静止放置2 h后上液相色谱测定。采用外标法定量,以待测物化合物浓度为横坐标,待测物化合物峰面积为纵坐标,绘制标准曲线和计算线性方程,考察EDTA和NTA的线性关系。EDTA和NTA的加标水平均为0.1,0.4,1.0 mg/L,每个水平重复6次,对方法的回收率、重复性和精密度进行考察。
1.3.6 数据分析 通过对方法学的考察,对生活饮用水中EDTA和NTA的含量进行数据分析。
2 结果与分析
2.1 衍生试剂的选择
Wang等[16]研究发现,EDTA与金属离子形成螯合物的条件稳定常数顺序为Mo6+>Bi3+>Fe3+>Cu2+>Zn2+>Al3+>Fe2+>Mn2+>K+>Ca2+>Mg2+,而NTA与金属离子形成螯合物的条件稳定常数顺序为Fe3+>Hg2+>Cu2+>Al3+>Zn2+>Co2+>Mn2+>Ca2+>Mg2+,相比之下,Fe3+与EDTA、NTA更容易形成络合物;魏峰等[17]研究发现,EDTA、NTA可以与多种金属离子形成稳定的络合物,所形成的络合物可以发生配位场跃迁,紫外吸收强度增大且吸收范围发生红移,因而可以提高检测的灵敏度,达到检测所需检出限要求,与其他金属离子相比,Fe3+形成的螯合物比较稳定,与GB 5009.287—2016中使用的衍生试剂一致。因此,试验选择三氯化铁与EDTA、NTA络合。由于高浓度的三氯化铁溶液络合后产生的杂峰响应高,经试验优化后选择0.22 mmol/L三氯化铁溶液作为衍生试剂。为减小溶剂效应,在加入衍生试剂时加入流动相中使用的磷酸盐缓冲液,可以提升检测物质的灵敏度。
2.2 仪器参数与测定条件
2.2.1 色谱柱的选择 选用Athena HILIC、Thermo-C18两种色谱柱进行测试。由图1可知,Athena HILIC得到的色谱峰型较差,而Thermo-C18对EDTA和NTA均有较好的分离效果,且色谱峰型良好。因此,选择Thermo-C18作为分离色谱柱。

图1 EDTA和NTA的液相色谱分离图
2.2.2 流动相优化 试验发现,未使用离子对试剂,只采用甲醇和水作为流动相时,通过液相色谱仪分析得到的峰形较差且响应较低,可能是目标物在该条件下的稳定性差,与色谱柱填料间的作用力加大而难以洗脱,因此无法对EDTA、NTA进行直接检测。GB 5009.278—2016中使用的流动相为四丁基溴化铵—乙酸钠溶液(V四丁基溴化铵∶V乙酸钠为85∶15),等度洗脱分离,适用EDTA一种物质的分离。而NTA是生产EDTA过程中的杂质,二者性质相似,更不易分离。故试验采用梯度程序进行洗脱分离,由于高浓度四丁基溴化铵溶液会导致液相色谱系统污染几率增加且不易清洗,因此,选择四丁基溴化铵—磷酸缓冲溶液浓度为0.2 mmol/L,并用磷酸调节pH值至2.5,此条件下,两种目标物的分离度较好。
2.2.3 波长的选择 EDTA和NTA在波长为210 nm以上的紫外吸收能力较弱,不能满足低含量检测的需要。由图2可知,EDTA和NTA络合物的最大吸收波长分别为260,248 nm,综合考虑选取λ=258 nm作为二者的检测波长,此时均能得到理想的色谱图。
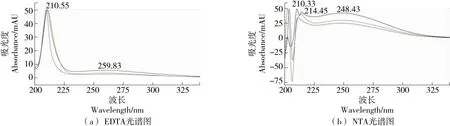
图2 EDTA和NTA光谱图
2.2.4 EDTA和NTA含量
(1) 线性方程:试验表明,EDTA和NTA在0.1~2.0 mg/L的质量浓度范围内线性良好,线性方程分别为Y=2.658 5X-0.057,Y=2.664X-0.183,相关系数分别为0.999 5,0.999 2,符合GB/T 27404—2008中对相关系数的要求。
(2) 回收率、重复性和精密度:由表1可知,水样中NTA的相对标准偏差为3.63%~5.71%,平均回收率为97.5%~109.2%;EDTA的相对标准偏差为4.79%~7.39%,平均回收率为99.4%~111.4%,两种物质的平行测定绝对差值未超过平均值的10%,说明试验方法具有良好的准确度和精密度,可满足GB/T 27404—2008中对化合物回收率、重复性及精密度试验的要求。

表1 EDTA和NTA的回收率及精密度
空白水样和加标水样的液相色谱如图3所示。该方法前处理加入衍生试剂,为避免试剂引入目标物,确保检测结果的准确性,同时检测空白水样。空白水样中的含量较低,定量后EDTA和NTA含量<0.001 mg/L,可忽略不计。当添加水平为1.0 mg/L时,EDTA和NTA依次出峰,峰形完整,分离效果较好,定量结果准确。

图3 空白水样和加标水样的液相色谱图
(3) 检出限和定量限:通过不断稀释标准样品溶液,得到次氮基三乙酸、乙二胺四乙酸的检出限为0.05 mg/L,定量限为0.1 mg/L,信噪比均>10,满足定量要求。
3 结论
研究建立了一种生活饮用水中乙二胺四乙酸和次氮基三乙酸的高效液相色谱测定方法。结果表明,乙二胺四乙酸和次氮基三乙酸在0.1~2.0 mg/L的质量浓度范围内与色谱峰面积线性关系良好,相关系数分别为0.999 5,0.999 2;两者的检出限为0.05 mg/L,定量限为0.1 mg/L,加标回收率>90%。该方法具有操作简便、重复性好、灵敏度高的特点。后续可以增加对生活废水中乙二胺四乙酸和次氮基三乙酸含量的检测;亦可尝试使用质谱联用仪进行试验以进一步提高检测灵敏度。

