茯苓甘草合剂辅助西药对慢性阻塞性肺疾病合并肌肉衰减患者NF-κB信号通路的影响
梁晔 庄洁 房晓华 张积友
肌肉衰减是慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)常见并发症,可引发活动能力减退、骨质疏松、残疾等不良事件,严重影响患者生活质量[1-2]。另有研究指出,肌肉衰减与COPD患者死亡率密切相关[3]。因此,临床应对COPD合并肌肉衰减给予足够重视。既往研究指出,机体炎症状态与骨骼肌消耗密切相关,炎性因子可加速蛋白质分解,促进骨骼肌消耗,引发肌肉衰减[4]。NF-κB作为调节炎性通路中最重要的转录因子,在肺组织及骨骼肌细胞均有表达,其磷酸化激活,可导致炎性因子过度分泌[5]。既往研究显示茯苓多糖、甘草酸可抑制NF-κB[6-7]。本研究探明茯苓甘草合剂对患者干预作用及机制,为临床治疗COPD合并肌肉衰减提供可能思路。
1 资料与方法
1.1 一般资料 本研究经山东青岛中西医结合医院伦理委员会审核批准,选取2020年8月至2022年8月我院104例COPD合并肌肉衰减患者,随机数字表法分为观察组和对照组,每组52例。2组性别比、年龄、病程、COPD严重程度、吸烟史、体重指数(BMI)等一般资料差异无统计学意义(P>0.05)。见表1。
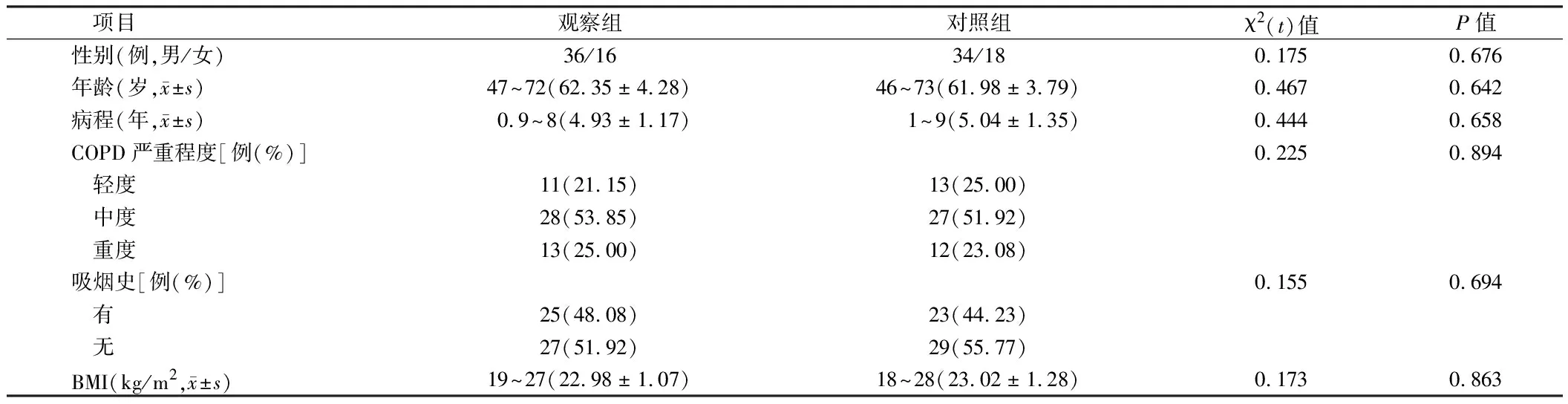
表1 2组一般资料比较 n=52
1.2 诊断、纳入与排除标准
1.2.1 诊断标准:①西医符合《慢性阻塞性肺疾病基层诊疗指南(2018年)》[8]中COPD诊断标准,符合亚洲老年肌肉减少症工作组肌肉减少症诊断标准[9];②中医符合《中医病证诊断疗效标准》[10]中脾胃虚弱型肌少症相关诊断标准,主症:乏力、肌肉萎缩、步履缓慢,次症:食欲不振、面白无华、畏寒肢冷、便溏、心悸气短,舌脉:舌质淡,脉细弱无力。符合任一主症加两项以上次症,结合舌脉象即可确诊。
1.2.2 纳入标准:均符合上述中西医诊断标准;经肺功能检查、影像学检查确诊为COPD;经6 m步速测定、人体成分分析仪检测存在肌肉衰减;认知正常;有自主活动能力,可配合调查研究;依从性较好;签署知情同意书。
1.2.3 排除标准:合并恶性肿瘤;精神病史;严重肝、肾、心功能不全;对本研究药物过敏;合并严重肺部感染、肺大疱等无法完成肺功能检查;伴有严重传染性疾病;沟通障碍。
1.3 方法 均给予祛痰、平喘、氧气支持、戒烟、肺康复训练等对症治疗。
1.3.1 对照组:针对COPD予以噻托溴铵粉吸入剂(正大天晴药业集团股份有限公司)吸入治疗,1次/吸,1粒/次;针对肌肉衰减给予营养支持及体育运动:为患者提供肠内营养剂,为其补充优质蛋白、维生素D、抗氧化营养素、氨基酸;根据患者心肺功能、肌肉衰减度为患者制定针对性体育运动计划,运动时间>40~60 min/次,2~3次/周。
1.3.2 观察组:在对照组基础上,加用茯苓甘草合剂,组方:茯苓15 g、甘草15 g。温水煎煮留汁200 mL,1剂/d,2次/d,分早晚2次温服。2组连续治疗3个月。
1.4 观察指标
1.4.1 中医疗效:比较2组中医疗效,其中显效:临床症状明显减轻,中医证候积分减少率≥95%;有效:临床症状有所缓解,中医证候积分减少率70%~94%;无效:未至上述标准;中医证候积分减少率=(治疗前积分-治疗后积分)/治疗前积分×100%;总有效率=显效率+有效率。
1.4.2 中医证候积分:比较2组治疗前、治疗1个月后、3个月后中医证候积分,包括乏力、肌肉萎缩、步履缓慢等中医证候,按严重程度分为正常(0分)、轻度(2分)、中度(4分)、重度(6分)。
1.4.3 NF-κB mRNA及蛋白表达:于治疗前、治疗1个月后、3个月后采集患者外周静脉血4 mL,分离外周血单核细胞,采用逆转录聚合酶链反应(RT-PCR)检测NF-κB mRNA的表达水平,采用免疫组织化学测定NF-κB蛋白表达。RNA提取试剂盒、荧光定量PCR试剂盒均由美国Invitrogen公司提供。
1.4.4 NF-κB信号通路相关因子:治疗前、治疗1个月后、3个月后采集2组晨起空腹静脉血3 mL,3 000 r/min离心12 min(离心半径10 cm),分离血清,以酶联免疫吸附法测定血清白细胞介素-6(IL-6)、白细胞介素-1(IL-1)、肿瘤坏死因子-α(TNF-α)。
1.4.5 营养状况指标:治疗前、治疗1个月后、3个月后抽取患者晨起空腹静脉血3 mL,以全自动生化分析仪(日本日立公司,型号:7600-110型)测定转铁蛋白(Tf)、血红蛋白(Hb)、白蛋白(ALB)水平。
1.4.6 握力试验:治疗前、治疗3个月后采用电子握力计(北京恒瑞鑫达科技有限公司,型号:LT-100)测量2组握力,男性握力<26 kg,女性握力<18 kg,即可判定为肌力下降。
1.4.7 起立-行走计时测试(TUGT)、5次坐立试验(FTSST):治疗前、治疗3个月后开展TUGT、FTSST。①TUGT:指导患者从椅子上由座位独立站起,按平时步态行走3 min,转身返回,再坐到椅子上。统计患者从脊柱离开椅子到再次坐到椅子上所用时间,共测试3次,取平均值。②FTSST:指导患者坐于无扶手的椅子上,双脚着地,背部不倚靠椅背,听到命令后迅速完成5次起立、坐下动作,站立时膝关节需完全伸直,坐下时需接触椅面。记录患者完成5次动作的时间,重复测量3次取平均值,每次测试间隔休息1 min。③数值越小,表明患者动作能力越好。
1.4.8 肌肉减少症筛查问卷(SARC-F):治疗前、治疗3个月后进行评估,包括上下楼能力、步行能力、坐下站起能力、跌倒史、肌肉力量5方面,每方面2分,共10分,评分与肌少症风险呈正相关。得分≥4分提示存在肌少症风险。
1.4.9 不良反应:比较2组恶心呕吐、腹泻、头痛、皮肤瘙痒等不良反应发生率。

2 结果
2.1 2组中医疗效比较 观察组中医治疗总有效率较对照组高(P<0.05)。见表2。
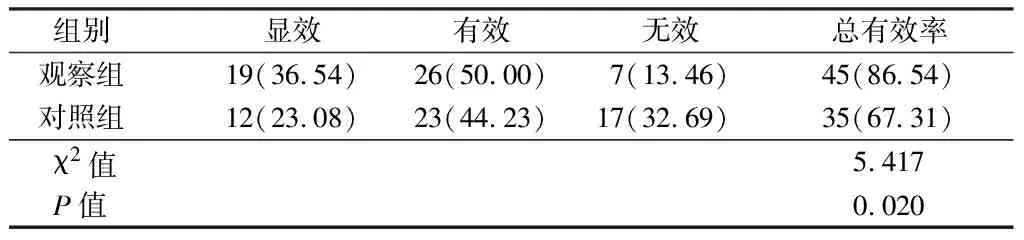
表2 2组中医疗效比较 n=52,例(%)
2.2 2组中医证候积分比较 组别因素与时间因素之间交互作用显著(P<0.05);2组中医证候积分时间效应差异有统计学意义(P<0.05);且观察组随着治疗时间延长呈降低趋势(P<0.05)。见表3。
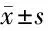
表3 2组中医证候积分比较 n=52,分,
2.3 2组NF-κB mRNA及蛋白表达比较 组别因素与时间因素交互作用显著(P<0.05);2组NF-κB mRNA及蛋白时间效应差异有统计学意义(P<0.05);且观察组随着治疗时间延长呈降低趋势(P<0.05)。见表4。
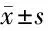
表4 2组NF-κB mRNA及蛋白表达比较 n=52,
2.4 2组NF-κB信号通路相关因子比较 组别因素与时间因素之间交互作用显著(P<0.05);2组IL-8、IL-1、TNF-α时间效应方面差异有统计学意义(P<0.05);观察组IL-8、IL-1、TNF-α随着治疗时间延长呈降低趋势,差异有统计学意义(P<0.05)。见表5。
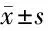
表5 2组NF-κB信号通路相关因子比较 n=52,
2.5 2组营养状况比较 组别因素与时间因素之间交互作用显著(P<0.05);2组Tf、ALB、Hb时间效应方面差异有统计学意义(P<0.05);观察组Tf、ALB、Hb随着治疗时间延长呈升高趋势(P<0.05)。见表6。
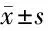
表6 2组营养状况指标比较 n=52,g/L,
2.6 2组肌肉衰减相关比较 治疗前2组肌肉衰减相关指标比较差异无统计学意义(P>0.05);治疗3个月后观察组握力高于对照组,FTSST、TUGT、SARC-F评分低于对照组(P<0.05)。见表7。
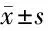
表7 2组肌肉衰减相关指标比较 n=52,
2.7 2组不良反应比较 治疗期间,2组均未出现明显不良反应。
3 讨论
COPD患者由于慢性缺氧、CO2潴留、营养及能量流失极易发生肌肉衰减[11-12]。Demirciolu等[13]调查结果显示,50岁以上COPD患者肌肉衰减患病率为37.5%,Perrot等[14]研究结果显示,48%COPD患者合并肌肉衰减,可见COPD患者肌肉衰减患病率较高,应引起临床广泛关注。
目前临床对COPD合并肌肉衰减的药物治疗方法尚处于研究阶段,主要以营养支持、运动干预等非药物治疗手段为主[15]。近年来,中医因标本兼治、安全性高等优点逐渐受到临床广泛关注[16-17],本研究在传统西药基础上,联合茯苓甘草合剂,结果显示,治疗后与对照组比较,观察组疗效较高,临床症状改善情况较好,提示茯苓甘草合剂联合治疗COPD合并肌肉衰减效果确切,可有效改善临床症状,分析为:中医认为COPD病位在肺,久病及脾,脾气不足则四肢失于濡养,因此,治则应以调脾补肺为主。茯苓甘草合剂由茯苓、甘草组成,其中茯苓具利水健脾之功效,甘草可润肺补脾,止咳祛痰,二者联合,共奏调脾补肺之功效,从而有效缓解临床症状。此外,本研究结果还显示,治疗3个月后观察组握力高于对照组,FTSST、TUGT、SARC-F评分低于对照组(P<0.05),表明茯苓甘草合剂联合治疗可增强患者肌力,分析为:COPD患者呼吸受限,运动耐量下降,随着病程的延长会导致肌肉受累,日常活动量减少,从而引发废用性肌萎缩。现代药理研究表明,甘草中所含生物碱、黄酮类等成分可祛痰镇咳,减小气管阻力,调节机体免疫,抗炎抗病毒[18];茯苓中茯苓多糖等活性成分可增强机体免疫力[19]。二者联用可有效减轻呼吸受限,提升机体免疫力,增强患者运动能力,因此,更有利于患者肌力恢复。
此外,研究显示,炎症与肌肉衰减密切相关[20]。NF-κB在炎性反应过程中发挥着重要作用,NF-κB激活可促进TNF-α等炎性因子释放,炎性因子水平过高会导致肌肉组织合成代谢失衡,促进蛋白分解代谢,增加肌肉量丢失风险[21-22]。NF-κB在肺组织及骨骼肌细胞中均有表达,既往研究指出,COPD患者体内NF-κB异常活跃[23]。另有研究指出,老年大鼠术后骨骼肌细胞内NF-κB处于显著激活状态,提示NF-κB在老年大鼠术后骨骼肌蛋白降解中发挥重要作用[24]。由此推测抑制NF-κB及NF-κB信号通路相关因子表达是改善COPD合并肌肉衰减的有效靶点。本研究结果显示,观察组NF-κB mRNA、NF-κB蛋白及IL-8、IL-1、TNF-α随着治疗时间延长呈降低趋势,表明茯苓甘草合剂联合治疗可通过抑制NF-κB信号通路减轻机体炎性反应,改善临床症状。分析为:现代药理研究证实,茯苓、甘草均具有抗炎功效[25-28]。Wu等[26]指出茯苓中所含茯苓多糖可抑制肝细胞中NF-κB途径的炎性应激;范晶等[27]研究结果显示,甘草中总黄酮可通过调控NF-κB蛋白表达,抑制机体炎性反应,可见茯苓甘草合剂可有效减轻机体炎性反应,从而进一步改善临床症状。此外,本研究还显示,治疗后观察组Tf、ALB、Hb等营养指标得到有效改善,其原因可能在于:丁婷婷等[28]指出炎性反应可加剧肌肉蛋白质分解代谢,抑制肌肉蛋白质合成,导致骨骼肌消耗性营养不良,本研究中所采用茯苓甘草合剂可有效减轻机体炎性反应,因此可有效改善患者营养状态,营养状态的改善则可进一步增强患者肌力,改善肌肉衰减症状。本研究结果还显示,治疗后2组均未发生不良反应,表明茯苓甘草合剂安全性高。
综上所述,茯苓甘草合剂辅助西药治疗COPD合并肌肉衰减效果确切,可通过抑制NF-κB信号通路,减轻炎性反应,改善患者营养状态,缓解临床症状,且安全性高。但本研究仍存在些许不足,本研究样本量较小,且来源单一,结果可能存在偏倚,临床还应多中心多渠道取样,做进一步研究探讨。

