壮药火索藤汤剂指纹图谱的建立及含量测定研究
罗鑫,陈彦洁,蒋学青,苏芳林,王志萍*,谢谭芳*,陈豪(.广西中医药大学,南宁 530200;2.广西高校中药制剂共性技术研发重点实验室,南宁 530200)
火索藤(BauhiniaaureaLevl.)亦称为牛蹄藤[1-3]、金毛羊蹄甲[4]、金叶羊蹄甲[5]、红绒毛羊蹄甲[6]、合掌风、黄麻藤、红毛藤,为豆科植物金毛羊蹄甲的根或茎,分布于广西、四川、贵州、云南等地。作为壮族民间用药的一种,其叶、藤和根均可供药用,化学成分复杂多样,主要有黄酮类、甾体类、芳香酸类等化合物,具有补肾涩精、祛风湿、活血止痛等作用[7-9]。由于火索藤药材基原地分布不均、药效成分和量效关系相关研究较少、《中国药典》历版无其收录等原因,目前学界尚未对火索藤进行系统研究。
近年来国内外围绕中药汤剂进行了大量研究,为火索藤标准汤剂及后续中药配方颗粒的标准制订提供了可借鉴的研究思路[10-24],其中通过HPLC指纹图谱结合化学计量分析是目前较为成熟且可行的研究路径。
本研究在前期研究基础上建立壮药火索藤汤剂样品的HPLC指纹图谱,结合聚类分析(CA)、主成分分析(PCA)、正交偏最小乘法-判别分析(OPLS-DA)等对各批次汤剂进行评价,并对金丝桃苷、槲皮苷进行含量测定,明确不同批次汤剂之间的含量差异,为其制剂的开发和研究提供参考。
1 材料
1.1 仪器
LC-2030C高效液相色谱仪(岛津公司);SHB-B95型循环水式多用真空泵(郑州长城科工贸有限公司);QUINTIX125D-1CN型十万分之一电子天平(德国赛多利斯);YTLG-10冷冻干燥机(上海叶拓科技有限公司);PL-FS40T康士洁超声波清洗机(东莞康士洁超声波科技有限公司)。
1.2 试药
磷酸[色谱纯,阿拉丁试剂(上海)有限公司];甲醇、乙腈(色谱纯,美国 Fisher 公司);甲醇、乙醇(分析纯,成都市科隆化学品有限公司)。
金丝桃苷对照品(纯度:98.4%,批号:MUST-22071210)、槲皮苷对照品(纯度:98.6%,批号:MUST-22112917)(成都曼思特生物科技有限公司)。10批火索藤药材分别从广西壮族自治区北流市、梧州市、南宁市等地采购所得,药材经广西中医药大学韦松基教授鉴定为豆科植物火索藤BauhiniaaureaLevl.的藤茎和叶,药材产地信息见表1。
2 方法与结果
2.1 色谱条件
色谱柱:Waters XBridge C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水(B),梯度洗脱(0~40 min,2%~6%A;40~60 min,6%~9%A;60~65 min,9%~10%A;65~80 min,10%~12%A;80~85 min,12%~12.5%A;85~95 min,12.5%~13%A;95~118 min,13%~16%A;118~130 min,16%~14%A;130~133 min,14%~8%A;133~136 min,8%~2%A;136~140 min,2%A);流速:1.0 mL·min-1;检测波长:320 nm;柱温:25℃;进样量:10 μL。
2.2 混合对照品溶液的配制
取金丝桃苷、槲皮苷对照品各适量,精密称定,70%甲醇定容,再分别精密吸取各对照品溶液2 mL置于10 mL棕色量瓶中,加70%甲醇稀释定容制成质量浓度分别为87.7、84.6 μg·mL-1的混合对照品溶液。
2.3 供试品溶液的制备
依照中药饮片标准汤剂工艺参数方法[24],取火索藤药材约100 g(茎∶叶=9∶1),精密称定,加8倍量水浸泡30 min,第一次煎煮30 min,趁热200目筛网滤过,残渣加7倍量水,第二次煎20 min,趁热200目筛网滤过,合并两次滤液,浓缩至500 mL,冷冻干燥成粉末。取粉末约0.2 g(过二号筛),精密称定,置于25 mL具塞锥形瓶,加70%甲醇10 mL,超声提取50 min(功率250 W,频率40 kHz),补足重量,摇匀,0.45 μm 微孔滤膜过滤,取续滤液,即得。
2.4 火索藤汤剂HPLC指纹图谱建立
2.4.1 精密度试验 取“2.3”项下供试品溶液(S2),按“2.1”项下色谱条件连续进样6次,分别进行测定。以12号峰槲皮苷作为参照峰(S)计算各共有峰得相对保留时间RSD值<0.30%,相对峰面积RSD值<2.7%(n=6),结果RSD均小于3.0%,表明仪器精密度良好。
2.4.2 重复性试验 取同一批汤剂冻干粉(S2)6份,按“2.3”项下方法制备6份供试品溶液,依照“2.1”项下色谱条件测定分析,以12号峰槲皮苷作为参照峰(S)计算得各共有得峰相对保留时间RSD值<0.60%,相对峰面积RSD值<2.9%(n=6),结果均小于3.0%,表明该方法重复性良好。
2.4.3 稳定性试验 取“2.3”项下供试品溶液(编号S2),室温分别放置0、3、6、9、12、24 h,依照“2.1”项下色谱条件测定分析,以12号峰槲皮苷作为参照峰(S)计算得各共有峰相对保留时间RSD值<0.90%,相对峰面积RSD值<2.9%(n=6),结果RSD均小于3.0%,表明供试品溶液室温放置24 h稳定性良好。
2.4.4 火索藤汤剂指纹图谱的建立和共有峰标识 取10批火索藤药材,按照“2.3”项下方法制备供试品溶液,照“2.1”项下色谱条件测定分析,将数据导入“中药色谱指纹图谱相似度评价系统(2012版)”中,S1为参照图谱,采用平均数法,时间窗宽度为0.1 min,进行多点校正,生成叠加共有峰图谱及对照图谱R(见图1),确定了12个共有峰,通过与混合对照品色谱图进行比对(见图2),识别出2个成分,其中9号峰为金丝桃苷、12号峰为槲皮苷。

图1 火索藤汤剂叠加共有峰图谱及对照图谱RFig 1 Huosuoteng decoction superposition common peak and control R

图2 混合对照品的HPLC色谱图Fig 2 HPLC chromatogram of mixed reference
2.5 相似度评价
在“中药色谱指纹图谱相似度评价系统(2012版)”中对10批火索藤汤剂指纹图谱和对照指纹图谱进行相似度计算,结果S1~S10批汤剂样品的相似度结果均大于0.91,表明不同批次的火索藤药材质量较为稳定,详见表2。

表2 10批火索藤汤剂样品相似度评价结果Tab 2 Similarity evaluation of 10 batches of Huosuoteng decoction
以12号峰槲皮苷作为参照峰(S)计算各共有得峰相对保留时间RSD值和相对峰面积RSD值,结果12个共有峰相对保留时间RSD值为0.10%~0.50%,相对峰面积RSD值为34%~119%(n=10),这表明不同批次的火索藤汤剂化学成分种类均一,但含量差异较大,可能是由于不同产地不同生长环境所致。
2.6 聚类分析
以12个共有特征峰的峰面积为变量,导入SPSS 25.0软件中,采用组间联接-平方欧氏距离法进行聚类分析。结果如图3所示,10批壮药火索藤汤剂可聚为3类,S1、S2、S3、S6、S9聚为一类,S4、S5为第二类,S7、S8、S10为第三类,说明不同批次的火索藤汤剂化学成分质量存在一定差异。
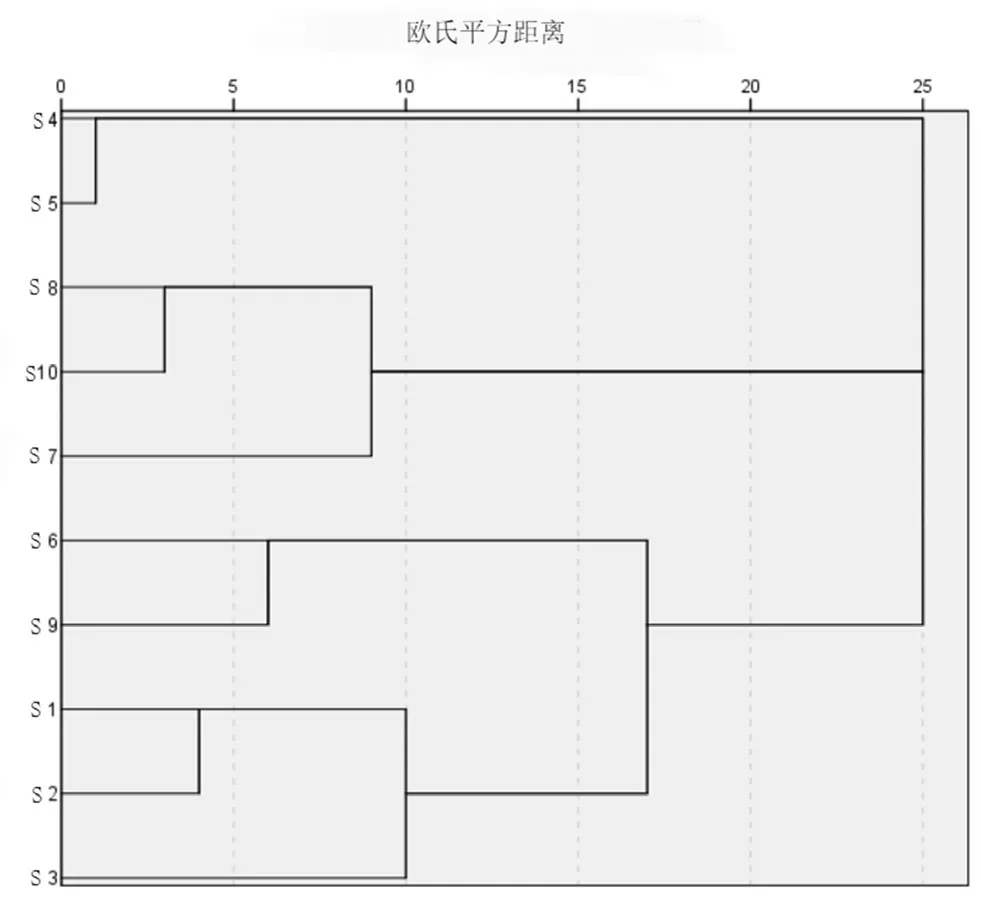
图3 不同批次壮药火索藤汤剂聚类分析Fig 3 Cluster analysis of different batches of Huosuoteng decoction
2.7 主成分分析
以12个共有特征峰的峰面积为变量,采用SPSS 25.0软件进行主成分分析,分析结果见表3,共提取出4个主成分,特征值分别为4.26、3.34、1.45、1.18,累计方差贡献率为85.27%,表明这4个主成分含有汤剂样品指纹图谱的主要信息,可反映不同产地不同批次火索藤汤剂样品的整体质量。
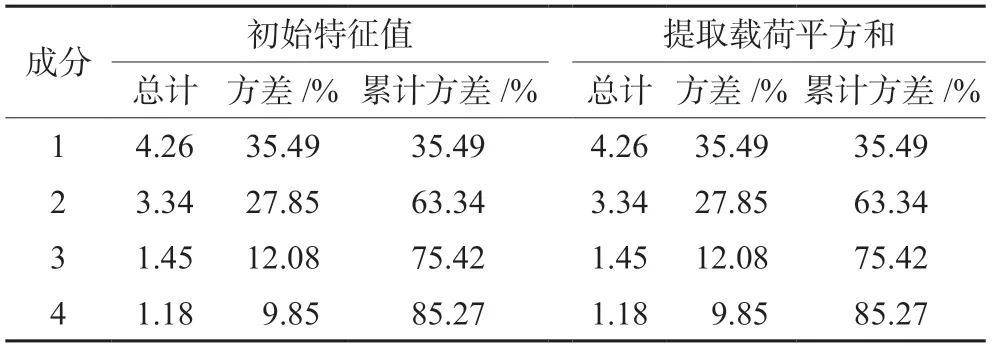
表3 主成分总方差解释Tab 3 Principal component total variance interpretation
再将标准化处理后的12个共有特征峰的峰面积作为变量,导入SIMAC 14.1软件中,进行主成分分析,生成主成分得分图见图4,可知,样品共聚为3类,S1、S2、S3、S6、S9聚为一类,S4、S5为第二类,S7、S8、S10为第三类,其结果同聚类分析一致。

图4 10批火索藤汤剂样品主成分分析得分图Fig 4 PCA score of 10 batches of Huosuoteng decoction
2.8 OPLS-DA
以12个共有峰的峰面积为变量,采用SIMAC 14.1软件,进行OPLS-DA分析,得到分散点图(见图5)。并对模型进行200次置换检验。结果,R2X、R2Y及Q2分别为0.62、0.80、0.67,均大于0.6,这表明建立的模型预测能力较好。置换检验显示模型无过拟合现象,说明模型结果真实可靠。此外,由图5可知,10批样品被分为3类,与聚类分析、主成分分析结果一致。

图5 火索藤汤剂样品OPLS-DA得分图Fig 5 OPLS-DA score of Huosuoteng decoction
其次,为明确火索藤汤剂样品质量具有显著影响的成分,进一步通过SIMAC 14.1软件,在OPLS-DA分析基础上进行变量投影重要度(VIP)分析,以VIP>0.95为标准进行筛选,共筛选出8个成分,分别为峰6、峰2、峰11、峰8、峰10、峰4、峰12(槲皮苷)、峰9(金丝桃苷),见图6。表明这8个成分可能是不同批次火索藤汤剂样品质量差异的主要因素。

图6 火索藤汤剂样品OPLS-DA-VIP图Fig 6 OPLS-DA-VIP diagram of Huosuoteng decoction
2.9 壮药火索藤汤剂中2个差异成分的含量测定
2.9.1 混合对照品溶液的配制 分别取金丝桃苷、槲皮苷对照品适量,70%甲醇定容,制成对照品溶液,精密吸取上述溶液各2 mL置于10 mL棕色量瓶中,加70%甲醇定容制成为43.89、43.11 μg·mL-1的混合对照品溶液。
2.9.2 线性关系考察 取金丝桃苷、槲皮苷对照品适量,70%甲醇定容,制成每1 mL含金丝桃苷175.36 μg、槲皮苷169.13 μg的混合对照品母液,再逐级稀释,依照“2.1”项下色谱条件进样测定,以质量浓度为横坐标(X),峰面积为纵坐标(Y)绘制标准曲线,结果金丝桃苷和槲皮苷线性回归方程分别为Y=1.48×104X-1.00×104,R2=0.9999及Y=1.44×104X-8.23×103,R2=0.9999,说明金丝桃苷质量浓度在0.7015~175.366 μg·mL-1,槲皮苷质量浓度在0.6766~169.1380 μg·mL-1内与峰面积线性关系良好。
2.9.3 精密度考察 取“2.9.1”项下混合对照品溶液,依照“2.1”项下色谱条件连续检测6次,记录各成分峰面积。结果金丝桃苷和槲皮苷峰面积的RSD值均为0.1%,这表明仪器的精密度良好。
2.9.4 稳定性考察 取“2.3”项下供试品溶液(S2),室温放置0、3、6、9、12、24 h,依照“2.1”项下色谱条件进行分析,记录各成分峰面积。结果金丝桃苷和槲皮苷峰面积的RSD值分别为2.7%、2.2%,均小于<3%,这表明24 h内火索藤汤剂样品稳定性良好。
2.9.5 重复性考察 精密称定火索藤汤剂样品6份(S2),按照“2.3”项下制备方法,平行制备6份,依照“2.1”项下色谱条件进行分析,记录各成分峰面积,依照回归方程计算各成分含量,结果金丝桃苷和槲皮苷的平均含量分别为0.50、1.79 mg·g-1,RSD值分别为2.9%、2.6%,表明该方法重复性较好。
2.9.6 加样回收试验 取已知含量火索藤汤剂冻干粉约0.2 g,按照1∶1加入金丝桃苷和槲皮苷峰对照品,按照“2.3”项下制备方法,平行制备供试品溶液6份,依照“2.1”项下色谱条件进行分析,记录各成分峰面积,计算各成分加样回收率,结果显示金丝桃苷的加样回收率均值为91.91%,RSD值为2.4%;槲皮苷加样回收率均值为96.72%,RSD值为1.8%,两者结果均符合《中国药典》2020年版四部通则9101的具体规定,证明该方法准确度良好。
2.9.7 不同批次火索藤汤剂中金丝桃苷与槲皮苷的含量测定 取10批不同产地批次的火索藤药材,按照“2.3”项下方法,制备成各供试品溶液(n=2),依照“2.1”项下色谱条件分析,采用外标法计算壮药火索藤汤剂中金丝桃苷和槲皮苷的含量,取平均值,结果见表4。10批火索藤汤剂中金丝桃苷含量范围为0.1520~0.6669 mg·g-1,槲皮苷含量范围为1.7108~6.5276 mg·g-1。
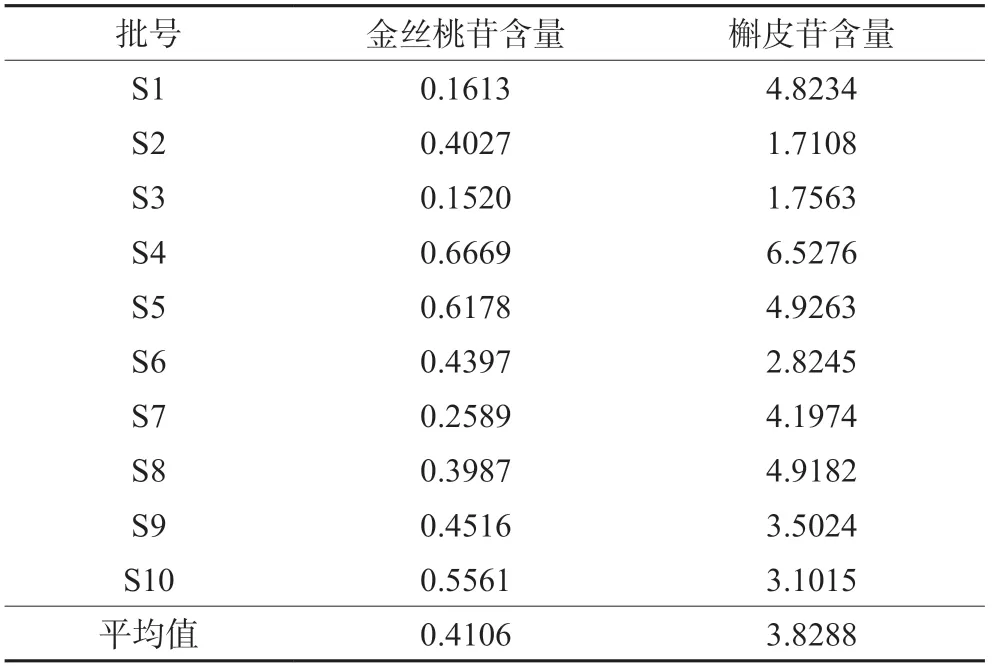
表4 10批火索藤汤剂中含量测定结果(mg·g-1)Tab 4 Content determination of 10 batches of Huosuoteng decoction (mg·g-1)
3 讨论
3.1 供试品制备方式的考察
通过比对纯汤剂样品和粉末进样后发现,汤剂样品在经过处理后所得图谱信息更为完整、稳定。故本试验考察了不同提取方式(超声、回流)确定以超声为提取方式,同时对不同提取溶剂(水、甲醇、乙醇)、超声时间(20、30、40、50、60 min)进行考察,确定了以70%甲醇10 mL超声提取50 min(功率250 W,频率40 kHz)的样品制备方式。
3.2 指纹图谱的建立及成分分析
通过对不同批次火索藤汤剂进行分析,确定了12个共有峰,与对照图谱比对其相似度均大于0.91,表明各批次火索藤药材所制汤剂质量一致性较好,其后的聚类分析、主成分分析等结果显示这10个批次可分为3类,最后基于OPLSDA分析的VIP指认结果发现了对这10批次药材制的样品间差异影响最大的8个成分,并根据前期研究基础,选取活性成分金丝桃苷与槲皮苷进行含量测定,以成分含量判断S4、S5批次两地区火索藤药材所制汤剂中金丝桃苷与槲皮苷含量均优于其他地区。
综上,本研究成功建立了壮药火索藤汤剂的HPLC指纹图谱,结合化学计量学分析筛选出8个主要差异性成分,并对其中2个成分的含量进行研究,用以评价样品质量,可为该药材汤剂质量控制和研究提供一定的参考。

