静脉注射吴茱萸碱-甘草酸纳米胶束后吴茱萸碱在大鼠体内药代动力学研究
邓英光,银雪艳,郭秀彩,张紫萍,李峰(广州市第十二人民医院,广州 510620)
吴茱萸碱(evodiamine,EVO)是芸香科植物吴茱萸、石虎和疏毛吴茱萸的干燥近成熟果实中的色胺吲哚类生物碱成分[1-2],具有抗炎、抗纤维化、抗脂毒性、抗肿瘤活性[3],但EVO存在水溶性差,代谢过快,靶向性差等缺点[4-5],使其临床应用受到限制。甘草酸(glycyrrhizic acid,GL)所具有的两亲性结构特点使其对难溶性药物具有增溶作用,大量研究表明以甘草酸作为载体的新型药物,其药物溶解度和生物利用度均有明显的提高[6],甘草酸作为天然药物活性成分,已被证实是安全无毒的生物材料,在一定条件下不会导致溶血[7],符合国家静脉注射的标准,因此甘草酸可以满足作为有前景的药物递送载体的静脉药物开发的基本要求。前期我们以甘草酸作为载体对EVO进行包封,采用薄膜分散法制备出吴茱萸碱-甘草酸纳米胶束[(EVOGL)-micelles],制备成胶束后EVO的溶解度明显增加[8],可作为静脉注射药物。为进一步了解(EVOGL)-micelles在大鼠体内的药代动力学过程,尾静脉分别注射EVO和(EVO-GL)-micelles后,采用HPLC测定大鼠血浆中EVO含量,评价胶束对EVO药代动力学的影响,以期为EVO新型给药系统提供依据。
1 材料
1.1 仪器
LC-20A岛津高效液相色谱仪(日本岛津有限公司);Quintix65-1CN电子天平(德国赛多利斯公司);5804R Eppendorf冷冻离心机(美国艾本德公司);减压真空干燥箱(上海高致精密仪器有限公司)。
1.2 试药
EVO(纯度>98%,批号:C16244049,Aladdin),EVO对照品(纯度>99%,Aladdin,批号:A1629030),甘草酸(纯度>98%,北京百灵威科技有限公司,批号:LS40R62),乙腈、甲醇(色谱级,德国Merck公司),乙醇等其他试剂为分析纯,水为超纯水。
1.3 动物
雄性SD大鼠,200~220 g[南方医科大学南方医院实验动物中心,动物使用许可证,SYXK(粤)2015-0056;合格证号:44002100013124]。
2 方法和结果
2.1 色谱条件
所用色谱柱为Ecosil C18反相液相色谱柱(4.6 mm×150 mm,5 μm);柱温40℃;流动相为乙腈-水=60∶40;流速1.0 mL·min-1;检测波长225 nm;检测器为二极管阵列紫外可见光检测器(SPD-M20A);进样量20 μL;分析时间7 min。
2.2 溶液的制备
精密称量10 mg EVO对照品,用甲醇溶解后转移至50 mL棕色量瓶,加入甲醇定容至50 mL,即得到200 μg·mL-1的EVO对照品储备液。精密吸取适量EVO对照品储备液,使用适量的甲醇稀释制成质量浓度为100、500、2000 ng·mL-1作为EVO对照品溶液。
2.3 动物给药方案及样品采集处理
将12只雄性SD大鼠随机平均分成(EVO-GL)-micelles组和EVO溶液组[用复合溶剂(5% DMSO,10%吐温80,85% 0.9%氯化钠溶液)超声溶解[9]]。给药前称量大鼠体重,按 3 mg·kg-1(以EVO计)的剂量分别尾静脉注射EVO溶液和(EVO-GL)-micelles。给药后分别于0、0.083、0.25、0.5、1、2、4、6、8、12、24 h进行眼底取血,置于肝素化离心管,4℃、3500 r·min-1离心10 min,吸取上层血浆到离心管,于-20℃保存备用。
2.4 样品的处理
取100 μL血浆样品,加入300 μL乙腈沉淀蛋白,涡旋混合3 min,12 000 r·min-1离心15 min,取上清液,50℃真空干燥挥干有机溶剂,加入100 μL甲醇复溶,涡旋3 min,12 000 r·min-1离心15 min。取上清液20 μL,按“2.1”项下色谱条件进样测定。
2.5 方法学考察
2.5.1 专属性 记录EVO对照品、空白血浆样品、空白血浆+EVO对照品溶液、静脉(EVOGL)-micelles给药后30 min血浆样品的HPLC图,结果如图1所示,血浆样品中的内源物质不干扰EVO的色谱峰,EVO出峰时间短,保留时间为4.7 min,峰形良好。
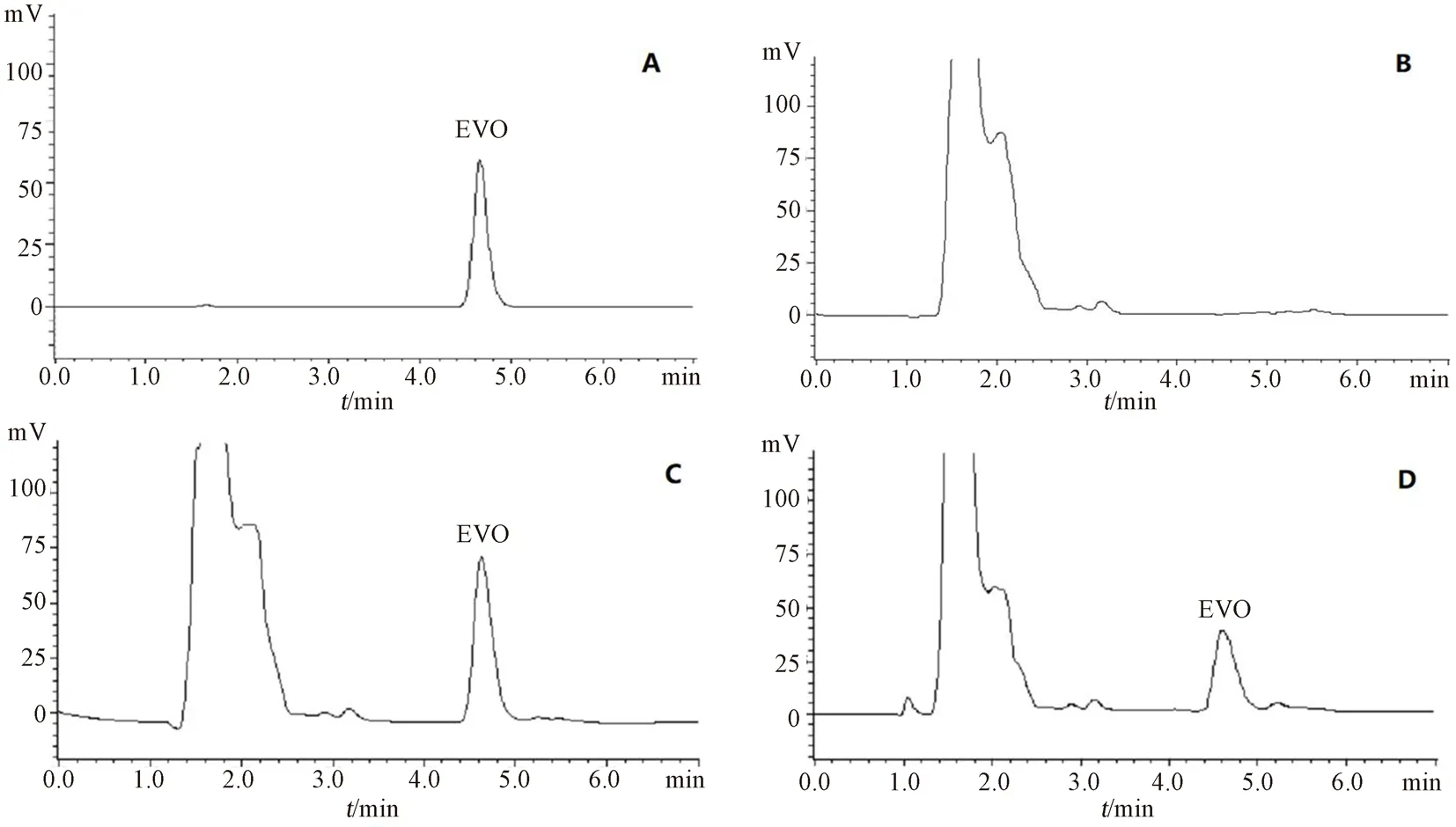
图1 吴茱萸碱-甘草酸纳米胶束的HPLC色谱图Fig 1 HPLC chromatogram of(EVO-GL)-micelles
2.5.2 标准曲线以及定量下限 空白血浆中加入不同浓度的EVO溶液,即得到含EVO质量浓度分别为25、50、100、250、500、1000、2000、4000 ng·mL-1的标准血浆样品,按照“2.4”项下方法处理血浆样品。按“2.1”项下色谱条件进样测定峰面积。以药物质量浓度(μg·mL-1,c)为横坐标,峰面积(A)为纵坐标进行回归拟合标准曲线,得到EVO的标准曲线方程:A=2.624×105c+2.234×104(r=0.998)。结果显示血浆样品中的EVO在25~4000 ng·mL-1与峰面积线性关系良好。根据信噪比(S/N)=10的原则,确定定量下限为25 ng·mL-1。
2.5.3 精密度 分别吸取100 μL空白血浆,制备低、中、高3个EVO质量浓度(100、500、2000 ng·mL-1)的血浆样品,每个浓度准备5份,按照“2.4”项下方法处理后,按“2.1”项下色谱条件进样测定峰面积。在同一天内每个浓度各测定3次,考察日内精密度;连续测定3 d,考察日间精密度。结果日内精密度RSD为4.5%~5.1%,日间精密度RSD为5.3%~8.5%,达到生物样品分析要求。
2.5.4 提取回收率 分别吸取100 μL空白血浆,制备低、中、高3个EVO质量浓度(100、500、2000 ng·mL-1)的血浆样品各5份,分别按照“2.4”方法处理后,按“2.1”项下色谱条件进样测定。通过标准曲线计算EVO的浓度,提取回收率(%)=提取后实测EVO浓度/理论浓度×100%。得出3个浓度EVO提取回收率为95.3%~98.4%,RSD范围为5.7%~8.1%。达到生物样品分析要求。
2.5.5 药代动力学实验数据处理及结果 数据处理后,得大鼠静脉注射后各时间点EVO的平均血药浓度,大鼠尾静脉给药 EVO和(EVO-GL)-micelles后吴茱萸碱的药物浓度-时间曲线见图2。使DAS 2.0软件用对血药浓度和时间采用静脉给药模型拟合,得到药代动力学参数见表1。数据显示EVO组在体内符合二室模型,(EVO-GL)-micelles组符合三室模型。(EVO-GL)-micelles组的Cmax明显高于EVO组(P<0.05)。(EVO-GL)-micelles组的AUC0~t是EVO组的2.30倍。(EVO-GL)-micelles组清除率(CL)较EVO组明显降低(P<0.05)。
表1 EVO和(EVO-GL)-micelles的药代动力学参数(±s,n=6)Tab 1 Pharmacokinetic parameters of EVO and (EVO-GL)-micelles(±s,n=6)

表1 EVO和(EVO-GL)-micelles的药代动力学参数(±s,n=6)Tab 1 Pharmacokinetic parameters of EVO and (EVO-GL)-micelles(±s,n=6)
注:与EVO组相比,*P<0.05。Note:Compared with the EVO group,* P<0.05.
参数(EVO-GL)-micellesEVO Cmax/(μg·mL-1)1.61±0.19*0.92±0.11 t1/2/h3.66±1.493.26±0.59 V1/(L·kg-1)1.91±0.20*3.42±0.48 CL/(L·h-1·kg-1)0.67±0.21*1.38±0.14 AUC0~t/(mg·L-1·h)4.76±1.41*2.07±0.22 AUC0~∞/(mg·L-1·h)4.88±1.47*2.19±0.22
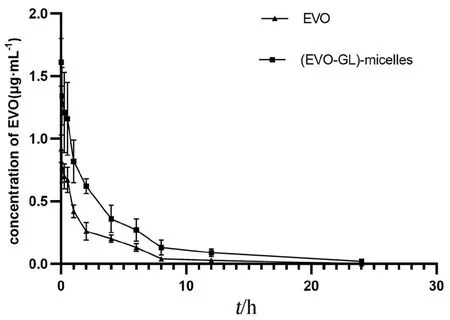
图2 大鼠尾静脉给药 EVO和(EVO-GL)-micelles后吴茱萸碱的药物浓度-时间曲线(±s,n=6)Fig 2 Plasma concentration-time profile of evodiamine after tail vein administration of EVO and(EVO-GL)-micelles in rats(±s,n=6)
3 讨论
本实验建立了HPLC法测定大鼠血浆中EVO含量,对(EVO-GL)-micelles和EVO进行了药代动力学评价,结果显示,EVO制备成(EVO-GL)-micelles纳米胶束后,(EVO-GL)-micelles组的AUC0~t是原药EVO的2.30倍,CL是原药EVO的0.48倍,说明制备成(EVO-GL)-micelles纳米胶束后,EVO在体内的血浆清除率降低,表明(EVOGL)-micelles组相比EVO原药在大鼠体内具有更好的缓释性,明显改善了EVO的药代动力学过程,提高EVO在血液中的浓度和滞留时间。前期我们体外释药实验证明(EVO-GL)-micelles累计释放量明显高于EVO原药,胶束中EVO 释放缓慢,可能是由于药物主要包载于胶束疏水性内核中,以胶束的形式存在,从而起到缓释作用[8]。同时可能与制备成甘草酸胶束后的靶向作用有关,甘草酸具有皂苷类两亲性物质结构特点,使其能够结合细胞膜上的胆固醇或磷脂,改变细胞膜上脂质的流动性,诱导细胞膜孔隙的形成,细胞膜通透性明显增加,胶束与细胞膜相互作用,释放大量的皂苷,从而在病变部位可达到高浓度的累积,甘草酸的直接跨膜递送机制可能影响了EVO的代谢,从而起到缓释的作用[10-11]。DAS 2.0拟合数据显示EVO组符合二室模型,(EVO-GL)-micelles组更符合三室模型,可能在组织分布上与EVO组存在差异,体内正常器官如肝脏中肝细胞膜上有甘草酸和甘草次酸的结合位点,有研究发现静脉注射甘草酸后,甘草酸快速被肝脏摄取及蓄积,由甘草酸修饰后的药物具有明显的肝靶向性[7],可用于肝脏疾病的治疗,利用甘草酸的直接跨膜递送机制及显著的肝靶向性能力,用于构建作用于肝纤维化组织的靶向药物具有良好的应用前景,需要进一步研究。

