经典名方清胃散物质基准特征图谱及指标成分含量测定研究
曹杰楠,李思,盛华
(1.南京中医药大学药学院,江苏 南京 210023;2.江阴天江药业有限公司,江苏 无锡 214400;3.南京大学医学院附属金陵医院,江苏 南京 210002)
经典名方是指至今仍广泛应用、疗效确切、具有明显特色与优势的古代中医典籍所记载的方剂[1]。经典名方是中药新药研发的重要源泉,长期以来多以核心方的形式在中医临床广泛应用,是中医防病治病的中坚力量[2],具有组方合理、疗效确切、安全性高等特点[3]。随着经典名方被广泛关注,政府也出台了一系列政策去帮助经典名方复方制剂的研究和发展。汤剂是中医临床用药的传统剂型,但在使用过程中煎煮不便、不易携带且没有统一的标准,严重影响临床应用,因此研究方便携带且有明确质量标准的现代经典名方复方制剂具有重大意义。经典名方复方制剂的开发研究有利于我们继承和创新中医药理论,振兴并开拓传统中国中药产业,从而推动我国中医药事业的高质量发展。
2018年4月,国家中医药管理局发布了《古代经典名方目录(第一批)》,其中就包括了李东垣《兰室秘藏》中的“清胃散”一方[4]。清胃散由当归、生地黄、黄连、牡丹皮、升麻5味药组成,是治疗胃热证的代表方剂[5]。本研究前期已通过古籍考证并结合实验考察,确定了清胃散方中黄连、地黄、当归、牡丹皮、升麻基原及产地、饮片炮制方法、处方剂量、物质基准制备工艺,本研究在此基础上制备了15批清胃散物质基准,建立了清胃散物质基准特征图谱及含量测定方法,指认了相关色谱峰,明确指标性成分含量范围,为提高清胃散物质基准复方制剂质量的稳定性和一致性提供依据和保障[6]。
1 材料
1.1 仪器
Waters e2695高效液相色谱仪(美国Waters公司);Waters 2998光电二极管矩阵检测器(美国Waters公司);TD6001型分析天平(天津市天马仪器厂);FA1104N型电子分析天平(上海精密科学仪器有限公司);MS-105DU型电子分析天平(梅特勒-托利多国际股份有限公司);Biosafer SB25-12DTD超声波清洗机(南京赛飞生物科技有限公司);400Y多功能粉碎机(永康市铂欧五金制品有限公司);AE-1106A型电陶炉(佛山市顺德区爱卡生活电器有限公司)。
1.2 试药
丹皮酚对照品(中国食品药品检定研究院,含量99.8%,批号:110708-201908)、阿魏酸对照品(中国食品药品检定研究院,含量99.0%,批号:110773-201614)、异阿魏酸对照品(中国食品药品检定研究院,含量99.3%,批号:111698-201904)、梓醇对照品(南京金益柏生物科技有限公司,含量99.53%,批号:20111003)、盐酸小檗碱对照品(中国食品药品检定研究院,含量85.9%,批号:110713-202015)、盐酸巴马汀对照品(中国食品药品检定研究院,含量85.7%,批号:110732-201913)、盐酸黄连碱对照品(中国食品药品检定研究院,含量95.1%,批号:112026-201601)、藁本内酯对照品(中国食品药品检定研究院,供薄层鉴别用,批号:111737-201910)。
甲酸(ACS,上海阿拉丁生化科技股份有限公司,批号:E1830032);磷酸(分析纯,南京化学试剂有限公司,批号:13040910475);冰醋酸(分析纯,上海阿拉丁生化科技股份有限公司,批号:B1911108);乙腈(色谱级,美国TEDIA公司,批号:21015182);甲醇(色谱级,美国TEDIA公司,批号:18012975);盐酸(分析纯,上海凌峰化学试剂有限公司,批号:20140611);磷酸二氢钾(分析纯,南京化学试剂有限公司,批号:080760460);十二烷基硫酸钠(超级纯,上海麦克林生化科技有限公司,批号:C10435036);实验用水为怡宝纯净水。
1.3 饮片
研究所用药材及饮片均由南京中医药大学刘训红教授鉴定且均按照2020版《中国药典》一部各药材项下检测合格,其中当归、黄连、升麻、牡丹皮4种药材按2020版《中国药典》四部“炮制”通则将药材炮制成相应饮片,地黄按照本项目组考察出的炮制方法进行炮制(因经典名方制剂暂未申报,故炮制工艺暂时保密)。药材、饮片信息见表1。

表1 清胃散物质基准中饮片产地信息
利用随机组合将不同批次当归、牡丹皮、黄连、升麻、地黄5味饮片进行组合,制备15批清胃散物质基准对应实物,批号为S1~S15,见表2。
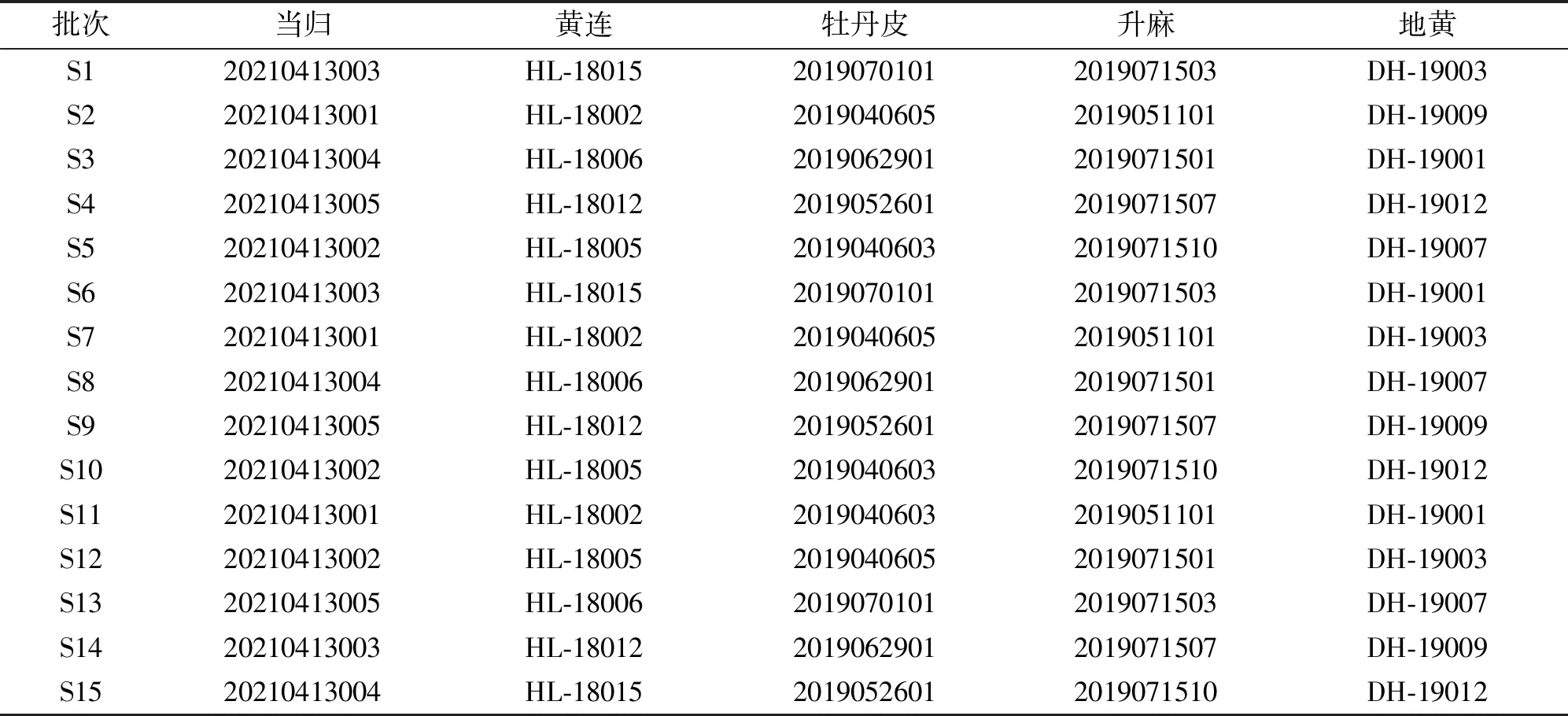
表2 15批清胃散物质基准饮片组合信息
2 方法与结果
2.1 清胃散物质基准样品制备
原文记载,清胃散用法用量为“当归身、择细黄连、生地黄(酒制)各三分,牡丹皮五分,升麻一钱,上为细末,都作一服,水一盏半,煎至一盏,去滓,带冷服之”[4]。称取全方饮片3倍剂量,共28.8 g,根据古籍记载和课题组前期研究所得制备工艺(因经典名方制剂暂未申报,故工艺暂时保密),制得粉末状清胃散物质基准。
2.2 清胃散物质基准特征图谱研究
2.2.1 色谱条件 色谱柱Waters Symmetry C18(4.6 mm×250 mm,5 μm);流动相乙腈(A)-0.1%磷酸水(B),梯度洗脱:0~10 min,1%A;10~15 min,1%~10%A;15~45 min,10%~15%A;45~70 min,15%A;70~75 min,15%~20%A;75~90 min,20%~25%A;90~95 min,25%~35%A;95~100 min,35%A;100~105 min,35%~90%A;105~115 min,90%~10%A;115~116 min,10%~1%A;116~120 min,1%A。检测波长210、330 nm,流速1.0 mL·min-1,柱温35 ℃,进样量20 μL。
2.2.2 溶液的制备 对照品溶液的制备:分别取梓醇、阿魏酸、异阿魏酸、盐酸小檗碱、盐酸巴马汀、丹皮酚及藁本内酯(仅用于指认,无具体含量)对照品适量,精密称定,加甲醇制成单标溶液,再分别吸取一定量混匀稀释成质量浓度为109.184、91.080、85.398、78.169、72.588、81.836 μg·mL-1的混合溶液,摇匀,即得。
供试品溶液的制备:取物质基准0.4 g,精密称定,精密加入10 mL 75%甲醇,称定质量,超声(功率500 W,频率45 kHz)45 min,放冷,再称定质量,用75%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
单味饮片样品的制备:按“2.1”项下清胃散物质基准制备工艺制备单味饮片物质基准粉末样品,并按“2.2.2”项下供试品溶液的制备方法制备单味饮片物质基准供试品溶液,即得。
阴性样品的制备:按“2.1”项下清胃散物质基准制备工艺制备单味饮片缺黄连、缺地黄、缺牡丹皮、缺当归、缺升麻的阴性物质基准粉末样品,并按“2.2.2”项下供试品溶液的制备方法制备阴性物质基准供试品溶液,即得。
2.2.3 方法学考察 精密度考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法制备供试品溶液,在“2.2.1”项色谱条件下连续进样6次,测定,以异阿魏酸的保留时间和峰面积为参照,记录各峰的相对保留时间和相对峰面积,计算RSD,各峰相对保留时间的RSD<0.38%、相对峰面积的RSD<3.24%,表明仪器精密度良好。
重复性考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法平行处理6份供试品溶液,在“2.2.1”项色谱条件下精密吸取各供试品溶液20 μL进样,测定,以异阿魏酸的保留时间和峰面积为参照,记录各峰的相对保留时间和相对峰面积,计算RSD,各峰相对保留时间的RSD<0.49%、相对峰面积的RSD<3.45%,表明该方法重现性良好。
稳定性考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法制备供试品溶液,在“2.2.1”项色谱条件下分别于0、2、4、6、8、10、12、24 h精密吸取供试品溶液20 μL进样,测定,以异阿魏酸的保留时间和峰面积为参照,记录各峰的相对保留时间和相对峰面积,计算RSD,各峰相对保留时间的RSD<0.84%、相对峰面积的RSD<3.08%,表明该供试品溶液在24 h内均能保持稳定。
2.2.4 15批清胃散物质基准特征图谱测定 利用中药色谱指纹图谱相似度评价系统(2012版)软件对15批清胃散物质基准供试品的特征图谱进行分析,以S1为参照图谱,采用平均数法,时间窗宽度为0.1,进行多点校正与色谱峰匹配,并进行相似度计算,15批清胃散物质基准色谱图相似度均≥0.975,表明各批次样品之间的相似度较好,见表3。
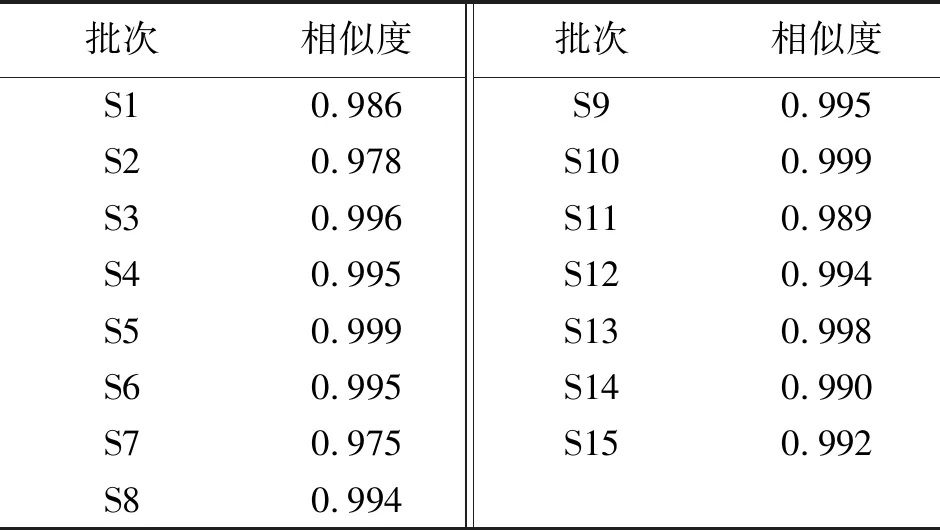
表3 15批清胃散物质基准相似度结果
得到了15批清胃散物质基准特征图谱叠加图,见图1。确定了13个共有峰,其中黄连特征峰为2、3、4、7、8号峰,升麻特征峰为5、6、9、10、11号峰,当归特征峰为5、13号峰,牡丹皮特征峰为12号峰,酒地黄特征峰为1号峰。通过对照品指认,指认出其中7个峰,分别为梓醇(1号峰)、阿魏酸(5号峰)、异阿魏酸(6号峰)、盐酸小檗碱(7号峰)、盐酸巴马汀(8号峰)、丹皮酚(12号峰)、藁本内酯(13号峰),见图2。在15批清胃散物质基准特征图谱中,6号异阿魏酸色谱峰居中且分离度良好,峰面积适中,所以确定6号峰为参照峰。供试品溶液、各单味物质基准及阴性物质基准溶液HPLC色谱图见图3~4。
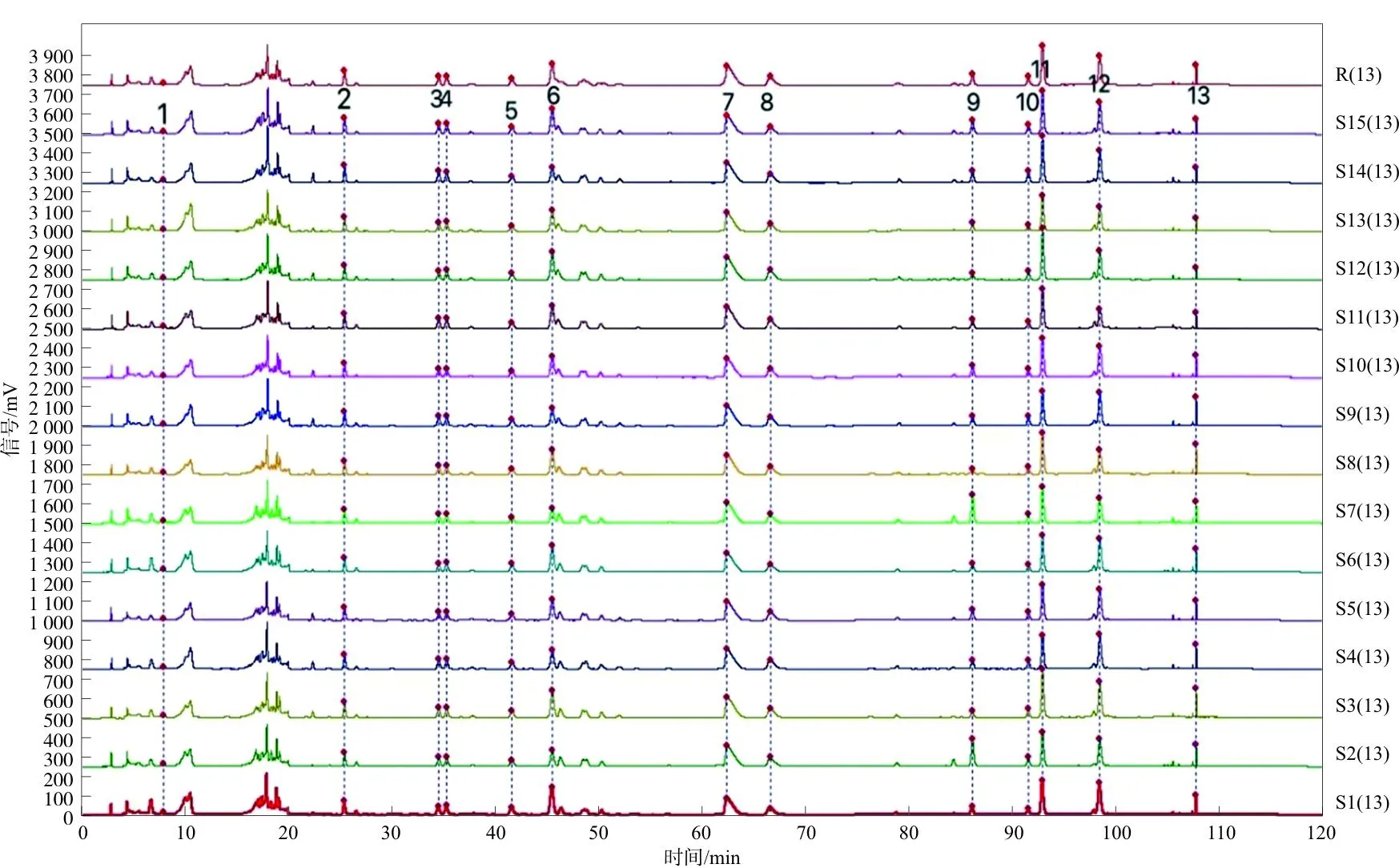
注:1.梓醇;5.阿魏酸;6.异阿魏酸;7.盐酸小檗碱;8.盐酸巴马汀;12.丹皮酚;13.藁本内酯
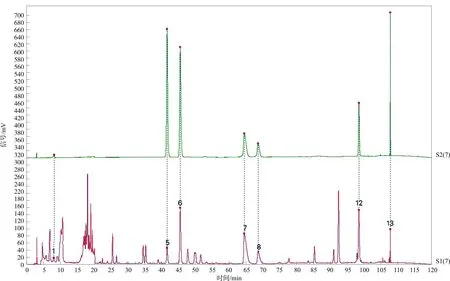
注:1.梓醇;5.阿魏酸;6.异阿魏酸;7.盐酸小檗碱;8.盐酸巴马汀;12.丹皮酚;13.藁本内酯
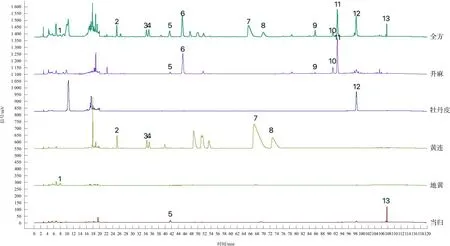
注:1.梓醇;5.阿魏酸;6.异阿魏酸;7.盐酸小檗碱;8.盐酸巴马汀;12.丹皮酚;13.藁本内酯
2.3 清胃散物质基准中梓醇、阿魏酸、异阿魏酸、丹皮酚指标成分含量测定
2.3.1 色谱条件 同“2.2.1”项下色谱条件。
2.3.2 溶液的制备 对照品溶液的制备:分别取梓醇、阿魏酸、异阿魏酸和丹皮酚对照品适量,精密称定,加甲醇制成单标溶液,再分别吸取一定量混匀稀释成每1 mL含梓醇109.184 μg,阿魏酸89.298 μg,异阿魏酸85.398 μg,丹皮酚81.836 μg的混合对照品溶液,即得。
供试品溶液的制备:同“2.2.2”项下供试品溶液的制备。
2.3.3 方法学考察 精密度考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法制备供试品溶液,在“2.2.1”项色谱条件下连续进样6次,测定,记录梓醇、阿魏酸、异阿魏酸、丹皮酚的保留时间和峰面积,计算RSD,保留时间的RSD<0.38%、峰面积的RSD<3.24%,表明仪器精密度良好。
重复性考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法平行处理6份供试品溶液,在“2.2.1”项色谱条件下精密吸取各供试品溶液20 μL进样,测定,记录梓醇、阿魏酸、异阿魏酸、丹皮酚的保留时间和峰面积,计算RSD,保留时间的RSD<0.13%、峰面积的RSD<1.93%,表明该方法重现性良好。
稳定性考察:取清胃散物质基准粉末(批号:S1),按“2.2.2”项下方法制备供试品溶液,在“2.2.1”项色谱条件下分别于0、2、4、6、8、10、12、24 h精密吸取供试品溶液20 μL进样,测定,记录梓醇、阿魏酸、异阿魏酸、丹皮酚的保留时间和峰面积,计算RSD,保留时间的RSD<0.39%、峰面积的RSD<3.08%,表明该供试品溶液在24 h内均能保持稳定。
线性关系考察:精密吸取质量浓度为902.737 μg·mL-1的梓醇对照品溶液、910.800 μg·mL-1的阿魏酸对照品溶液、853.980 μg·mL-1的异阿魏酸对照品溶液、909.178 μg·mL-1的丹皮酚对照品溶液一定量,加甲醇稀释定容,配制成6种不同质量浓度的对照品溶液,分别吸取20 μL注入高效液相色谱仪,进行测定,记录峰面积,以对照品溶液的质量浓度为横坐标(X),以峰面积为纵坐标(Y)进行线性回归,结果见表4。
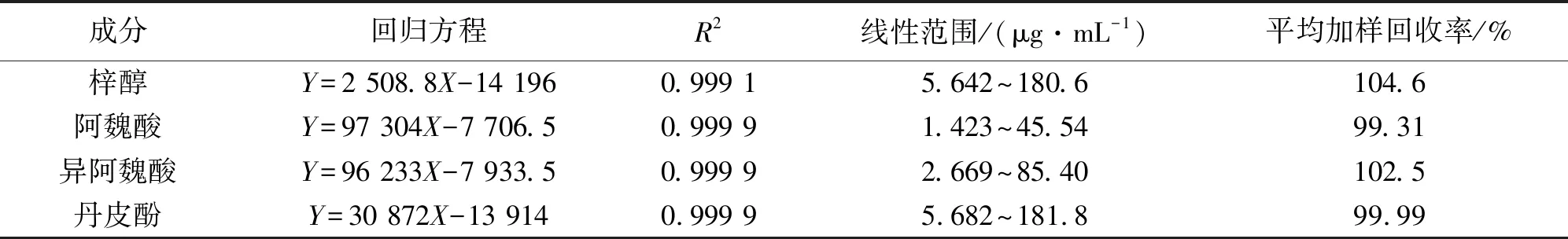
表4 清胃散物质基准中指标性成分含量测定方法学考察
加样回收率考察:取6份同一批次的清胃散物质基准(批号:S15)粉末,其中梓醇、阿魏酸、异阿魏酸及丹皮酚的含量分别为713.011、83.750、324.450、781.870 μg·g-1,按“2.2.2”项下方法制备供试品溶液,精密称量粉末,再精密加入一定量的已知质量浓度的被测成分对照品溶液,依法测定,计算其加样回收率,结果见表4。
2.3.4 样品的含量测定 分别精密称取15批清胃散物质基准样品,按“2.2.2”项下方法制备对照品和供试品溶液,分别精密吸取对照品溶液及供试品溶液各20 μL,注入高效液相色谱仪,测定峰面积,计算样品中梓醇、阿魏酸、异阿魏酸、丹皮酚的含量,结果见表5。
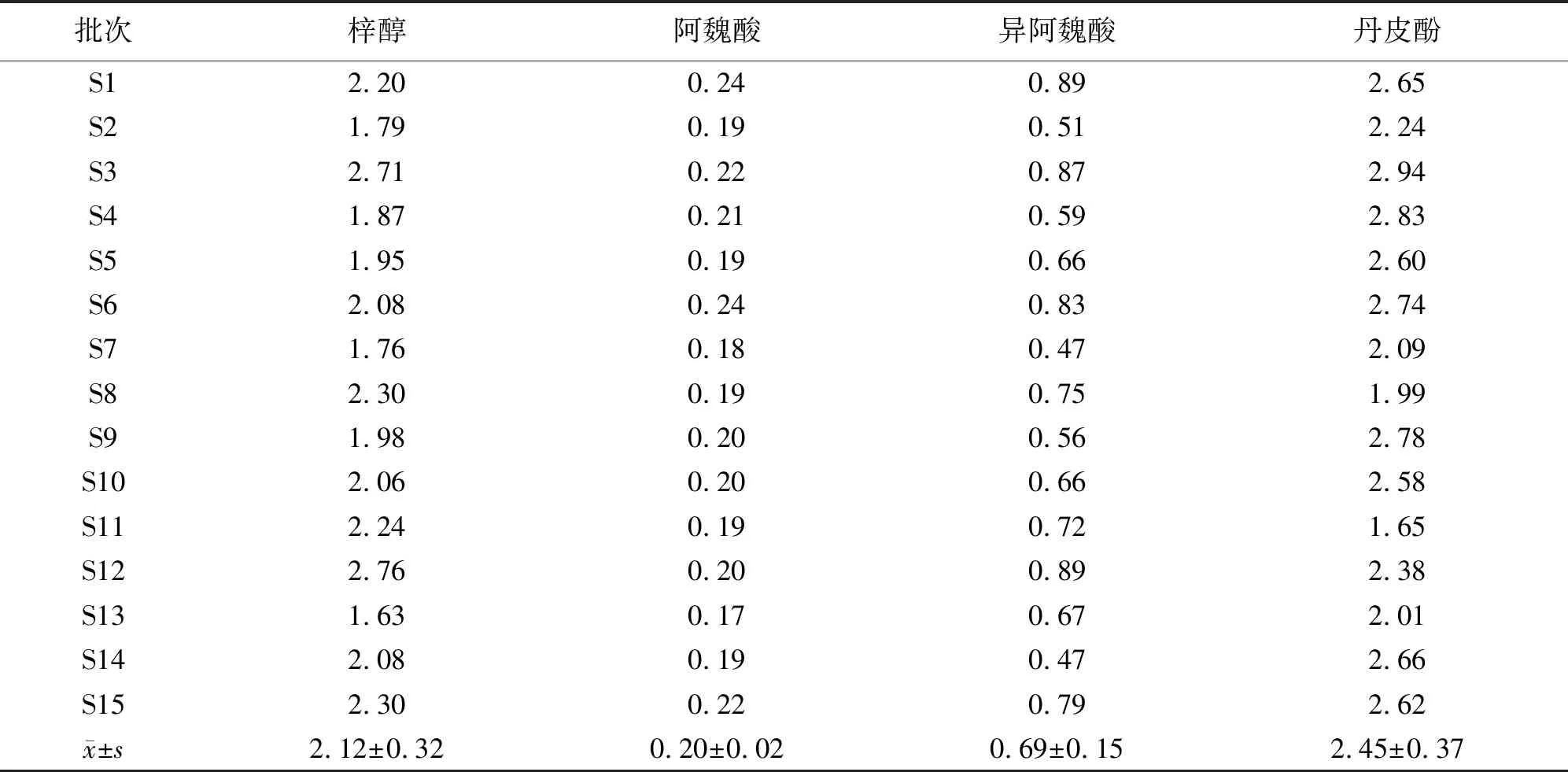
表5 清胃散物质基准中指标性成分含量测定结果(mg·g-1)
2.4 清胃散物质基准中生物碱类指标成分含量测定
2.4.1 色谱条件 色谱柱Waters Symmetry C18(4.6 mm×250 mm,5 μm);流动相乙腈(A)-0.05 mol·L-1磷酸二氢钾溶液(B)(每100 mL中加十二烷基硫酸钠0.4 g,再以磷酸调节pH值为4.0)(1∶1),检测波长345 nm,流速1.0 mL·min-1,柱温30 ℃,进样量10 μL。
2.4.2 溶液的制备 对照品溶液的制备:分别取盐酸黄连碱对照品、盐酸巴马汀对照品、盐酸小檗碱对照品适量,精密称定,加甲醇制成单标溶液,再分别吸取一定量混匀稀释成每1 mL分别含10.650、7.260、40.415 μg的溶液,即得。
供试品溶液的制备:取清胃散物质基准粉末约0.2 g,精密称定,置具塞锥形瓶中,精密加入甲醇-盐酸(100∶1)的混合溶液25 mL,密塞,称定质量,超声处理(功率250 W,频率40 kHz)15 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密量取续滤液2 mL,置10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
2.4.3 方法学考察 精密度考察:取清胃散物质基准粉末(批号:S1),按“2.4.2”项下方法制备供试品溶液,在“2.4.1”项色谱条件下连续进样6次,测定,记录盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的保留时间和峰面积,计算RSD,保留时间的RSD<0.05%、峰面积的RSD<2.88%,表明仪器精密度良好。
重复性考察:取清胃散物质基准粉末(批号:S1),按“2.4.2”项下方法平行处理6份供试品溶液,在“2.4.1”项色谱条件下精密吸取各供试品溶液10 μL进样,测定,记录盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的保留时间和峰面积,计算RSD,保留时间的RSD<0.23%、峰面积的RSD<2.87%,表明该方法重现性良好。
稳定性考察:取清胃散物质基准粉末(批号:S1),按“2.4.2”项下方法制备供试品溶液,在“2.4.1”项色谱条件下分别于0、2、4、6、8、10、12、24 h精密吸取供试品溶液10 μL进样,测定,记录盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的保留时间和峰面积,计算RSD,保留时间的RSD<0.15%、峰面积的RSD<2.27%,表明该供试品溶液在24 h内均能保持稳定。
线性关系考察:精密吸取质量浓度为106.500、72.600、404.150 μg·mL-1的盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的混合对照品溶液,加甲醇稀释溶液,配制成6种不同质量浓度的对照品溶液,分别吸取10 μL注入高效液相色谱仪,进行测定,记录峰面积,以对照品溶液的质量浓度为横坐标(X),以峰面积为纵坐标(Y)进行线性回归,结果见表6。
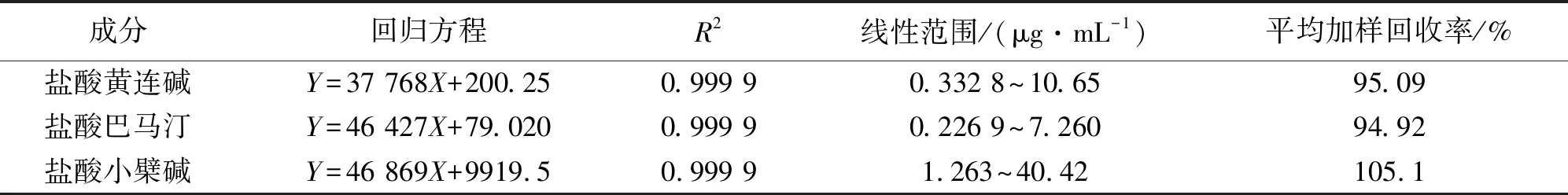
表6 清胃散物质基准中生物碱类指标性成分含量测定方法学考察
加样回收率考察:取6份同一批次的清胃散物质基准(批号:S1)粉末,其中盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的含量分别为922.791、775.155、2 281.759 μg·g-1,按“2.4.2”项下方法制备供试品溶液,精密称量粉末,再精密加入一定量的已知质量浓度的被测成分对照品溶液,依法测定,计算其加样回收率,结果见表6。
2.4.4 样品的含量测定 分别精密称取15批清胃散物质基准样品,按“2.4.2”项下方法制备对照品和供试品溶液,分别精密吸取对照品溶液及供试品溶液各10 μL,注入高效液相色谱仪,测定峰面积,计算样品中盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的含量,结果见表7。
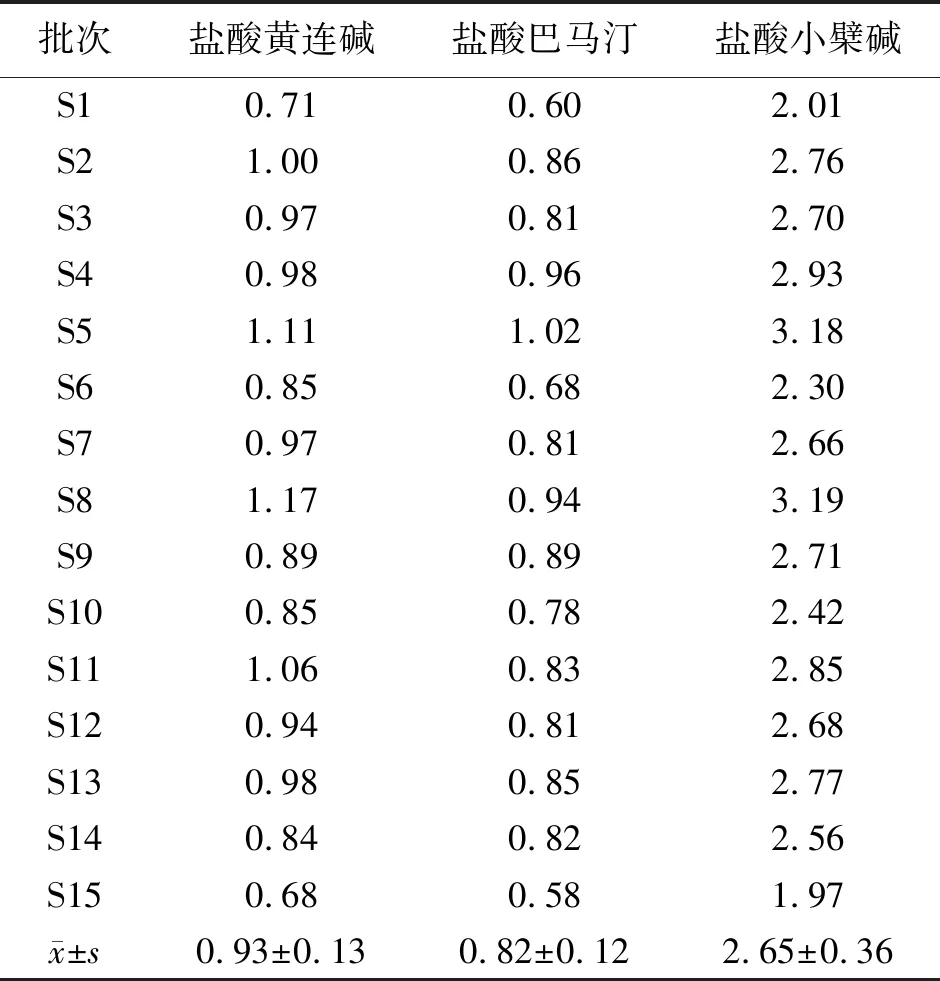
表7 清胃散物质基准中生物碱类指标性成分含量测定结果(mg·g-1)
3 讨论
3.1 特征图谱色谱条件及样品制备方法考察
3.1.1 流动相的选择 本研究考察了乙腈-0.1%甲酸水、乙腈-0.1%磷酸水、乙腈-0.1%乙酸水等流动相条件,发现乙腈-0.1%磷酸水条件下,各色谱峰分离度较好,峰形也较好[7],符合实验要求,因此选择乙腈-0.1%磷酸水作为流动相,并采用梯度洗脱进行检测。
3.1.2 波长的选择 经典名方清胃散由当归、地黄、牡丹皮、黄连、升麻5种药材组成,其化学成分复杂,单一波长检测很难完整反映整方的化学成分。根据DAD检测及3D图谱优选最佳波长[8]。发现330 nm下基线较平稳,共有峰数量较多,具有较高响应值,故选择330 nm作为检测波长1。但330 nm下无地黄特征峰(梓醇),210 nm时梓醇具有吸收峰,且梓醇在210 nm下具有较好吸收,故选择210 nm作为检测波长2[9]。最终确定0~4 min波长为330 nm、4~15 min波长为210 nm、15 min后波长为330 nm。本研究建立的特征图谱可以反映经典名方清胃散物质基准的整体化学成分特征和主要物质群,检测方法简单可行。
3.1.3 不同提取溶剂及时间的考察 选用25%、50%、75%及100%甲醇溶液[10]对供试品的提取溶剂进行比较,发现75%甲醇为提取溶剂时,特征图谱中峰数最多,且7种已知成分分离度较好[11],优于其他浓度的甲醇,因此,选择提取溶剂为75%甲醇。选用15、30、45、60 min这4种超声时间对供试品的提取时间进行比较,发现超声45 min时特征图谱中特征峰的峰面积较为合适,因此,选择超声提取时间为45 min。
3.1.4 流速及柱温的考察 考察不同流速,包括:0.95、1.00、1.05 mL·min-1。不同流速对特征峰的数目、峰形、分离度均无影响,说明建立的条件合理、稳定、可行,本实验选择流速为1.0 mL·min-1。考察不同柱温,包括:33、35、37 ℃。不同柱温对特征峰的数目、峰形、分离度均无影响,说明建立的条件合理、稳定、可行,本实验选择柱温为35 ℃。
3.2 生物碱类成分含量测定样品制备方法考察
3.2.1 不同提取时间及料液比的考察 选用15、30、45、60 min这4种超声时间对供试品的提取时间进行比较,发现超声15 min时特征图谱中特征峰的峰面积较为合适,因此,选择超声提取时间为15 min。选择1∶25、1∶50以及1∶100这3种料液比进行比较,发现选择1∶25这一种料液比时,指纹图谱中特征峰的峰面积较为合适且节省原料。
3.2.2 流速及柱温的考察 考察不同流速,包括:0.95、1.00、1.05 mL·min-1。不同流速对特征峰的数目、峰形、分离度均无影响,说明建立的条件合理、稳定、可行,本实验选择流速为1.0 mL·min-1。考察不同柱温,包括:28、30、32 ℃。不同柱温对特征峰的数目、峰形、分离度均无影响,说明建立的条件合理、稳定、可行,本实验选择柱温为30 ℃。
3.3 指标性成分的选择
本研究建立了经典名方清胃散物质基准的HPLC特征图谱,共指认全方特征峰13个,其中升麻5个,黄连5个,当归2个,牡丹皮1个,地黄1个,其中升麻与当归有1个共有峰(阿魏酸),指认了梓醇、阿魏酸、异阿魏酸、盐酸小檗碱、盐酸巴马汀、丹皮酚、藁本内酯7种成分。
梓醇为地黄定量的指标性成分,异阿魏酸为升麻定量的指标性成分,丹皮酚为牡丹皮定量的指标性成分,这3种成分对应的色谱峰在清胃散特征图谱中分离度较好,且无阴性干扰,可作为定量分析成分。阿魏酸为当归定量的指标性成分,升麻中也含有阿魏酸,并且阿魏酸色谱峰在清胃散特征图谱中分离度也较好,可以作为共有成分进行定量;藁本内酯也是当归的有效成分之一,但其化学性质不稳定,不适于定量分析。盐酸小檗碱及盐酸巴马汀虽然在清胃散特征图谱中分离度较好,但是峰形较差,不适用于定量,后期将参考2020年版《中国药典》中黄连含量测定的方法进行定量分析。
将15批清胃散物质基准中7种成分含量测定均值的70%~130%作为波动范围,即本品含梓醇、阿魏酸、异阿魏酸、丹皮酚、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱应分别在1.48~2.76、0.14~0.26、0.48~0.90、1.72~3.19、0.65~1.21、0.57~1.07、1.86~3.45 mg·g-1之间。
本研究对清胃散物质基准的质量标准进行研究,建立完整的清胃散物质基准的特征图谱,并对清胃散物质基准中的盐酸黄连碱、盐酸巴马汀、盐酸小檗碱、梓醇、阿魏酸、异阿魏酸及丹皮酚等化学成分进行定量研究,可用于清胃散物质基准的质量控制,便于后续清胃散复方制剂开发研究的质量控制及一致性评价。

