骆驼蓬子生物碱化学成分研究
刘永建,刘 浩,李华爽,杨宇萍,刘永刚
北京中医药大学中药学院 北京 100029
骆驼蓬PaganumharmalaL.是蒺藜科骆驼蓬属多年生草本植物,在我国广泛分布于新疆、内蒙古西部、陕西、甘肃、宁夏等地区,在美国、印度、非洲和伊朗的干旱和半干旱地区亦有分布。该植物的种子和全草均可入药,是我国维吾尔族、哈萨克族和蒙古族等民族沿用已久的民族药物,其种子的药用成分较高,经常被用于治疗消化道癌症、感冒、风湿病、疟疾、健忘症和一些皮肤病等。现代药理研究表明其具有抗肿瘤、消炎镇痛、驱虫杀菌等作用[1]。种子中富含生物碱,主要为β-卡波林(βcarboline)和喹唑啉(quinazoline)类,例如去氢骆驼蓬碱(harmine)、骆驼蓬碱(harmaline)、鸭嘴花碱(vasicine)、脱氧鸭嘴花碱(deoxyvasicine)等[2]。骆驼蓬种子中,总生物碱量为3.2%~7.7%,主要含去氢骆驼蓬碱与骆驼蓬碱(图1),也有文献报道二者在干燥种子中的质量分数分别为4.3%和5.6%,另外包含骆驼蓬酚(harmalol)0.6%,四氢骆驼蓬碱(tetrahydroharmine)0.1%[3-4]。骆驼蓬子生物碱有着广泛的药理作用,例如抗肿瘤[5]、抗菌[6]、抗病毒[7]、抗抑郁[8]、抗阿尔茨海默[9]、镇痛[10]等。
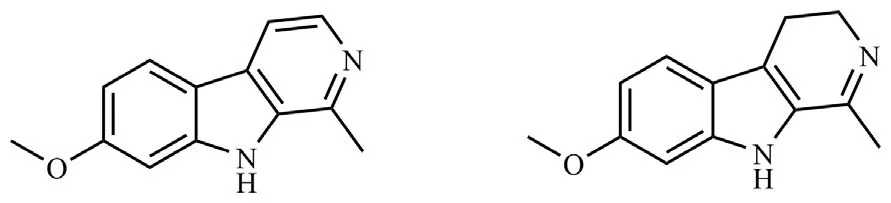
图1 去氢骆驼蓬碱 (左) 与骆驼蓬碱 (右) 的结构Fig.1 Structures of harmine (left) and harmaline (right)
为了进一步探究骆驼蓬子生物碱的活性成分,本研究从骆驼蓬子醇提-酸溶碱沉后的总生物碱中分离得到了12 个化合物,分别为1-甲基-2-甲氧甲基-7-甲氧基-9H-吡啶并[3,4-b]吲哚-2-盐酸盐(7-methoxy-2-(methoxymethyl)-1-methyl-9H-pyrido[3,4-b]indol-2-ium chloride,1),对苯二甲酸二(2-乙基)己酯 [bis(2-ethylhexyl) terephthalate,2],鸭嘴花酮碱(vasicione,3)、鸭嘴花碱(vasicine,4)、harmalanine(5)、去氢骆驼蓬碱(harmine,6)、哈尔满(harmane,7)、哈尔酚(harmol,8)、norharmane(9)、骆驼蓬碱( harmaline , 10 )、 四氢骆驼蓬碱(tetrahydroharmine,11)、骆驼蓬酚(harmalol,12)。其中化合物1 为新发现的化合物,命名为氮杂缩醛去氢骆驼蓬碱A(图2)。化合物2 为非生物碱,从骆驼蓬植物中首次分离得到(图2)。化合物1、2 及5 对HCT116 细胞的半数抑制浓度(median inhibition concentration,IC50)分别为(88.49±4.65)、(113.91±12.19)、(36.41±1.91)μmol/L。

图2 化合物1、2 和5 的结构Fig.2 Structures of compounds 1, 2 and 5
1 仪器与材料
BT224S 型十万分之一电子天平(德国Sartorius公司);AVANCE NEO 400/600 型核磁共振波谱仪(德国Bruker 公司);UPLC-MS(美国赛默飞世尔科技公司);SpectraMax i3x 型酶标仪(美国BioTek 公司);SW-CJ-2FD(标准型)双人单面净化工作台(苏州博莱尔净化设备有限公司);Series Ⅱ型二氧化碳培养箱、Revco PLUS 型-80 ℃低温冰箱(美国Thermo 公司);FC5515R 型高速低温离心机(美国Ohaus 公司);磁力搅拌器(冠森生物科技有限公司);96 孔板(美国Corning Incorporated 公司)。
分析纯醋酸乙酯、石油醚、二氯甲烷、甲醇(北京化工厂);95%溴甲基甲基醚、65%顺铂(上海麦克林生化科技股份有限公司);柱色谱硅胶(200~300 目)、GF254硅胶薄层色谱板(青岛海洋化工厂);葡聚糖凝胶Sephadex LH-20(美国GE 公司);CCK-8 试剂盒、磷酸缓冲盐溶液、胎牛血清(FBS)、链霉素-青霉素双抗(PS)、高糖DMEM 培养基(美国Corning Incorporated 公司);胰蛋白酶(美国Sigma公司);HCT116 细胞来自中国科学院细胞库。
骆驼蓬子购自新疆,经北京中医药大学刘永刚教授鉴定为蒺藜科植物骆驼蓬P.harmalaL.的种子。
2 方法
2.1 提取与分离
取骆驼蓬种子4.8 kg,经过粉碎机高速粉碎,用80%乙醇温浸,滤过后减压浓缩得到浸膏1.5 kg。于浸膏中加入5%盐酸调pH 值为2~3,过夜,滤过。滤液用氨水调pH 值至11~12,静置后抽滤,得到总碱333.4 g。总碱经硅胶柱色谱分离,以二氯甲烷-甲醇(1∶0→0∶1)梯度洗脱。收集二氯甲烷-甲醇(1∶0)的洗脱液,得到流分Fr. 1(1.4 g)。收集二氯甲烷-甲醇(100∶1)的洗脱液,得到流分Fr. 8(3.8 g)。收集80∶1~30∶1 的蓝色荧光部分,得到流分Fr. 17(98.0 g)。继续收集20∶1~8∶1 的洗脱液,在紫外灯下为绿色荧光,得到流分Fr. 20(103.0 g)。
Fr. 1 经硅胶柱色谱分离,以石油醚-二氯甲烷(1∶1)为洗脱剂,得到化合物2(20.0 mg)。Fr. 8经硅胶柱色谱分离,以二氯甲烷-甲醇(80∶1)为洗脱剂,收集254 nm 有荧光斑点但365 nm 下无荧光斑点的流分Fr. 8.1,经甲醇重结晶,得到化合物3(210.0 mg)。继续收集洗脱液,得到365 nm 下强蓝色荧光流分Fr. 8.2,经Sephadex LH-20 进一步分离,以甲醇为洗脱剂,得到化合物5(7.1 mg)。Fr.17 经硅胶柱色谱分离,以二氯甲烷-甲醇(60∶1→30∶1)梯度洗脱,得到3 个流分Fr. 17-1~17-3。Fr. 17-1 经甲醇重结晶得到化合物6(25.0 g)。Fr. 17-2 继续用硅胶柱色谱分离,以二氯甲烷-二乙胺(150∶1)洗脱,得到化合物6(39.0 g)与流分Fr. 17-2-2。Fr. 17-2-2 经硅胶制备薄层分离,以二氯甲烷-甲醇(9∶1)为展开剂得到化合物7(2.1 mg)和1(8.0 mg)。Fr. 17-3 经Sephadex LH-20 分离,用甲醇-水(4∶1)洗脱,得到化合物9(1.1 mg)和4(0.9 mg)。Fr. 20 经硅胶柱色谱分离,以二氯甲烷-甲醇(15∶1→10∶1)为洗脱剂,得到流分Fr.20-1~20-3。Fr. 20-1 经硅胶制备薄层分离,以二氯甲烷-甲醇(8∶1)展开得到化合物8(10.6 mg)。Fr. 20-2 经硅胶柱色谱分离,以二氯甲烷-甲醇-二乙胺(100∶1∶1)为洗脱剂,得到流分Fr. 20-2-1 和Fr. 20-2-2。Fr. 20-2-1 再次经硅胶柱色谱分离,以二氯甲烷-甲醇(10∶1)为洗脱剂,洗脱液减压浓缩后以甲醇重结晶得化合物10(72.0 g)。Fr. 20-3 经ODS 柱色谱分离,以甲醇-水(1∶1)洗脱得化合物11(30.0 mg)。Fr. 20-2-2 经硅胶制备薄层分离,展开缸氨水饱和后,以二氯甲烷-甲醇(15∶1)展开得化合物12(3.0 mg)。
2.2 化合物1(氢溴酸盐)的合成
参考去氢骆驼蓬碱常用的2 位成盐修饰[11]。将1 mmol(212.2 mg)去氢骆驼蓬碱溶解于50 mL 醋酸乙酯中,再加入20 mmol(2.63 g)溴甲基甲基醚,90 ℃回流12 h,TLC 跟踪。反应完成后,停止回流,反应液冷却,过滤,适量醋酸乙酯洗涤。产物经硅胶柱色谱分离,以二氯甲烷-甲醇(5∶1)洗脱,减压浓缩后得到白色晶体为化合物1 的氢溴酸盐(219.18 mg),收率为65%。
2.3 HCT116 细胞毒性实验
取生长状态良好的细胞,加入胰蛋白酶消化,待完全消化后,加入DMEM 完全培养基终止消化,移入无菌离心管,离心5 min(转速为3 000 r/min)后弃上清,加入2 mL 完全培养基,制备细胞混悬液。将细胞悬液充分吹打均匀后,取20 μL 细胞悬液加入到细胞计数板中,使用细胞计数仪进行计数,并用DMEM 完全培养基将细胞悬液的浓度稀释到1×105/mL,种入96 孔板中,每孔加入细胞混悬液100 μL。置于37 ℃、5% CO2细胞培养箱培养。24 h 细胞贴壁后,加入相应剂量的药物刺激,设定7~8 个浓度梯度。在药物刺激24 h 后,吸出药物与培养基,将CCK-8 与DMEM 基础培养基按照1∶9 混合,96 孔板每孔加入100 μL CCK-8 稀释液,孵育0.5~1.5 h 后,用全波长酶标仪检测各孔在450 nm波长下的吸光度(A)值,以不加药A值在1 左右时终止孵化,每组设置3 个复孔,重复3 次。按照公式计算不同浓度梯度下的细胞存活率,以Graphpad Prism 9 软件计算IC50。
细胞存活率=(As-Ab)/(Ac-Ab)As为实验孔吸光度(含细胞、培养基、CCK-8 溶液和药物溶液);Ac为对照孔吸光度(含细胞、培养基、CCK-8 溶液,不含药物);Ab为空白孔吸光度(含培养基、CCK-8 溶液,不含细胞、药物)
3 结果
3.1 提取化合物的结构鉴定
化合物 1:淡黄色粉末,HR-ESI-MSm/z:257.128 27 [M-Cl]+(计算值为257.128 45),分子式为C15H17N+2O2Cl-。质谱二级碎片m/z213.102 16提示结构可能为去氢骆驼蓬碱母核。氘代甲醇氢谱中δH8.25、7.17 及7.08 为去氢骆驼蓬碱苯环ABX偶合系统质子信号,δH8.54 及8.36 的偶合常数J=6.5 Hz 为吡啶环H-3 与H-4 特征偶合,1H-1H COSY验证了上述邻位偶合关系(图3),同时结合碳谱数据可确定此母核。与去氢骆驼蓬碱(化合物6)氢碳信号相比,多了2 个氢信号δH3.46 (3H)及5.86(2H),2 个碳信号δC57.7 与87.2,推测存在-OCH3及-N-CH2-O-。氘代氯仿氢谱δH13.91 提示存在1 个活泼氢,为N-9 位活泼氢。综上推测-N-CH2-O-的N为N-2 位。HMBC (CDCl3) 中质子δH5.86 (H-16) 与δC130.9 (C-3) 和139.1 (C-1) 以及甲氧基δC57.7 (C-17) 相关,可确定甲氧基甲基侧链连在N-2 位上(图3)。因谱图中未见其它含碳阴离子,而提取方法为盐酸提取,所以阴离子推断为氯离子。故该化合物鉴定为1-甲基-2-甲氧甲基-7-甲氧基-9H-吡啶并[3,4-b]吲哚-2-盐酸盐,经SciFinder 检索,为未见文献报道的新化合物,命名为氮杂缩醛去氢骆驼蓬碱A(azaacetal harmine A)。其NMR 数据归属见表1。另外,“2.2”项进行了合成验证,数据见“3.2”项。
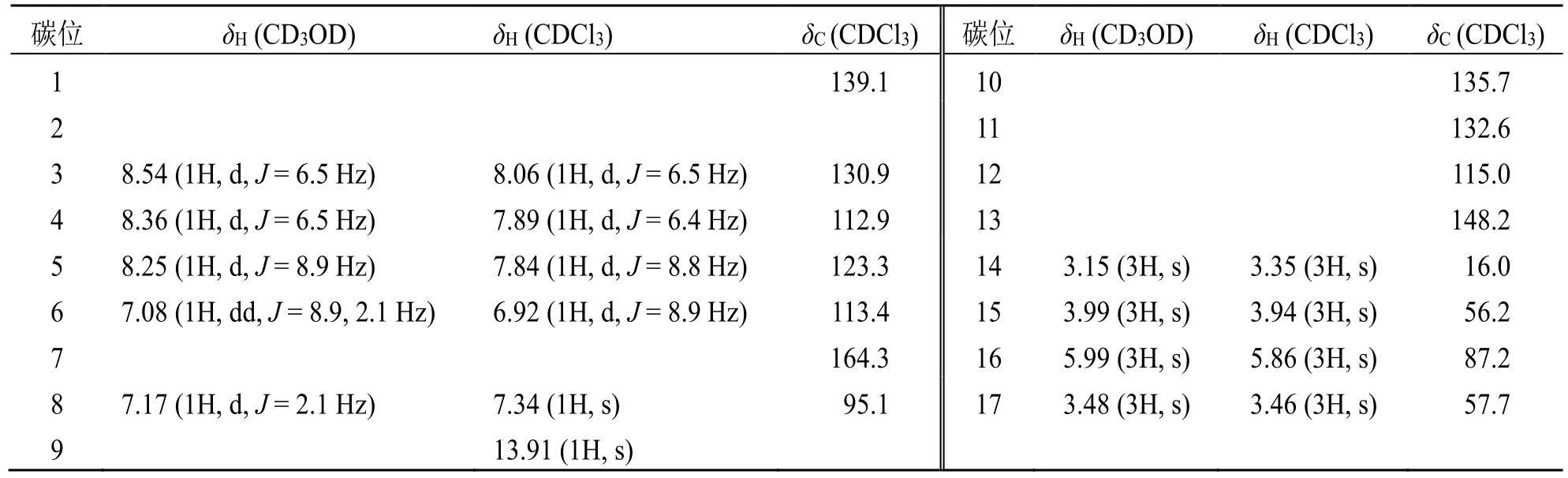
表1 化合物1 的1H-NMR 和13C-NMR 数据 (400/600/100 MHz)Table 1 1H-and 13C-NMR data of compound 1 (400/600/100 MHz)

图3 化合物1 的的关键1H-1H COSY、HMBC 相关信号Fig.3 Key 1H-1H COSY and HMBC correlations of compound 1
化合物 2:黄色油状物,HR-ESI-MSm/z:391.283 91 [M+H]+,分子式为C24H38O4。1H-NMR(400 MHz, CDCl3)δ: 8.08 (4H, s, H-2, 3, 5, 6), 4.30~4.19 (4H, m, H-1', 1″), 1.71 (2H, m, H-2', 2″), 1.49~1.41 (4H, m, H-3', 3″), 1.41~1.30 (12H, m, H-4', 4″,5', 5″, 7', 7″), 0.93~0.86 (12H, m, H-6', 6″, 8', 8″);13C-NMR (100 MHz, CDCl3)δ: 166.0 (C=O), 134.3(C-1, 4), 129.6 (C-2, 3, 5, 6), 67.8 (C-1', 1″), 39.0 (C-2', 2″), 30.7 (C-3', 3″), 29.1 (C-4', 4″), 24.1 (C-7', 7″),23.1 (C-5', 5″), 14.1 (C-7', 7″), 11.2 (C-8', 8″)。以上波谱数据与文献对比基本一致[12],鉴定化合物2 为对苯二甲酸二(2-乙基)己酯。
化合物3:白色晶体(甲醇),ESI-MSm/z:203.081 3 [M+H]+,分子式为C11H10N2O2。1H-NMR(400 MHz, CDCl3)δ: 8.42~8.15 (1H, m, H-8), 7.87-7.67 (2H, m, H-5, 6), 7.49 (1H, m, H-7), 5.26 (1H, td,J= 7.0, 2.2 Hz, H-3), 4.37 (1H, m, H-1a), 4.04 (1H, m,H-1b), 2.88~2.54 (1H, m, H-2a), 2.44~2.14 (1H, m,H-2b);13C-NMR (150 MHz, CDCl3)δ: 160.7 (C-3a),160.6 (C-9), 148.6 (C-4a), 134.6 (C-6), 127.1 (C-7),126.8 (C-8), 126.7 (C-5), 121.1 (C-8a), 71.9 (C-3), 43.6(C-1), 29.5 (C-2)。以上波谱数据与文献比对基本一致[13],鉴定化合物3 为鸭嘴花酮碱。
化合物4:白色晶体(甲醇),ESI-MSm/z:189.198 1 [M+H]+,分子式为C11H12N2O。1H-NMR(600 MHz, CD3OD)δ: 7.39~7.32 (1H, m, H-5), 7.28(1H, td,J= 7.5, 1.3 Hz, H-6), 7.21 (1H, d,J= 7.7 Hz,H-7), 7.19~7.10 (1H, m, H-8), 5.12 (1H, t,J= 8.1 Hz,H-3), 4.87 (2H, m, H-9), 3.76 (1H, m, H-1α), 3.67 (1H,dt,J= 10.8, 7.8 Hz, H-1β), 2.66 (1H, dtd,J= 13.0, 7.6,2.5 Hz, H-2α), 2.12 (1H, dq,J= 12.9, 8.5 Hz, H-2β);13C-NMR (150 MHz, CD3OD)δ: 164.8 (C-3a), 132.2(C-4a), 130.5 (C-6), 128.5 (C-8), 128.3 (C-7), 118.3 (C-8a), 118.2 (C-5), 72.6 (C-3), 52.0 (C-9), 47.5 (C-1),30.9 (C-2)。以上波谱数据经文献比对基本一致[13],鉴定化合物4 为鸭嘴花碱。
化合物5:淡黄色粉末,ESI-MSm/z: 267.112 6[M+H]+,分子式为C16H14N2O2。1H-NMR (400 MHz,CDCl3)δ: 8.24 (1H, s, H-1), 7.46 (1H, d,J= 8.5 Hz,H-9), 7.33 (1H, dd,J= 8.9, 7.0 Hz, H-15), 6.87 (1H, s,H-12), 6.83 (1H, dd,J= 8.7, 2.3 Hz, H-10), 6.48 (1H,d,J= 8.9 Hz, H-16), 6.24 (1H, d,J= 7.0 Hz, H-14),4.44 (2H, t,J= 6.9 Hz, H-5), 3.87 (3H, s, H-18), 3.07(2H, t,J= 7.0 Hz, H-6);13C-NMR (100 MHz, CDCl3)δ: 163.8 (C-17), 157.9 (C-11), 138.6 (C-13), 135.6 (C-15), 120.5 (C-9), 118.0 (C-16), 115.6 (C-7), 111.2 (C-10), 98.9 (C-14), 94.8 (C-12), 55.8 (C-18), 40.4 (C-5)。以上波谱数据经文献比对一致[14],鉴定化合物5 为harmalanine。
化合物6:淡黄色针状晶体(甲醇),ESI-MSm/z:213.192 0 [M+H]+,分子式为C13H12N2O。1H-NMR(400 MHz, CD3OD)δ: 8.10 (1H, d,J= 5.5 Hz, H-3),7.98 (1H, d,J= 8.7 Hz, H-5), 7.79 (1H, d,J= 5.5 Hz,H-4), 7.04 (1H, d,J= 2.2 Hz, H-8), 6.87 (1H, dd,J=8.7, 2.3 Hz, H-6), 3.91 (3H, s, H-15), 2.77 (3H, s, H-14);13C-NMR (100 MHz, CD3OD)δ: 162.6 (C-7),144.2 (C-1), 142.1 (C-13), 138.0 (C-3), 136.3 (C-10),130.2 (C-11), 123.5 (C-5), 116.4 (C-12), 113.3 (C-4),110.9 (C-6), 95.4 (C-8), 56.0 (C-15), 19.5 (C-14)。所得化合物的波谱数据经文献比对一致[15],鉴定化合物6 为去氢骆驼蓬碱。
化合物7:淡黄色粉末,ESI-MSm/z: 183.028 5[M+H]+,分子式C12H10N2。1H-NMR (600 MHz,CDCl3)δ: 8.38 (1H, d,J= 6.1 Hz, H-3), 8.12 (1H, d,J= 8.9 Hz, H-5), 7.83 (1H, d,J= 6.1 Hz, H-4), 7.55(2H, m, H-7, 8), 7.30 (1H, m, H-6), 2.84 (3H, s, H-14);13C-NMR (150 MHz, CDCl3)δ: 141.8 (C-1), 140.1 (C-13), 138.8 (C-3), 134.6 (C-10), 128.3 (C-11), 128.2 (C-7), 122.1 (C-12), 121.9 (C-5), 120.1 (C-6), 112.9 (C-4),111.6 (C-8), 20.4 (C-14)。以上波谱数据经文献比对一致[16],鉴定化合物7 为哈尔满。
化合物8:淡黄色粉末,ESI-MSm/z: 199.101 8[M+H]+,分子式为C12H10N2O。1H-NMR (400 MHz,CD3OD)δ: 8.08 (1H, d,J= 5.5 Hz, H-3), 7.92 (1H, d,J= 8.6 Hz, H-5), 7.77 (1H, d,J= 5.4 Hz, H-4), 6.92(1H, d,J= 2.1 Hz, H-8), 6.77 (1H, dd,J= 8.5, 2.1 Hz,H-6), 2.75 (3H, s, H-14);13C-NMR (100 MHz, DMSOd6)δ: 158.7 (C-7), 142.7 (C-13), 141.4 (C-1), 138.1 (C-3), 134.9 (C-10), 128.0 (C-11), 123.0 (C-5), 114.3 (C-12), 112.1 (C-4), 110.1 (C-6), 97.1 (C-8), 20.7 (C-14)。以上波谱数据经文献比对基本一致[17],鉴定化合物8 为哈尔酚。
化合物9:淡黄色粉末,ESI-MSm/z: 169.165 6[M+H]+,分子式为C11H8N2。1H-NMR (600 MHz,DMSO-d6)δ: 12.50 (1H, s, N-H), 9.19 (1H, s, H-1),8.60 (1H, d,J= 5.8 Hz, H-3), 8.52 (1H, d,J= 5.9 Hz,H-4), 8.44 (1H, d,J= 8.0 Hz, H-5), 7.79~7.74 (1H, m,H-8), 7.74~7.70 (1H, m, H-7), 7.39 (1H, ddd,J= 8.0, 6.8,1.1 Hz, H-6);13C-NMR (150 MHz, DMSO-d6)δ: 142.7(C-12), 135.0 (C-3), 131.7 (C-1), 131.5 (C-10), 130.6 (C-11), 128.8 (C-12), 123.0 (C-7), 120.7 (C-5), 119.7 (C-6),116.6 (C-4), 112.7 (C-8)。所得化合物的波谱数据经文献比对一致[18],鉴定化合物9 为norharmane。
化合物10:淡黄色粉末,ESI-MSm/z: 215.117 7[M+H]+,分子式为C13H14N2O。1H-NMR (400 MHz,CDCl3)δ: 12.56 (1H, s, -NH), 7.44 (1H, dd,J= 9.1, 2.6 Hz, H-5), 7.07 (1H, s, H-8), 6.83 (1H, dd,J= 9.1, 2.4 Hz, H-6), 3.91 (2H, t,J= 8.8 Hz, H-3), 3.85 (3H, d,J=2.6 Hz, H-15), 3.17 (2H, td,J= 9.0, 8.6, 2.5 Hz, H-4),3.06~3.00 (3H, m, H-14);13C-NMR (100 MHz,DMSO-d6)δ: 157.6 (C-1), 157.2 (C-7), 138.0 (C-13),129.0 (C-11), 120.3 (C-10), 119.9 (C-5), 115.0 (C-12),110.7 (C-6), 95.0 (C-8), 55.6 (C-15), 48.1 (C-3), 22.5(C-14), 19.6 (C-4)。以上波谱数据经文献比对一致[19],鉴定化合物10 为骆驼蓬碱。
化合物11:灰白色粉末,ESI-MSm/z: 217.243 5[M+H]+,分子式为C13H16N2O。1H-NMR (400 MHz,DMSO-d6)δ: 10.48 (1H, s, -NH), 7.20 (1H, d,J= 8.5 Hz, H-5), 6.78 (1H, d,J= 2.2 Hz, H-8), 6.59 (1H, dd,J= 8.6, 2.3 Hz, H-6), 3.96 (1H, q,J= 6.8 Hz, H-1), 3.73(3H, s, H-15), 3.12 (1H, dt,J= 12.5, 4.5 Hz, H-3), 2.80(1H, ddd,J= 12.9, 8.6, 4.9 Hz, H-4a), 2.63~2.52 (1H,m, H-4b), 1.32 (3H, d,J= 6.6 Hz, H-14);13C-NMR(150 MHz, DMSO-d6)δ: 155.0 (C-7), 137.0 (C-13),136.2 (C-10), 121.6 (C-12), 117.9 (C-5), 107.7 (C-6),106.5 (C-11), 94.6 (C-8), 55.2 (C-15), 47.8 (C-1), 42.2(C-3), 22.5 (C-4), 20.6 (C-14)。以上波谱数据经文献比对一致[19],鉴定化合物11 为四氢骆驼蓬碱。
化合物12:淡黄色粉末,ESI-MSm/z: 201.127 6[M+H]+,分子式为C12H12N2O。1H-NMR (400 MHz,DMSO-d6)δ: 11.86 (1H, s, -NH), 9.96 (1H, s, -OH),7.50 (1H, d,J= 8.8 Hz, H-5), 6.82 (1H, s, H-8), 6.70(1H, d,J= 8.8 Hz, H-6), 3.75 (2H, t,J= 8.7 Hz, H-4),2.99 (2H, t,J= 8.7 Hz, H-3), 2.53 (3H, s, H-14);13CNMR (150 MHz, DMSO-d6)δ: 164.4 (C-1), 159.1 (C-7), 142.9 (C-13), 125.4 (C-10), 123.1 (C-11), 118.2 (C-12), 114.2 (C-6), 96.2 (C-8), 41.8 (C-3), 19.1 (C-14),18.5 (C-4)。以上谱数据经文献比对一致[20],鉴定化合物12 为骆驼蓬酚。
3.2 合成化合物1(氢溴酸盐)的鉴定
化合物1(氢溴酸盐):白色晶体(甲醇),HRESI-MSm/z: 257.128 30 [M-Br]+,分子式为C15H17N+2O2Br-。1H-NMR (600 MHz, CD3OD)δ: 8.54(1H, d,J= 6.6 Hz, H-3), 8.35 (1H, d,J= 6.7 Hz, H-4),8.25 (1H, m, H-5), 7.17 (1H, d,J= 2.2 Hz, H-8), 7.06(1H, dd,J= 8.9, 2.6 Hz, H-6), 5.99 (2H, s, H-16), 3.99(3H, s, H-15), 3.48 (3H, s, H-17), 3.15 (3H, s, H-14)。其质谱、氢谱数据与化合物1 的相同。去氢骆驼蓬碱的2 位成盐修饰较为常见,所以通过比对分离的天然化合物1 及合成化合物的质谱、氢谱亦可辅助验证化合物1 的结构推测。
3.3 HCT116 细胞毒性实验
HCT116 细胞体外实验抑制结果(表2)显示,3 个化合物在一定浓度下均具有一定的抗癌活性。化合物1、2、5 的IC50(24 h)分别为(88.49±4.65)、(113.91±12.19)、(36.41±1.91)μmol/L。阳性药顺铂的IC50为(6.63±0.22)μmol/L。
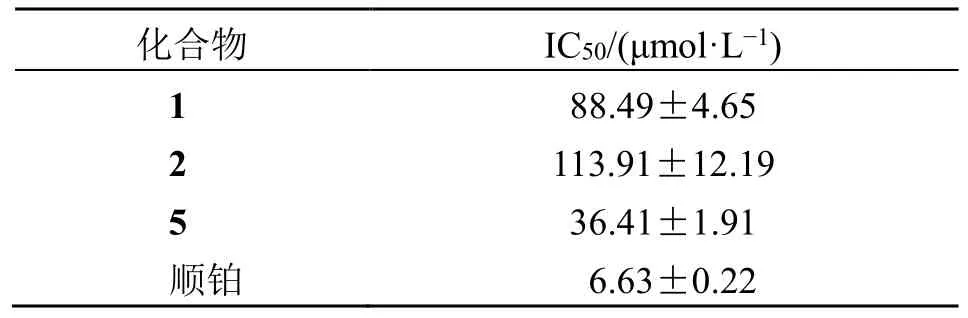
表2 化合物1、2、5 对HCT116 细胞的IC50Table 2 IC50 of compounds 1, 2 and 5 on HCT116 cells
4 讨论
本研究通过对骆驼蓬子醇提-酸溶碱沉的总生物碱进行分离,得到了12 个化合物。化合物1 为新化合物,而化合物2 为从骆驼蓬植物中首次分离得到。HCT116 细胞体外抗增殖实验表明,化合物1 和化合物2 对HCT116 细胞的抑制能力并不强,而具有较强共轭系统的化合物5 对其具有潜在的抑制能力,24 h 的IC50为(36.41±1.91)μmol/L。本实验不仅丰富了骆驼蓬子的化学成分信息,亦为其药用价值提供了一定的依据。
利益冲突所有作者均声明不存在利益冲突

