CircBICD2调节miR-218-5p/RhoA轴对口腔鳞状细胞癌细胞增殖、凋亡和上皮间质转化的影响
谢耕耘 安晓燕 王佳
口腔鳞状细胞癌(oral squamous cell carcinoma,OSCC)是最常见的口腔癌类型,局部淋巴结转移的高发生率以及远处器官的侵袭是OSCC相关死亡的主要原因[1-2]。目前对于OSCC的诊断和治疗水平有了很大的提升,但相关数据统计表明OSCC晚期患者的5年生存率依然居高不下[3]。因此,深入研究调节OSCC细胞生物学行为的分子生物标志物,可能为OSCC的早期诊断和治疗提供新的机会。环状RNA(Circular RNA, CircRNA)是一种特殊类型的具有环状结构的非编码RNA,越来越多的证据表明CircRNA在OSCC进展中发挥着关键作用[4]。已有研究报道,环状RNABICD2(CircBICD2)在OSCC组织和细胞中高表达, 干扰CircBICD2可抑制OSCC细胞增殖、迁移侵袭, 促进细胞凋亡[5]。但CircBICD2调控OSCC细胞恶性生物学行为的具体分子机制尚不完全明确。已有文献阐明CircRNA-miRNA-mRNA 信号轴参与OSCC的发生和进展[6]。本研究通过生物信息学分析发现CircBICD2与miR-218-5p、miR-218-5p与Ras同源基因家族成员A(Ras Homolog Gene Family Member A,RhoA)存在结合位点。相关研究显示,沉默miR-218-5p可促进OSCC细胞增殖[7];过表达RhoA可促进OSCC细胞迁移与侵袭[8]。而CircBICD2能否通过调控miR-218-5p/RhoA轴影响OSCC细胞恶性生物学行为尚不清楚。本研究主要探究CircBICD2对OSCC细胞生物学行为的影响以及其作用机制。
1 材料与方法
1.1 临床样本收集及细胞来源
25 对OSCC组织及癌旁组织(距离癌组织3 cm处)来自于2018 年9 月~2021 年9 月期间在本院首次确诊为OSCC的患者。所有患者均提供知情同意书,且本研究获得本院伦理委员会的批准(批准号: R-202209)。
人口腔上皮细胞系HOEC及OSCC细胞系HSC-4、CAL-27、SCC-15(浙江美森细胞科技有限公司)。
1.2 主要试剂
Annexin V-FITC/PI凋亡检测试剂盒(XYS0185,上海信裕生物公司);CCK-8试剂盒(MH1003,江苏麦格生物公司);兔源一抗波形蛋白(Vimentin)、E-钙黏蛋白(E-cadherin)、RhoA、神经钙粘蛋白(N-cadherin)、GAPDH及羊抗兔IgG二抗(货号:ab8978、ab76055、ab187027、ab245117、ab9484、ab6721)(Abcam公司,英国)。
1.3 细胞培养与分组
在含有10%胎牛血清的DMEM培养基中培养HOEC、HSC-4、CAL-27、SCC-15细胞。将SCC-15细胞分为si-NC组(B:转染si-NC)、si-CircBICD2组(C:转染si-CircBICD2)、miR-NC组(D:转染mimic NC)、miR-218-5p组(E:转染miR-218-5p mimic)、si-CircBICD2+anti-NC组(F:同时转染si-CircBICD2和anti-NC)、si-CircBICD2+anti-miR-218-5p 组(G:同时转染si-CircBICD2和anti-miR-218-5p),另将未经任何处理的SCC-15细胞命名为Ct组(A)。各组细胞转染48 h。
1.4 qRT-PCR检测CircBICD2和miR-218-5p表达
向组织匀浆和细胞中加入TRIzol,用于分离并提取总RNA,将2 μg RNA逆转录为cDNA后开始进行定量反应。CircBICD2、miR-218-5p的相对表达量是分别以GAPDH、U6为内参,通过2-ΔΔct法计算的。引物序列:GAPDH:正向5′-TTTAACTCTGGTAAAGTGGATAT-3′,反向5′-GGTGGAATCATATTGGAACA-3′;CircBICD2:正向5′-TTGGCTCTCCTGCTGTGC-3′,反向5′-GGTCATCCACAATCAGCCCA-3′;U6:正向5′-CG-CTTCGGCAGCACATATAC-3′,反向5′-TTCACGAATTTGCGTGTCAT-3′;miR-218-5p:正向5′-AACACGAACTAGATTGGTACA-3′,反向5′-AGTCTCAGGGTCCGAGGTATTC-3′。
1.5 CCK-8法检测细胞增殖
将各组SCC-15细胞(1×104个/孔)加入到96 孔板中孵育48 h,再向各孔加入10 μL CCK-8试剂在37 ℃下孵育2 h。通过酶标仪检测A值(450 nm处)。
1.6 细胞克隆形成的检测
将SCC-15细胞(280 个)放入细胞培养板中培养15 d后,除去培养液,将细胞经甲醇固定、结晶紫染色后,开始观察细胞克隆形成。
1.7 细胞凋亡的检测
将各组SCC-15细胞用预冷的PBS洗涤2次。然后将细胞以1×106个/mL的浓度重新悬浮在1×结合缓冲液中。取100 μL细胞悬液转移到5 mL培养管中。将5 μL Annexin V-FITC和5 μL碘化丙啶添加到样品中,然后在室温下避光孵15 min。将400 mL 1×结合缓冲液添加到每个管中,并立即通过流式细胞术分析样品。FlowJo软件用于数据分析。
1.8 RhoA、E-cadherin、N-cadherin、Vimentin蛋白表达的检测
组织匀浆以及细胞样品在RIPA缓冲液中裂解以获得总蛋白。取出40 μg蛋白质进行SDS/PAGE,然后转移到PVDF膜上,脱脂牛奶封闭后,在4 ℃下将膜与一抗RhoA(1∶1 000)、E-cadherin(1∶1 000)、Vimentin(1∶1 000)、N-cadherin(1∶4 000)、GAPDH(1∶3 000)孵育过夜,再在25 ℃下与二抗(1∶3 000) 一起孵育2 h。通过ImageJ软件评估蛋白灰度值。
1.9 双荧光素酶报告基因实验
构造BICD2野生型质粒(BICD2-WT)、突变型质粒(BICD2-MUT)、RhoA野生型质粒(RhoA-WT)和突变型质粒(RhoA-MUT),将BICD2-WT、BICD2-MUT、RhoA-WT、RhoA-MUT分别与miR-218-5p mimic或mimic NC共转染于SCC-15细胞,48 h后,统计荧光素酶活性的变化。
1.10 统计学分析
2 结 果
2.1 在组织和细胞中CircBICD2、 miR-218-5p表达及RhoA蛋白表达情况
与癌旁组织相比,OSCC组织中CircBICD2表达及RhoA蛋白表达量升高,miR-218-5p相对表达量降低(P<0.05)(图1A, 表1);与HOEC细胞比较,HSC-4、CAL-27、 SCC-15细胞中CircBICD2、 RhoA蛋白表达升高,miR-218-5p表达降低,且SCC-15细胞中CircBICD2、RhoA蛋白表达量最高,miR-218-5p表达量最低, 因此, 选取SCC-15细胞进行转染实验(图1B, 表2)。
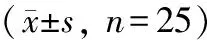
表1 在组织中CircBICD2、miR-218-5p表达及RhoA蛋白表达比较
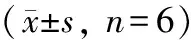
表2 在细胞中CircBICD2、 miR-218-5p表达及RhoA蛋白表达比较
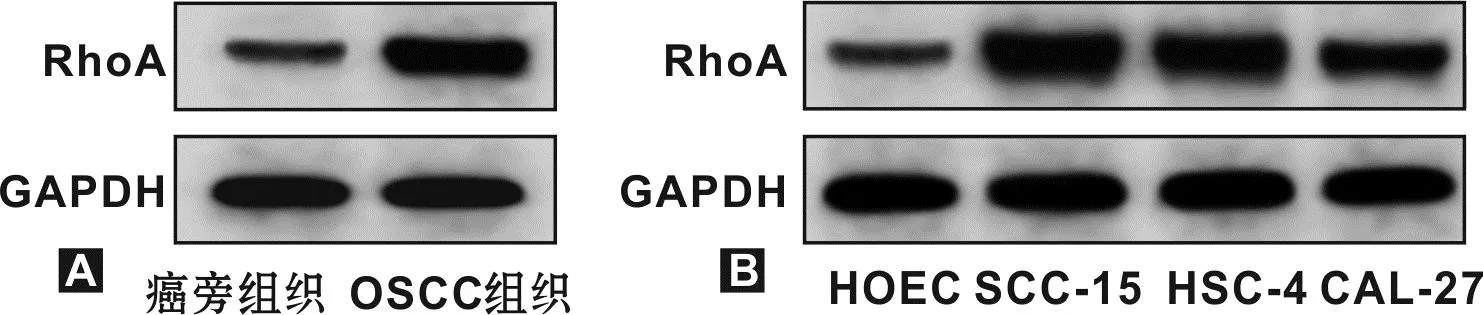
图1 组织中RhoA蛋白的表达(Western blot)
2.2 CircBICD2、miR-218-5p、RhoA蛋白在SCC-15细胞中的表达
与Ct组、si-NC组比较,si-CircBICD2组CircBICD2、RhoA蛋白表达降低,miR-218-5p表达升高(P<0.05);与Ct组、miR-NC组相比,miR-218-5p组CircBICD2表达变化差异无统计学意义(P>0.05),RhoA蛋白表达下调,miR-218-5p表达上调(P<0.05);与si-CircBICD2组、si-CircBICD2+anti-NC组相比,si-CircBICD2+anti-miR-218-5p组CircBICD2表达量变化差异无统计学意义(P>0.05),miR-218-5p表达降低,RhoA蛋白表达升高(P<0.05)(图2, 表3)。
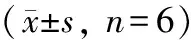
表3 各组SCC-15细胞中CircBICD2、miR-218-5p表达及RhoA蛋白表达比较
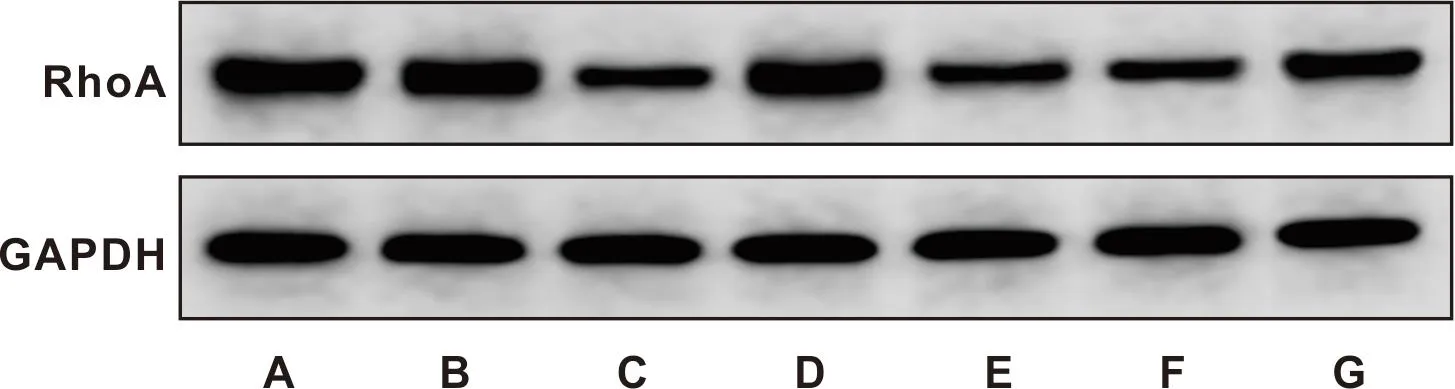
图2 各组SCC-15细胞中RhoA蛋白的表达(Western blot)
2.3 沉默CircBICD2或过表达miR-218-5p抑制SCC-15细胞增殖
与Ct组、si-NC组相比,si-CircBICD2组A450值及克隆形成率显著降低(P<0.05);与Ct组、miR-NC组相比,miR-218-5p组A450值、克隆形成率显著降低(P<0.05);与si-CircBICD2组和si-CircBICD2+anti-NC组相比,si-CircBICD2+anti-miR-218-5p组SCC-15细胞A450值、克隆形成率升高(P<0.05)(图3, 表4)。
表4 各组SCC-15细胞A450值、克隆形成率、凋亡率比较
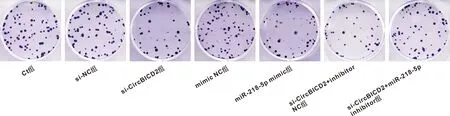
图3 沉默CircBICD2或过表达miR-218-5p对SCC-15细胞克隆形成的影响
2.4 下调CircBICD2或上调miR-218-5p促进SCC-15细胞凋亡
与Ct组、si-NC组对比,si-CircBICD2组SCC-15细胞凋亡率上升(P<0.05);与Ct组、miR-NC组比较,miR-218-5p组SCC-15细胞凋亡率升高(P<0.05);与si-CircBICD2组、si-CircBICD2+anti-NC组比较,si-CircBICD2+anti-miR-218-5p组SCC-15细胞凋亡率降低(P<0.05)(图4, 表4)。

图4 各组SCC-15细胞凋亡(流式细胞术)
2.5 沉默CircBICD2或过表达miR-218-5p对SCC-15细胞EMT的影响
与Ct组、si-NC组对比,si-CircBICD2组E-cadherin蛋白上调表达,N-cadherin、Vimentin蛋白下调表达(P<0.05);与Ct组、miR-NC组比较,miR-218-5p组E-cadherin蛋白上调表达,N-cadherin、Vimentin蛋白下调表达(P<0.05);与si-CircBICD2组、si-CircBICD2+anti-NC组相比,si-CircBICD2+anti-miR-218-5p组E-cadherin蛋白下调表达,N-cadherin、Vimentin蛋白上调表达(P<0.05)(图5、 表5)。
表5 各组SCC-15细胞中E-cadherin、N-cadherin、Vimentin蛋白表达比较
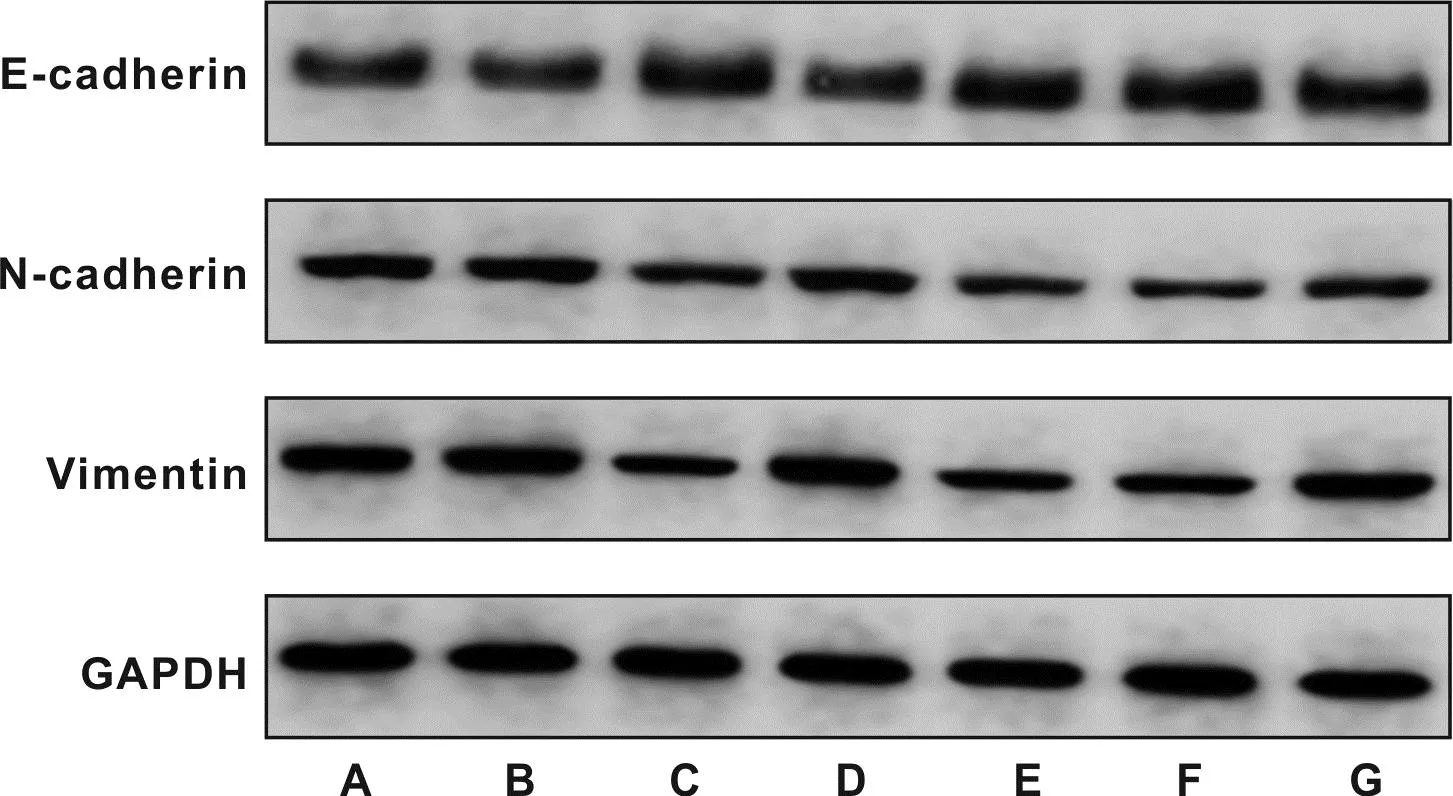
图5 各组SCC-15细胞中E-cadherin、N-cadherin、Vimentin蛋白表达(Western blot)
2.6 CircBICD2靶向调控miR-218-5p/RhoA轴
starbase预测CircBICD2与miR-218-5p、miR-218-5p与RhoA的结合位点(图6)。与mimic NC和BICD2-WT共转染组相比,miR-218-5p mimic和BICD2-WT共转染组荧光素酶活性下调(P<0.05);与mimic NC和BICD2-MUT共转染组对比,miR-218-5p mimic和BICD2-MUT共转染组荧光素酶活性变化不显著(P>0.05)。miR-218-5p mimic和RhoA-WT共转染组SCC-15细胞的荧光素酶活性显著低于mimic NC和RhoA-WT共转染组(P<0.05);与mimic NC和RhoA-MUT共转染组相比,miR-218-5p mimic和RhoA-MUT共转染组的荧光素酶活性变化差异不显著(P>0.05)(表6)。
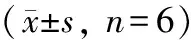
表6 荧光素酶活性比较
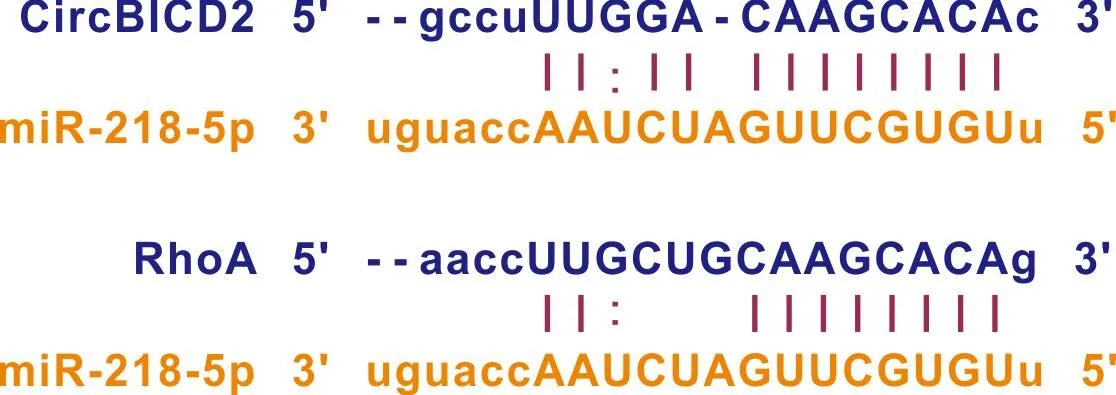
图6 Starbase预测CircBICD2与miR-218-5p、miR-218-5p与RhoA的结合位点
3 讨 论
CircRNA呈闭合环状结构,由于其特殊的结构,使CircRNAs比其线性mRNAs更稳定,这确保了它们的高度保守性[9]。据报道,CircRNA在人类肿瘤中表达异常,参与了肿瘤的进展[10]。如CircBICD2在OSCC 组织和细胞系中上调,抑制其表达显著降低了OSCC细胞增殖、迁移和侵袭能力[11];下调CircBICD2抑制了肝癌细胞增殖[12]。以上研究表明CircBICD2在OSCC、肝癌等肿瘤中具有促癌的作用。
本研究显示, CircBICD2在OSCC组织以及OSCC细胞CAL-27、HSC-4、SCC-15中CircBICD2呈高表达状态,且SCC-15细胞中CircBICD2表达量最高,因此研究对象指定为SCC-15细胞。上皮间质转化(epithelial-mesenchymal transition, EMT)在肿瘤发生和发展中起重要作用,其涉及细胞极性丧失和细胞间粘附过程,使肿瘤细胞具有迁移和转移的能力[13]。E-cadherin、N-cadherin、Vimentin是参与肿瘤细胞EMT的重要蛋白质,N-cadherin和vimentin的减少和E-cadherin的增加通常预示着EMT受到抑制[14]。本研究显示,沉默CircBICD2可抑制SCC-15细胞中N-cadherin、Vimentin蛋白表达,促进E-cadherin表达,提示,沉默CircBICD2可抑制SCC-15细胞EMT过程。此外,本研究还发现沉默CircBICD2可抑制SCC-15细胞增殖,促进细胞凋亡。
CircRNA可通过海绵化miRNA来调控肿瘤进展[15]。生物信息学发现CircBICD2可与miR-218-5p靶向结合。miR-218-5p作为一种miRNA,相关研究表明,下调miR-218-5p可促进骨肉瘤细胞增殖,抑制细胞凋亡[16];上调miR-218-5p抑制了喉鳞状细胞癌细胞增殖和侵袭能力[17];沉默miR-218-5p可促进胃癌细胞EMT[18]。表明miR-218-5p在骨肉瘤、喉鳞状细胞癌、胃癌等肿瘤中具有抑癌的作用。本研究阐明,在OSCC组织及细胞中miR-218-5p低表达,过表达miR-218-5p可抑制SCC-15细胞增殖和EMT,促进细胞凋亡。此外,本研究还发现,沉默CircBICD2后,SCC-15细胞中miR-218-5p表达升高,且双荧光素酶报告基因实验证实了CircBICD2与miR-218-5p的靶向关系,推测沉默CircBICD2可能通过上调miR-218-5p表达抑制SCC-15细胞增殖和EMT,促进细胞凋亡。为了验证该假设,本研究在下调CircBICD2的基础上再通过抑制miR-218-5p表达的方式来干预SCC-15细胞,结果发现,anti-miR-218-5p减弱了沉默CircBICD2对SCC-15细胞增殖和EMT的抑制作用以及对细胞凋亡的促进作用。证实了猜想是正确的。
miRNAs是一类小的单链非编码RNA,调节mRNA的转录或转录后的稳定性[19]。miRNA参与一系列生理活动,包括新陈代谢、细胞分化和肿瘤发生[20]。本研究为了进一步阐明CircBICD2靶向miR-218-5p调控OSCC细胞生物学行为的分子机制。本研究证实了RhoA为miR-218-5p的靶基因。RhoA是一种Rho家族GTP酶,它是细胞骨架功能的关键调节剂,RhoA激活已被证明可促进体外和体内肿瘤发生[21]。据报道,上调RhoA可促进OSCC细胞增殖和迁移[22]。提示RhoA在OSCC中发挥癌基因的作用。本研究显示,在OSCC组织和细胞中RhoA蛋白上调表达,沉默CircBICD2后,SCC-15细胞中miR-218-5p表达升高,RhoA蛋白表达降低;过表达miR-218-5p后,SCC-15细胞中RhoA蛋白表达降低,且CircBICD2与miR-218-5p、miR-218-5p与RhoA存在靶向结合关系,证明了沉默CircBICD2可能通过上调miR-218-5p来抑制RhoA表达,进而抑制SCC-15细胞增殖和EMT,促进细胞凋亡。
综上所述,沉默CircBICD2可能通过调控miR-218-5p/RhoA轴来抑制SCC-15细胞增殖、EMT,诱导细胞凋亡。本研究证明了CircBICD2/miR-218-5p/RhoA轴参与OSCC的肿瘤发生。这些发现揭示了OSCC中一个新的调控网络,并可能有助于确定OSCC的新治疗靶点。

