加味温胆汤联合西药治疗痰热内扰证失眠伴焦虑抑郁的临床观察*
蒋进珍,陈国华,宋昕桦,张逸寒,罗智毓,王广,梅俊华
(1.湖北中医药大学第一临床学院,武汉 430065;2.武汉市第一医院神经内科,睡眠医学中心,武汉 430022)
1 资料与方法
1.1临床资料 根据纳排标准选取2022年5月—2023年5月武汉市第一医院收治患者120例。本研究由我院伦理委员会予以批准,患者具有知情权并签署知情同意书。
纳入标准:(1)年龄 18~65岁,性别不限。(2)符合西医诊断标准:ICSD-3[8]中关于失眠的诊断标准;汉密尔顿抑郁量表(Hamilton depression scale,HAMD)≥8分或汉密尔顿焦虑量表(Hamilton anxiety scale,HAMA)评分≥14分。(3)符合中医诊断标准,失眠诊断根据《2016年失眠症中医临床实践指南(WHO/WPO)》[9]制定:①凡是以不易入睡,睡中易醒,甚至彻夜难眠为主要临床表现者,均可诊断为失眠;②常因失眠而产生疲乏、倦怠、不欲饮食、工作能力下降等符合症状;③临床检查未见器质性病变,多导睡眠监测(Polysomnograghy,PSG)检查可见睡眠结构紊乱表现;结合睡眠量表、有关生物化学检查加以确立;④排除郁证等精神疾病所导致的睡眠障碍。郁病诊断参考《中医病证诊断疗效标准》[10]:①精神不振,忧郁不畅,胸闷胁胀,善太息,或不思饮食,失眠多梦,易怒、善哭等;②有多虑、悲哀、郁怒、忧愁等情志所伤史。(4)符合中医痰热内扰证型:参照《中医病证诊断疗效标准》[11]制定。临床主要表现:睡眠不安,心烦懊憹,胸闷脘痞,口苦痰多,头晕目眩。舌红,苔黄腻,脉滑或滑数。(5)受试者自愿参加,签署知情同意书。同时满足以上5条者符合纳入标准。排除标准:①药物性失眠患者;②具有严重器质性疾病的患者(如恶性肿瘤,心脑血管事件恢复期等);③具有明确诊断的焦虑症和严重抑郁症以外的精神类疾病(如精神分裂症、双向情感障碍、自闭症等);精神发育迟滞患者;乙醇或药物导致的精神障碍患者;④认知功能受损而无法与研究者正常沟通的患者[简易精神状态评价量表评分(mini-mental state examination,MMSE)<20分];⑤既往有严重食物药物过敏史者;⑥同期采用其他中医药治疗措施,如物理疗法、针灸等措施,影响疗效判断者。
脱落标准:经知情同意、并筛选合格进入试验的受试者,因故未完成本方案所规定的疗程及观察周期,或符合中止试验标准:①出现不良反应事件,不适合继续治疗者;②受试者经过观察分析考虑患者不适合继续治疗,均作为脱落病例。
1.2方法
1.2.1分组方法 采用随机数字表法按1:1比例分为对照组和治疗组,各60例,两组患者连续治疗6周。基线期纳入对照组和治疗组各60例,两组性别、年龄、身高、体质量、身体质量指数(body mass index,BMI)、文化程度、个人史等一般临床资料比较差异无统计学意义(P>0.05),资料具有可比性,见表1。最终完成人数对照组和治疗组分别为53例、55例,两组脱落率比较差异无统计学意义(P>0.05)。

表1 两组患者一般资料比较
1.2.2治疗方法 对照组给予草酸艾司西酞普兰片(山东京卫制药有限公司,批准文号:国药准字H20080599,规格:每片10 mg),每次10 mg,每早1次。右佐匹克隆片(成都康弘药业集团股份有限公司,批准文号:国药准字H20100074,规格:每片3 mg),每次1.5 mg,每晚1次。治疗组在对照组的基础上予以加味温胆汤治疗,方剂组方:竹茹20 g,枳实10 g,陈皮15 g,半夏20 g,茯神30 g,炙甘草6 g,龙骨30 g(先煎),牡蛎 30 g(先煎),石菖蒲30 g,制远志15 g。以此为基本方,临床视症状适当加减化裁。如,心热烦甚者,加黄连6 g、山栀10 g;胸闷甚者加薤白10 g,瓜蒌12 g;伴口苦者,加黄芩15 g、柴胡15 g;伴脘痞者加厚朴10 g;伴纳差者加砂仁6 g;伴头晕甚者加天麻10 g;伴痰多者加杏仁10 g。每天1剂,先浸泡,后用水煎煮2次,得煎液400 mL,分早饭后、入睡前1 h各服1次,每次200 mL。汤剂100 mL中至少含生药51.5 g,本研究代煎中药汤剂由武汉市第一医院中药房代煎,成品均采用快速检验颜色、气味、煎液得量以进行质量评价。
1.3观察指标 两组均在基线期采集基本信息,基线期、3个月采集PSG参数和心率变异性(heart rate variability,HRV)数据,基线期、6周、3个月均采集两组量表评分。
1.3.1PSG检查 采用澳大利亚康迪Greal 系列PSG仪记录夜间12 h的睡眠状况。连续两个晚上以消除“首夜效应”,采用第2晚监测结果作为疗效评价指标。睡眠阶段及参数是按照AASM2.4版睡眠分期及相关事件判读标准进行分析。参数主要包括:①睡眠效率(sleep efficiency,SE):监测时总睡眠时间与总卧床时间之间的百分比值,总睡眠时间包括所有的睡眠时间,不包括醒来的时间;②入睡潜伏期(sleep latency,SL):从关灯到第1次睡眠分期记录的时间;③觉醒时间(wake during sleep,SW):从入睡到睡眠结束期间觉醒时间总和;④觉醒次数(number of awakenings,NW):从入睡到睡眠结束期间清醒的次数;⑤睡眠结构:记录N1,N2,N3期百分比和快速眼动睡眠(rapid eye movement sleep,REM) 各期睡眠所占百分比。
场景革命就是在电商过程中,忘掉生意及商业关系。除突出品牌产品功能,更重要的是为消费者构思场景,抓住场景的代入感、愉悦感、期待感,讲商品的情感故事,把消费行为变成一个个场景社区。如:消费的食品是袁隆平的米……要么是新农人故事,要么是原产地的追根溯源,以感情引领消费。故事的场景化成为电商的购买核心和经济价值的源动力。
1.3.2HRV检查 采用动态心电图仪(DMS300-4,USA)监测24 h动态心电图。①时域分析[12]:按照标准化程序计算所有正态区间的标准差(SDNN)和相邻RR间期差值的均方根(RMSSD)。②频域分析:低频(LF:0.04~0.15 Hz),高频(HF:>0.15~0.40 Hz),以及它们的比值LF/HF[13]。检查者提前告知受检者禁止在检查前1 d及当日饮酒、喝浓茶及咖啡,避免剧烈运动。
1.3.3量表评估 (1)睡眠量表评估,①匹兹堡睡眠质量指数量表(Pittsburgh sleep quality index,PSQI):评估由入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物、日间功能障碍、睡眠质量7个维度及总分,该量表有较高的可靠性和有效性[14]。②失眠严重指数量表(insomnia severity index,ISI)总分:量表总分得分越高,代表失眠程度越严重。(2)情绪量表评估,①HAMD及HAMA总分:HAMD≥8分有抑郁症状;HAMA≥7分有焦虑。②抑郁症自我评估量表(patient health questionnare-9,PHQ-9)总分:≥5分表示有抑郁。③广泛性焦虑障碍量表(generalized anxiety disorder-7,GAD-7)总分:≥5分表示有焦虑。以上量表评分总分分值越高表示程度越重。
1.3.4安全性指标 生命体征、血常规、肝肾功能、心电图等。在整个观察周期中收集并详细记录不良事件的表现、程度、时间,发生的过程、特点、程度,处理措施与转归,及时判断该不良事件与试验药物的因果关系,并追踪观察和记录。
1.3.5药物不良反应情况 采用不良反应量表(TESS)评分标准,分无症状(0分),偶有(1分),轻度(2分),中度(3分)和重度(4分)。
2 结果
2.1两组患者PSG参数治疗前后比较 在基线期,两组患者各睡眠参数无明显差别(P>0.05),均表现为睡眠效率下降(<85%)、入睡潜伏期延长(>30 min)、觉醒时间延长(>20 min)、觉醒次数增加(>4次)、睡眠结构紊乱。在3个月时,对照组对REM期百分比影响无统计学差异(P>0.05),余参数均有明显改善,治疗组均可明显改善各睡眠参数(均P<0.05)。其中,治疗组的觉醒时间明显短于对照组,觉醒次数明显少于对照组,N3、REM期百分比均明显高于对照组(均P<0.05)。见表2。

表2 两组患者PSG参数比较
2.2两组患者HRV结果治疗前后比较 在基线期,两组患者HRV均异常,表现为SDNN、RMSSD、LF、HF值低,LF/HF值高。在3个月时,两组SDNN、RMSSD、LF、HF值均明显高于基线期,LF/HF值较基线期下降,其中,治疗组RMSSD、HF值明显高于对照组,LF/HF值明显低于对照组(均P<0.05)。见表3。

表3 两组患者HRV结果比较
2.3两组患者量表评分 治疗前后比较基线期,两组患者PSQI各维度和总分、ISI总分无明显差异,均高于正常值,提示均存在失眠。6周时,两组各量表评分均明显低于基线期(P<0.05),其中,治疗组患者的睡眠质量、催眠药物、日间功能障碍、PSQI总分明显低于对照组(P<0.05)。3个月时,两组各量表评分均明显低于基线期,治疗组患者的睡眠质量、催眠药物、日间功能障碍总分明显低于对照组(P<0.05)。见表4。
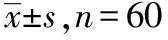
表4 两组患者睡眠量表和情绪量表评分比较
基线期,两组患者HAMA、HAMD、GAD-7、PHQ-9评分差异无统计学意义,均高于正常值,提示均存在焦虑、抑郁。6周时,两组以上量表评分均明显低于基线期(P<0.05),其中,治疗组HAMA、HAMD、GAD-7量表评分明显低于对照组(P<0.05)。3个月时,两组以上量表评分均明显低于基线期(P<0.05),其中,治疗组HAMA、GAD-7量表评分明显低于对照组(P<0.05)。见表4。
2.4不良反应比较 治疗组不良反应累积发生率为8.33%,明显低于对照组16.67%(χ2=5.174,P<0.05),治疗组 TESS 评分低于对照组(P<0.05)。见表5。
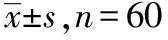
表5 两组患者不良反应情况比较
3 讨论
失眠与焦虑抑郁双向相关[16],睡眠神经通路与调节情感神经通路紧密相连并部分重叠,因此,失眠常与焦虑抑郁共病,常伴睡眠结构紊乱、自主神经功能失调等表现。本研究结果提示加味温胆汤联合西药既可该改善失眠又可改善焦虑抑郁。在既往研究中,缺乏对睡眠结构、自主神经功能方面疗效量化的客观依据,因此,本研究首次基于PSG、HRV量化疗效。
3.1加味温胆汤联合西药优化睡眠结构 除REM期百分比外,对照组治疗后对其余睡眠参数均有改善,既往研究显示右佐匹克隆片虽然可明显改善睡眠效率、入睡后觉醒时间,但不会改变REM睡眠[17]。而治疗组可明显缩短患者的觉醒时间、减少觉醒次数的同时,还可提高N3、REM期百分比,这展现加味温胆汤联合西药可明显优化睡眠结构,主要体现在提高睡眠连续性、加深睡眠深度。深睡眠占比与睡眠质量[18]、情绪调节有关[19],这解释加味温胆汤联合西药优化睡眠结构的同时又改善睡眠质量、焦虑、抑郁症状。
3.2加味温胆汤联合西药调节自主神经功能 SDNN代表自主神经的总体功能,RMSSD、HF均能反映副交感神经活动,LF代表交感/迷走神经双重调控能力,LF/HF被认为是交感/迷走神经平衡性指标[20]。自主神经系统可影响睡眠,CORREIA等[21]研究发现交感神经占主导地位可导致睡眠期间过度觉醒,这可能解释加味温胆汤联合西药通过改善交感/迷走神经均衡性来改善觉醒。HRV目前被认为可作为抗抑郁药物治疗反应的生物标记物[22],尤其是HF可用于预测焦虑抑郁患者对治疗反应的影响。本研究展示加味温胆汤联合西药可明显改善副交感神经功能活动。副交感神经系统在安静和放松状态下占主导地位,可调节焦虑情绪[23],这也揭示加味温胆汤联合西药改善焦虑症状的机制。不同睡眠阶段的自主神经功能表现不同,未来还可进一步讨论加味温胆汤联合西药在不同睡眠阶段中自主功能方面的疗效体现。
3.3加味温胆汤联合西药治疗本病的临床意义 右佐匹克隆属于环吡咯酮类化合物,半衰期短,主要经过CYP3A4系统代谢,不良反应主要有口苦、头晕、乏力等;艾司西酞普兰属于SSRIs类药物,具有起效快、效果稳定的特点,可有头晕、恶心呕吐、便秘、口干等不良反应[24]。温胆汤可治疗失眠、焦虑、抑郁、精神分裂症[25]等情志病,以及消化系统疾病[26]、心脑血管疾病[27]等疾病,临床应用范围广。现代药理学研究表明温胆汤主要包含黄酮化合物、三萜类、生物碱等化合成分[28],以上活性成分具有天然镇静催眠作用[29]的同时,还具有抗抑郁、抗焦虑、神经保护[30]等作用。加味中药中,石菖蒲中的α-细辛醚、β-细辛醚能透过血脑屏障入脑,可影响抑制P-糖蛋白功能、上调脑内5-羟色胺水平等提高血脑屏障的通透性以促进其他药物进入血脑屏障,可以有效提高生物利用度[31]。
综上所述,与西药治疗组相比,加味温胆汤联合西药可明显改善痰热内扰证失眠伴焦虑抑郁共病患者近期失眠、抑郁症状,短期焦虑症状的同时,还可优化睡眠结构、调节自主神经功能,且安全性好。体现多途径、多成分、不良反应少等优势的同时,加味温胆汤可能还通过提高西药生物利用度、血药浓度以辅助治疗,这还需药理实验进一步验证,以体现中西医药物联合治疗的优势。本研究也存在一定的局限性:①为单中心研究,存在一定的混杂因素影响;②药物对不同程度失眠伴焦虑抑郁共病疗效不同,本研究未对患者失眠、焦虑、抑郁程度进行分层深入探讨;③本研究未设立单用加味温胆汤组,未来或可观察单用加味温胆汤的疗效。

